Медь - это химический элемент с символом Cu(от латинского : купрум) и атомный номер 29. Это мягкий, ковкий и пластичный металл с очень высокой термической и электрической проводимостью. Свежеоткрытая поверхность из чистой меди имеет розово-оранжевый цвет. Медь используется как проводник тепла и электричества, как строительный материал и как составная часть различных металлических сплавов, таких как стерлинговое серебро, используемое в ювелирные изделия, мельхиор, используемый для изготовления морского оборудования и монет, и константан, используемый в тензодатчиках и термопары для измерения температуры.
Медь - один из немногих металлов, которые могут встречаться в природе в металлической форме, пригодной для непосредственного использования (самородные металлы ). Это привело к очень раннему использованию человеком в нескольких регионах, начиная с ок. 8000 г. до н.э. Тысячи лет спустя это был первый металл, выплавленный из сульфидных руд, c. 5000 г. до н.э.; первый металл, который нужно отлить в форму в форме, c. 4000 г. до н.э.; и первый металл, который будет целенаправленно сплавлен с другим металлом, оловом, для создания бронзы, c. 3500 г. до н.э.
В римскую эпоху медь добывалась в основном на Кипре, происхождение названия металла от aes сyprium (металл Кипра), позже преобразованный в сuprum (лат.). От него произошли копер (древнеанглийский ) и медь, более позднее написание впервые использовалось около 1530 года.
Обычно встречающиеся соединения - это соли меди (II), которые часто придают синий или зеленый цвет такие минералы, как азурит, малахит и бирюза, и исторически широко использовались в качестве пигментов.
Медь, используемая в зданиях, обычно для кровли, окисляется, образуя зеленую зеленоватую (или патину ). Медь иногда используется в декоративном искусстве как в форме элементарного металла, так и в виде соединений в качестве пигментов. Соединения меди используются в качестве бактериостатических агентов, фунгицидов и консервантов для древесины.
Медь важна для всех живых организмов в качестве микроэлемента диетического минерала, поскольку она является ключевым компонентом комплекса респираторных ферментов цитохром с оксидазы. У моллюсков и ракообразных медь является составной частью пигмента крови гемоцианина, замененного комплексным с железом гемоглобином у рыб и других животных. позвоночные. У людей медь содержится в основном в печени, мышцах и костях. В организме взрослого человека содержится от 1,4 до 2,1 мг меди на килограмм массы тела.
 Медь диск (чистота 99,95%), изготовленный методом непрерывной разливки ; протравливание для выявления кристаллитов
Медь диск (чистота 99,95%), изготовленный методом непрерывной разливки ; протравливание для выявления кристаллитов  Медь чуть выше точки плавления сохраняет свой розовый блеск, когда достаточно света затмевает оранжевый накал цвет
Медь чуть выше точки плавления сохраняет свой розовый блеск, когда достаточно света затмевает оранжевый накал цвет Медь, серебро и золото находятся в группе 11 периодической таблицы; эти три металла имеют один s-орбитальный электрон на верхней части заполненной d- электронной оболочки и характеризуются высокой пластичностью, а также электрической и теплопроводностью. Заполненные d-оболочки в этих элементах мало способствуют межатомным взаимодействиям, в которых доминируют s-электроны через металлические связи. В отличие от металлов с неполными d-оболочками, металлические связи в меди не имеют ковалентного характера и являются относительно слабыми. Это наблюдение объясняет низкую твердость и высокую пластичность монокристаллов меди. В макроскопическом масштабе введение протяженных дефектов в кристаллическую решетку , таких как границы зерен, препятствует течению материала под действием приложенного напряжения, тем самым увеличивая его твердость. По этой причине медь обычно поставляется в мелкозернистой поликристаллической форме, которая имеет большую прочность, чем монокристаллические формы.
Мягкость меди частично объясняет ее высокую электропроводность (59,6 × 10 S / м) и высокой теплопроводностью, второй по величине (второй после серебра) среди чистых металлов при комнатной температуре. Это связано с тем, что сопротивление переносу электронов в металлах при комнатной температуре возникает в основном из-за рассеяния электронов на тепловых колебаниях решетки, которые относительно слабы в мягком металле. Максимально допустимая плотность тока меди на открытом воздухе составляет примерно 3,1 × 10 А / м площади поперечного сечения, выше которой она начинает чрезмерно нагреваться.
Медь - один из немногих металлических элементов с естественным цветом кроме серого или серебристого. Чистая медь имеет оранжево-красный цвет и при контакте с воздухом приобретает красноватый потускнение. Характерный цвет меди является результатом электронных переходов между заполненными 3d и полупустыми 4s-оболочками атомов - разность энергий между этими оболочками соответствует оранжевому свету.
Как и в случае с другими металлами, если медь соприкасается с другим металлом, гальваническая коррозия возникнет.
 Неокисленная медная проволока (слева) и окисленная медная проволока (справа)
Неокисленная медная проволока (слева) и окисленная медная проволока (справа)  Восточная башня Королевской обсерватории, Эдинбург. Отчетливо виден контраст между восстановленной медью, установленной в 2010 году, и зеленым цветом оригинальной меди 1894 года.
Восточная башня Королевской обсерватории, Эдинбург. Отчетливо виден контраст между восстановленной медью, установленной в 2010 году, и зеленым цветом оригинальной меди 1894 года. Медь не реагирует с водой, но медленно реагирует с атмосферным кислородом с образованием слоя коричнево-черного оксида меди. которая, в отличие от ржавчины, которая образуется на железе во влажном воздухе, защищает лежащий под ней металл от дальнейшей коррозии (пассивация ). Зеленый слой verdigris (карбонат меди) часто можно увидеть на старых медных конструкциях, таких как крыши многих старых зданий и Статуя Свободы. Медь тускнеет при воздействии некоторых соединений серы, с которыми она реагирует с образованием различных сульфидов меди.
Существует 29 изотопов из меди. Cu и Cu стабильны, причем Cu составляет примерно 69% от встречающейся в природе меди; оба имеют спин , равный ⁄ 2. Другие изотопы являются радиоактивными, наиболее стабильным из которых является Cu с периодом полураспада 61,83 часа. Были охарактеризованы семь метастабильных изотопов ; Cu является самым долгоживущим с периодом полураспада 3,8 минуты. Изотопы с массовым числом выше 64 распадаются на β, тогда как изотопы с массовым числом ниже 64 распадаются на β. Cu с периодом полураспада 12,7 часа, распадаются в обе стороны..
Cu и Cu имеют важные применения. Cu используется в Cu-PTSM в качестве радиоактивного индикатора для позитронно-эмиссионной томографии.
 Самородная медь с полуострова Кивино, штат Мичиган, длиной около 2,5 дюймов (6,4 см)
Самородная медь с полуострова Кивино, штат Мичиган, длиной около 2,5 дюймов (6,4 см) Медь производится в массивных звездах и присутствует в земной коре в количестве около 50 частей на миллион (ppm). В природе медь встречается в различных минералах, включая самородную медь, сульфиды меди, такие как халькопирит, борнит, дигенит, ковеллит и халькоцит, сульфосоли меди , такие как тетраэдит-теннантит, и энаргит, карбонаты меди, такие как азурит и малахит, а также в виде оксидов меди (I) или меди (II), таких как куприт и тенорит, соответственно. Самая большая обнаруженная масса элементарной меди весила 420 тонн и была обнаружена в 1857 году на полуострове Кевино в Мичигане, США. Самородная медь - это поликристалл с самым большим из когда-либо описанных монокристаллов размером 4,4 × 3,2 × 3,2 см.
 Chuquicamata в Чили является одним из крупнейших в мире крупнейший карьер медь рудники
Chuquicamata в Чили является одним из крупнейших в мире крупнейший карьер медь рудники  Мировая динамика производства
Мировая динамика производства  Цены на медь в 2003–2011 гг. в долларах США за тонну
Цены на медь в 2003–2011 гг. в долларах США за тонну Большая часть меди добывается или добывается в виде меди сульфиды из крупных карьеров в медно-порфировых месторождениях, которые содержат от 0,4 до 1,0% меди. Сайты включают Chuquicamata в Чили, Bingham Canyon Mine в Юте, США, и El Chino Mine в Нью-Мексико, США. По данным Британской геологической службы, в 2005 году Чили была крупнейшим производителем меди с долей не менее одной трети в мире, за ней следовали США, Индонезия и Перу. Медь также может быть извлечена посредством процесса выщелачивания на месте. Несколько сайтов в штате Аризона считаются первыми кандидатами на использование этого метода. Количество используемой меди увеличивается, а доступного количества едва хватает для того, чтобы позволить всем странам достичь уровня использования в развитых странах.
Медь использовалась не менее 10 000 лет, но более 95% всей когда-либо добытой и выплавленной меди было добыто с 1900 года, и более половины было добыто за последние 24 года. Как и в случае со многими другими природными ресурсами, общее количество меди на Земле огромно: около 10 тонн в верхнем километре земной коры, что составляет около 5 миллионов лет при нынешних темпах добычи. Однако только малая часть этих запасов экономически жизнеспособна при нынешних ценах и технологиях. Оценки запасов меди, доступных для добычи, варьируются от 25 до 60 лет, в зависимости от основных предположений, таких как темпы роста. Переработка - основной источник меди в современном мире. Из-за этих и других факторов будущее производства и поставок меди является предметом многочисленных споров, включая концепцию пика меди, аналогичного пику добычи.
. Цена на медь исторически менялась. была нестабильной, и его цена выросла с 60-летнего минимума 0,60 доллара США за фунт (1,32 доллара США за кг) в июне 1999 года до 3,75 доллара США за фунт (8,27 доллара США за кг) в мае 2006 года. Она упала до 2,40 доллара США за фунт (5,29 доллара США за кг).) в феврале 2007 года, а затем восстановился до 3,50 доллара за фунт (7,71 доллара за килограмм) в апреле 2007 года. В феврале 2009 года из-за ослабления мирового спроса и резкого падения цен на сырьевые товары с максимумов предыдущего года цены на медь составили 1,51 доллара за фунт (3,32 доллара за кг).
 Схема процесса взвешенной плавки
Схема процесса взвешенной плавки Средняя концентрация меди в рудах составляет всего 0,6%, и большинство промышленных руд представляют собой сульфиды, особенно халькопирит (CuFeS 2), борнит (Cu 5 FeS 4) и, в меньшей степени, ковеллит (CuS) и халькоцит (Cu 2 S). Эти минералы концентрируются из дробленых руд до уровня 10–15% меди путем пенной флотации или биовыщелачивания. Нагревание этого материала с диоксидом кремния при мгновенной плавке удаляет большую часть железа в виде шлака. В процессе используется более легкое превращение сульфидов железа в оксиды, которые, в свою очередь, реагируют с кремнеземом с образованием силикатного шлака , который плавает поверх нагретой массы. Полученный медный штейн, состоящий из Cu 2 S, обжигают для превращения всех сульфидов в оксиды:
Закись меди при нагревании превращается в черновую медь:
Процесс Садбери штейна преобразовал только половину сульфида в оксид, а затем использовали этот оксид для удаления остальной серы в виде оксида. Затем он был подвергнут электролитической очистке, и анодный раствор был использован для получения платины и золота, которое он содержал. На этом этапе используется относительно легкое восстановление оксидов меди до металлической меди. Природный газ продувается через блистер для удаления большей части оставшегося кислорода, и электрорафинирование производится на полученном материале для получения чистой меди:

Как алюминий, медь подлежит вторичной переработке без потери качества как в сыром виде, так и в производимой продукции. По объему медь является третьим по величине перерабатываемым металлом после железа и алюминия. По оценкам, 80% всей когда-либо добытой меди все еще используется. Согласно отчету «Запасы металлов в обществе» Международной группы ресурсов, глобальные запасы меди на душу населения, используемой в обществе, составляют 35–55 кг. Большая часть этого приходится на более развитые страны (140–300 кг на душу населения), а не на менее развитые страны (30–40 кг на душу населения).
Процесс переработки меди примерно такой же, как и при извлечении меди, но требует меньшего количества шагов. Медный лом высокой чистоты плавится в печи , а затем восстанавливается и отливается в заготовки и слитки ; Лом низкой чистоты очищается путем гальваники в ванне с серной кислотой.
 Медные сплавы широко используются в производстве чеканки монет; здесь показаны два примера - американские десятицентовые монеты после 1964 года, которые состоят из сплава мельхиора и канадские монеты до 1968 года, которые состоят из сплава мельхиора. сплав 80 процентов серебра и 20 процентов меди.
Медные сплавы широко используются в производстве чеканки монет; здесь показаны два примера - американские десятицентовые монеты после 1964 года, которые состоят из сплава мельхиора и канадские монеты до 1968 года, которые состоят из сплава мельхиора. сплав 80 процентов серебра и 20 процентов меди. Было разработано множество медных сплавов , многие из которых имеют важное применение. Латунь - это сплав меди и цинка. Бронза обычно относится к сплавам медь-олово, но может относиться к любому сплаву меди, например, алюминиевой бронзе. Медь является одним из наиболее важных компонентов припоев из серебра и золота <29 карат, используемых в ювелирной промышленности, изменяя цвет, твердость и температуру плавления получаемых сплавов. Некоторые бессвинцовые припои состоят из олова, легированного небольшой долей меди и других металлов.
Сплав меди и никеля, называемый мельхиора, используется в монетах малого достоинства, часто для внешней облицовки. Американская пятицентовая монета (в настоящее время называемая никелем) состоит из 75% меди и 25% никеля в однородном составе. До появления мельхиора, который получил широкое распространение в странах во второй половине 20-го века, также использовались сплавы меди и серебра, а в США использовался сплав, состоящий из 90% серебра и 10% серебра. % меди до 1965 года, когда находящееся в обращении серебро было удалено из всех монет, за исключением полдоллара - они были обесценены до сплава 40% серебра и 60% меди в период с 1965 по 1970 год. Сплав 90% меди и 10% никеля, замечательный своей устойчивостью к коррозии, используется для различных объектов, подверженных воздействию морской воды, хотя он уязвим для сульфидов, которые иногда встречаются в загрязненных гаванях и устьях. Сплавы меди с алюминием (около 7%) имеют золотистый цвет и используются в украшениях. Шакудо - японский декоративный сплав меди, содержащий низкий процент золота, обычно 4–10%, который может быть патинированный до темно-синего или черного цвета.
 Образец оксида меди (I).
Образец оксида меди (I).Медь образует множество разнообразных соединений, обычно с окислением состояния +1 и +2, которые часто называют медью и медью соответственно. Соединения меди, будь то органические комплексы или металлоорганические соединения, способствуют или катализируют многочисленные химические и биологические процессы.
Как и другие элементы, простейшие соединения меди - это бинарные соединения, то есть соединения, содержащие только два элемента, основными примерами которых являются оксиды, сульфиды и галогениды. Известны как оксиды меди, так и оксиды меди. Среди множества сульфидов меди, важные примеры включают сульфид меди (I) и сульфид меди (II).
Галогениды меди (с хлором, бром и йод ), а также галогениды меди с фтором, хлором и бромом. Попытки получить иодид меди (II) дают только йодид меди и йод.
 Медь (II) дает темно-синюю окраску в присутствии аммиака лиганды. Используемый здесь сульфат тетраамминмеди (II).
Медь (II) дает темно-синюю окраску в присутствии аммиака лиганды. Используемый здесь сульфат тетраамминмеди (II).Медь образует координационные комплексы с лигандами. В водном растворе медь (II) существует в виде [Cu (H. 2O). 6].. Этот комплекс демонстрирует самую быструю скорость водообмена (скорость присоединения и отсоединения водных лигандов) для любого комплекса переходного металла и водного комплекса. гидроксид натрия вызывает осаждение светло-голубого твердого вещества гидроксид меди (II). Упрощенное уравнение:
 диаграмма Пурбе для меди в несложных средах (анионы, кроме ОН- не рассматриваются Концентрация ионов 0,001 м (моль / кг воды). Температура 25 ° C.
диаграмма Пурбе для меди в несложных средах (анионы, кроме ОН- не рассматриваются Концентрация ионов 0,001 м (моль / кг воды). Температура 25 ° C. Водный раствор аммиака дает такой же осадок. При добавлении избытка аммиака осадок растворяется с образованием тетраамминмеди (II) :
Многие другие оксианионы образуют комплексы; к ним относятся ацетат меди (II), нитрат меди (II) и карбонат меди (II). Сульфат меди (II) образует синий кристаллический пента гидрат, самое знакомое соединение меди в лаборатории. Он используется в фунгициде, называемом бордосской смесью.
 Шаровидная модель комплекса [Cu (NH 3)4(H2O)2], иллюстрирующая октаэдрическую координацию геометрия общая для меди (II).
Шаровидная модель комплекса [Cu (NH 3)4(H2O)2], иллюстрирующая октаэдрическую координацию геометрия общая для меди (II). Полиолы, соединения, содержащие более одной спиртовой функциональной группы, обычно взаимодействуют с солями двухвалентной меди. Например, соли меди используются для проверки на восстанавливающие сахара. В частности, при использовании реагента Бенедикта и раствора Фелинга присутствие сахара сигнализируется изменением цвета с синего Cu (II) на красноватую медь ( I) оксид. Реагент Швейцера и родственные комплексы с этилендиамином и другими аминами растворяют целлюлозу. Аминокислоты образуют очень стабильный хелат комплексы с медью (II). Существует множество мокрых химических тестов на ионы меди, в том числе с участием ферроцианида калия, который дает коричневый осадок с солями меди (II).
Соединения содержащие связь углерод-медь, известны как медноорганические соединения. Они очень реактивны по отношению к кислороду с образованием оксида меди (I) и имеют множество применений в химии. Их синтезируют обработкой соединений меди (I) реагентами Гриньяра, концевыми алкинами или литийорганическими реагентами ; в частности, последняя описанная реакция дает реагент Гилмана. Они могут подвергаться замещению на алкилгалогениды с образованием продуктов сочетания ; как таковые, они важны в области органического синтеза. Ацетилид меди (I) очень чувствителен к ударам, но является промежуточным звеном в таких реакциях, как сочетание Кадио-Ходкевича и сочетание Соногашира. Конъюгат присоединение к енонам и карбокупрация алкинов также может быть достигнуто с помощью медноорганических соединений. Медь (I) образует множество слабых комплексов с алкенами и оксидом углерода, особенно в присутствии аминных лигандов.
Медь (III) чаще всего встречается в оксидах. Простым примером является купрат калия, KCuO 2, сине-черное твердое вещество. Наиболее изученными соединениями меди (III) являются купратные сверхпроводники . Иттрий-барий-оксид меди (YBa 2Cu3O7) состоит из центров Cu (II) и Cu (III). Как и оксид, фторид является высокоосновным анионом и, как известно, стабилизирует ионы металлов в высоких степенях окисления. Известны как фториды меди (III), так и даже фториды меди (IV), K3CuF 6 и Cs2CuF 6, соответственно.
Некоторые белки меди образуют оксокомплексы, которые также содержат медь (III). С помощью тетрапептидов пурпурные комплексы меди (III) стабилизируются депротонированными амидными лигандами.
Комплексы меди (III) также встречаются в качестве промежуточных продуктов в реакциях медьорганических соединений. Например, в реакции Хараша – Сосновского.
Хронология меди показывает, как металл продвигал человеческую цивилизацию за последние 11000 лет.
 Корродированный медный слиток из Закрос, Крит, имеющий форму шкуры животного, типичной для той эпохи.
Корродированный медный слиток из Закрос, Крит, имеющий форму шкуры животного, типичной для той эпохи.  Многие орудия энеолита включали медь, например, лезвие этой копии топора Эци
Многие орудия энеолита включали медь, например, лезвие этой копии топора Эци  Медная руда (хризоколла ) в кембрийский песчаник из энеолита рудников в долине Тимна на юге Израиля.
Медная руда (хризоколла ) в кембрийский песчаник из энеолита рудников в долине Тимна на юге Израиля.Медь встречается в природе как самородная металлическая медь и была известен некоторым из древнейших известных цивилизаций. История использования меди восходит к 9000 г. до н.э. на Ближнем Востоке; медный кулон был найден в северном Ираке и датируется 8700 годом до нашей эры. Факты свидетельствуют о том, что золото и метеоритное железо (но не плавленое железо) были единственными металлами, которые использовались людьми до меди. Считается, что история металлургии меди следует такой последовательности: сначала холодная обработка самородной меди, затем отжиг, плавка и, наконец, литье по выплавляемым моделям. В юго-восточной Анатолии все четыре этих метода появляются более или менее одновременно в начале неолита c. 7500 г. до н.э.
Выплавка меди была изобретена независимо в разных местах. Вероятно, оно было обнаружено в Китае до 2800 г. до н.э., в Центральной Америке около 600 г. н.э. и в Западной Африке около 9–10 века нашей эры. Литье по выплавляемым моделям было изобретено в 4500–4000 гг. До н.э. в Юго-Восточной Азии и <58 г.>углеродное датирование установило добычу на Олдерли Эдж в Чешире, Великобритания, в период с 2280 по 1890 год до н.э. Эци-Ледяной человек, мужчина, датируемый 3300 годом. до 3200 г. до н.э. был найден с топором с медной головкой чистотой 99,7%; высокие уровни мышьяка в его волосах предполагают участие в плавлении меди. Опыт работы с медью помог развитию других металлов; в частности, выплавка меди привела к открытию выплавки железа. Производство в Старом медном комплексе в Мичигане и Висконсине датируется периодом между 6000 и 3000 годами до нашей эры. Природная бронза, разновидность меди, сделанная из руд, богатых кремнием, мышьяком и (реже) оловом, стала широко использоваться на Балканах около 5500 г. до н.э.
Легирование меди с олово для изготовления бронзы впервые стало применяться примерно через 4000 лет после открытия плавки меди и примерно через 2000 лет после того, как «натуральная бронза» стала широко использоваться. Бронзовые артефакты культуры Винча датируются 4500 годом до нашей эры. Шумерские и египетские изделия из меди и бронзовых сплавов датируются 3000 годом до нашей эры. Бронзовый век начался в Юго-Восточной Европе около 3700–3300 гг. До н.э., в Северо-Западной Европе около 2500 г. до н.э. Он закончился началом железного века, 2000–1000 гг. До н.э. на Ближнем Востоке и 600 г. до н.э. в Северной Европе. Переход между неолитическим периодом и бронзовым веком ранее назывался энеолитическим периодом (медь-камень), когда медные орудия использовались с каменными. Этот термин постепенно потерял популярность, потому что в некоторых частях мира энеолит и неолит совпадают с обоих концов. Латунь, сплав меди и цинка, возникла гораздо позже. Он был известен грекам, но стал важным дополнением к бронзе во времена Римской Империи.
 В алхимии символ меди был также символом для богиня и планета Венера.
В алхимии символ меди был также символом для богиня и планета Венера. энеолитический медный рудник в долине Тимна, пустыня Негев, Израиль.
энеолитический медный рудник в долине Тимна, пустыня Негев, Израиль. В Греции медь была известна под названием халкос (χαλκός). Это был важный ресурс для римлян, греков и других древних народов. В римские времена он был известен как aes Cyprium, aes - общий латинский термин для обозначения медных сплавов и Cyprium с Кипра, где добывалось много меди. Фраза была упрощена до меди, отсюда и английская медь. Афродита (Венера в Риме) олицетворяла медь в мифологии и алхимии из-за ее блестящей красоты и древнего использования в производстве зеркал; Кипр был священным для богини. Семь небесных тел, известных древним, были связаны с семью металлами, известными в древности, а Венера была отнесена к меди.
Медь впервые использовалась в древней Британии примерно в III или II веке до нашей эры. В Северной Америке добыча меди началась с незначительных разработок коренных американцев. Известно, что самородная медь добывалась на участках Isle Royale с помощью примитивных каменных орудий между 800 и 1600 годами. Медная металлургия процветала в Южной Америке, особенно в Перу около 1000 года нашей эры. Были обнаружены медные погребальные украшения 15 века, но коммерческое производство металла началось только в начале 20 века.
Медь играет важную роль в культуре, особенно в денежном выражении. Romans in the 6th through 3rd centuries BC used copper lumps as money. At first, the copper itself was valued, but gradually the shape and look of the copper became more important. Julius Caesar had his own coins made from brass, while Octavianus Augustus Caesar 's coins were made from Cu-Pb-Sn alloys. With an estimated annual output of around 15,000 t, Roman copper mining and smelting activities reached a scale unsurpassed until the time of the Industrial Revolution ; the provinces most intensely mined were those of Hispania, Cyprus and in Central Europe.
The gates of the Temple of Jerusalem used Corinthian bronze treated with depletion gilding. The process was most prevalent in Alexandria, where alchemy is thought to have begun. In ancient India, copper was used in the holistic medical science Ayurveda for surgical instruments and other medical equipment. Ancient Egyptians (~2400 BC ) used copper for sterilizing wounds and drinking water, and later to treat headaches, burns, and itching.
 Copper Ornaments
Copper Ornaments Acid mine drainage affecting the stream running from the disused Parys Mountain copper mines
Acid mine drainage affecting the stream running from the disused Parys Mountain copper mines 18th century copper kettle from Norway made from Swedish copper
18th century copper kettle from Norway made from Swedish copperThe Great Copper Mountain was a mine in Falun, Sweden, that operated from the 10th century to 1992. It satisfied two-thirds of Europe's copper consumption in the 17th century and helped fund many of Sweden's wars during that time. It was referred to as the nation's treasury; Sweden had a copper backed currency.
Copper is used in roofing, currency, and for photographic technology known as the daguerreotype. Copper was used in Renaissance sculpture, and was used to construct the Statue of Liberty ; copper continues to be used in construction of various types. Copper plating and copper sh eathing широко использовались для защиты подводных корпусов кораблей - метод, впервые примененный британским адмиралтейством в 18 веке. Norddeutsche Affinerie в Гамбурге было первым современным гальваническим заводом, начавшим производство в 1876 году. Немецкий ученый Готфрид Осанн изобрел порошковую металлургию в 1830 г. при определении атомной массы металла; Примерно тогда же было обнаружено, что количество и тип легирующего элемента (например, олова) в медь влияют на тона звонка.
Во время роста спроса на медь в эпоху электричества, с 1880-х до Великой депрессии 1930-х годов, Соединенные Штаты производили от одной трети до половины мировой добычи меди. Основные районы включали район Кевинау на севере Мичигана, в основном месторождения самородной меди, который в конце 1880-х годов затмил обширные сульфидные месторождения Бьютта, Монтана, которые сами по себе были затмины порфировыми месторождениями Южного Запада США., особенно в Бингем-Каньон, Юта и Моренси, Аризона. Внедрение технологии открытой добычи с применением паровой лопаты и инновации в плавке, рафинировании, флотационном обогащении и других этапах обработки привело к массовому производству. В начале двадцатого века Аризона заняла первое место, за ней следовали Монтана, затем Юта и Мичиган.
Мгновенная плавка была разработана Outokumpu в Финляндии и впервые подала заявку в Harjavalta в 1949 году; на энергоэффективный процесс приходится 50% мирового производства первичной меди.
Межправительственный совет стран-экспортеров меди, образованный в 1967 году Чили, Перу, Заиром и Замбией, действовал в рынок меди, как ОПЕК в нефти, хотя он никогда не достиг такого же влияния, особенно потому, что второй по величине производитель, Соединенные Штаты, никогда не был членом; он был распущен в 1988 году.
 Медная арматура в ассортименте
Медная арматура в ассортименте Основными областями применения меди являются электрические провода (60%), кровля и водопровод (20%), а также промышленное оборудование (15%). Медь используется в основном как чистый металл, но когда требуется более высокая твердость, его добавляют в такие сплавы, как латунь и бронза (5% от общего использования). Более двух столетий медная краска использовалась на корпусах лодок, чтобы рост растений и моллюсков. Небольшая часть меди используется для пищевых добавок и фунгицидов в сельском хозяйстве. Механическая обработка меди возможна, хотя сплавы предпочтительны из-за хорошей обрабатываемости при создании сложных деталей.
Несмотря на конкуренцию со стороны других материалов, медь остается предпочтительным электрическим проводником почти во всех категориях электропроводки, кроме воздушных передача электроэнергии где алюминий часто является предпочтительным. Медный провод используется в производстве электроэнергии, передаче энергии, распределении энергии, телекоммуникациях, электронных схемах и бесчисленное количество типов электрического оборудования. Электропроводка - самый важный рынок для медной промышленности. Сюда входят структурная силовая проводка, силовой распределительный кабель, приборный провод, коммуникационный кабель, автомобильный провод и кабель, а также магнитный провод. Примерно половина добываемой меди используется для изготовления электрических проводов и кабельных жил. Многие устройства используют медную проводку из числа присущих ей свойств, таких как высокая электрическая проводимость, предел прочности, пластичность, ползучесть. (деформация) стойкость, коррозионная стойкость, низкое тепловое расширение, теплопроводность, простота пайки, пластичность и простота монтажа.
В течение короткого периода с конца 1960-х до конца 1970-х годов медная проводка была заменена алюминиевой проводкой во многих проектах жилищного строительства в Америке. Новая электропроводка была причастна к нескольким домашним пожарам, и промышленность вернулась к производству меди.
 Медные электрические шины, распределяющие мощность в большом здании
Медные электрические шины, распределяющие мощность в большом здании Интегрированные в схемах и печатных плат все используются чаще медь вместо алюминия из-за ее превосходной электропроводности; радиаторы и теплообменники используют медь из-за ее превосходных свойств рассеивания тепла. Электромагниты, электронные лампы, электронно-лучевые трубки и магнетроны в микроволновых печах использовать медь, как и волноводы для микроволнового излучения.
Превосходная проводимость повышает эффективность электрических двигателей. Это важно, поскольку на двигатели и моторные системы приходится 43–46% всего потребления электроэнергии и 69% всей электроэнергии, используемой в промышленности. Увеличение массы и поперечного сечения меди в катушке увеличивает КПД двигателя. Медные роторы электродвигателей, новая технология, разработанная для электродвигателей, где экономия энергии является первоочередной задачей при проектировании, позволяет универсальным асинхронным электродвигателям соответствует и превосходить показатели Национальные ассоциации электрооборудования 512>( NEMA) повышенная эффективность стандарты.
 Медная крыша на ратуше Миннеаполиса, покрытая патиной
Медная крыша на ратуше Миннеаполиса, покрытая патиной  Старая медь посуда в ресторане Иерусалима
Старая медь посуда в ресторане Иерусалима Медь использовалась с древних времен как прочный, атмосферный коррозионно-стойкий и атмосферный коррозионный материал. Крыши, кровли, водосточные желоба, водосточные трубы, купола, шпили, своды и двери сотни или несколько сотен лет делали из меди. тысячи лет. Архитектурное использование меди в наше время расширилось за счет включения внутренней и внешней облицовки стен, строительных компенсаторов, радиочастотного экранирования и антимикробного средства <512.>и предметы интерьера, такие как привлекательные поручни, сантехника и столешницы. Некоторые из других важных преимуществ использования как архитектурного материала включают низкое тепловое движение, легкий вес, молниезащиту и возможность вторичной переработки
Характерная естественная зеленая патина металла. уже давно пользуется популярностью у архитекторов и дизайнеров. Финальная патина представляет собой прочный слой, который обладает высокой устойчивостью к атмосферной коррозии, защищая тем самым металл от дальнейшего атмосферного воздействия. Это может быть смесь карбонатных и сульфатных соединений в различных количествах, в зависимости от условий окружающей среды, таких как серосодержащие кислотные дожди. Архитектурная медь и ее сплавы также могут быть «обработаны» для придания определенного внешнего вида, ощущений или цвета. Отделка включает механическую обработку поверхности, химическое окрашивание и нанесение покрытий.
Медь имеет превосходные свойства пайки и пайки и может сварена ; Наилучшие достигаются при дуговой сварке металлическим газом.
Медь биостатична, что означает, что бактерии и многие другие формы жизни не будут расти на ней. По этой причине он давно используется для защиты частей кораблей от ракушек и мидий. Первоначально она использовалась в чистом виде, но с тех пор была вытеснена металлической краской Muntz и краской на основе меди. Точно так же, как обсуждается в разделе медные сплавы в аквакультуре, медные сплавы стали важными сеточными материалами в отрасли аквакультуры, поскольку они антимикробны и предотвращают биообрастание, даже в экстремальных условиях и обладают сильными структурными и коррозионно-стойкими свойствами в морской среде.
сенсорные поверхности из медного сплава обладают естественными свойствами, уничтожают широкий спектр микроорганизмов (например, E. coli O157: H7, метициллин -резистентный Staphylococcus aureus (MRSA ), Staphylococcus, Clostridium difficile, вирус гриппа A, аденовирус и грибы ). Было доказано, что около 355 медных сплавов убивают более 99,9% болезнетворных бактерий всего за два часа при регулярной очистке. Агентство по охране окружающей среды США (EPA) одобрило регистрацию этих медных сплавов как «антимикробных материалов, полезных для здоровья населения»; это разрешение позволяет производителям предъявлять юридические претензии в отношении пользы для здоровья продуктов, изготовленных из зарегистрированных сплавов. Кроме того, EPA утвердило длинный список антимикробных изделий из меди, изготовленных из этих сплавов, таких как перила, поручни, прикроватные столики, раковины, смесители <512.>, дверные ручки, туалеты оборудование, компьютерные клавиатуры, клуб здоровья оборудование и ручки тележки (полный список см.: Антимикробные сенсорные поверхности из медного сплава # Одобренные продукты ). Медные дверные ручки используются в больницах для уменьшения распространения болезней, а болезнь легионеров подавляется медными трубками в водопроводных системах. Антимикробные изделия из медного сплава в настоящее время установлены в медицинских учреждениях Великобритании, Ирландии, Японии, Кореи, Франции, Дании и Бразилии, а также востребованы в США и системе транзита метро в Санго, Чили, где Поручни из медно-цинкового сплава установлены. примерно на 30 станциях в период с 2011 по 2014 год. Текстильные волокна можно смешивать с медью для создания противомикробных защитных тканей.
Медь может сообщить как спекулятивную помощь в связи с прогнозируемым использованием в производстве ветряных турбин, солнечных панелей и других возобновляемых источников энергии. Другой причиной прогнозируемого роста является тот факт, что электромобили содержат в среднем в 3,6 раза больше меди, чем обычные автомобили, хотя влияние электромобилей на спрос на медь обсуждается. Некоторые инвестируют в медь через акции горнодобывающих компаний, ETF и фьючерсы. Другие хранятся физическую медь в форме медных слитков или круглых изделий, хотя они, как правило, имеют более высокое разрешение за использование драгоценных металлов. Те, кто хочет избежать наценки на медь слиток, в качестве альтернативы хранят старую медную проволоку, медные трубки или американские гроши, сделанные до 1982 года.
Медь обычно используется в ювелирных изделиях, и через некоторые фольклорам, медные браслеты облегчают симптомы артрита. В одном исследовании остеоартрита и в одном исследовании ревматоидного артрита не было обнаружено различий между медным браслетом и контрольным браслетом (не из меди). Нет доказательств того, что медь может всасываться через кожу. Если бы это было так, это могло бы привести к отравлению медью.
В последнее время на рынке продается некоторая компрессионная одежда с медным переплетением с заявлениями о здоровье, аналогичными народным. претензии к медицине. Эта услуга может иметь преимущества, кроме эффекта плацебо.
Chromobacterium violaceum и Pseudomonas fluorescens может мобилизовать твердую медь в виде цианидного соединения. Эрикоидные микоризные грибы, связанные с Calluna, Erica и Vaccinium, могут расти на металлоносных почвах, содержащих медь. Эктомикоризный гриб Suillus luteus древние сосны от токсичности меди. Образец гриба Aspergillus niger был обнаружен растущим из раствора для добычи золота, и было обнаружено, что он содержит цианокомплексы таких металлов, как золото, серебро, медь, железо и цинк. Грибок также играет роль в солюбилизации сульфидов тяжелых металлов.
 Богатые источники включают устрицы, говяжью и ягненую печень, бразильские орехи, мелассу, какао и черный перец. Хорошие источники включают омаров, орехи и семена подсолнечника, зеленые оливки, авокадо и пшеничные отруби.
Богатые источники включают устрицы, говяжью и ягненую печень, бразильские орехи, мелассу, какао и черный перец. Хорошие источники включают омаров, орехи и семена подсолнечника, зеленые оливки, авокадо и пшеничные отруби. Медные белки играют разнообразную роль в биологическом переносе кислорода, в процессах, используемых в легком взаимном превращении Cu. (I) и Cu (II). Медь необходима для аэробного дыхания всех эукариот. В митохондриях он обнаружен в цитохром с оксидазе, который является последним белком в окислительном фосфорилировании. Цитохром с оксидаза представляет собой белок, который связывает O 21 2 928 между медью и железом; белок передает 8 электронов молекуле O 2, чтобы восстановить ее до двух молекул воды. Медь также во многих супероксиддисмутазах, белках, которые катализируют разложение супероксидов, превращая их (посредством диспропорционирования ) в кислород и пероксид водорода :
Белок гемоцианин является переносчиком кислорода у многих моллюсков и некоторых членистоногие, такие как подковообразный краб (Limulus polyphemus). Гемоцианин имеет синий цвет, эти организмы имеют голубую кровь, а не красную кровь железосодержащего гемоглобина. Структурно с гемоцианином связаны лакказы и тирозиназы. Вместо обратного связывания кислорода эти белки гидроксилируют субстраты, о чем свидетельствует их роль в образовании лаков. Биологическая роль меди началась с появления кислорода в атмосфере Земли. Некоторые белки меди, такие как «белки голубой меди», не взаимодействуют напрямую с субстратами; следовательно, они не ферменты. Эти белки передают электроны посредством процесса, называемого переносом электронов.
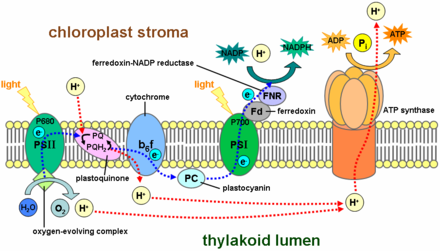 Функции фотосинтеза посредством сложной цепи переноса электронов внутри тилакоидной мембраны. Центральный звеном в этой цепи является пластоцианин, белок голубой меди.
Функции фотосинтеза посредством сложной цепи переноса электронов внутри тилакоидной мембраны. Центральный звеном в этой цепи является пластоцианин, белок голубой меди. Уникальный четырехъядерный центр меди был обнаружен в редуктазе закиси азота.
Химические соединения, которые были разработаны для лечения Болезнь Вильсона, исследована на предмет использования в терапии рака.
Медь является важным микроэлементом для растений и животных, но не для всех микроорганизмов. В человеческом организме медь содержится в количестве от 1,4 до 2,1 мг на кг массы тела.
Медь всасывается в кишечнике, транспортируется в печень, связанный с альбумин. После обработки в печени распределяется по другим тканям во второй фазе, в котором участвует несущий большую часть меди в крови церулоплазмин. Церулоплазмин также передает в себе медь, выделяется с молоком, и особенно хорошо усваивается как источник меди. Медь в организме обычно подвергается энтерогепатической циркуляции (около 5 мг в день по примерно 1 мг в день, абсорбируемой пищей и выводимой из организма), и организм может выделять излишки меди, при необходимости, через желчь, которая переносит часть меди из печени, которая не всасывается в кишечнике.
США Институт медицины (IOM) обновил расчетные средние потребности (EAR) и рекомендуемые диетические нормы (RDA) для меди в 2001 году. Если нет достаточной информации для использования EAR и RDA, обозначена как Адекватное потребление (AI) используется вместо этого. AI для меди составляет: 200 мкг меди для мужчин и женщин в возрасте 0–6 месяцев и 220 мкг меди для мужчин и женщин в возрасте 7–12 месяцев. Для полов РСНП составляет: 340 мкг меди для детей 1–3 лет, 440 мкг меди для детей 4–8 лет, 700 мкг меди для детей 9–13 лет, 890 мкг меди для детей 14–14 лет. 18 лет и 900 мкг меди для людей в возрасте 19 лет и старше. При беременности 1000 мкг. При кормлении грудью 1300 мкг. Что касается безопасности, IOM также устанавливает допустимые верхние уровни потребления (UL) для витаминов и минералов, когда доказательств достаточно. В случае меди верхний предел установлен на уровне 10 мг / день. В совокупности EAR, RDA, AI и UL называются рекомендуемыми диетическими потребностями.
. Европейское управление по безопасности пищевых продуктов (EFSA) именует совокупный набор информации как диетические справочные значения с учетом населения. Эталонное потребление (PRI) вместо RDA и среднее требование вместо EAR. AI и UL ориентированная так же, как в США. Для женщин и мужчин в возрасте 18 лет и старше ИА на уровне 1,3 и 1,6 мг / день соответственно. ИВ при беременности и кормлении грудью - 1,5 мг / сут. Для детей в возрасте от 1 до 17 лет ИА увеличиваются с 0,7 до 1,3 мг / день. Эти AI выше, чем RDA США. Европейское управление по безопасности пищевых продуктов рассмотрело тот же вопрос о безопасности и установило UL на уровне 5 мг / день, что составляет половину значения в США.
Для целей маркировки пищевых продуктов и пищевых добавок в США количество в порции выражается как процент от дневной нормы (% DV). Для целей маркировки меди 100% дневной нормы составляющей 2,0 мг, но по состоянию на 27 мая 2016 года она была пересмотрена до 0,9 мг, чтобы привести ее в соответствие с RDA. Соблюдение обновленных правил маркировки требовалось к 1 января 2020 года для производителей с годовым объемом продаж продуктов питания 10 миллионов долларов США и более и к 1 января 2021 года для производителей с годовым объемом продаж продуктов питания менее 10 миллионов долларов США. В течение первых шести месяцев после даты соответствия 1 января 2020 года FDA планирует сотрудничать с производителями, чтобы соответствовать новым требованиям к этикеткам Nutrition Facts, и не будет сосредоточиваться на принудительных мерах в отношении этих требований в течение этого времени. Таблица старых и новых суточных значений для взрослых приведена в разделе Референсное суточное потребление.
Из-за своей роли в облегчении усвоения железа дефицит меди может производить анемия -подобные симптомы, нейтропения, аномалии костей, гипопигментация, нарушение роста, повышенная частота инфекций, остеопороз, гипертиреоз и нарушения метаболизма глюкозы и холестерина. И наоборот, болезнь Вильсона вызывает накопление меди в тканях организма.
Тяжелый дефицит может быть обнаружен при тестировании на низкий уровень меди в плазме или сыворотке, низкий уровень церулоплазмина и низкий уровень супероксиддисмутазы красных кровяных телец; они не чувствительны к маргинальному статусу меди. «Активность цитохром-с-оксидазы лейкоцитов и тромбоцитов» была заявлена как еще один фактор дефицита, но результаты не были подтверждены репликацией.
Граммовые количества различных солей меди имеют были взяты в попытках самоубийства и вызвали острую токсичность меди у людей, возможно, из-за окислительно-восстановительного цикла и образования активных форм кислорода, которые повреждают ДНК. Соответствующие количества солей меди (30 мг / кг) токсичны для животных. Сообщалось, что минимальная диетическая ценность для здорового роста кроликов составляет не менее 3 ppm в рационе. Однако более высокие концентрации меди (100 ppm, 200 ppm или 500 ppm) в рационе кроликов могут благоприятно влиять на эффективность преобразования корма, скорость роста и процент разделки туш.
Хронический Токсичность меди обычно не возникает у людей из-за транспортных систем, регулирующих абсорбцию и выведение. Аутосомно-рецессивные мутации в транспортных белках меди могут вывести из строя эти системы, что приведет к болезни Вильсона с накоплением меди и циррозу печени у людей, унаследовавших два дефектных гена.
Повышенный уровень меди также был связан с ухудшением симптомов болезни Альцгеймера.
В США Управление по безопасности и гигиене труда (OSHA) определило допустимый предел воздействия (PEL) для медной пыли и дыма на рабочем месте как средневзвешенный по времени (TWA) 1 мг / м3. Национальный институт профессиональной безопасности и здоровья (NIOSH) установил Рекомендуемый предел воздействия (REL), равный 1 мг / м3, средневзвешенному по времени. Значение IDLH (непосредственно опасное для жизни и здоровья) составляет 100 мг / м.
Медь входит в состав табачного дыма. Табак легко поглощает и накапливает тяжелые металлы, такие как медь, из окружающей почвы в своих листьях. Они легко всасываются в тело пользователя после вдыхания дыма. Последствия для здоровья не ясны.
 |  |  |  |
| в чистой воде, кислотных или щелочных условиях. Медь в нейтральной воде благороднее водорода. | в воде, содержащей сульфид | в 10 М растворе аммиака | в растворе хлорида |
| Викицитатник содержит цитаты, связанные с: Медь |
| На Викискладе есть материалы, связанные с Медью. |
| Найдите медь в Викисловаре, бесплатном словаре. |
| Wikisource содержит исходный текст, относящийся к этой статье: Медь |