Плутоний является радиоактивным химическим элементом с символ Puи атомный номер 94. Это актинид металл серебристо-серого цвета, который тускнеет при контакте с воздухом и образует тусклое покрытие при окислении. Элемент обычно имеет шесть аллотропных и четыре степени окисления. Он реагирует с углеродом, галогенами, азотом, кремнием и водородом. Под воздействием влажного воздуха он образует оксиды и гидриды, которые могут расширять образец до 70% по объему, который, в свою очередь, отслаивается в виде порошка, который пирофорен. Он радиоактивен и может накапливаться в костях, что делает обращение с плутонием опасным.
Плутоний был впервые произведен и выделен 14 декабря 1940 года при бомбардировке дейтроном из урана-238 на 1,5-метровом (60 дюймов) циклотроне. в Калифорнийский университет в Беркли. Сначала был синтезирован нептуний-238 (период полураспада 2,1 дня), который имел бета-распад с образованием нового элемента с атомным номером 94 и атомным весом. 238 (период полураспада 88 лет). Времен уран был назван в честь планеты Уран и нептуний в честь планеты Нептун, элемент 94 был назван в честь Плутона, который в то время тоже считался планетой. Секретность военного времени не позволяла команде Калифорнийского университета опубликовать свое открытие до 1948 года.
Плутоний - элемент с самым высоким атомным номером, который встречается в природе. Следы количества образуются в месторождениях природного урана-238, когда уран-238 захватывает нейтроны, испускаемые при распаде других элементов урана-238. Плутоний чаще встречается на Земле с 1945 года как продукт захвата нейтронов и бета-распада, где некоторые из нейтронов высвобождаются в результате деления процесс преобразования ядер урана-238 в плутоний-239.
 Расчет количества с помощью функций Бейтмана для Pu
Расчет количества с помощью функций Бейтмана для Pu Количество изотопов в цепочках распада в определенный момент времени рассчитывается с помощью уравнения Бейтмана. И плутоний-239, и плутоний-241 являются делящимися, что означает, что они могут выдерживать ядерную цепную реакцию, что приводит к применение в ядерное оружие и ядерные реакторы. Плутоний-240 Высокая скорость спонтанного деления, повышенная нейтронный поток любого содержащего его образца. Присутствие плутония-240 ограничивает пригодность пробы плутония для оружия или его качество в реакторном топливе, процент плутония-240 определяет его сорт (оружейный, топливный, или реакторного качества). Плутоний-238 имеет период полураспада 87,7 лет и испускает альфа-частицы. Это источник тепла в радиоизотопных термоэлектрических генераторов, которые используются для питания некоторых космических аппаратов. Изотопы плутония дороги и их неудобно разделять, поэтому изотопы обычно производятся в заводе реакторах.
Производство плутония в полезных количествах впервые было основной частью Манхэттенского проекта во время Второй мировой войны, в ходе которого были разработаны первые атомные бомбы. Бомбы Толстяка, использованные в ядерных испытаниях Тринити в июле 1945 года и во время бомбардировки Нагасаки в августе 1945 года, содержали плутоний. сердечники. Эксперименты по облучению человека по изучению плутония проводились без информированного согласия, и после войны произошло несколько аварий с критичностью, некоторые соискательством исходом. Удаление плутониевых отходов с атомных электростанций и демонтированного ядерного оружия, построенного во время холодной войны, распространением ядерного оружия и забота об окружающей среде. Другими источниками плутония в окружающей среде являются выпадения в условиях наземных ядерных испытаний, в настоящее время запрещено.
Плутоний, как и большинства металлов, сначала имеет ярко-серебристый вид, как и никель, но он очень быстро окисляется до тускло-серого, хотя и желтого и также сообщается о оливково-серого. При комнатной температуре плутоний находится в своей α (альфа) форме. Это наиболее распространенная структурная форма элемента (аллотроп ), примерно такая же твердая и хрупкая, как серый чугун, если только он не легирован другими металлами для сделать его мягким и пластичным. В отличие от других металлов, он не является хорошим проводником тепла или электричества. Он имеет низкую точку плавления (640 ° C) и необычно высокую точку кипения (3228 ° C).
Альфа-распад, высвобождение высокоактивного вещества. энергия ядра гелия, наиболее распространенная форма радиоактивного распада плутония. Масса 5 кг Pu содержит около 12,5 × 10 атомов. При периоде полураспада 24 100 лет около 11,5 × 10 его атомы распадаются каждую секунду с испусканием альфа-частиц 5,157 МэВ. Это составляет 9,68 Вт мощности. Тепло, выделяющееся при замедлении этих альфа-частиц, делает его теплым на ощупь.
Удельное сопротивление - это мера того, насколько сильно материал противостоит потоку электрического тока. Удельное сопротивление плутония при комнатной температуре очень велико для металла. Эта тенденция продолжается до 100 K, ниже которой удельное сопротивление сокращается для свежих образцов. Повышение удельного сопротивления увеличивается со временем примерно при 20 К из-за радиационного повреждения со скоростью, определяемой изотопным составом образца.
Из-за самооблучения образец плутония претерпевает усталость по всей своей кристаллической структуре, это означает, что упорядоченное расположение его атома со временем нарушается излучением. Самооблучение также может привести к отжигу, который противодействует некоторым испытаниям при повышении температуры выше 100 К.
В отличие от материалов, плутоний увеличивает плотность при плавлении на 2,5%, но жидкий металл демонстрирует линейное уменьшение плотности с температурой. Вблизи точки плавления жидкий плутоний имеет очень высокую вязкость и поверхностное натяжение по сравнению с другими металлами.
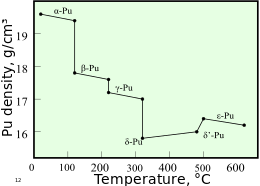 Плутоний имеет шесть аллотропов при атмосферном давлении: альфа (α), бета (β), гамма (γ), дельта (δ), простое дельта (δ '), эпсилон (ε)
Плутоний имеет шесть аллотропов при атмосферном давлении: альфа (α), бета (β), гамма (γ), дельта (δ), простое дельта (δ '), эпсилон (ε) Плутоний обычно имеет шесть аллотропов и образует седьмой (дзета, ζ) при высокой температуре в ограниченном диапазоне давлений. Эти аллотропы, которые имеют различные структурные модификации или элементы, имеют очень похожие внутренние энергии, но значительно различаются плотностями и кристаллическими структурами. Это делает плутоний очень чувствительным к изменению температуры, допускает резкие изменения объема после фазовых переходов из одной аллотропной формы в другую. Плотность различных аллотропов оценивается от 16,00 г / см до 19,86 г / см.
Присутствие этого множества аллотропов очень затрудняет механическую обработку плутония, так как он очень легко меняет состояние. Например, α-форма существует при температуре в нелегированном плутонии. Он имеет характеристики механической обработки, аналогичные чугуну, но при несколько более высоких температурах он переходит в пластичную и пластичную форму β (бета). Причины сложной фазовой диаграммы до конца не электрические. Форма α имеет низкосимметричную моноклинную потерю, отсюда ее хрупкость, прочность, сжимаемость и плохая теплопроводность.
Плутоний в форме δ (дельта) обычно существует в области от 310 ° C до 452 ° C, но он стабилен при комнатной температуре при легировании с небольшим процентным содержанием галлия, алюминия или церия, что улучшает обрабатываемость и позволяет быть сварным. Форма δ имеет более типичный металлический характер и примерно такая же прочная и пластичная, как алюминий. В оружии деления взрывные ударные волны, используется для сжатия плутониевого ядра, также вызовут переход от обычного плутония в δ-фазе к более плотной α-форме, значительно помогая достичь сверхкритичности. Ε-фаза, твердый аллотроп с самой высокой температурой, демонстрирует аномально высокую атомную самодиффузию по сравнению с другими элементами.
 Кольцо оружейного качества Электроочищенный плутоний с чистотой 99,96% достаточно для одной активной зоны бомбы. Кольцо весит 5,3 кг, это ок. 11 в диаметре, а его форма способствует безопасности по критичности.
Кольцо оружейного качества Электроочищенный плутоний с чистотой 99,96% достаточно для одной активной зоны бомбы. Кольцо весит 5,3 кг, это ок. 11 в диаметре, а его форма способствует безопасности по критичности.Плутоний - это радиоактивный актинид металл, изотоп, плутоний-239, является одним из трех первичных делящихся изотопов (два других - уран-233 и уран-235 ); плутоний-241 также очень делящийся. Чтобы считаться делящимся, атомное ядро изотопа должно быть способно разрушиться или делиться при ударе медленно движущимся нейтроном и высвободить достаточно дополнительных нейтронов для поддержания ядерная цепная реакция путем расщепления дополнительных ядер.
Чистый плутоний-239 может иметь коэффициент размножения (k eff) больше единицы, это означает, что если металл присутствует в достаточном количестве и имеет соответствующую геометрию (например, сфераного размера), он может образовывать критическую массу. Во время деления часть энергии связи ядра, которая удерживает ядро вместе, высвобождается в виде большого количества электромагнитной и кинетической энергии (большая часть последней быстро преобразуется в тепловую энергию). При делении килограмма плутония-239 может произойти взрыв, эквивалентный 21 000 тоннам в тротиловом эквиваленте (88000 ГДж ). Именно эта энергия делает плутоний-239 полезный в ядерном оружии и реакторах.
. Присутствие изотопа плутония-240 в образце ограничивает его потенциал ядерной бомбы. плутоний-240 имеет высокую скорость спонтанного деления (~ 440 делений в секунду на грамм - более 1000 нейтронов в секунду на грамм), что повышает фоновые уровни нейтронов и, таким образом, увеличивает риск преддонации. Плутоний идентифицируется как оружейный, топливный или реакторный на основе процентного содержания плутония-240, он содержит. Плутоний оружейного качества содержит менее 7% плутония-240. Топливный плутоний содержит от 7% до менее 19%, а плутоний-240 для энергетических реакторов содержит 19% или более плутония-240. Плутоний высшего качества с содержанием плутония-240 менее 4%, используется в США. Оружие ВМФ хранится в непосредственной близости от экипажей кораблей и подводных лодок из-за его более низкой радиоактивности. Изотоп плутоний-238 не делящийся, но может легко подвергаться ядерному делению с быстрыми нейтронами, а также альфа-распадом.
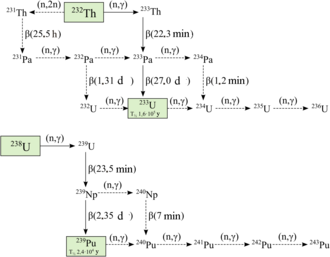 Уран-плутониевые и торий-урановые цепочки
Уран-плутониевые и торий-урановые цепочки Были охарактеризованы двадцать радиоактивных изотопов плутония. Самыми долгоживущими являются плутоний-244 с периодом полураспада 80,8 миллиона лет, плутоний-242 с периодом полураспада 373 300 лет и плутоний-239 с периодом полураспада 24 110 лет. Все радиоактивные изотопы имеют период полураспада менее 7000 лет. Этот элемент также имеет восемь метастабильных состояний, хотя все они имеют период полураспада менее одной секунды.
Известные изотопы плутония находятся в диапазоне массовое число от 228 до 247. Основные способы распада изотопов с массовыми числами ниже, чем у наиболее стабильного изотопа плутония-244, - это спонтанное деление и альфа-излучение, в основном с образованием урана (92 протонов ) и изотопы нептуния (93 протона) как продукты распада (без учета широкого круга дочерних ядер, образованных в процессе деления). Основной режим распада для изотопов с массовыми числами выше, чем плутоний-244, - это бета-излучение, в основном образование изотопов америция (95 протонов) в качестве продуктов распада. Плутоний-241 является родительским изотопом серии распада нептуния, распадаясь до америция-241 посредством бета-излучения.
Плутоний-238 и 239 синтезируются наиболее широко изотопы. Плутоний-239 синтезируется посредством следующей реакции с использованием урана (U) и нейтронов (n) посредством бета-распада (β) с нептунием (Np) в качестве промежуточного соединения:
![{\displaystyle {\ce {{^{238}_{92}U}+{^{1}_{0}n}->{^ {239} _ {92} U} ->[\ beta ^ {-} ] [23.5 \ {\ ce {min}}] {^ {239} _ {93} Np} ->[\ beta ^ {-}] [2.3565 \ {\ ce {d}}] {^ {239} _ {94} Pu}}}}]( https://wikimedia.org/api/rest_v1/media/math/render/svg/f9ba9e4744226a97ce8a41fd5b5e50b18cc259a9 )
Нейтроны от деления урана-235 захватываются ядрами урана-238 с образованием урана-239; бета-распад превращает нейтрон в протон с образованием нептуний-239 ( период полураспада 2,36 дня), а при другом бета-ра спаде образуется плутоний-239. Эгон Бретчер, работающий над британским проектом Tube Alloys, предсказал это s теоретически в 1940 году.
Плутоний-238 синтезируется путем бомбардировки урана-238 дейтронами (D, ядра тяжелого водорода ) в следующей реакции:
![{\displaystyle {\begin{aligned}{\ce {{^{238}_{92}U}+{^{2}_{1}D}->}} {\ ce {{^ {238} _ {93} Np} + 2_ {0} ^ {1} n}} \\ {\ ce {^ {238} _ {93} Np ->[\ beta ^ {-}] [2.117 \ {\ ce {d}}] {^ {238} _ {94} Pu}}} \ end { align}}}]( https://wikimedia.org/api/rest_v1/media/math/render/svg/1b584c932e52212178b2befe7a512a7b28f87d35 )
В этом процесс уран попадает в -238 производит два нейтрона и нептуний-238, который самопроизвольно распадается, испуская отрицательные бета-частицы с образованием плутония-238.
Изотопы плутония подвергаются воздействию Активный распад, который производит остаточное тепло. Различные изотопы выделяют разное количество энергии на массу. Теплота распада обычно указывается в ватт / килограмм или милливатт / грамм. В больших кусках плутония (например, например, яма) и при недостаточном отводе тепла результирующий самонагревание может быть значительным.
| Изотоп | Режим распада | Период полураспада (лет) | Теплота распада (Вт / кг) | Самопроизвольное деление нейтронов (1 / (г · С)) | Комментарий от |
|---|---|---|---|---|---|
| Pu | альфа до U | 87,74 | 560 | 2600 | Очень высокая теплота распада. Даже в небольших количествах может вызвать значительное самонагревание. Самостоятельно используется в радиоизотопных термоэлектрических генераторов от. |
| Pu | альфа до U | 24100 | 1,9 | 0,022 | Основной инструмент делящийся изотоп. От |
| Pu | альфа до U, спонтанное деление | 6560 | 6,8 | 910 | Основной примесь в образцах Pu изотоп. Содержание плутония обычно указывается в процентах от Pu. Высокая степень самопроизвольного деления препятствует использованию ядерного оружия. |
| Pu | бета-минус, до Am | 14,4 | 4,2 | 0,049 | Распадается на америций-241; его накопление представляет радиационную опасность в старых образцах. |
| Pu | альфа до U | 376000 | 0,1 | 1700 |
 Различные степени окисления плутония в растворе
Различные степени окисления плутония в растворе При комнатной температуре чистый плутоний серебристый по цвету, но при окислении тускнеет. Элемент отображает четыре ионных степени окисления в водном растворе и одно редкое:
Цвет, показываемый растворами плутония, зависит от степени окисления, так и от природы кислотного аниона.. Именно кислотный анион влияет на степень комплексообразования - как атомы соединяются с центральным атомом - разновидностями плутония. Кроме того, формальная степень окисления плутония +2 известна в комплексе [K (2.2.2-криптанд)] [PuCp ″ 3 ], Cp ″ = C 5H3(SiMe 3)2.
металлический плутоний получает реакцию тетрафторида плутония с барием, кальцием или литием при 1200 ° C.Он подвергается воздействию кислот , кислород и пар, но не щелочами и легко растворяется в концентрированной соляной, иодоводородной и хлорной кислотах. При 135 ° C металл воспламеняется на воздухе и взрывается, если его помещается в четыреххлористый углерод.
 Плутоний <, хранится в инертной атмосфере, чтобы избежать реакции с воздухом. 444>пирофорность при определенных условиях может привести к тому, что он будет выглядеть как тлеющий тлеющий уголь.
Плутоний <, хранится в инертной атмосфере, чтобы избежать реакции с воздухом. 444>пирофорность при определенных условиях может привести к тому, что он будет выглядеть как тлеющий тлеющий уголь. 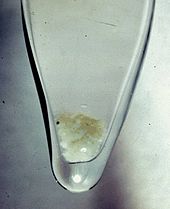 Двадцать микрограммов чистого гидроксида плутония
Двадцать микрограммов чистого гидроксида плутония Плутоний - химически активный металл. Или влажный аргон, металл быстр о окисляется, образует смесь оксидов и гидридов. Если металл подвергается достаточно продолжительному воздействию ограниченного количества водяного пара, образует порошкообразное поверхностное покрытие из PuO 2. Также образует гидрид плутония, но при избытке водяного пара образует только PuO 2.
Плутоний демонстрирует огромные и обратимые скорости реакции с чистым водородом, образуя гидрид плутония. Он также легко реагирует с кислородом, образует PuO и PuO 2, а также промежуточные оксиды; Оксид плутония заполняет на 40% больше объема, чем металлический плутоний. Металл реагирует с галогенами, давая соединения с общей формулой PuX 3, где X может быть F, Cl, Br или I и PuF <100.>4 тоже видно. Наблюдаются следующие оксигалогениды: PuOCl, PuOBr и PuOI. Он будет реагировать с углеродом с образованием PuC, азотом с образованием PuN и кремнием с образованием PuSi 2.
Порошки плутония, его гидридов и некоторых оксидов, таких как Pu 2O3, пирофорны Это означает, что они могут самовоспламеняться при температуре окружающей среды, поэтому с ними обращаются в инертной атмосфере азота или аргона. Объемный плутоний воспламеняется только при нагревании выше 400 ° C. Pu 2O3самопроизвольно нагревается и превращается в PuO 2, который устойчиво в сухом воздухе, но реагирует с водяным паром при нагревании.
Тигли, используемые для содержания плутония, должны иметь возможность выдерживать его сильно уменьшающие свойства. тугоплавкие металлы, такие как тантал и вольфрам, а также более стабильные оксиды, бориды, карбиды, нитриды и силициды могут терпеть это. Плавка в дуговой электропечи может быть предложено для производства небольших слитков металла без необходимости в тигле.
Церий используется в качестве химического имитатора плутония для разработки защитной оболочки, извлечения и другие технологии.
Плутоний - это элемент, в котором 5f-электроны являются переходной границей между делокализованными и локализованными; поэтому он считается одним из самых сложных элементов. Аномальное поведение плутония вызвано его электронной структурой. Разница в энергии между подоболочками 6d и 5f очень мала. Размер оболочки 5f достаточен как раз для того, чтобы электроны образовывали связи внутри решетки, на максимальной границе между локализованным и связывающим поведением. Близость энергетических уровней приводит к множеству низкоэнергетических электронных конфигураций с почти равными энергетическими уровнями. Это сравнивает к конкурирующим конфигурациям 5f7s и 5f6d7s, что усложняет его химическое поведение. Высоконаправленная природа 5f-орбиталей отвечает за ковалентные связи в молекулах и комплексах плутония.
Плутоний может образовывать сплавы и промежуточные соединения с большинством других металлов. Исключения включают литий, натрий, калий <4646>, рубидий и цезий из щелочных металлов ; и магний, кальций, стронций и барий щелочноземельных металлов ; и европий и иттербий из редкоземельных металлов. Частичные исключения включают тугоплавкие металлы хром, молибден, ниобий, тантал и вольфрам, которые растворимы в жидком плутонии, но нерастворимы или слабо растворимы в твердом плутоний. Галлий, алюминий, америций, скандий и церий могут стабилизировать δ-фазу плутония при комнатной температуре. Кремний, индий, цинк и цирконий допускают образование метастабильного δ-состояния при быстром охлаждении. Высокие количества гафния, гольмия и таллия также позволяют некоторое удерживание δ-фазы при комнатной температуре. Нептуний - единственный элемент, который может стабилизировать α-фазу при более высоких температурах.
Сплавы плутония могут быть получены путем добавления металла к расплавленному плутонию. Если легирующий металл является достаточно восстановительным, плутоний может быть добавлен в форме оксидов или галогенидов. Сплавы плутоний-галлий с δ-фазой и плутоний-алюминиевые сплавы производятся путем добавления фторида плутония (III) к расплавленному галлию или алюминию, что позволяет избежать прямого контакта с высокореакционным плутонием.
 Образец металлической плутония, выставленный в музее Questacon
Образец металлической плутония, выставленный в музее Questacon Следы плутония-238, плутония-239, плутония-240 и плутония-244 можно найти в природе. Небольшие следы плутония-239, несколько частей на триллион, и продукты его распада естественным образом появляются в некоторых концентрированных рудах урана, таких как естественный ядерный реактор деления в Окло, Габон. Отношение плутония-239 к урану на урановом месторождении Шахта Сигар Лейк колеблется от 2,4 × 10 до 44 × 10. Эти следовые количества возникают следующим образом: в редких случаях U подвергается спонтанному делению, и при этом ядро Испускает один или два свободных нейтрона с некоторой некоторой энергией. Когда один из этих нейтронов ударяется о ядро другого атома U, он поглощается атомом, который становится U. При относительно коротком периоде полураспада U распадается до Np, который распадается на Pu. Наконец, в образцах природного урана были обнаружены очень небольшие количества плутония-238, очень редким двойным бета-распадом урана-238.
Из-за его относительно длинной половинной длины. продолжительность жизни около 80 миллионов лет, было высказано предположение, что плутоний-244 встречается в природе как первичный нуклид, но ранние сообщения о его обнаружении не могли быть подтверждены. Однако его длительный период полураспада обеспечил его циркуляцию по Солнечной системе до его исчезновения, и действительно, доказательства спонтанного деления потухшего Пу были обнаружены в метеоритах. Прежнее присутствие Pu в ранней Солнечной системе было подтверждено, поскольку сегодня он проявляется в избытке его дочерних элементов, либо Th (из пути альфа-распада), либо изотопов ксенона (из его спонтанного деления ). Последние, как правило, более полезны, потому что химический состав тория и плутония довольно схож (оба являются преимущественно четырехвалентными), и, следовательно, избыток тория не может быть убедительным доказательством того, что часть его образовалась в виде дочернего плутония. -жизнь всех трансурановых нуклидов и производится только в r-процессе в сверхновых и сталкивающихся нейтронных звездах ; когда ядра выбрасываются из этих событий с высокой скоростью, чтобы достичь Земли, только Pu среди трансурановых нуклидов имеет достаточно длительный период полураспада, чтобы пережить путешествие, и, следовательно, крошечные следы живого межзвездного Pu были обнаружены на глубоком морском дне. Поскольку Pu также присутствует в цепочке распада Pu, поэтому он также должен присутствовать в вековом равновесии, хотя и в еще меньших количествах.
Минутные следы плутония - это обычно обнаруживается в человеческом теле в результате проведенных 550 атмосферных и подводных ядерных испытаний, а также небольшого числа крупных ядерных аварий. Большинство атмосферных и подводных ядерных испытаний было остановлено Договором об ограниченном запрещении ядерных испытаний в 1963 году, который был подписан и ратифицирован США, Соединенным Королевством, Советским Союзом и другими странами.. Продолжающиеся испытания ядерного оружия в атмосфере с 1963 года странами, не являющимися участниками договора, включая испытания Китая (испытание атомной бомбы над пустыней Гоби в 1964 году, водородная бомба испытание в 1967 г. и последующие испытания) и во Франции (испытания проводились совсем недавно, в 1990-х годах). Поскольку плутоний-239 преднамеренно производится для ядерного оружия и ядерных реакторов, он является наиболее распространенным изотопом плутония.
Энрико Ферми и его команда ученых из Римского университета сообщили, что они открыли элемент 94 в 1934 году. Ферми назвал элемент гесперием и упомянул его в своей Нобелевской лекции в 1938 году. На самом деле образец представлял собой смесь бария, криптона и других элементов, но в то время об этом не было известно. Ядерное деление было открыто в 1938 году Отто Ганом и Фрицем Штрассманном. Затем Лиз Мейтнер и Отто Фриш.
 Гленн Т. Сиборг и его команда в Беркли теоретически объяснили механизм деления.
Гленн Т. Сиборг и его команда в Беркли теоретически объяснили механизм деления. Плутоний (в частности, плутоний-238) был впервые произведен, выделен и затем химически идентифицирован в период с декабря 1940 по февраль 1941 года Гленном Т. Сиборгом, Эдвином Макмилланом, Эмилио Сегре, Джозеф В. Кеннеди и Артур Уол путем бомбардировки урана дейтронами в 60-дюймовом (150 см) циклотроне в радиационной лаборатории Беркли в Калифорнийском университете в Беркли. Нептуний-238 был создан непосредственно в результате бомбардировки, но распался в результате бета-излучения с периодом полураспада немногим более двух дней, что указывает на образование элемент 94.
Документ, документирующий открытие, был подготовлен командой и отправлен в журнал Physical Review в марте 1941 года, но публикация была отложена до года после окончания Второй мировой войны из соображений безопасности. В Кавендишской лаборатории в Кембридже Эгон Бретчер и Норман Фезер осознал, что реактор на медленных нейтронах, работающий на урановом топливе, теоретически может иметь большое количество плутония-239 в как побочный продукт. Они подсчитали, что элемент 94 будет делящимся и имеет дополнительное преимущество в том, что он химически отличается от урана.
Макмиллан недавно назвал первый трансурановый элемент нептунием в честь планеты Нептун, и использует назвать элемент 94, являющийся следующим элементом в ряду, в честь того, что тогда считалось следующей планетой, Плутон. Николас Кеммер из Кембриджской команды независимо предложили то же название, что и команда Беркли. Первоначально Сиборгал название «плутоний», но позже подумал, что оно считается не так хорошо, как «плутоний». Он выбрал буквы «Пу» в качестве шутки, имея в виду междометие «P U», чтобы указать на особенно отвратительный запах, который незаметно перешел в таблицу Менделеева. Альтернативные названия, рассмотренные Сиборгом и другими были "ultimium" или "extremium" из-за ошибочного убеждения, что они нашли последний возможный элемент в периодической таблице.
 карликовая планета Плутон, в честь которого назван плутоний
карликовая планета Плутон, в честь которого назван плутоний После нескольких месяцев начальных исследований было обнаружено, что химический состав плутония похож на уран. Ранние исследования были продолжены в секретной Металлургической лаборатории Чикагского университета. 20 августа 1942 г. было выделено и измерено следовое количество этого элемента. Было произведено около 50 микрограмм плутония-239 в сочетании с ураном и продуктами деления, и только около 1 микрограмма было выделено. Эта процедура позволила химикам определить атомный вес нового элемента. 2 декабря 1942 года на площадке для игры в ракетки под западной трибуной в Стэг-Филд Чикагского университета исследователи во главе с Энрико Ферми достигли первой самоподдерживающейся цепной реакции в куче графита и урана, известной как СР-1. Используя теоретическую, полученную при эксплуатации CP-1, DuPont построила экспериментальный производственный реактор с воздушным охлаждением, известный как X-10, и пилотную установку химического разделения информации в Ок-Ридже. Установка для использования с использованием методов, разработанных Гленном Т. Сиборгом и группа исследователей из Met Lab, удалила плутоний из урана, облученного в реакторе X-10. Информация с CP-1 была также полезна для ученых Met Lab, проектирующих водоохлаждаемые реакторы для производства плутония для Хэнфорда. Строительство на площадке началось в середине 1943 года.
В ноябре 1943 года было уменьшено трифторида плутония, чтобы создать первый образец металлической плутонии: несколько микрограммов металлических шариков. Было произведено достаточно плутония, чтобы сделать его первым синтетическим глазом.
Были также изучены ядерные свойства плутония-239; исследователи обнаружили, что когда в него попадает нейтрон, он распадается (делится), высвобождая больше нейтронов и энергии. Эти нейтроны могут поражать другие атомы плутония-239 и т.д. в результате экспоненциально быстрой цепной реакции. Это может привести к взрыву, чтобы разрушить город, если изотопа будет сконцентрировано достаточно для образования критической массы.
. На ранних этапах исследования животных использовали для изучения воздействия радиоактивных веществ на здоровье. Эти исследования начались в 1944 году в Радиационной лаборатории Калифорнийского университета в Беркли и проводились Джозефом Г. Гамильтоном. Гамильтон хотел ответить на вопросы о том, как плутоний будет формироваться в зависимости от режима (воздействия пероральный прием, вдыхание, абсорбция через кожу), степени удерживания и того, как плутоний будет фиксироваться в тканях и распределяться между различными различными. Гамильтон начал вводить крысам растворимые порции плутония-239 в дозах микрограмм, используя различные валентные состояния и различные методы введения плутония (перорально, внутривенно и т. Д.). В конце концов, лаборатория в Чикаго также провела собственные эксперименты с использованием инъекций плутония с использованием различных животных, таких как мыши, кролики, рыбы и даже собаки. Результаты в Беркли и Чикаго исследований показали, что физиологическое поведение плутония значительно отличается от поведения радия. Наиболее тревожным результатом было то, что в печени и в «активно метаболизирующейся» части кости произошло значительное отложение плутония. Более того, скорость выведения плутония с экскрементами различалась между видами животных в пять раз. Из-за такого разброса было очень сложно оценить, какой будет процент для людей.
Во время Второй мировой войны правительство США учредило Манхэттенский проект, которому было поручено разработать атомную бомбу. Тремя воздействующими исследовательскими и производственными объектами проекта были установка по производству плутония на территории, которая сейчас называется Хэнфордская площадка, и объекты по обогащению урана в Ок-Ридж, Теннесси, и лаборатория исследования и разработки оружия, ныне известная как Лос-Аламосская национальная лаборатория.
 Строящийся реактор Хэнфорд B - первый реактор для производства плутония
Строящийся реактор Хэнфорд B - первый реактор для производства плутония  The Хэнфорд Площадка представляет две трети объема высокоактивных радиоактивных отходов страны. Ядерные реакторы выстроились вдоль берега реки на участке Хэнфорд вдоль реки Колумбия в январе 1960 года.
The Хэнфорд Площадка представляет две трети объема высокоактивных радиоактивных отходов страны. Ядерные реакторы выстроились вдоль берега реки на участке Хэнфорд вдоль реки Колумбия в январе 1960 года. Первым промышленным реактором, производившим плутоний-239, был Графитовый реактор X-10. Он был введен в эксплуатацию в 1943 году и был построен на предприятии в Ок-Ридже, которое позже стало Национальной лабораторией Ок-Ридж.
. В 1944 году рабочие заложили фундамент для первого химического разделения T Plant, расположение в 200-Запад.. К октябрю были завершены строительство завода T и его дочернего предприятия в 200-West, U Plant. (Завод U использовался только для обучения во время Манхэттенского проекта.) Разделительное здание в 200-Ист, завод B было завершено в феврале 1945 года. Второй объект, запланированный на 200-Востока, был отменен. Строиванные их рабочие, прозванные королевой Марис, представляющие собой потрясающие сооружения, похожие на каньон, длиной 800 футов, шириной 65 футов и высотой 80 футов, в которых находилось сорок технологических бассейнов. Внутреннее пространство выглядело жутковато, поскольку операторы за семифутовым бетонным экраном управляли оборудованием дистанционного управления, просматривая телевизионные мониторы и перископы из верхней галереи. Даже с массивными бетонными крышками технологических бассейнов, меры предосторожности против радиационного облучения необходимы и повлияли на все аспекты конструкции завода.
5 апреля 1944 года Эмилио Сегре в Лос-Аламосе получил первый образец плутония, произведенного в реакторе из Ок-Риджа. В течение десяти дней он обнаружил, что плутоний, полученный в реакторе, имеет более высокую оценку изотопа плутония-240, чем плутоний, произведенный на циклотроне. Плутоний-240 обеспечивает высокий фоновый уровень нейтронов в образце плутония. Первоначальное плутониевое оружие пушечного типа под кодовым названием «Тонкий человек » пришлось отказаться в результате увеличенного количества спонтанных нейтронов означало, что предварительная ядерная детонация (шипение ) было вероятно.
Все усилия по разработке плутониевого оружия в Лос-Аламосе вскоре были заменены на более сложное взрывное устройство под кодовым названием «Толстяк ». В имплозивном оружии плутоний сжимается до высокой плотности с помощью взрывных линз - технически более сложная задача, чем простая конструкция пушечного типа, но необходима для использования плутония в оружейных целях. Обогащенный уран, напротив, можно использовать любым методом.
Строительство реактора Хэнфорд B, первый ядерный реактор промышленного размера для материалов Производство было завершено в марте 1945 года. Реактор B производил делящийся материал для плутониевого оружия, использовавшегося во время Второй мировой войны. B, D и F были построены дополнительными реакторами, построенными в Хэнфорде, и шесть дополнительных реакторов для производства плутония были построены на этом объекте.
К января 1945 года высокоочищенный плутоний подвергся воздействию продолжения в завершенном здании изоляции, где удалены оставшиеся загрязнения. Лос-Аламос получил свой первый плутоний из Хэнфорда 2 февраля. Хотя до конца войны еще не было достаточно плутония для использования в бомбах, Хэнфорд к началу 1945 года уже был в эксплуатации. Прошло всего два года с тех пор, как полковник Франклин Матиас впервые основал свой временный штаб на берегу реки Колумбия.
Согласно Кейт Браун, производство плутония заводы в Хэнфорде и Маяк в России за четыре десятилетия "оба выбросили в среду более 200 миллионов кюри радиоактивных изотопов - вдвое больше, Большая часть этого радиоактивного загрязнения на протяжении многих лет являлась нормальным функционированием, но непредвиденные аварии действительно происходили, и руководство завода держало этот секрет, чем было выброшено во время Чернобыльской катастрофы в каждом случае ». В секрете, поскольку загрязнение продолжалось.
В 2004 году был найден сейф, обнаруженный при раскопках могильной траншеи на ядерном полигоне Хэнфорд. жидкостью, которая была идентифицирована как старый из известных образцов оружейного плутония. Изотопный анализ, проведенный Тихоокеанской северо-американской национальной лаборатории. ей, показал, что плутоний в баллоне был произведен в графитовом реакторе X-10 в Ок-Ридже в 1944 году.
 Из-за присутствия плутония-240 в плутонии, полученном в реакторе, была конструкция имплозии для оружия «Толстяк » и «Тринити »
Из-за присутствия плутония-240 в плутонии, полученном в реакторе, была конструкция имплозии для оружия «Толстяк » и «Тринити »Первое испытание атомной бомбы, под кодовым названием « Тринити » и взорвавшийся 16 июля 1945 года около Аламогордо, Нью-Мексико, в качестве делящего материала использовался плутоний. В конструкции имплозии «устройство », как было кодовое название устройства Trinity, использовались обычные взрывные линзы для сжатия сферы плутония до сверхкритической массы, которая одновременно была осыпана нейтронами из «Urchin», инициатор, сделанная из полония и бериллия (источник нейтронов : (α, n) реакция ). Вместе это обеспечило безудержную цепную реакцию и взрыв. Общее оружие весило более 4 тонны, хотя в его ядре использовалось всего 6,2 кг плутония. Около 20% плутония, использованного в оружии Тринити, подверглось делению, что произошло к взрыву с энергией, эквивалентной примерно 20 000 тонн в тротиловом эквиваленте.
Такая же конструкция была в атомной бомбе «Толстяк», сброшенной на Нагасаки, Япония, 9 августа 1945 года, в результате чего погибло 35 000–40 000 человек и было уничтожено 68–80% военной продукции в Нагасаки. Только после объявления о первых атомных бомбах существование и название плутония стало известно общественности в отчете Смита.
Большие запасы из Манхэттенского проекта. оружейный плутоний производился как Советским Союзом, так и Соединенными Штатами во время холодной войны. Реакторы США в Хэнфорде и Саванна-Ривер в Южной Каролине произвели 103 тонны, а в СССР было произведено примерно 170 тонн плутония военного назначения. Каждый год около 20 тонн этого элемента все еще как производится продукт ядерной энергетики. В хранилище может находиться до 1000 тонн плутония, более 200 тонн которого находится внутри или извлечено из ядерного оружия. СИПРИ оценивает мировые запасы плутония в 2007 году примерно в 500 тонн.
Радиоактивное загрязнение на заводе в Скалистых Флэтсах в первую очередь было вызвано двумя крупными пожарами плутония в 1957 и 1969 годах. Значительно более низкие уровни радиоактивных изотопов были выброшены на всей территории срока службы станции с 1952 по 1992 год. Преобладающие ветры с завода разносили воздушное загрязнение на юг и восток, населенные районы к северо-западу от Денвера. О загрязнении района Денвера плутонием от пожаров и других источников не сообщалось публично до 1970-х годов. Согласно исследованию 1972 года, проведенному в соавторстве с Эдвардом Мартеллом, «В более густонаселенных районах Денвера уровень загрязнения плутонием в поверхностных почвах в нескольких размах радиоактивные осадки», загрязнение плутонием «к востоку от Скалистых равнин в заводе в сотни раз больше, чем от ядерных испытаний ». Как отмечает Карл Джонсон в статье Амбио, «облучение большой части населения в районе Денвера плутонием и другими радионуклидами в выхлопных газах завода датируется 1953 годом». Производство оружия на заводе в Роки-Флэтс было остановлено после объединенного рейда ФБР и EPA в 1989 году и нескольких лет протестов. С тех пор завод был остановлен, а его здания снесены и полностью удалены с площадки.
В США часть плутония, извлеченного из демонтированного ядерного оружия, переплавляют образование стеклянных бревен из оксида плутония, которые весят две тонны. Стекло изготовлено из боросиликатов, смешанных с кадмием и гадолинием. Планируется, что эти бревна будут заключены в корпус из нержавеющей стали и будут храниться на глубине 4 км (2 мили) под землей в буровых скважинах, которые будут засыпаны бетоном. США планировали таким образом хранить плутоний в хранилище ядерных отходов Юкка-Маунтин, которое находится примерно в 100 милях (160 км) к северо-востоку от Лас-Вегаса, Невада.
5 марта, 2009 г., министр энергетики Стивен Чу заявил на слушаниях в Сенате, что «участок Юкка-Маунтин больше не рассматривался как вариант для хранения отходов реактора». Начиная с 1999 г. ядерные отходы военного происхождения захоронены на экспериментальной установке по изоляции отходов в Нью-Мексико.
Президентским меморандумом от 29 января 2010 года президент Обама учредил Комиссию голубой ленты по ядерному будущему Америки. В заключительном отчете Комиссия выдвинула рекомендации по одной разработке всеобъемлющей стратегии, которую необходимо реализовать, в том числе:
Во время и после окончания Второй мировой войны ученые, работающие над Манхэттенским проектом и другими исследовательскими проектами в области ядерного оружия провели исследования воздействия плутония на лабораторных животных и людей. Исследования на животных показали, что несколько миллиграммов плутония на килограмм ткани являются смертельной дозой.
В случае с людьми, это включало инъекции ожидаемых растворов, (обычно) пять микрограммов плутония, больничным пациентом, которые считались неизлечимо больным или иметь продолжительность жизни менее десяти лет из-за возраста или хронических заболеваний. Это количество уменьшено до одного микрограмма в июле 1945 года после того, как исследования на животных показали, что плутоний распределяется по костям более опасно, чем радий. Эйлин Уэлсом говорит, что большинством субъектов были бедными, бессильными и больными.
С 1945 по 1947 год восемнадцати испытуемым вводили плутоний без информированного согласия. Испытания используются для создания диагностических инструментов для определения способности плутония с целью разработки стандартов безопасности при работе с плутонием. Эбб Кейд неохотно участвовал в медицинских экспериментах, включающих инъекцию 4,7 мкг Плутоний 10 апреля 1945 г., Ок-Ридж, Теннесси. Этот эксперимент проводился под наблюдением Гарольда Ходжа. Другие эксперименты, проводившиеся под руководством Комиссии по атомной энергии США и Манхэттенского проекта, продолжались до 1970-х годов. «Плутониевые файлы» ведет хронику жизни участников секретной программы, называя каждого участника и обсуждая этические и медицинские исследования, тайно проводимые учеными и врачами. В настоящее время этот эпизод считается серьезным нарушением медицинской этики и Клятвы Гиппократа.
Правительство скрыло большую часть этих радиационных неудач до 1993 года, когда президент Билл Клинтон приказал изменить политику, и федеральные агентства затем предоставили соответствующие записи. Получившееся в результате расследование было предпринято президентским Консультативным комитетом по радиационным экспериментам при президенте, и оно выявило большую часть материала об исследованиях плутония на людях. Комитет опубликовал неоднозначный отчет 1995 года, в котором говорилось, что «были совершены злодеяния», но не осуждал тех, кто их совершил.
 атомная бомба, сброшенная на В Нагасаки, Япония, в 1945 г. было плутониевое ядро.
атомная бомба, сброшенная на В Нагасаки, Япония, в 1945 г. было плутониевое ядро. Изотоп плутоний-239 является ключевым делящимся компонентом ядерного оружия из-за легкости деления и доступности. Заключение плутониевой ямы бомбы в тампер (необязательный слой плотного материала) уменьшает количество плутония, необходимое для достижения критической массы, за счет отражения на выходе нейтроны обратно в плутониевую активную зону. Это уменьшает количество плутония, необходимое для достижения критичности, с 16 кг до 10 кг, что представляет собой сферу диаметром около 10 сантиметров (4 дюйма). Эта критическая масса составляет примерно треть от критической массы урана-235.
Плутониевые бомбы Fat Man использовали взрывное сжатие плутония для получения значительно более высоких плотностей, чем обычно, в сочетании с центральным источником нейтронов для начала реакции и увеличения эффективность. Таким образом, для получения взрывной мощности, эквивалентной 20 килотоннам в тротиловом эквиваленте, требовалось всего 6,2 кг плутония. Гипотетически всего 4 кг плутония - а может быть и меньше - можно было бы использовать для изготовления одной атомной бомбы с использованием очень сложных конструкций.
Отработанное ядерное топливо от нормального легководные реакторы содержат плутоний, но он представляет собой смесь плутония-242, 240, 239 и 238. Смесь недостаточно обогащена для эффективного ядерного оружия, но может быть использована один раз. как МОКС-топливо. Случайный захват нейтронов приводит к увеличению количества плутония-242 и 240 каждый раз, когда плутоний облучается в реакторе низкоскоростными "тепловыми" нейтронами, так что после второго цикла плутоний может потребляться только быстрыми нейтронные реакторы. Если реакторы на быстрых нейтронах недоступны (нормальный случай), избыток плутония обычно выбрасывается и образует один из самых долгоживущих компонентов ядерных отходов. Желание потреблять этот плутоний и другое трансурановое топливо и снизить радиотоксичность отходов - обычная причина, по которой инженеры-ядерщики создают реакторы на быстрых нейтронах.
Самый распространенный химический процесс, PUREX (Экстракция плутония и урана) перерабатывает отработанное ядерное топливо для извлечения плутония и урана, которые могут быть использованы для образования смешанного оксидного топлива (МОКС) для повторного использования в ядерных реакторах. В топливную смесь можно добавлять оружейный плутоний. МОКС-топливо используется в легководных реакторах и состоит из 60 кг плутония на тонну топлива; через четыре года три четверти плутония сгорают (превращаются в другие элементы). Реакторы-размножители специально разработаны для создания большего количества делящегося материала, чем они потребляют.
МОКС-топливо использовалось в используется с 1980-х годов и широко используется в Европе. В сентябре 2000 года Соединенные Штаты и Российская Федерация подписали Соглашение об обращении с плутонием и его утилизации, по которому каждая из них согласилась утилизировать 34 тонны оружейного плутония. США Министерство энергетики планирует утилизировать 34 тонны оружейного плутония в Соединенных Штатах до конца 2019 года путем преобразования плутония в МОКС-топливо, которое будет использоваться в коммерческих ядерных энергетических реакторах.
МОКС-топливо. топливо улучшает полное выгорание. После трех лет использования топливный стержень подвергается переработке для удаления отходов, которые к тому времени составляют 3% от общего веса стержней. Любые изотопы урана или плутония, произведенные в течение этих трех лет, остаются, а стержень возвращается в производство. Присутствие до 1% галлия на массу в оружейном плутониевом сплаве может помешать длительной эксплуатации легководного реактора.
Плутоний, извлеченный из отработавшего топлива реактора. представляет небольшую опасность распространения из-за чрезмерного загрязнения неделящимся плутонием-240 и плутонием-242. Разделение изотопов невозможно. Для производства материала, пригодного для эффективного использования, обычно требуется специальный реактор, работающий с очень низким выгоранием (следовательно, минимальное воздействие на вновь образованный плутоний-239 дополнительных нейтронов, которое вызывает его преобразование в более тяжелые изотопы плутония). ядерное оружие. В то время как плутоний «оружейного качества» определяется как содержащий не менее 92% плутония-239 (от общего количества плутония), Соединенным Штатам удалось взорвать устройство мощностью менее 20 кт, используя плутоний, который, как считается, содержит только около 85% плутония-239, так называемого «топливного» плутония. Плутоний «реакторного качества», производимый с помощью обычного цикла выгорания LWR, обычно содержит менее 60% Pu-239, до 30% паразитного Pu-240 / Pu-242 и 10–15% делящегося Pu-241. Неизвестно, может ли взорваться устройство, использующее плутоний, полученный из переработанных ядерных отходов гражданского назначения, однако такое устройство может гипотетически взорваться и распространить радиоактивные материалы по большой городской территории. МАГАТЭ консервативно классифицирует плутоний всех изотопных векторов как материал «прямого использования», то есть «ядерный материал, который может быть использован для производства компонентов ядерных взрывчатых веществ без трансмутации или дальнейшего обогащения».
 Светящийся цилиндр из PuO 2
Светящийся цилиндр из PuO 2 Радиоизотопный термоэлектрический генератор PuO 2 марсохода Curiosity
Радиоизотопный термоэлектрический генератор PuO 2 марсохода Curiosity Изотоп плутоний-238 имеет период полураспада. 87,74 года. Он излучает большое количество тепловой энергии с низкими уровнями как гамма-лучей / фотонов, так и спонтанных нейтронных лучей / частиц. Являясь альфа-излучателем, он сочетает в себе излучение высокой энергии с низким проникновением и поэтому требует минимального экранирования. Лист бумаги можно использовать для защиты от альфа-частиц, испускаемых плутонием-238. Один килограмм изотопа может генерировать около 570 ватт тепла.
Эти характеристики делают его хорошо подходящим для выработки электроэнергии для устройств, которые должны работать без прямого обслуживания в течение времени,приближающегося к продолжительности жизни человека.. Поэтому он используется в радиоизотопных термоэлектрических генераторах и нагревателях радиоизотопов, например, в Cassini, Voyager, Galileo и New Horizons, а также марсоходы Curiosity и Perseverance (Mars 2020 ) Mars Rovers.
. В 1977 году были запущены два космических корабля "Вояджер", каждый из которых содержал плутониевый источник питания мощностью 500 Вт. Спустя более 30 лет каждый источник все еще производит около 300 Вт, что позволяет ограниченную работу каждого космического корабля. Более ранняя версия той же технологии использовалась в пяти Аполлонах для экспериментов на Лунной поверхности, начиная с Аполлона-12 в 1969 году.
Плутоний-238 также успешно использовался для питания искусственное сердце кардиостимуляторы, чтобы снизить риск повторных операций. Он был в значительной степени заменен литиевыми первичными элементами, но по состоянию на 2003 год в Соединенных Штатах было где-то от 50 до 100 кардиостимуляторов с питанием от плутония, которые все еще имплантировались и функционировали в живых пациентах. К концу 2007 года количество кардиостимуляторов, работающих на плутонии, сократилось до девяти. Плутоний-238 изучался как способ обеспечения дополнительного тепла при нырянии с аквалангом. Плутоний-238, смешанный с бериллием, используется для генерации нейтронов в исследовательских целях.
Есть два аспекта вредного воздействия плутония: радиоактивность и яд тяжелого металла эффекты. Изотопы и соединения плутония радиоактивны и накапливаются в костном мозге. Загрязнение оксидом плутония произошло в результате ядерных катастроф и радиоактивных инцидентов, включая военные ядерные аварии, в результате которых сгорело ядерное оружие. Исследования последствий этих небольших выбросов, а также широко распространенных болезней и смертей от радиационного отравления после атомных бомбардировок Хиросимы и Нагасаки предоставили значительную информацию об опасностях, симптомах и прогнозе радиационное отравление, которое в случае выживших японцев было в значительной степени не связано с прямым воздействием плутония.
При распаде плутония выделяются три типа радиации - альфа, бета, и гамма. Альфа, бета и гамма-излучение - это все формы ионизирующего излучения. Острое или длительное облучение несет опасность серьезных последствий для здоровья, включая лучевую болезнь, генетическое повреждение, рак и смерть. Опасность возрастает с увеличением воздействия. Альфа-излучение может распространяться только на короткие расстояния и не может проходить через внешний мертвый слой кожи человека. Бета-излучение может проникать через кожу человека, но не может проходить через все тело. Гамма-излучение может проходить через все тело. Несмотря на то, что альфа-излучение не может проникнуть через кожу, проглоченный или вдыхаемый плутоний облучает внутренние органы. Альфа-частицы, образующиеся при вдыхании плутония, вызывают рак легких у группы европейских ядерщиков. скелет, где накапливается плутоний, и печень, где он накапливается и концентрируется, находятся под угрозой. Плутоний не всасывается в организм эффективно при попадании внутрь; только 0,04% оксида плутония всасывается после приема внутрь. Плутоний, абсорбированный организмом, выводится из организма очень медленно, с периодом биологического полураспада 200 лет. Плутоний медленно проходит через клеточные мембраны и границы кишечника, поэтому абсорбция при приеме внутрь и включение в структуру кости происходит очень медленно.
Плутоний более опасен при вдыхании, чем при приеме внутрь. Риск рака легких увеличивается, если общая радиационная эквивалентная доза вдыхаемого плутония превышает 400 мЗв. По оценкам Министерства энергетики США, риск рака в течение жизни при вдыхании 5000 частиц плутония, каждая размером около 3 мкм шириной, составляет 1% по сравнению со средним фоновым показателем по США. Проглатывание или вдыхание больших количеств может вызвать острое радиационное отравление и, возможно, смерть. Однако известно, что ни одно человеческое существо не умерло из-за вдыхания или проглатывания плутония, и у многих людей есть измеримые количества плутония в своих телах.
Теория «горячей частицы », в которой Частица плутониевой пыли облучает локализованное пятно легочной ткани, что не подтверждается основными исследованиями - такие частицы более подвижны, чем первоначально предполагалось, и их токсичность не увеличивается заметно из-за формы частиц. При вдыхании плутоний может попасть в кровоток. Попадая в кровоток, плутоний перемещается по всему телу в кости, печень или другие органы. Плутоний, который достигает органов тела, обычно остается в организме в течение десятилетий и продолжает подвергать окружающие ткани воздействию радиации и, таким образом, может вызвать рак.
Часто цитируемая цитата Ральфа Надера утверждает, что фунт распространения плутониевой пыли в атмосферу было бы достаточно, чтобы убить 8 миллиардов человек. Это оспаривал Бернард Коэн, противник общепринятой линейной беспороговой модели радиационной токсичности. Коэн подсчитал, что один фунт плутония может убить не более 2 миллионов человек при вдыхании, таким образом, токсичность плутония примерно равна токсичности нервно-паралитического газа.
Несколько групп людей, подвергшихся воздействию плутониевой пыли (например, люди живущие под ветром испытательных полигонов Невады, выжившие в Нагасаки, работники ядерных установок и «неизлечимо больные» пациенты, которым вводили Pu в 1945–46 годах для изучения метаболизма Pu), были тщательно изучены и проанализированы. Коэн нашел эти исследования несовместимыми с высокими оценками токсичности плутония, сославшись на такие случаи, как Альберт Стивенс, который дожил до преклонного возраста после инъекции плутония. «Около 25 сотрудников Лос-Аламосской национальной лаборатории вдыхали значительное количество плутониевой пыли в течение 1940-х годов; согласно теории горячих частиц, к настоящему времени у каждого из них есть шанс 99,5% умереть от рака легких, но есть среди них не было ни одного рака легких ».
Плутоний имеет металлический привкус.
 Сфера искусственного плутония, окруженная отражающим нейтроны карбидом вольфрама блоки в реконструкции эксперимента Гарри Дагляна 1945 года
Сфера искусственного плутония, окруженная отражающим нейтроны карбидом вольфрама блоки в реконструкции эксперимента Гарри Дагляна 1945 года Следует проявлять осторожность, чтобы избежать накопления количества плутония, которое приближается к критической массе, особенно потому, что критическая масса плутония составляет лишь треть от массы урана-235. Критическая масса плутония испускает смертельное количество нейтронов и гамма-лучей. Плутоний в растворе с большей вероятностью образует критическую массу, чем в твердой форме, из-за замедления водородом в воде.
Аварии, связанные с критичностью, произошли в прошлом, некоторые из них со смертельным исходом. Неосторожное обращение с кирпичиками из карбида вольфрама вокруг плутониевой сферы весом 6,2 кг привело к смертельной дозе радиации в Лос-Аламосе 21 августа 1945 года, когда ученый Гарри Даглиан получил дозу, равную примерно 5,1 зиверта (510 бэр ) и умер через 25 дней. Девять месяцев спустя другой ученый из Лос-Аламоса, Луи Слотин, погиб в аналогичной аварии с участием бериллиевого отражателя и того же плутониевого ядра (так называемое «ядро демона »), которое имело ранее унес жизни Дагляна.
В декабре 1958 года во время процесса очистки плутония в Лос-Аламосе в смесительном сосуде образовалась критическая масса, что привело к смерти химического оператора по имени Сесил Келли. Другие ядерные аварии произошли в Советском Союзе, Японии, США и многих других странах.
Металлический плутоний является пожароопасным, особенно если материал мелкодисперсный. Во влажной среде плутоний образует на своей поверхности гидриды, которые являются пирофорными и могут воспламениться на воздухе при комнатной температуре. Плутоний расширяется до 70% в объеме при окислении и, таким образом, может разрушить свой контейнер. Дополнительную опасность представляет радиоактивность горящего материала. Оксид магния песок, вероятно, является наиболее эффективным материалом для тушения плутониевого пожара. Он охлаждает горящий материал, действуя как теплоотвод , а также блокирует кислород. При хранении или обращении с плутонием в любой форме необходимы особые меры предосторожности; обычно требуется сухая атмосфера инертного газа.
Обычная транспортировка плутония осуществляется через более стабильный оксид плутония в запечатанный пакет. Типичный транспорт состоит из одного грузовика, перевозящего один защищенный транспортный контейнер, вмещающий несколько упаковок с общим весом от 80 до 200 кг оксида плутония. Морская партия может состоять из нескольких контейнеров, в каждом из которых находится запечатанная упаковка. Комиссия по ядерному регулированию США требует, чтобы он был твердым, а не порошком, если его содержание превышает 0,74 ТБк (20 Кюри ) радиоактивной активности. В 2016 году суда Pacific Egret и Pacific Heron of Pacific Nuclear Transport Ltd. перевезли 331 кг (730 фунтов) плутония на правительственный объект США в Саванна-Ривер, Южная Каролина.
Правила воздушного транспорта США разрешают перевозку плутония по воздуху с учетом ограничений на другие опасные материалы, перевозимые тем же рейсом, требований к упаковке и размещению в самой задней части
В 2012 году СМИ сообщили, что плутоний вывозится из Норвегии коммерческими пассажирскими авиакомпаниями - примерно раз в два года, в том числе один раз в 2011 году. Правила разрешают самолету перевозить 15 граммов делящегося материала. По словам старшего советника (Seniorrådgiver) в Statens strålevern.