аргон - химический элемент с символом Arи атомным номером 18. Он находится в 18 группе таблицы Менделеева и является благородным газом. Аргон является третьим по содержанию газом в атмосфере Земли с 0,934% (9340 ppmv ). Его более чем в два раза больше, чем водяного пара (который в среднем составляет около 4000 ppmv, но сильно варьируется), в 23 раза больше, чем диоксида углерода (400 ppmv), и более 500 раз больше, чем неон (18 частей на миллион по объему). Аргон - самый распространенный благородный газ в земной коре, составляющий 0,00015% коры.
Почти весь аргон в атмосфере Земли является радиоактивным аргоном-40, полученным в результате распада калия-40. в земной коре. Во Вселенной аргон-36 на сегодняшний день является наиболее распространенным изотопом аргона , так как он наиболее легко образуется при звездном нуклеосинтезе в сверхновых.
Название «аргон» происходит от греческого слова ἀργόν, среднего единственного числа от ργός, означающего «ленивый» или «неактивный», как указание на тот факт, что элемент почти не вступает в химические реакции. Полный октет (восемь электронов) во внешней оболочке атома делает аргон стабильным и устойчивым к связыванию с другими элементами. Его тройная точка температура 83,8058 K является определяющей фиксированной точкой в Международной температурной шкале 1990 года.
Аргон получают промышленным способом путем фракционной перегонки из жидкий воздух. Аргон в основном используется в качестве инертного защитного газа при сварке и других высокотемпературных промышленных процессах, где обычно инертные вещества становятся реактивными; например, в электрических печах графита используется атмосфера аргона для предотвращения горения графита. Аргон также используется в лампах накаливания, люминесцентном освещении и других газоразрядных трубках. Аргон делает отличительный сине-зеленый газовый лазер. Аргон также используется в стартерах люминесцентного свечения.
 Небольшой кусочек быстро плавящегося твердого аргона
Небольшой кусочек быстро плавящегося твердого аргона Аргон имеет примерно такую же растворимость в вода в качестве кислорода и в 2,5 раза более растворима в воде, чем азот. Аргон не имеет цвета, запаха, негорючего вещества и нетоксичен как твердое вещество, жидкость или газ. Аргон химически инертен в большинстве условий и не образует подтвержденных стабильных соединений при комнатной температуре.
Хотя аргон является благородным газом, он может образовывать некоторые соединения в различных экстремальных условиях. Фторгидрид аргона (HArF), соединение аргона с фтором и водородом, которое стабильно ниже 17 К (-256,1 ° C; -429,1 ° F), был продемонстрирован. Хотя нейтральные химические соединения аргона в основном состоянии в настоящее время ограничиваются HArF, аргон может образовывать клатраты с водой, когда атомы аргона захватываются решеткой из молекул воды. Были продемонстрированы ионы, такие как ArH., и комплексы возбужденного состояния, такие как ArF. Теоретический расчет предсказывает еще несколько соединений аргона, которые должны быть стабильными, но еще не синтезированы.
 A: пробирка, B: разбавленная щелочь, C: U-образная стеклянная трубка, D: платиновый электрод
A: пробирка, B: разбавленная щелочь, C: U-образная стеклянная трубка, D: платиновый электрод Аргон (греч. ἀργόν, среднее единственное число of ἀργός, означающее «ленивый» или «неактивный») назван в связи с его химической неактивностью. Это химическое свойство этого первого обнаруженного благородного газа произвело впечатление на авторов названий. Генри Кавендиш в 1785 году предположил, что инертный газ является компонентом воздуха.
Аргон был впервые изолирован из воздуха в 1894 году лордом Рэли и сэром <520.>Уильям Рамзи в Университетском колледже Лондона путем удаления кислорода, диоксида углерода, воды и азота из образца чистой воздух. Они впервые достигли этого, повторив эксперимент Генри Кавендиша. Они захватили смесь атмосферного воздуха с дополнительным кислородом в пробирке (A) вверх ногами над большим количеством разбавленного раствора щелочи (B), который в первоначальном эксперименте Канвендиша был гидроксидом калия, и передали ток через провода, изолированные U-образными стеклянными трубками (CC), которые герметизированы вокруг электродов из платиновой проволоки, оставляя концы проводов (DD) открытыми для газа и изолированными от раствора щелочи. Дуга питалась от батареи из пяти ячеек Гроува и катушки Румкорфа среднего размера. Щелочь поглощала оксиды азота, образующиеся при дуге, а также диоксид углерода. Они включали дугу до тех пор, пока уменьшение объема газа не прекращалось в течение по крайней мере часа или двух, а спектральные линии азота не исчезали при исследовании газа. Оставшийся кислород прореагировал с щелочным пирогаллатом, оставив после себя явно неактивный газ, который они назвали аргоном.
Перед выделением газа они определили, что азот, полученный из химических соединений, на 0,5% легче, чем азот из атмосферы. Разница была небольшой, но достаточно важной, чтобы привлекать их внимание на многие месяцы. Они пришли к выводу, что в воздухе есть еще один газ, смешанный с азотом. Аргон также был обнаружен в 1882 году в результате независимых исследований Х. Ф. Ньюолла и У. Н. Хартли. Каждый наблюдал новые линии в спектре излучения воздуха, которые не соответствовали известным элементам.
До 1957 года символ аргона был «A», но теперь это «Ar».
Аргон составляет 0,934% по объему и 1,288% по массе атмосферы Земли, а воздух является основным промышленным источником продуктов очищенного аргона. Аргон выделяют из воздуха фракционированием, чаще всего с помощью криогенной фракционной перегонки, процесса, который также дает очищенный азот, кислород, неон, криптон и ксенон. Земная кора и морская вода содержат 1,2 и 0,45 промилле аргона, соответственно.
Основными изотопами аргона, обнаруженными на Земле, являются. Ar (99,6 %),. Ar (0,34%) и. Ar (0,06%). Встречающийся в природе. K, с периодом полураспада 1,25 × 10 лет, распадается до стабильного. Ar (11,2%) в результате захвата электронов или испускания позитронов, а также до стабильного. Ca (88,8%) посредством бета-распада. Эти свойства и соотношения используются для определения возраста горных пород с помощью датирования K – Ar.
В атмосфере Земли. Ar образуется в результате активности космических лучей в первую очередь нейтронным захватом. Ar с последующим испусканием двух нейтронов. В подповерхностной среде он также образуется за счет захвата нейтронов. К с последующим испусканием протонов.. Ar создается в результате захвата нейтронов. Ca с последующим выбросом альфа-частиц в результате подземных ядерных взрывов. Его период полураспада составляет 35 дней.
В разных местах в Солнечной системе изотопный состав аргона сильно различается. Если основным источником аргона является распад . K в горных породах,. Ar будет доминирующим изотопом, как и на Земле. В аргоне, образующемся непосредственно при звездном нуклеосинтезе, преобладает альфа-процесс нуклид. Ar. Соответственно, солнечный аргон содержит 84,6%. Ar (согласно измерениям солнечного ветра ), а соотношение трех изотопов Ar: Ar: Ar в атмосферах внешних планет составляет 8400: 1600: 1. Это контрастирует с низким содержанием первичного. Ar в атмосфере Земли, которое составляет всего 31,5 ppmv (= 9340 ppmv × 0,337%), что сравнимо с содержанием неона (18,18 ppmv) на Земле и с межпланетными газами. измерено зондами .
Атмосферы Марса, Меркурия и Титана (самый большой спутник Сатурна ) содержат аргон, преимущественно как. Ar, и его содержание может достигать 1,93% (Марс).
Преобладание радиогенного. Ar является причиной стандартной атомной массы земного аргона больше, чем у следующего элемента, калия, факт, который озадачил, когда аргон был открыт. Менделеев расположил элементы в своей таблице Менделеева в порядке атомного веса, но инертность аргона предполагала размещение элементов перед химически активным щелочным металлом. Генри Мозли позже решил эту проблему, показав, что периодическая таблица на самом деле организована в порядке атомного номера (см. История периодической таблицы ).
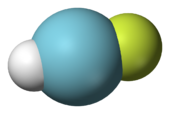 Модель, заполняющая пространство из фторгидрида аргона
Модель, заполняющая пространство из фторгидрида аргона Полный октет аргона электронов указывает на полные s- и p-подоболочки. Эта оболочка с полной валентностью делает аргон очень стабильным и чрезвычайно устойчивым к связыванию с другими элементами. До 1962 года аргон и другие благородные газы считались химически инертными и неспособными образовывать соединения; однако с тех пор были синтезированы соединения более тяжелых благородных газов. Первое соединение аргона с пентакарбонилом вольфрама, W (CO) 5 Ar, было выделено в 1975 году. Однако в то время оно не было широко признано. В августе 2000 года другое соединение аргона, фторгидрид аргона (HArF), было образовано исследователями из Университета Хельсинки, направив ультрафиолетовый свет на замороженный аргон, содержащий небольшое количество фтороводород с иодидом цезия. Это открытие вызвало осознание того, что аргон может образовывать слабосвязанные соединения, хотя и не первое. Он стабилен до 17 кельвин s (-256 ° C). метастабильный ArCF. 2дикатион, который является валентно- изоэлектронным с карбонилфторидом и фосгеном, наблюдался в 2010 году. Аргон-36 в форме ионов гидрида аргона (аргоний ) был обнаружен в межзвездной среде, связанной с Крабовидной туманностью сверхновая ; это была первая молекула благородного газа, обнаруженная в космическом пространстве.
Твердый аргон гидрид (Ar (H 2)2) имеет ту же кристаллическую структуру, что и MgZn 2Фаза Лавеса. Она образуется при давлениях от 4,3 до 220 ГПа, хотя измерения комбинационного рассеяния показывают, что молекулы H 2 в Ar (H 2)2диссоциируют выше 175 ГПа.
Аргон получают промышленным способом путем фракционной перегонки жидкого воздуха в криогенной блок разделения воздуха ; процесс, который отделяет жидкий азот, который кипит при 77,3 K, от аргона, который кипит при 87,3 K, и жидкого кислорода, который кипит при 90,2 K. Ежегодно во всем мире производится около 700 000 тонн аргона.
Ar самый распространенный изотоп аргона образуется при распаде K с периодом полураспада 1,25 × 10 лет за счет захвата электрона или испускания позитрона. Из-за этого i t используется в калий-аргоновом датировании для определения возраста горных пород.
 Баллоны, содержащие газообразный аргон, для использования при тушении пожара без повреждения серверного оборудования
Баллоны, содержащие газообразный аргон, для использования при тушении пожара без повреждения серверного оборудования Аргон обладает несколькими желательными свойствами:
Другие благородные газы также подходят для большинства этих применений, но аргон, безусловно, самый дешевый. Аргон недорог, поскольку он естественным образом встречается в воздухе и легко получается как побочный продукт криогенного разделения воздуха при производстве жидкого кислорода и жидкости. азот : основные компоненты воздуха используются в крупных промышленных масштабах. Другие благородные газы (кроме гелия ) также производятся таким образом, но аргон, безусловно, является наиболее распространенным. Основная часть применений аргона возникает просто потому, что он инертен и относительно дешев.
Аргон используется в некоторых высокотемпературных промышленных процессах, где обычно нереактивные вещества становятся реактивными. Например, в графитовых электрических печах используется атмосфера аргона для предотвращения горения графита.
Для некоторых из этих процессов присутствие азота или кислорода может вызвать дефекты в материале. Аргон используется в некоторых типах дуговой сварки, таких как дуговой сварке металлическим металлом и дуговой сварке вольфрамовым электродом, а также при обработке титана. и другие реактивные элементы. Атмосфера аргона также используется для выращивания кристаллов кремния и германия.
. Аргон используется в птицеводстве для удушения птиц либо для массового уничтожения после вспышек заболеваний, либо для массового уничтожения птиц. или как средство убоя более гуманное, чем электрическое оглушение. Аргон плотнее воздуха и вытесняет кислород вблизи земли во время удушения инертным газом. Его нереактивная природа делает его подходящим в пищевом продукте, а поскольку он заменяет кислород в мертвой птице, аргон также увеличивает срок хранения.
Аргон иногда используется для тушения пожаров, где ценно оборудование может быть повреждено водой или пеной.
Жидкий аргон используется в качестве мишени для нейтринных экспериментов и прямого поиска темной материи. Взаимодействие между гипотетическими WIMP и ядром аргона дает сцинтилляционный свет, который обнаруживается фотоэлектронными умножителями. Двухфазные детекторы, содержащие газообразный аргон, используются для обнаружения ионизированных электронов, образующихся во время рассеяния WIMP-ядра. Как и большинство других сжиженных благородных газов, аргон имеет высокий выход сцинтилляционного света (около 51 фотона / кэВ), прозрачен для собственного сцинтилляционного света и относительно легко очищается. По сравнению с ксеноном, аргон дешевле и имеет отчетливый временной профиль сцинтилляции, что позволяет отделить отдачу электронов от отдачи ядер. С другой стороны, его собственный фон бета-излучения больше из-за загрязнения. Ar, если только не используется аргон из подземных источников, который имеет гораздо меньше загрязнения. Ar. Большая часть аргона в атмосфере Земли была произведена в результате электронного захвата долгоживущего. K (. K + e →. Ar + ν), присутствующего в природном калии на Земле. Активность. Ar в атмосфере поддерживается за счет космогенного образования посредством реакции выбивания. Ar (n, 2n). Ar и подобных реакций. Период полураспада. Ar составляет всего 269 лет. В результате подземный Ar, защищенный камнями и водой, имеет гораздо меньшее загрязнение. Ar. Детекторы темной материи, в настоящее время работающие с жидким аргоном, включают DarkSide, WArP, ArDM, microCLEAN и DEAP. Эксперименты с нейтрино включают ICARUS и MicroBooNE, оба из которых используют жидкий аргон высокой чистоты в проекционной камере для мелкозернистого трехмерного изображения взаимодействий нейтрино.
В университете Линчёпинга, Швеция, инертный газ используется в вакуумной камере, в которую вводится плазма для ионизации металлических пленок. В результате этого процесса получается пленка, которую можно использовать для производства компьютерных процессоров. Новый процесс устранит необходимость в химических ваннах и использовании дорогих, опасных и редких материалов.
 Образец цезия упаковывают в атмосфере аргона, чтобы избежать реакции с воздухом.
Образец цезия упаковывают в атмосфере аргона, чтобы избежать реакции с воздухом. Аргон используется для вытеснения кислород- и влагосодержащего воздуха в упаковочном материале для увеличения срока службы. срок годности содержимого (аргон имеет европейский код пищевой добавки E938). Воздушное окисление, гидролиз и другие химические реакции, приводящие к разложению продуктов, замедляются или полностью предотвращаются. Химические вещества высокой чистоты и фармацевтические препараты иногда упаковываются и запечатываются в аргоне.
В виноделии аргон используется в различных сферах деятельности, чтобы создать барьер против кислорода на поверхности жидкости, который может портить вино, подпитывая как микробный метаболизм (как в случае уксуснокислых бактерий ), так и стандартный окислительно-восстановительный химический состав.
Аргон иногда используется в качестве пропеллента в аэрозольных баллонах.
Аргон также используется в качестве консерванта для таких продуктов, как лак, полиуретан и краска, вытесняя воздух для подготовки контейнера для хранения.
С 2002 года Американский национальный архив хранит важные национальные документы, такие как Декларация независимости и Конституция в заполненных аргоном ящиках, чтобы предотвратить их разрушение. Аргон предпочтительнее гелия, который использовался в предыдущие пять десятилетий, потому что газообразный гелий выходит через межмолекулярные поры в большинстве контейнеров и должен регулярно заменяться.
 Перчаточные боксы часто используются заполненный аргоном, который рециркулирует через скрубберы для поддержания кислорода -, азота - и атмосферы без влаги
Перчаточные боксы часто используются заполненный аргоном, который рециркулирует через скрубберы для поддержания кислорода -, азота - и атмосферы без влаги В качестве инертного газа <141 может использоваться аргон.>внутри линий Шленка и перчаточных ящиков. Аргон предпочтительнее менее дорогого азота в тех случаях, когда азот может реагировать с реагентами или аппаратом.
аргон может использоваться в качестве газа-носителя в газовой хроматографии и в масс-спектрометрии с ионизацией электрораспылением ; это предпочтительный газ для плазмы, используемой в ICP спектроскопии. Аргон является предпочтительным для нанесения покрытия распылением образцов для растровой электронной микроскопии. Газ аргон также обычно используется для напыления тонких пленок, как в микроэлектронике, и для очистки пластин в микропроизводстве.
Криохирургия процедуры, такие как в качестве криоабляции используйте жидкий аргон для разрушения ткани, такой как раковые клетки. Он используется в процедуре, называемой «коагуляция с усилением аргона», форма плазменного луча аргона электрохирургия. Процедура сопряжена с риском возникновения газовой эмболии и привела к смерти как минимум одного пациента.
Голубые аргоновые лазеры используются в хирургии для сварки артерий, разрушать опухоли и исправлять дефекты глаз.
Аргон также экспериментально использовался для замены азота в дыхательной смеси или смеси для декомпрессии, известной как Argox, для ускорения удаления растворенного азота из крови.
 Аргон газоразрядная лампа, образующая символ аргона «Ar»
Аргон газоразрядная лампа, образующая символ аргона «Ar» Лампы накаливания заполнены аргоном для сохранения нитей при высокой температуре из-за окисления. Он используется для определенного способа ионизации и излучения света, например, в плазменных шарах и калориметрии в экспериментальной физике элементарных частиц. Газоразрядные лампы, наполненные чистым аргоном, излучают сиреневый / фиолетовый свет; с аргоном и немного ртути, синий свет. Аргон также используется для синих и зеленых аргон-ионных лазеров.
Аргон используется для теплоизоляции в энергоэффективных окнах. Аргон также используется в техническом подводном плавании с аквалангом для надувания сухого костюма, потому что он инертен и имеет низкую теплопроводность.
Аргон используется в качестве топлива при разработке Магнитоплазменной Ракеты с переменным удельным импульсом (ВАСИМР). Сжатый газ аргон может расширяться для охлаждения головок ГСН некоторых версий ракеты AIM-9 Sidewinder и других ракет, в которых используются охлаждаемые головки ГСН. Газ хранится при высоком давлении..
Аргон-39, с периодом полураспада 269 лет, использовался для ряда применений, в основном ледяной керн и грунтовые воды. свидание. Кроме того, калий-аргоновое датирование и связанное с ним аргоно-аргоновое датирование используется для датировки осадочных, метаморфических и магматических пород..
Аргон использовался спортсменами в качестве допинга для имитации гипоксических состояний. В 2014 году Всемирное антидопинговое агентство (WADA) добавило аргон и ксенон в список запрещенных веществ и методов, хотя в настоящее время нет надежного теста на злоупотребление. 358>
Хотя аргон не токсичен, он на 38% плотнее, чем воздух, и поэтому считается опасным удушающим веществом в закрытых помещениях. Его трудно обнаружить, потому что он не имеет цвета, запаха и вкуса. Инцидент 1994 года, когда мужчина задохнулся после входа в заполненную аргоном секцию нефтепровода, строящуюся на Аляске, подчеркивает опасность утечки аргона из резервуара в замкнутом пространстве и подчеркивает необходимость правильного использования, хранения и обращения.
.