 | |||
| |||
| Наименования | |||
|---|---|---|---|
| Другие наименования | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| 3DMet | |||
| Ссылка Beilstein | 1900390 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.004.271 | ||
| ЕС |
| ||
| Номер E | E290 (консерванты) | ||
| Ссылка Гмелина | 989 | ||
| KEGG | |||
| MeSH | Углерод + диоксид | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1013 (газ), 1845 (твердый) | ||
| Па нель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБАЕТСЯ
| |||
| Свойства | |||
| Химическая формула | CO2 | ||
| Молярная масса | 44 009 г · моль | ||
| Внешний вид | Бесцветный газ | ||
| Запах |
| ||
| Плотность |
| ||
| точка плавления | -56,6 ° C; -69,8 ° F; 216,6 K (тройная точка при 5,1 атм) | ||
| Критическая точка (T, P) | 31,1 ° C (304,2 K), 7,38 мегапаскалей (73,8 бар) | ||
| Условия сублимации. | -78,5 ° C; -109,2 ° F; 194,7 К (1 атм) | ||
| Растворимость в воде | 1,45 г / л при 25 ° C (77 ° F), 100 кПа | ||
| Давление пара | 5,73 МПа (20 ° C) | ||
| Кислотность (pK a) | 6,35, 10,33 | ||
| Магнитная восприимчивость (χ) | -20,5 · 10 см / моль | ||
| Теплопроводность | 0,01662 Вт · м · K (300 K) | ||
| Показатель преломления (nD) | 1.00045 | ||
| Вязкость |
| ||
| Дипольный момент | 0 D | ||
| Структура | |||
| Кристаллическая структура | Тригональная | ||
| Молекулярная форма | Линейная | ||
| Термохимия | |||
| Теплоемкость ( C) | 37,135 Дж / К · моль | ||
| Станд. Моляр. энтропия (S 298) | 214 Дж · моль · K | ||
| Стандартная энтальпия образования. (ΔfH298) | -393,5 кДж · моль | ||
| Фармакология | |||
| Код АТС | V03AN02 (ВОЗ ) | ||
| Опасности | |||
| Паспорт безопасности | См.: страница данных. Sigma-Aldrich | ||
| NFPA 704 (огненный алмаз) |  0 2 0 SA 0 2 0 SA | ||
| Смертельная доза или концентраци я (LD, LC): | |||
| LCLo(самая низкая опубликованная ) | 90000 частей на миллион (человек, 5 мин) | ||
| NIOSH (пределы воздействия на здоровье США): | |||
| ПЕЛ (Пермь выпускается) | TWA 5000 ppm (9000 мг / м) | ||
| REL (рекомендуется) | TWA 5000 ppm (9000 мг / м), ST 30 000 ppm (54000 мг / м) | ||
| IDLH (Непосредственная опасность) | 40,000 ppm | ||
| Родственные соединения | |||
| Другие анионы | |||
| Прочие катионы | |||
| Связанные углерода оксиды | |||
| Связанные | |||
| Страница дополнительных данных | |||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. д. | ||
| Термодинамические. данные | Фазовое поведение. твердое тело - жидкость - газ | ||
| Спектральные данные | UV, IR, ЯМР, MS | ||
| Если не указаны данные, данные приведены для материалов в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на ink | |||
Углерод диоксид (химическая форма ula CO. 2) представляет собой бесцветный газ с плотностью примерно на 53% выше, чем у сухого воздуха. Молекулы двуокиси углерода состоят из атома углерода , ковалентно двойной связи с двумя кислородом атомы. Он естественным образом примеси в атмосфере Земли в виде газовых примесей. Текущая деятельность составляет около 0,04% (412 ppm ) по объему, увеличившись с доиндустриальных уровней 280 ppm. Природные источники включают вулканы, горячие источники и гейзеры, и он выделен от карбонатных пород путем растворения в вода и кислоты. Углекислый газ растворим в воде, он естественным образом встречается в подземных водах, реках и озерах, ледяных шапках, ледниках и морская вода. Он присутствует в месторождениях нефти и природного газа. Двуокись углерода имеет резкий и кислый запах и создает во рту привкус газированной воды. Однако запах при обычных веществх он не имеет запаха.
Как источник доступного углерода в углеродном цикле, атмосферный диоксид углерода является основным источником углерода для жизнь на Земле и ее источник в доиндустриальной атмосфере Земли с конца докембрия регулировалась фотосинтетическими организмами и геологическими явлениями. Растения, водоросли и цианобактерии используют легкую энергию для фотосинтеза углеводов из диоксида углерода воды, причем кислород образуется как отходы.
CO. 2 производится всеми аэробными организмами, когда они метаболизируют органические соединения для производства энергии дыхание. Он возвращается в воду через жабры рыб и в воздух через легкие дышащих воздухом наземных животных, включая человека. Углекислый газ образуется в процессе распада материалов и брожения сахаров в хлебе, пиве и вине. изготовление. Получение путем сжигания древесины и других материалов и ископаемого топлива, такого как уголь, торф, нефть и природный газ. Это нежелательный побочный продукт во многих крупномасштабных процессах окисления, например, при производстве акриловой кислоты (более 5 миллионов тонн в год).
Это универсальный промышленный материал, используемый, например, в качестве газа под давлением в пневматических пистолетах и нефтедобыче, в качестве химического сырья и в качестве в качестве газа жидкого растворителя в сверхкритическом состоянии при декофеинизации кофе и сверхкритическая сушка. Его добавляют в питьевую воду и газированные напитки, включая пиво и игристое вино для придания шипучести. Замороженная твердая форма CO. 2, известная как сухой лед, используется в качестве хладагента и в качестве абразива при струйной очистке сухим льдом. Это сырье для синтеза топлива и химикатов.
Двуокись углерода наиболее значительным долгоживущим парниковым газом в атмосфере Земли. После промышленной революции антропогенные выбросы - в первую очередь от использования ископаемого топлива и обезлесения - быстро увеличили его концентрацию в атмосфере, что привело к глобальному потеп. Углекислый газ также вызывает закисление океана, потому что он растворяется в воде с образованием угольной кислоты.
 Кристаллическая структура сухого льда
Кристаллическая структура сухого льда Диоксид углерода был первым газом быть описанным как дискретное вещество. Примерно в 1640 году фламандский химик Ян Баптист ван Гельмонт заметил, что когда он сжигал древесный уголь в закрытом сосуде, образовавшейся золы был намного меньше, чем у оригинального древесного угля. Его интерпретация заключалась в том, что остальная часть древесного угля была преобразована в невидимое вещество, которое он назвал «газом» или «диким духом» (spiritus sylvestris).
Свойства углекислого газа были изучены в 1750-х годах. шотландский врач Джозеф Блэк. Он обнаружил, что известняк (карбонат кальция ) можно нагреть или обработать кислотами, чтобы получить газ, который он назвал «неподвижным воздухом». Он заметил, что неподвижный воздух был плотнее воздуха и не поддерживал ни пламя, ни жизнь животных. Блэк также обнаружил, что при барботировании через известковую воду (насыщенный водный раствор гидроксида кальция ) он осаждает карбонат кальция. Он использовал это явление, чтобы проиллюстрировать, что углекислый газ образует эффект в результате дыхания животных и микробной ферментации. В 1772 году английский химик Джозеф Пристли опубликовал статью, озаглавленную «Пропитка воды фиксированным воздухом», в которой он описал процесс капания серной кислоты (или купоросного масла, как знал Пристли) на мел. для образования диоксида углерода и принуждения газа к растворению емкости с водой, контактирующей с газом.
Впервые диоксид углерода был сжижен (при повышенном давлении) в 1823 году Хамфри Дэви и Майкл Фарадей. Самое раннее описание твердого диоксида углерода (сухой лед ) было дано французским изобретателем Адрианом-Жан-Пьером Тилорье, который в 1835 году открыл контейнер с жидким диоксидом углерода под давлением только для того, чтобы создание, что охлаждение, вызванное быстрым испарением жидкости, привело к образованию «снега» твердого CO. 2.
Молекула диоксида углерода линейна и центросимметричный в состоянии равновесия. Длина связи углерод-кислород составляет 116,3 пм, что заметно короче, чем длина связи одинарной связи CO, и даже короче, чем у других других CO многосвязные функциональные группы. Она центросимметрична, молекула не имеет электрических дипольных.
 колебаний растяжения и изгиба молекулы диоксида углерода CO. 2. Вверху слева: симметричная растяжка. Вверху справа: антисимметричное растяжение. Нижняя линия: вырожденная пара изгибных мод.
колебаний растяжения и изгиба молекулы диоксида углерода CO. 2. Вверху слева: симметричная растяжка. Вверху справа: антисимметричное растяжение. Нижняя линия: вырожденная пара изгибных мод. Как линейная трехатомная молекула, CO 2 имеет четыре колебательные моды, как показано на диаграмме. Однако симметричная мода растяжения не создает диполь и поэтому не наблюдается в ИК-спектре. Две изгибные моды являются вырожденными, что означает, что они соответствуют только одной частоте. Следовательно, в ИК-спектре наблюдаются только две колебательные полосы - антисимметричная мода растяжения при волновом числе 2349 см и пара вырожденных изгибных мод при 667 см (длина волны 15 мкм). Существует также симметричная мода растяжения на 1388 см, которая наблюдается только в рамановском спектре .
. В результате двух мод изгиба молекула является строго линейной только тогда, когда величина изгиба равна нулю. Это было доказано как теорией, так и экспериментами по визуализации кулоновского взрыва. что на самом деле это никогда не верно для обоих режимов одновременно. В газовой фазе диоксида углерода одна из молекул не является линейной из-за колебательных движений. Однако геометрия молекулы по-прежнему описывается как линейная, которая представляет средние положения атомов, соответствующей минимальной потенциальной энергии. То же верно и для других «линейных» молекул.
Двуокись углерода растворима в воде, в которой он обратимо образует H. 2CO. 3(угольную кислоту ), которая слабая кислота, так как ее ионизация в воде неполная.
Константа равновесия гидратации угольной кислоты равна ![K _ {\ mathrm {h}} = {\ frac {\ rm {[H_ {2} CO_ {3}]}} {\ rm {[CO_ {2} (водн.)]} }} = 1,70 \ tim es 10 ^ {- 3}](https://wikimedia.org/api/rest_v1/media/math/render/svg/880be9280cefa51b14dc80f037e4296c81a15e6b)
Относительные концентрации CO. 2, H. 2CO. 3и депротонированных форм HCO. 3(бикарбоната ) и CO. 3(карбоната ) зависят на pH. Как показано на графике Бьерма, нейтральная или слабощелочная (pH>6,5) преобладает бикарбонатная форма воды (>50%), становясь наиболее распространенной (>95%) при pH морской воды. В очень щелочной воде (pH>10,4) преобладающая (>50%) форма представляет собой карбонат. Океаны, содержат около 120 мг бикарбоната на литр, будучи умеренно щелочным типичным pH = 8,2–8,5.
Будучи дипротонной, угольная кислота имеет две константы кислотной диссоциации, первая из которых предназначена для диссоциации на бикарбонатный (также называемый гидрокарбонатным) ион (HCO 3):
Это истинная первая константа диссоциации кислоты, определяемая как ![K_ {a1} = {\ frac {\ rm {[HCO_ {3} ^ {-}] [H ^ {+}]}} {\ rm {[H_ {2} CO_ {3 }]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/81950791f8b36374241d6fa82828522bd875668a)
![K _ {\ mathrm {a1}} {\ rm {(кажущееся)}} = {\ frac {\ rm {[HCO_ {3} ^ { -}] [H ^ {+}]}} {\ rm {[H_ {2} CO_ {3}] + [CO_ {2} (aq)]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d4cac9482fd21cb58444f2621f245d7b1d835485)
Ион бикарбоната представляет собой амфотерный вид, который может действовать как кислота или как основание, в зависимости от pH раствора. При высоком pH он значительно диссоциирует на карбонат ион (CO 3):
В организме происходит образование угольной кислоты катализатором ферментом, карбоангидразой.
CO. 2 являются сильнодействующими электрофил, обладающий электрофильной реакционной способностью, сравнимой с бензальдегидом или сильными α, β-ненасыщенными карбонильными соединениями. В отличие от электрофилов с аналогичной реакционной способностью, нуклеофилов с CO. 2 термодинамически менее предпочтительны и часто оказываются в высокой степени обратимыми. Только очень сильные нуклеофилы, такие как карбанионы, защищаемые реактивами Гриньяра и литийорганическими соединениями, реагируют с CO. 2 образованием карбоксилатов :
In диоксид углерода металла комплексов, CO. 2 служит лигандом , который может превращать CO. 2 в другие химические вещества.
Восстановление CO. 2 на CO обычно сложной и медленной реакцией:
Фотоавтотрофы (т. е. растения и цианобактерии ) используют энергию, содержащаяся в солнечном свете для фотосинтеза простых сахаров из CO. 2, поглощенных из воздуха и воды:
окислительно-восстановительный потенциал для этой реакции pH 7 составляет около -0,53 В по сравнению со стандартным водородным электродом . Никельсодержащий фермент дегидрогеназа монооксида углерода катализирует этот процесс.
 Гранулы «сухого льда», обычная форма твердого диоксида углерода
Гранулы «сухого льда», обычная форма твердого диоксида углерода Диоксид углерода бесцветен При стандартной температуре и давлении плотность диоксида углерода составляет около 1,98. кг / м3, что примерно в 1,67 раза больше плотности воздуха.
Двуокись углерода не имеет жидкого состояния при давлениих ниже 5,1 стандарт. атмосферы (520 кПа). При давлении 1 атмосфера (близкое к среднему давлению на уровне моря) газ осаждается непосредственно в твердое тело при температурех ниже -78,5 ° C (-109,3 ° F; 194,7 K), а твердое вещество возгоняется непосредственно в газе с температурой выше −78,5 ° C. В твердом состоянии диоксида углерода обычно называют сухим льдом.
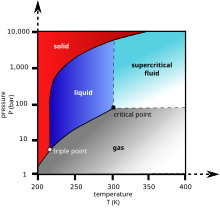 Давление-температура диаграмма состояния диоксида углерода
Давление-температура диаграмма состояния диоксида углерода Жидкий диоксид углерода образуется только при давлениях выше 5,1 банкомат; тройная точка диоксида углерода составляет около 5,1 бар (517 кПа ) при 217 К (см. Фазовую диаграмму). Критическая точка составляет 7,38 МПа при 31,1 ° C. Другой вид твердого диоксида углерода, наблюдаемой при высоком давлении, является аморфное стеклообразное твердое вещество. Эта форма стекла, называемая карбония, производится путем переохлаждения нагретого CO. 2 при экстремальном давлении (40–48 ГПа или около 400000 атмосфер) в алмазная наковальня. Это открытие подтвердило теорию о том, что диоксид углерода может существовать в стеклянном состоянии, аналогичном другим членам его элементного семейства, таким как кремний (кварцевое стекло ) и диоксид германия. Однако, в отличие от кварцевых и германиевых стекол, карбониевое стекло нестабильно при нормальном давлении и превращается в газ при сбросе давления.
При температурах и давлениях выше критической точки диоксид углерода ведет себя как сверхкритический флюид, известный как сверхкритический диоксид углерода.
Диоксид углерода можно получить перегонкой из воздуха, но этот метод неэффективен. В промышленности двуокись углерода представляет собой преимущественно неизвлекаемые отходы, производимые несколькими способами, которые могут применяться в различных масштабах.
сжигание всех углеродных топлив, такие как метан (природный газ ), нефтяные дистилляты (бензин, дизельное топливо, керосин, пропан ), уголь, древесина и обычные органические вещества образуют двуокись углерода и, за исключением чистого углерода, воду. Например, химическая реакция между метаном и кислородом:
Она производится термическим разложением известняка CaCO. 3при нагревании (прокаливание ) при температуре около 850 ° C (1560 ° F) при производстве негашеной извести (оксид кальция, CaO), соединения, которое имеет множество промышленных применений:
Железо восстанавливается из оксидов с помощью кокса в доменной печи, производя чугун и диоксид углерода:
Диоксид углерода является побочным продуктом промышленного производства водорода посредством парового риформинга и реакции конверсии водяного газа в производстве аммиака. Эти процессы начинаются с реакции воды и природного газа (в основном метана). Это основной источник углекислого газа пищевого качества для использования при газировании пива и безалкогольных напитков, а также используется для оглушения животных, таких как домашняя птица. Летом 2018 года в Европе возник дефицит углекислого газа для этих целей из-за временной остановки нескольких аммиачных заводов на техническое обслуживание.
Кислоты высвобождают CO. 2 из большинства карбонатов металлов. Следовательно, он может быть получен непосредственно из природных источников двуокиси углерода источников, где он образуется под действием подкисленной воды на известняк или доломит. Реакция между соляной кислотой и карбонатом кальция (известняком или мелом) показана ниже:
угольная кислота (H. 2CO. 3) затем разлагается на воду и CO. 2:
Такие реакции сопровождаются вспениванием или выделением пузырьков, или и тем, и другим, когда выделяется газ. Они широко используются в промышленности, так как могут использоваться для нейтрализации отработанных кислотных потоков.
Двуокись углерода является побочным продуктом ферментации сахара при пивоварении пива, виски и другие алкогольные напитки и при производстве биоэтанола. Дрожжи метаболизируют сахар с образованием CO. 2 и этанола, также известного как алкоголь, следующим образом:
Все аэробные организмы производят CO. 2, когда они окисляют углеводы, жирные кислоты и белки. Большое количество вовлеченных реакций чрезвычайно сложны и нелегко описать. См. (клеточное дыхание, анаэробное дыхание и фотосинтез ). Уравнение для дыхания глюкозы и других моносахаридов :
Анаэробные организмы разлагают органический материал с образованием метана и двуокись углерода вместе со следами других соединений. Независимо от типа органического материала образование газов следует четко определенной кинетической схеме. Двуокись углерода составляет около 40–45% газа, который выделяется при разложении на свалках (называемый «свалочный газ »). Большая часть остальных 50–55% приходится на метан.
Двуокись углерода используется в пищевой, нефтяной и химической промышленности. Соединение имеет разнообразное коммерческое использование, но одно из самых больших его применений в качестве химического вещества - производство газированных напитков; он придает блеск газированным напиткам, таким как газированная вода, пиво и игристое вино.
В химической промышленности диоксид углерода в основном используется в качестве ингредиента при производстве мочевины, при этом меньшая фракция используется для производства метанол и ряд других товаров. Некоторые производные карбоновых кислот, такие как салицилат натрия, получают с использованием CO. 2 по реакции Кольбе-Шмитта.
В дополнение к обычным процессам с использованием CO. 2 для химического производства, электрохимического методы также изучаются на исследовательском уровне. В частности, использование возобновляемых источников энергии для производства топлива из CO. 2 (например, метанола) является привлекательным, поскольку это может привести к получению топлива, которое можно было бы легко транспортировать и использовать в традиционных технологиях сжигания, но не содержало бы чистого CO. 2.
 Пузырьки двуокиси углерода в безалкогольном напитке.
Пузырьки двуокиси углерода в безалкогольном напитке. Двуокись углерода - это пищевая добавка, используемая в качестве пропеллента и регулятора кислотности в пищевой промышленности. Он одобрен для использования в ЕС (обозначен как E номер E290), США, Австралии и Новой Зеландии (перечислен под своим номером INS 290).
Конфета под названием Pop Rocks находится под давлением углекислого газа примерно 4 × 10 Па (40 бар, 580 фунтов на квадратный дюйм). При помещении в рот он растворяется (как и другие леденцы) и выпускает пузырьки газа с слышимым хлопком.
Разрыхлители заставляют тесто подниматься, выделяя углекислый газ. Пекарские дрожжи производят углекислый газ путем ферментации сахаров в тесте, а химические закваски, такие как разрыхлитель и пищевая сода выделяет двуокись углерода при нагревании или при воздействии кислот.
Двуокись углерода используется для производства газированных безалкогольных напитков и газированная вода. Традиционно карбонизация пива и игристого вина происходила путем естественной ферментации, но многие производители карбонизируют эти напитки углекислым газом, полученным в процессе ферментации. В случае пива в бутылках и кегах наиболее распространенным методом является карбонизация переработанным углекислым газом. За исключением британского настоящего эля, разливное пиво обычно переносится из бочонков в холодильной камере или погребе в разливные краны на баре с помощью углекислого газа под давлением, иногда смешанного с азотом.
Вкус газированной воды (и связанные с ним вкусовые ощущения в других газированных напитках) - это результат растворенного углекислого газа, а не лопнувших пузырьков газа. Карбоангидраза 4 преобразуется в угольную кислоту, что приводит к кислому вкусу, а также растворенный диоксид углерода вызывает соматосенсорный ответ.
 Сухой лед, используемый для сохранения винограда после сбора урожая.
Сухой лед, используемый для сохранения винограда после сбора урожая. Двуокись углерода в форме сухого льда часто используется на этапе виноделия для охлаждения грозди винограда сразу после сбора, чтобы предотвратить спонтанное брожение дикими дрожжами. Основное преимущество использования сухого льда над водяным льдом заключается в том, что он охлаждает виноград без добавления какой-либо дополнительной воды, которая может снизить концентрацию сахара в виноградном сусле, и, следовательно, концентрация алкоголя в готовом вине. Двуокись углерода также используется для создания гипоксической среды для угольной мацерации, процесса, используемого для производства вина Божоле.
Двуокись углерода иногда используется для наполнения винных бутылок или других емкостей для хранения, таких как бочки, для предотвращения окисления, хотя у него есть проблема, заключающаяся в том, что он может растворяться в вине, делая ранее перегонный куб вино слегка газированное. По этой причине профессиональные виноделы предпочитают другие газы, такие как азот или аргон.
Углекислый газ часто используется для «оглушения» животных перед забоем. Термин «оглушение» может быть неправильным, поскольку животные не вырубаются сразу и могут страдать.
Это один из наиболее часто используемых сжатых газов для пневматики (сжатый газ) системы в переносных инструментах под давлением. Двуокись углерода также используется в качестве атмосферы для сварки, хотя в сварочной дуге он реагирует на окисление большинства металлов. Использование в автомобильной промышленности является обычным явлением, несмотря на значительные доказательства того, что сварные швы, выполненные в диоксиде углерода, более хрупкие, чем сварные швы, выполненные в более инертной атмосфере. Он используется в качестве сварочного газа в первую очередь потому, что он намного дешевле, чем более инертные газы, такие как аргон или гелий. При использовании для MIG-сварки использование CO. 2 иногда называют MAG-сваркой для металлического активного газа, поскольку CO. 2 может реагировать при таких высоких температурах. Обычно это приводит к образованию более горячей лужи, чем в действительно инертной атмосфере, что улучшает характеристики потока. Хотя это может быть связано с атмосферными реакциями, происходящими на месте лужи. Обычно это противоположно желаемому эффекту при сварке, так как это приводит к охрупчиванию участка, но может не быть проблемой для обычной сварки низкоуглеродистой стали, где предельная пластичность не является серьезной проблемой.
Он используется во многих потребительских товарах, для которых требуется сжатый газ, потому что он недорогой и негорючий, а также потому, что он претерпевает фазовый переход из газа в жидкость при комнатной температуре и достижимом давлении примерно 60 бар (870 фунтов на квадратный дюйм, 59 атм), позволяя гораздо большему количеству углекислого газа поместиться в данный контейнер, чем в противном случае. Спасательные жилеты часто содержат баллончики с углекислым газом под давлением для быстрого надувания. Алюминиевые капсулы CO. 2 также продаются в качестве запаса сжатого газа для пневматических пистолетов, маркеров / ружей для пейнтбола, накачивания велосипедных шин и для изготовления газированная вода. Быстрое испарение жидкой двуокиси углерода используется для взрывных работ на угольных шахтах. Высокие концентрации углекислого газа также можно использовать для уничтожения вредителей. Жидкий диоксид углерода используется в сверхкритической сушке некоторых пищевых продуктов и технологических материалов, при подготовке образцов для сканирующей электронной микроскопии и в декафеинизации из <468.>кофе в зернах.
 Использование огнетушителя CO. 2.
Использование огнетушителя CO. 2. Для тушения пламени можно использовать углекислый газ, затопив окружающую среду вокруг пламени газом. Сам по себе он не реагирует на гашение пламени, но лишает пламя кислорода, вытесняя его. Некоторые огнетушители, особенно предназначенные для электрических пожаров, содержат жидкий углекислый газ под давлением. Огнетушители с углекислым газом хорошо работают при небольших горючих жидкостях и электрических пожарах, но не при обычных горючих пожарах, потому что, хотя они исключают кислород, они не охлаждают значительно горящие вещества, а когда углекислый газ рассеивается, они могут загореться при воздействии атмосферного кислород. Их желательность при электрическом пожаре проистекает из того факта, что, в отличие от методов на основе воды или других химических веществ, углекислый газ не вызывает коротких замыканий, что приводит к еще большему повреждению оборудования. Поскольку это газ, также легко автоматически распределять большие объемы газа в помещениях ИТ-инфраструктуры, где непосредственно возгорание может быть труднодоступным, поскольку он находится за дверями стойки и внутри шкафов. Углекислый газ также широко используется в качестве огнетушащего вещества в стационарных системах противопожарной защиты для локального применения особых опасностей и полного затопления защищенного пространства. Стандарты Международной морской организации также признают системы углекислого газа для противопожарной защиты судов. трюмы и машинные отделения. Системы противопожарной защиты на основе двуокиси углерода были связаны с несколькими смертельными случаями, поскольку в достаточно высоких концентрациях они могут вызвать удушье. Обзор систем CO. 2 выявил 51 инцидент между 1975 и датой отчета (2000), в результате чего 72 человека погибли и 145 были ранены.
Жидкий диоксид углерода является хорошим растворителем для многих липофильных органических соединений и используется для удаления кофеина из кофе. Углекислый газ привлек внимание в фармацевтической и других отраслях химической промышленности как менее токсичная альтернатива более традиционным растворителям, таким как хлорорганические соединения. По этой причине он также используется некоторыми химчистками (см. зеленая химия ). It is used in the preparation of some aerogels because of the properties of supercritical carbon dioxide.
Plants require carbon dioxide to conduct photosynthesis. The atmospheres of greenhouses may (if of large size, must) be enriched with additional CO. 2 to sustain and increase the rate of plant growth. At very high concentrations (100 times atmospheric concentration, or greater), carbon dioxide can be toxic to animal life, so raising the concentration to 10,000 ppm (1%) or higher for several hours will eliminate pests such as whiteflies and spider mites in a greenhouse.
In medicine, up to 5% carbon dioxide (130 times atmospheric concentration) is added to oxygen for stimulation of breathing after apnea and to stabilize the O. 2/CO. 2balance in blood.
Carbon dioxide can be mixed with up to 50% oxygen, forming an inhalable gas; this is known as Carbogen and has a variety of medical and research uses.
Carbon dioxide is used in enhanced oil recovery where it is injected into or adjacent to producing oil wells, usually under сверхкритические условия, когда становится смешиваемым с маслом. Этот подход может увеличить исходную нефтеотдачу за счет снижения остаточной нефтенасыщенности на 7–23% в дополнение к первичной добыче. Он действует как агент, повышающий давление, и, будучи растворенным в подземной сырой нефти, значительно снижает ее вязкость и изменяет химический состав поверхности, позволяя нефти быстрее проходить через пласт к скважине для удаления. На зрелых месторождениях нефти используются разветвленные трубопроводные сети для транспортировки углекислого газа к точкам закачки.
В улучшенном извлечении метана из угольных пластов диоксид углерода будет закачиваться в угольный пласт для вытеснения метана, в отличие от существующих методов, которые в первую очередь основаны на удалении воды (для снижения давления) чтобы заставить угольный пласт высвободить захваченный метан.
Было предложено, чтобы CO. 2 от выработки электроэнергии подавался в пруды, чтобы стимулировать рост водорослей, которые могут затем преобразовать в биодизельное топливо. Штамм цианобактерии Synechococcus elongatus был генетически модифицирован для производства топлива изобутиральдегид и изобутанол из CO. 2 с помощью фотосинтеза..
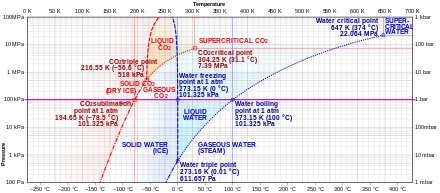 Сравнение фазовых диаграмм диоксида углерода (красный) и воды (синий) в виде логарифмической диаграммы с точками фазовых переходов при 1 атмосфере
Сравнение фазовых диаграмм диоксида углерода (красный) и воды (синий) в виде логарифмической диаграммы с точками фазовых переходов при 1 атмосфере Жидкий и твердый диоксид углерода важны хладагенты, особенно в пищевой промышленности, где они используются при транспортировке и хранении мороженого и других замороженных продуктов. Твердый диоксид углерода называется «сухим льдом» и используется для небольших грузов, где холодильное оборудование нецелесообразно. Твердый диоксид углерода всегда ниже −78,5 ° C (−109,3 ° F) при обычном атмосферном давлении, независимо от температуры воздуха.
Жидкий диоксид углерода (промышленная номенклатура R744 или R-744) использовался в качестве хладагента до открытия R-12 и может пережить возрождение из-за того, что R134a способствует изменению климата больше, чем CO. 2. Его физические свойства очень подходят для целей охлаждения, охлаждения и нагрева, имея высокую объемную охлаждающую способность. Из-за необходимости работать при давлениях до 130 бар (1880 psi ), системы CO. 2 требуют высокопрочных компонентов, которые уже были разработаны для массового производства во многих странах. секторов. В автомобильном кондиционировании воздуха более чем в 90% всех условий движения на широтах выше 50 ° R744 работает более эффективно, чем системы, использующие R134a. Его экологические преимущества (GWP из 1, не разрушающий озоновый слой, нетоксичный, невоспламеняющийся) могут сделать его будущей рабочей жидкостью для замены существующих ГФУ в автомобилях, супермаркетах и водонагревателях с тепловыми насосами, среди прочего. другие. Coca-Cola представила охладители напитков на основе CO. 2 и США. Армия интересуется технологией охлаждения и обогрева CO. 2.
Ожидается, что мировая автомобильная промышленность примет решение о выборе хладагента нового поколения для автомобильного кондиционирования воздуха. CO. 2 - один из обсуждаемых вариантов. (См. Экологичное автомобильное кондиционирование воздуха использует )
 A углекислый лазер.
A углекислый лазер.Углекислый газ является лазерной средой в углекислый лазер, который одним из самых ранних
Углекислый газ можно использовать в средствах контроля pH плавательных бассейнов путем непрерывного добавления газа в воду, тем самым предотвращая повышение pH. Точно так же он также используется при содержании рифовых аквариумов, где он обычно используется в кальциевые реакторы для временного понижения pH воды, пропускаемой через карбонат кальция Чтобы использовать карбонату кальция более свободно растворяться в воде там, где он используется для построения их скелета, используется
Используется в качестве теплоносителя первого контура в воде усовершенствованного реактора с газовым охлаждением для производства ядерной энергии.
Углеродный диоксид xide индукция обычно используется для эвтаназии лабораторных животных. Способы введения CO. 2 включают в себя помещение животных непосредственно в закрытую, содержащую CO. 2, или постепенно увеличивающую среду CO. 2. В 2013 году Американская ветеринарная медицинская ассоциация выпустила новое руководство по индукции углекислого газа, в котором говорится, что скорость вытеснения от 30% до 70% объема газовой камеры в минуту является оптимальной для гуманной эвтаназии мелких грызунов. Однако есть возражения против практики использования диоксида углерода для этого на том основании, что это жестоко.
Диоксид углерода также используется в нескольких связанных методх очистки и подготовки поверхности.
 Кривая Килинга атмосферных концентраций CO. 2, измеренных в обсерватории Мауна-Лоа
Кривая Килинга атмосферных концентраций CO. 2, измеренных в обсерватории Мауна-Лоа Углекислый газ в атмосфере Земли - это следовой газ, в настоящее время (начало 2020 г.) имеющий глобальную среднюю концентрацию 412 частей на миллион по объему (или 622 частей на миллион по массе). Концентрации углекислого газа в атмосфере незначительно колеблются в зависимости от, падая в течение Северного полушария весной и летом, когда растения потребляют газ, и повышаются в течение периода северной осени и зимы, когда растения уходят в спячку или разлагаются. Концентрации также существуют в зависимости от региона, наиболее сильно у земли с гораздо меньшими вариациями на высоте. В городских районах обычно выше, а в городских районах достигается 10-кратного фонового уровня.
 Ежегодное увеличение содержания CO в атмосфере. 2: В 1960-е годы среднегодовое увеличение составляло 35% от среднего показателя за 2009-2018 годы.
Ежегодное увеличение содержания CO в атмосфере. 2: В 1960-е годы среднегодовое увеличение составляло 35% от среднего показателя за 2009-2018 годы. Концентрация углекислого газа выросла из-за деятельности человека. Сжигание ископаемого топлива и обезлесение привело к концентрации углекислого газа в атмосфере примерно на 43% с начала эпохи индустриализации . Большая часть углекислого газа в результате деятельности человека выделяется при сжигании угля и других ископаемых видов топлива. Другая деятельность человека, включая вырубку лесов, сжигание биомассы и производство цемента, также производит углекислый газ. Человеческая деятельность выбрасывает около 29 миллиардов тонн углекислого газа в год, а вулканы - от 0,2 до 0,3 миллиарда тонн. Человеческая деятельность привела к тому, что CO. 2 поднялся выше уровня, невиданных за сотни тысяч лет. В настоящее время около половины углекислого газа, выделяемого в результате сжигания ископаемого топлива, остается в атмосфере и не поглощается растительностью и океанами.
Хотя прозрачный для видимый свет, углекислый газ - это парниковый газ, поглощающий и испускающий инфракрасное излучение на своих двух активных инфракрасных частотах колебаний (см. Раздел «Структура и связь »над). Световое излучение земной поверхности наиболее интенсивно в инфракрасной области между 200 и 2500 см, отличие от наиболее интенсивно в инфракрасной области. Поглощение инфракрасного света на частотах атмосферного углекислого газа улавливает энергию у поверхности, нагревая поверхность и нижние слои атмосферы. Меньше энергии демонстрирует верхних слоев атмосферы, которая из-за этого становится более прохладными. Повышение уровня в атмосфере CO. 2 и других долгоживущих парниковых газов, как метан, закись азота и озон, соответственно усилило их поглощение и испускание инфракрасного излучения, что привело к повышению средней глобальной температуры с середины 20 века. Увеличивает срок службы в атмосфере, оказывает большее влияние на общее потепление, чем все эти другие газы вместе взятые, и, что он имеет длительный срок службы в атмосфере (от сотен до тысяч лет).
 CO. 2 в атмосфере Земли , если половина химических элементов глобального потепления не поглощается.. (NASA компьютерное моделирование ).
CO. 2 в атмосфере Земли , если половина химических элементов глобального потепления не поглощается.. (NASA компьютерное моделирование ).Увеличение углекислого газа не только приводит к повышению глобальной температуры поверхности, но повышение глобальной температуры также приводит к повышению концентрации углекислого газа. обратная связь для изменений, вызванных другими процессами, такими как орбитальные циклы. Пятьсот миллионов лет назад углекислого газа было в 20 раз выше, чем сегодня, уменьшаясь до 4–5 раз в юрского периода, а затем медленно снижаясь с особенно быстрым снижением произошедшие 49 лет назад.
Местные концентрации углекислого газа достигли высоких показателей сильных источников, тех, которые изолированы окружающую среду На горячих источниках Босолето около Раполано Терме в Тоскане, Италия, расположен в чашеобразной впадине около 100 м (330 футов) в диаметре, содержит CO. 2 за ночь повышаются до более 75%, что достаточно для уничтожения насекомых и мелких животных. После восхода солнца газ рассеивается конвекцией. Считается, что высокие уровни CO. 2, образовавшиеся в результате нарушения водоемов глубокого озера, насыщенного CO. 2, стали причиной 37 погибших в озере Монун, Камерун в 1984 и 1700 лет. жертвы на озере Ниос, Камерун в 1986 году.
 панцирь птерапода, растворенный в морской воде, с поправкой на химический состав океана, прогнозируемый на 2100 год.
панцирь птерапода, растворенный в морской воде, с поправкой на химический состав океана, прогнозируемый на 2100 год. Двуокись углерода растворяется в океане с образованием угольной кислоты (H2CO3), бикарбоната (HCO 3) и карбоната (CO 3). В океане растворено примерно в пятьдесят раз больше углекислого газа, чем в атмосфере. Окианы как огромный поглотитель углерода и поглощают около трети CO. 2, выбрасываемого в результате деятельности человека.
Углекислого газа в атмосфере увеличивает, Повышенное поглощение углекислого газа вызывает ощутимое снижение pH океанов, что называется закислением океана. Это снижение pH влияет на биологические системы в океанах, в первую очередь на океанические кальцифицирующие организмы. Эти эффекты охватывают пищевую цепочку от автотрофов до гетеротрофов и включают такие организмы, как кокколитофориды, кораллы, фораминиферы, иглокожие, ракообразные и моллюски. При нормальных условиях карбонат кальция стабилен в поверхностных водах, так как карбонат-ион находится в перенасыщающей концентрации. Однако, когда уровень pH в океане падает, его структура становится уязвимыми, и карбонат становится недонасыщенным. Кораллы, кокколитофоридные водоросли, кораллиновые водоросли, фораминиферы, моллюски и pteropods испытывают меньшую кальцификацию или повышенное растворение при воздействии повышенного содержания CO. 2.
. Глубокие геотермальные жерл, увеличивающиеся до глубины 393 К, показывают только глубокие геотермальные воды, и, следовательно, скорость из воздуха снижается с повышением температуры океана.
Большая часть CO. 2, поглощаемого океаном, что составляет около 30% от общего количества, выбрасываемого в атмосферу, образует угольную кислоту в равновесии с бикарбонатом. Некоторые из этих химических веществ потребляются фотосинтезирующими организмами, которые удаляют из круговорота. Повышенное содержание CO. 2 в атмосфере привело к снижению щелочности морской воды, и есть опасения, что это может отрицательно повлиять на организмы, живущие в воде. В частности, с уменьшением щелочности уменьшается доступность карбонатов для образования раковин, хотя есть свидетельства увеличения производства некоторых видов приточного содержания CO. 2.
NOAA заявляет в своем документе «Состояние научный бюллетень по подкислению океана », который:. «Океаны поглотили около 50% углекислого газа (CO. 2), выделяющегося при сжигании ископаемого топлива, что привело к химическим реакциям это более низкое значение pH океана. Это к увеличению содержания водорода (кислоты) примерно на 30% из начала индустриальной эпохи в результате процесса, известного как «подкисление океана». Растущее число испытаний на испытания на морские организмы, в том числе:
Кроме того, Межправительственная группа экспертов по изменению климата (МГЭИК) пишет в своем «Изменение климата 2007: сводный доклад»:. «Освоение антропогенного углерода с 1750 года привел к, что океан стал более кислым со средним снижением pH на 0,1 единицы. Повышение концентрации CO. 2 в атмосфере к дальнейшему подкислению... В то время как влияние наблюдаемого закисления океана на морскую биосферу еще не подтверждено документально, ожидается, что прогрессирующее закисление океанов неожидетное воздействие на морские ракушечные организмы (например, кораллы) и зависимые от них виды ».
Некоторые морские кальцифицирующие организмы (включая коралловые рифы) были выделены крупными исследовательскими агентствами, включая NOAA, комиссию OSPAR, NANOOS и IPCC, поскольку их исследования показывают, что следует ожидать, что закисление океана может вызвать негативное воздействие.
Двуокись углерода также попадает в океаны через гидротермальные источники. Гидротермальный источник Шампань, обнаруженный на северо-западе вулкана Эйфуку в Марианской впадине, производит почти чистый жидкий углекислый газ, одно из двух известных мест в мире по состоянию на 2004 год, другое находится в Окинавском желобе. Обнаружение подводного жидкого озера О двуокиси углерода в Окинавском желобе сообщалось в 2006 году.
Углекислый газ является конечным продуктом клеточного дыхания в организме, которые получают энергию за счет расщепления сахаров, жиры и аминокислоты с кислородом как часть их метаболизма. Сюда входят все растения, водоросли и животные, а также аэробные грибы и бактерии. У позвоночных углекислый газ перемещается с кровью из тканей тела в кожу (например, земноводные ) или в жабры (например, рыбы ), от где он растворяется в воде или в легкие, откуда он выдыхается. Во время активного фотосинтеза растения могут поглощать из атмосферы больше углекислого газа, чем выделяются при дыхании.
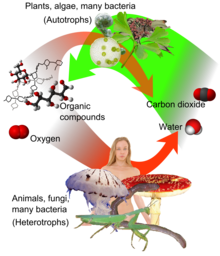 Обзор фотосинтеза и дыхания. Двуокись углерода (справа) вместе с водой образуют кислород и органические соединения () посредством фотосинтеза, которые могут быть вдыхаемыми в воде и (CO. 2).
Обзор фотосинтеза и дыхания. Двуокись углерода (справа) вместе с водой образуют кислород и органические соединения () посредством фотосинтеза, которые могут быть вдыхаемыми в воде и (CO. 2). 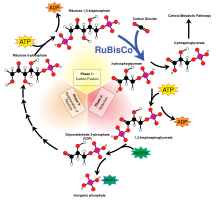 Обзор цикла Кальвина и фиксации углерода
Обзор цикла Кальвина и фиксации углерода Фиксация углерода - это биохимический процесс, посредством которого атмосферный углекислый газ включается в растения, водоросли и (цианобактерии ) в богатые энергией органические молекулы, такие как глюкоза, таким образом создавая себе пищу путем фотосинтеза.. Фотосинтез использует двуокись углерода и воду для производства сахаров, из других источников органические соединения, а кислород образует как побочный товар.
Рибулозо-1,5-бисфосфаткарбоксилаза-оксигеназа, обычно сокращенно RuBisCO, представляет собой фермент, участвующий в первой основной стадии фиксации углерода, в производстве двух молекул 3 -фосфоглицерат из CO. 2 и рибулозобисфосфат, как показано на диаграмме слева.
RuBisCO считается самым распространенным белком на Земле.
Фототрофы используют продукты своего фотосинтеза в качестве внутренних источников питания и сырья для биосинтеза более сложные органические молекулы, такие как полисахариды, нуклеиновые кислоты и белки. Они используются для собственного роста, а также в качестве цепей пищевых цепей и сетей, питающих другие организмы, включая таких животных, как мы. Некоторые важные фототрофы, кокколитофориды, синтезируют твердую чешуйку карбоната кальция. Глобально значимым видом кокколитофорид является Emiliania huxleyi, чьи чешуйки кальцита сформировали основу многих осадочных пород, таких как известняк, где что ранее атмосферный углерод может оставаться фиксированным в геологических масштабах времени.
При использовании 1000 ppm CO. 2 растения могут расти на 50 процентов быстрее по сравнению с окружающими условиями, хотя это предполагает отсутствие изменений и отсутствие ограничений на другие питательные вещества. Повышенные уровни CO. 2 вызывают повышенный рост, отражающийся в урожайности сельскохозяйственных культур, причем пшеница, рис и соя демонстрируют увеличение урожайности на 12–14% при повышенном CO. 2 в экспериментах FACE.
Повышенные концентрации CO. 2 в атмосфере приводят к уменьшению расхода воды и повышению эффективности водопользования. Использование с использованием FACE продемонстрировало, что обогащение CO. 2 приводит к концентрации концентраций питательных микроэлементов в образовании. Это может иметь косвенные последствия для других частей экосистем, поскольку травоядным нужно будет больше пищи, чтобы получить такое же количество белка.
Концентрация вторичных метаболитов такие как фенилпропаноиды и флавоноиды также могут изменяться в растениях, подвергающихся воздействию высоких концентраций CO. 2.
Растения также выделяют CO. 2 во время дыхания, и поэтому большинство растений и водорослей, которые используют C3-фотосинтез, днем служат только чистые поглотители. Хотя растущий лес будет поглощать много тонн CO. 2 каждый год, зрелый лес будет производить столько же CO. 2 в результате дыхания и разложения мертвых особей (например, упавших веток), сколько используется в фотосинтезе растущих растений.. Вопреки давно устоявшемуся мнению, что они углеродно-нейтральные, зрелые леса могут продолжать накапливать углерод и оставаться ценными поглотителями углерода, помогая поддерживать углеродный баланс атмосферы Земли. Кроме того, что крайне важно для жизни на Земле, фотосинтез фитопланктона потребляет растворенный CO. 2 в верхних слоях океана и тем самым способствует поглощению CO. 2 из атмосферы.
 Основные симптомы токсичности углекислого газа за счет увеличения объемных процентов в воздухе.
Основные симптомы токсичности углекислого газа за счет увеличения объемных процентов в воздухе. Содержание углекислого газа в свежем воздухе (усредненное между уровнем моря и уровнем 10 кПа, т. е. на высоте около 30 км (19 миль)) варьируется от 0,036% (360 частей на миллион) до 0,041% (412 частей на миллион), в зависимости от местоположения.
CO. 2 представляет собой удушающий газ и не классифицируется как токсичный или вредный в соответствии с согласованной на глобальном уровне системой стандартов классификации и маркировки химических веществ из Европейской экономической комиссии Организации Объединенных Наций с использованием Руководства ОЭСР по тестированию химических веществ. В концентрациях до 1% (10 000 ppm) он вызывает у некоторых людей сонливость и ощущение заложенности в легких. Концентрации от 7% до 10% (от 70 000 до 100 000 частей на миллион) могут вызвать удушье даже при наличии достаточного количества кислорода, проявляясь в виде головокружения, головной боли, нарушения функции зрения и слуха и потери сознания в течение от нескольких минут до часа. Физиологические эффекты острого воздействия углекислого газа сгруппированы вместе под термином гиперкапния, подмножество удушья.
, потому что он тяжелее воздуха в местах, где газ просачивается из-под земли (из-за к подповерхностной вулканической или геотермальной активности) в относительно высоких концентрациях, без рассеивающего воздействия ветра, он может накапливаться в защищенных / карманных местах ниже среднего уровня земли, вызывая удушение находящихся там животных. Затем убивают тех, кто поедает падаль, привлеченных к тушам. Таким же образом погибли дети недалеко от города Гома из-за выбросов CO. 2 из соседнего вулкана Mt. Ньирагонго. На языке суахили это явление обозначается как «мазуку ».
 Повышение уровня CO. 2 угрожало астронавтам Аполлона 13, которым пришлось адаптировать патроны из командного модуля для снабжения скруббера углекислого газа в лунном модуле, который они используется в качестве спасательной шлюпки.
Повышение уровня CO. 2 угрожало астронавтам Аполлона 13, которым пришлось адаптировать патроны из командного модуля для снабжения скруббера углекислого газа в лунном модуле, который они используется в качестве спасательной шлюпки. У людей происходит адаптация к повышенным концентрациям CO. 2, включая измененное дыхание и выработку бикарбоната в почках, чтобы сбалансировать эффекты закисления крови (ацидоз ). Несколько исследований показали, что 2,0% вдыхаемой концентрации можно использовать для закрытых воздушных пространств (например, подводная лодка ), поскольку адаптация является физиологической и обратимой, поскольку ухудшение работоспособности или нормальной физической активности не происходит на этом уровне выдержка в течение пяти дней. Тем не менее, другие исследования показывают снижение когнитивной функции даже на гораздо более низких уровнях. Кроме того, при продолжающемся респираторном ацидозе адаптационные или компенсаторные механизмы не смогут изменить это состояние..
Существует мало исследований воздействия на здоровье длительного длительного воздействия CO. 2 воздействие на людей и животных на уровнях ниже 1%. Пределы воздействия CO. 2 на рабочем месте были установлены в США на уровне 0,5% (5000 частей на миллион) в течение восьмичасового периода. При такой концентрации CO. 2 экипаж Международной космической станции испытывал головные боли, летаргию, замедленное умственное развитие, эмоциональное раздражение и нарушение сна. Исследования на животных при 0,5% CO. 2 продемонстрировали кальцификацию почек и потерю костной массы после восьми недель воздействия. Исследование людей, подвергшихся воздействию в течение 2,5-часовых сеансов, продемонстрировало значительные отрицательные эффекты на когнитивные способности при таких низких концентрациях, как 0,1% (1000 ppm) CO. 2, вероятно, из-за индуцированного CO. 2 увеличения церебрального кровотока. В другом исследовании наблюдалось снижение базового уровня активности и использования информации при 1000 ppm по сравнению с 500 ppm.
 CO. 2 измеритель концентрации с использованием недисперсного инфракрасного датчика
CO. 2 измеритель концентрации с использованием недисперсного инфракрасного датчика Плохо вентиляция - одна из основных причин чрезмерной концентрации CO. 2 в закрытых помещениях. Дифференциал углекислого газа выше наружных концентраций в устойчивых условиях (когда рабочая среда и система вентиляции достаточно продолжительны, чтобы концентрация CO. 2 стабилизировалась) иногда используется для оценки интенсивности вентиляции на человека. Более высокие концентрации CO. 2 связаны со здоровьем людей, их комфортом и ухудшением рабочих характеристик. ASHRAE Нормы вентиляции по стандарту 62.1–2007 могут привести к концентрациям в помещении на 2100 ppm выше окружающих условий снаружи. Таким образом, если концентрация на открытом воздухе составляет 400 частей на миллион, концентрация в помещении может достигать 2500 частей на миллион при скорости вентиляции, соответствующей данному отраслевому стандарту. Концентрации в плохо вентилируемых помещениях могут быть даже выше (диапазон от 3000 до 4000).
Шахтеры, которые особенно уязвимы для воздействия газа из-за недостаточной вентиляции, называли смеси углекислого газа и азота «blackdamp », «дроссельной заслонкой» или «стилусом». До того, как были разработаны более эффективные технологии, горняки часто отслеживали опасные уровни черной влаги и других газов в шахтных стволах, принося с собой в клетку канарейку во время работы. Канарейка более чувствительна к удушающим газам, чем люди, и когда она теряла сознание, перестала петь и падала с насеста. лампа Дэви может также обнаруживать высокие уровни черной влаги (которая тонет и собирается у пола) за счет менее яркого горения, в то время как метан, другой удушающий газ и опасность взрыва, может вызвать лампы горят ярче.
В феврале 2020 года три человека умерли от удушья на вечеринке в Москве, когда в бассейн добавили сухой лед (замороженный CO2) для его охлаждения.
| кПа | мм рт.ст. | |
|---|---|---|
| Венозный углекислый газ в крови | 5,5–6,8 | 41–51 |
| Альвеолярное легочное. давление газа | 4,8 | 36 |
| Углекислый газ артериальной крови | 4,7–6,0 | 35–45 |
Организм вырабатывает приблизительно 2,3 фунта (1,0 кг) углекислого газа в день на человека, содержащего 0,63 фунта (290 г) углерода. У людей этот углекислый газ переносится через венозную систему и выдыхается через легкие, что приводит к более низким концентрациям в артериях. Содержание углекислого газа в крови часто выражается как парциальное давление, которое представляет собой давление, которое имел бы двуокись углерода, если бы она одна занимала весь объем. У людей содержание углекислого газа в крови показано в соседней таблице:
CO. 2 переносится кровью тремя различными путями. (Точные проценты варьируются в зависимости от того, артериальная это кровь или венозная).
Гемоглобин, основная молекула, переносящая кислород в красных кровяных тельцах, переносит как кислород, так и углекислый газ. Однако CO. 2, связанный с гемоглобином, не связывается с тем же участком, что и кислород. Вместо этого он соединяется с N-концевыми группами на четырех цепях глобина. Однако из-за аллостерического воздействия на молекулу гемоглобина связывание CO. 2 снижает количество кислорода, связанного при заданном парциальном давлении кислорода. Это известно как эффект Холдейна и играет важную роль в транспортировке углекислого газа из тканей в легкие. И наоборот, повышение парциального давления CO. 2 или более низкое значение pH вызовут выгрузку кислорода из гемоглобина, что известно как эффект Бора.
Двуокись углерода. является одним из медиаторов локальной ауторегуляции кровоснабжения. Если его концентрация высока, капилляры расширяются, обеспечивая больший приток крови к этой ткани.
Ионы бикарбоната имеют решающее значение для регулирования pH крови. Частота дыхания человека влияет на уровень CO. 2 в его крови. Слишком медленное или поверхностное дыхание вызывает респираторный ацидоз, в то время как слишком быстрое дыхание приводит к гипервентиляции, которая может вызвать респираторный алкалоз.
Хотя организму требуется кислород для метаболизм, низкий уровень кислорода обычно не стимулирует дыхание. Скорее, дыхание стимулируется повышенным уровнем углекислого газа. В результате вдыхание воздуха низкого давления или газовой смеси без кислорода (например, чистого азота) может привести к потере сознания без чувства голода . Это особенно опасно для летчиков-высотников. Именно поэтому бортпроводники инструктируют пассажиров в случае потери давления в салоне, прежде чем помогать другим, надеть на себя кислородную маску ; в противном случае существует риск потери сознания.
Дыхательные центры пытаются поддерживать артериальное давление CO. 2 на уровне 40 мм рт. При преднамеренной гипервентиляции содержание CO. 2 в артериальной крови может быть снижено до 10–20 мм рт. Ст. (Содержание кислорода в крови мало затронуто), а дыхательная активность снижается. Вот почему после гипервентиляции можно задерживать дыхание дольше, чем без гипервентиляции. Это сопряжено с риском потери сознания до того, как потребность дышать станет непреодолимой, поэтому гипервентиляция особенно опасна перед фридайвингом.
| Викискладе есть носители, связанные с двуокисью углерода. |