Ртуть является химическим элементом с символом Hg и атомным номером 80. Это обычно известные как ртуть, и ранее был им Hydrargyrum ( / ч aɪ d г ɑːr dʒ ər ə м / гигиеническое DRAR -jər-əm ). Тяжелый, серебристый д-блок элемент, ртуть является единственным металлическим элементом, который находится в жидком состоянии при стандартных условиях температуры и давлении ; единственный другой элемент, который находится в жидком состоянии при этих условиях является галоген брома, хотя металлы, таких как цезий, галлий, и рубидий расплава чуть выше комнатной температуры.
Ртуть встречается в месторождениях по всему миру в основном в виде киновари ( сульфида ртути ). Красный пигмент киноварь получают путем измельчения натуральной киновари или синтетического сульфида ртути.
Ртуть используется в термометрах, барометрах, манометрах, сфигмоманометрах, поплавковых клапанах, ртутных переключателях, ртутных реле, люминесцентных лампах и других устройствах, хотя опасения по поводу токсичности элемента привели к тому, что ртутные термометры и сфигмоманометры в значительной степени отказались от использования в клинических условиях в пользу альтернативы, такие как стеклянные термометры, наполненные спиртом или галинстаном, и термистор, или электронные приборы на основе инфракрасного излучения. Точно так же механические манометры и электронные тензометрические датчики заменили ртутные сфигмоманометры.
Ртуть по-прежнему используется в научных исследованиях и в некоторых регионах в амальгаме для восстановления зубов. Он также используется в люминесцентном освещении. Электричество, пропущенное через пары ртути в люминесцентной лампе, производит коротковолновый ультрафиолетовый свет, который затем вызывает флуоресценцию люминофора в трубке, создавая видимый свет.
Отравление ртутью может быть результатом воздействия водорастворимых форм ртути (таких как хлорид ртути или метилртути ), вдыхания паров ртути или проглатывания ртути в любой форме.
 Фунт монета (плотность \ 7,6 г / см 3) плавает на ртуть из - за сочетание выталкивающей силы и поверхностным натяжение.
Фунт монета (плотность \ 7,6 г / см 3) плавает на ртуть из - за сочетание выталкивающей силы и поверхностным натяжение. Ртуть - тяжелый жидкий металл серебристо-белого цвета. По сравнению с другими металлами, это плохой проводник тепла, но хороший проводник электричества.
Он имеет температуру замерзания -38,83 ° C и точку кипения 356,73 ° C, оба являются самыми низкими из всех стабильных металлов, хотя предварительные эксперименты с коперницием и флеровием показали, что они имеют еще более низкие температуры кипения (коперниций является элементом ниже ртути. в периодической таблице, следуя тенденции снижения точки кипения вниз по группе 12). При замораживании объем ртути уменьшается на 3,59%, а ее плотность изменяется с 13,69 г / см 3 в жидком состоянии до 14,184 г / см 3 в твердом состоянии. Коэффициент объемного расширения составляет 181,59 × 10 -6 при 0 ° C, 181,71 × 10 -6 при 20 ° С и 182,50 × 10 -6 при 100 ° С (в ° С). Твердая ртуть податлива и пластична, и ее можно разрезать ножом.
Полное объяснение чрезвычайной летучести ртути глубоко погружается в сферу квантовой физики, но его можно резюмировать следующим образом: ртуть имеет уникальную электронную конфигурацию, в которой электроны заполняют все доступные 1s, 2s, 2p, 3s, 3p, 3d, 4s., 4p, 4d, 4f, 5s, 5p, 5d и 6s подоболочки. Поскольку эта конфигурация сильно сопротивляется удалению электрона, ртуть ведет себя аналогично благородным газам, которые образуют слабые связи и, следовательно, плавятся при низких температурах.
Устойчивость оболочки 6s обеспечивается наличием заполненной оболочки 4f. Оболочка f плохо экранирует заряд ядра, что увеличивает притягивающее кулоновское взаимодействие оболочки 6s и ядра (см. Сжатие лантаноидов ). Отсутствие заполненной внутренней f-оболочки является причиной несколько более высокой температуры плавления кадмия и цинка, хотя оба эти металла все еще легко плавятся и, кроме того, имеют необычно низкие температуры кипения.
Ртуть не реагирует с большинством кислот, таких как разбавленная серная кислота, хотя окисляющие кислоты, такие как концентрированная серная кислота и азотная кислота или царская водка, растворяют ее с образованием сульфата, нитрата и хлорида. Как и серебро, ртуть реагирует с атмосферным сероводородом. Ртуть вступает в реакцию с твердыми хлопьями серы, которые используются в наборах для разлива ртути для поглощения ртути (в наборах для разлива также используется активированный уголь и порошкообразный цинк).
 Лампа калибровочная спектральная ртутно-разрядная
Лампа калибровочная спектральная ртутно-разрядная Ртуть растворяет многие металлы, такие как золото и серебро, с образованием амальгам. Железо является исключением, и железные колбы традиционно использовались для торговли ртутью. Некоторые другие переходные металлы первого ряда, за исключением марганца, меди и цинка, также устойчивы к образованию амальгам. Другие элементы, которые не образуют амальгамы с ртутью, включают платину. Амальгама натрия является обычным восстановителем в органическом синтезе, а также используется в натриевых лампах высокого давления.
Ртуть легко соединяется с алюминием с образованием ртуть-алюминиевой амальгамы, когда два чистых металла вступают в контакт. Поскольку амальгама разрушает слой оксида алюминия, который защищает металлический алюминий от глубокого окисления (как при ржавлении железа), даже небольшое количество ртути может серьезно повредить алюминий. По этой причине в большинстве случаев ртуть не допускается на борт самолета из-за риска образования амальгамы с открытыми алюминиевыми частями самолета.
Охрупчивание ртутью является наиболее распространенным типом охрупчивания жидким металлом.
Есть семь стабильных изотопов ртути, с202 Наиболее распространена Hg (29,86%). Самыми долгоживущими радиоизотопами являются194 Hg с периодом полураспада 444 года, и203 Hg с периодом полураспада 46,612 дней. Большинство оставшихся радиоизотопов имеют период полураспада менее суток.199 Hg и201 Hg - наиболее часто изучаемые ЯМР- активные ядра со спинами 1 ⁄ 2 и 3 ⁄ 2 соответственно.
«Hg» - это современный химический символ ртути. Он поставляется с ртуть, Латинизируется форма древнегреческого слова ὑδράργυρος ( hydrargyros), который представляет собой сложное слово, означающее «вода-серебро» (от ὑδρ - ( гидр -), корень ὕδωρ «воды», и ἄργυρος ( Argyros) 'silver'), поскольку он жидкий, как вода, и блестящий, как серебро. Элемент был назван в честь римского бога Меркурия, известного своей скоростью и подвижностью. Он связан с планетой Меркурий ; астрологический символ планеты также является одним из алхимических символов металла. Ртуть - единственный металл, для которого алхимическое планетарное название стало общепринятым.
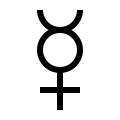 Символ планеты Меркурий (☿) использовался с древних времен для обозначения элемента.
Символ планеты Меркурий (☿) использовался с древних времен для обозначения элемента. Меркурий был найден в египетских гробницах, датируемых 1500 годом до нашей эры.
В Китае и Тибете считалось, что использование ртути продлевает жизнь, лечит переломы и поддерживает в целом хорошее здоровье, хотя теперь известно, что воздействие паров ртути приводит к серьезным неблагоприятным последствиям для здоровья. Первый император объединенного Китая Цинь Шоу Хуан Ди - якобы похороненный в гробнице, в которой текли реки ртути на модели страны, которой он правил, представителя рек Китая, - как сообщается, был убит, выпив ртуть и порошкообразный нефрит. смесь, разработанная алхимиками Цинь, задуманная как эликсир бессмертия. Хумаравайх ибн Ахмад ибн Тулун, второй тулунидский правитель Египта (годы правления 884–896), известный своей экстравагантностью и расточительностью, как сообщается, построил чашу, наполненную ртутью, в которой он лежал на наполненных воздухом подушках и качался. спать.
В ноябре 2014 года «большие количества» ртути были обнаружены в камере на 60 футов ниже 1800-летней пирамиды, известной как « Храм Пернатого Змея », «третьей по величине пирамиды Теотиуакана » в Мексике вместе с нефритовыми статуями., останки ягуара, ящик, наполненный резными ракушками и резиновыми шарами ».
В древних греках использовали киноварь (ртутная сульфид) в мазях; древние египтяне и римляне использовали его в косметике. В Ламанаи, когда-то крупном городе цивилизации майя, лужа ртути была обнаружена под маркером на мезоамериканской площадке для игры в мяч. К 500 г. до н.э. ртуть использовалась для изготовления амальгам (средневековая латинская амальгама, «сплав ртути») с другими металлами.
Алхимики считали ртуть первой материей, из которой образовались все металлы. Они считали, что различные металлы можно производить, варьируя качество и количество серы, содержащейся в ртути. Самым чистым из них было золото, и ртуть использовалась в попытках трансмутации основных (или нечистых) металлов в золото, что было целью многих алхимиков.
Рудники в Альмадене (Испания), Монте-Амиата (Италия) и Идрия (ныне Словения) доминировали в производстве ртути с момента открытия рудника в Альмадене 2500 лет назад до открытия новых месторождений в конце XIX века.
Ртуть - чрезвычайно редкий элемент в земной коре, ее среднее содержание в коре по массе составляет всего 0,08 частей на миллион (ppm). Поскольку ртутные руды не смешиваются геохимически с теми элементами, которые составляют большую часть массы земной коры, они могут быть чрезвычайно концентрированными, учитывая изобилие элемента в обычных породах. Самые богатые ртутные руды содержат до 2,5% ртути по массе, и даже самые бедные концентрированные месторождения содержат не менее 0,1% ртути (в 12000 раз больше среднего содержания ртути в земной коре). Он встречается либо в виде самородного металла (редко), либо в киновари, метациннабаре, сфалерите, кордероите, ливингстоните и других минералах, причем киноварь (HgS) является наиболее распространенной рудой. Ртутные руды обычно встречаются в очень молодых орогенных поясах, где породы высокой плотности вытеснены в земную кору, часто в горячих источниках или других вулканических регионах.
Начиная с 1558 года, с изобретением внутреннего дворика для извлечения серебра из руды с использованием ртути, ртуть стала важным ресурсом в экономике Испании и ее американских колоний. Ртуть использовалась для извлечения серебра из прибыльных рудников Новой Испании и Перу. Первоначально рудники испанской короны в Альмадене на юге Испании поставляли всю ртуть для колоний. Ртутные месторождения были открыты в Новом Свете, и более 100000 тонн ртути были добыты из области Huancavelica, Перу, в течение трех столетий после открытия месторождений там в 1563. Процесс патио и позже амальгамация процесса непрерывное создать большой спрос на ртуть для обработки серебряных руд до конца 19 века.
 Самородная ртуть с киноварью, шахта Сократ, округ Сонома, Калифорния. Киноварь иногда превращается в самородную ртуть в окисленной зоне ртутных отложений.
Самородная ртуть с киноварью, шахта Сократ, округ Сонома, Калифорния. Киноварь иногда превращается в самородную ртуть в окисленной зоне ртутных отложений. Бывшие шахты в Италии, США и Мексике, которые когда-то производили значительную часть мировых запасов, теперь полностью выработаны или, в случае Словении ( Идрия ) и Испании ( Альмаден ), закрыты из-за падения цены на ртуть. Nevada «s McDermitt Mine, последний ртутный рудник в Соединенных Штатах, закрытый в 1992 году цена ртути была крайне нестабильной в течение многих лет, и в 2006 году составила $ 650 за 76 фунтов (34,46 кг) колбу.
Ртуть извлекается путем нагревания киновари в потоке воздуха и конденсации пара. Уравнение для этого извлечения:
В 2005 году Китай был крупнейшим производителем ртути с почти двумя третями мировой доли, за которым следовал Кыргызстан. Считается, что в некоторых других странах не регистрируется производство ртути в результате процессов электролитического извлечения меди и рекуперации из сточных вод.
Из-за высокой токсичности ртути как добыча киновари, так и переработка ртути являются опасными историческими причинами отравления ртутью. В Китае тюремный труд использовался частной горнодобывающей компанией еще в 1950-х годах для разработки новых рудников киновари. Тысячи заключенных использовались горнодобывающей компанией Луо Си для строительства новых туннелей. Здоровье рабочих на действующих шахтах находится под высоким риском.
Газета утверждала, что неопознанная директива Европейского Союза, призывающая к обязательному введению энергоэффективных лампочек к 2012 году, побудила Китай вновь открыть киноварные рудники для получения ртути, необходимой для производства ламп КЛЛ. Опасности для окружающей среды вызывают беспокойство, особенно в южных городах Фошань и Гуанчжоу, а также в провинции Гуйчжоу на юго-западе.
Заброшенные места переработки ртути шахты часто содержат очень опасные отвалы жареных киноварных огарков. Водостоки с таких участков - признанный источник экологического ущерба. Бывшие ртутные рудники могут быть пригодны для конструктивного повторного использования. Например, в 1976 году округ Санта-Клара, штат Калифорния, приобрел историческую шахту Almaden Quicksilver Mine и создал на этом месте окружной парк после проведения обширного анализа безопасности и окружающей среды.
Ртуть существует в двух степенях окисления I и II. Несмотря на заявления об обратном, соединения Hg (III) и Hg (IV) остаются неизвестными, хотя короткоживущая Hg (III) была получена посредством электрохимического окисления.
В отличие от своих более легких соседей, кадмия и цинка, ртуть обычно образует простые стабильные соединения со связями металл-металл. Большинство соединений ртути (I) диамагнитны и содержат димерный катион Hg2+ 2. Стабильные производные включают хлорид и нитрат. Обработка комплексообразования соединений Hg (I) сильными лигандами, такими как сульфид, цианид и т. Д., Вызывает диспропорционирование до Hg.2+ и элементарная ртуть. Хлорид ртути (I), бесцветное твердое вещество, также известное как каломель, на самом деле представляет собой соединение с формулой Hg 2 Cl 2 со связностью Cl-Hg-Hg-Cl. Это стандарт в электрохимии. Он реагирует с хлором с образованием хлорида ртути, который сопротивляется дальнейшему окислению. Гидрид ртути (I), бесцветный газ, имеет формулу HgH, не содержащий связи Hg-Hg.
Показывая свою тенденцию связываться с собой, ртуть образует поликатионы ртути, которые состоят из линейных цепей центров ртути, покрытых положительным зарядом. Одним из примеров является Hg2+ 3(AsF- 6) 2.
Ртуть (II) является наиболее распространенной степенью окисления, а также является основной в природе. Все четыре галогенида ртути известны. Они образуют тетраэдрические комплексы с другими лигандами, но галогениды принимают линейную координационную геометрию, что-то вроде того, что делает Ag +. Наиболее известен хлорид ртути (II), легко сублимирующее белое твердое вещество. HgCl 2 образует координационные комплексы, которые обычно являются тетраэдрическими, например HgCl.2- 4.
Оксид ртути (II), основной оксид ртути, образуется, когда металл подвергается длительному воздействию воздуха при повышенных температурах. Он превращается в элементы при нагревании около 400 ° C, как было продемонстрировано Джозефом Пристли в ходе раннего синтеза чистого кислорода. Гидроксиды ртути плохо охарактеризованы, как и для ее соседей - золота и серебра.
Как мягкий металл, ртуть образует очень стабильные производные с более тяжелыми халькогенами. Особо следует отметить сульфид ртути (II), HgS, который встречается в природе в виде руды киновари и представляет собой ярко- красный пигмент. Подобно ZnS, HgS кристаллизуется в двух формах : красноватой кубической форме и форме черной цинковой обманки. Последнее иногда встречается в природе как метациннабар. Ртути (II) селенида (HgSe) и ртути (II), теллурида (HgTe) также известны, эти, а также различные производные, например, ртуть, кадмий теллурида и ртути теллурида цинка является полупроводники, используемые в качестве инфракрасных детекторов материалов.
Соли ртути (II) образуют множество сложных производных с аммиаком. К ним относятся основание Миллона (Hg 2 N +), одномерный полимер (соли HgNH+ 2) п), и «плавкий белый осадок» или [Hg (NH 3) 2 ] Cl 2. Известный как реагентом Несслера, tetraiodomercurate калия (II), ( HgI2- 4) до сих пор иногда используется для проверки аммиака из-за его тенденции к образованию сильно окрашенной йодидной соли основания Миллона.
Молниеносный ртуть - детонатор, широко используемый во взрывчатых веществах.
Органические соединения ртути имеют историческое значение, но не имеют большого промышленного значения в западном мире. Соли ртути (II) являются редким примером простых комплексов металлов, которые напрямую реагируют с ароматическими кольцами. Ртутьорганические соединения всегда двухвалентны и обычно имеют двухкоординатную и линейную геометрию. В отличие от кадмийорганических и цинкорганических соединений, ртутьорганические соединения не вступают в реакцию с водой. Обычно они имеют формулу HgR 2, который часто является летучим, или HgRX, который часто является твердым веществом, где R представляет собой арил или алкил, а X обычно представляет собой галогенид или ацетат. Метилртуть, общий термин для соединений с формулой CH 3 HgX, представляет собой опасное семейство соединений, которые часто встречаются в загрязненной воде. Они возникают в результате процесса, известного как биометилирование.
 Колба ртутного стеклянного термометра
Колба ртутного стеклянного термометра Ртуть используется в основном для производства промышленных химикатов или для электрических и электронных устройств. Он используется в некоторых жидкостных стеклянных термометрах, особенно в тех, которые используются для измерения высоких температур. Все больше и больше используется в качестве газообразной ртути в люминесцентных лампах, в то время как большинство других применений постепенно прекращается из-за требований по охране здоровья и безопасности. В некоторых применениях ртуть заменяют менее токсичным, но значительно более дорогим сплавом Галинстан.
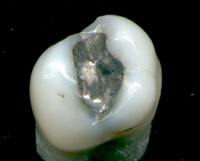 Пломба из амальгамы
Пломба из амальгамы Ртуть и ее соединения использовались в медицине, хотя сегодня они гораздо реже, чем когда-то, теперь, когда токсические эффекты ртути и ее соединений стали более широко понятными. Первое издание Руководства Мерка (1899 г.) включало многие соединения ртути, такие как:
Ртуть входит в состав зубных амальгам. Тиомерсал ( в США его называют тимеросалом) - это органическое соединение, используемое в качестве консерванта в вакцинах, хотя его применение сокращается. Тиомерсал метаболизируется до этилртути. Хотя широко предполагалось, что этот консервант на основе ртути может вызывать или вызывать аутизм у детей, научные исследования не показали никаких доказательств, подтверждающих какую-либо такую связь. Тем не менее, тиомерсал был удален или уменьшен до следовых количеств во всех вакцинах США, рекомендованных для детей в возрасте 6 лет и младше, за исключением инактивированной вакцины против гриппа.
Еще одно соединение ртути, мербромин ( Меркурохром ), представляет собой антисептик местного действия, используемый для небольших порезов и царапин, который все еще используется в некоторых странах.
Ртуть в виде одной из обычных руд, киновари, используется в различных традиционных лекарствах, особенно в традиционной китайской медицине. Обзор его безопасности показал, что киноварь может привести к значительной интоксикации ртутью при нагревании, употреблении в передозировке или длительном приеме, а также может иметь побочные эффекты при терапевтических дозах, хотя эффекты от терапевтических доз обычно обратимы. Хотя эта форма ртути кажется менее токсичной, чем другие формы, ее использование в традиционной китайской медицине еще не оправдано, поскольку терапевтическая основа использования киновари не ясна.
Сегодня использование ртути в медицине сильно сократилось во всех отношениях, особенно в развитых странах. Термометры и сфигмоманометры, содержащие ртуть, были изобретены в начале 18 и конце 19 веков соответственно. В начале 21 века их использование сокращается и было запрещено в некоторых странах, штатах и медицинских учреждениях. В 2002 году Сенат США принял закон о поэтапном отказе от продажи ртутных термометров без рецепта. В 2003 году Вашингтон и Мэн стали первыми штатами, которые запретили ртутные устройства для измерения кровяного давления. Соединения ртути содержатся в некоторых безрецептурных лекарствах, включая местные антисептики, стимулирующие слабительные, мазь от опрелостей, глазные капли и спреи для носа. У FDA есть «неадекватные данные для общего признания безопасности и эффективности» ртутных ингредиентов в этих продуктах. Ртуть по-прежнему используется в некоторых диуретиках, хотя в настоящее время существуют ее заменители для большинства терапевтических целей.
Хлор получают из хлорида натрия (поваренная соль, NaCl) с помощью электролиза для отделения металлического натрия от газообразного хлора. Обычно соль растворяют в воде для получения рассола. Побочными продуктами любого такого хлорщелочного процесса являются водород (H 2) и гидроксид натрия (NaOH), который обычно называют каустической содой или щелоком. Безусловно, наибольшее использование ртути в конце 20-го века было в процессе ртутных элементов (также называемом процессом Кастнера-Келлнера ), где металлический натрий образуется в виде амальгамы на катоде, сделанном из ртути; этот натрий затем реагирует с водой с образованием гидроксида натрия. Многие промышленные выбросы ртути в 20 веке произошли в результате этого процесса, хотя современные предприятия утверждали, что они безопасны в этом отношении. Примерно после 1985 года все новые предприятия по производству хлористой щелочи, которые были построены в Соединенных Штатах, использовали технологии мембранных или мембранных элементов для производства хлора.
Некоторые медицинские термометры, особенно термометры для высоких температур, наполнены ртутью; они постепенно исчезают. В Соединенных Штатах продажа термометров для ртутной лихорадки без рецепта запрещена с 2003 года.
Некоторые транзитные телескопы используют резервуар с ртутью для формирования плоского и абсолютно горизонтального зеркала, полезного для определения абсолютной вертикальной или перпендикулярной точки отсчета. Вогнутые горизонтальные параболические зеркала могут быть сформированы путем вращения жидкой ртути на диске, причем параболическая форма жидкости, образованной таким образом, отражает и фокусирует падающий свет. Такие телескопы с жидкостными зеркалами дешевле обычных больших зеркальных телескопов до 100 раз, но зеркало не может быть наклонено и всегда направлено прямо вверх.
Жидкая ртуть является частью популярного вторичного электрода сравнения (называемого каломельным электродом ) в электрохимии в качестве альтернативы стандартному водородному электроду. Каломельный электрод используется, чтобы отработать потенциал электрода из половины клеток. И последнее, но не менее важное: тройная точка ртути, −38,8344 ° C, является фиксированной точкой, используемой в качестве температурного стандарта для Международной температурной шкалы ( ITS-90 ).
В полярографии и в падающем ртутном электроде, и в висящем в капле ртутного электрода используется элементарная ртуть. Такое использование позволяет использовать новый незагрязненный электрод для каждого измерения или каждого нового эксперимента.
Ртутьсодержащие соединения также используются в области структурной биологии. Соединения ртути, такие как хлорид ртути (II) или тетраиодомеркурат (II) калия, могут быть добавлены к кристаллам белка с целью создания производных с тяжелыми атомами, которые могут быть использованы для решения фазовой проблемы в рентгеновской кристаллографии с помощью методов изоморфного замещения или аномального рассеяния..
Газообразная ртуть используется в ртутных лампах, некоторых рекламных знаках типа « неоновая вывеска » и люминесцентных лампах. Эти лампы низкого давления излучают очень узкие в спектральном отношении линии, которые традиционно используются в оптической спектроскопии для калибровки спектрального положения. Для этой цели продаются коммерческие калибровочные лампы; отражение люминесцентного потолочного света в спектрометр - обычная практика калибровки. Газообразная ртуть также содержится в некоторых электронных лампах, включая игнитроны, тиратроны и ртутные дуговые выпрямители. Он также используется в специальных медицинских лампах для загара и дезинфекции кожи. Газообразная ртуть добавляется в лампы с холодным катодом, заполненные аргоном, для увеличения ионизации и электропроводности. Лампа без ртути, наполненная аргоном, будет иметь тусклые пятна и не сможет правильно загореться. Освещение, содержащее ртуть, можно подвергнуть бомбардировке / прокачке печи только один раз. При добавлении в пробирки, заполненные неоном, излучаемый свет будет представлять собой непостоянные красные / синие точки до тех пор, пока не будет завершен начальный процесс прожигания; в конечном итоге он загорится постоянным тусклым не совсем синим цветом.

Глубокое фиолетовое свечение разряда паров ртути в бактерицидной лампе, спектр которой богат невидимым ультрафиолетовым излучением.

Средство для загара, содержащее ртутную лампу низкого давления и две инфракрасные лампы, которые действуют как источник света и электрический балласт.

Ассортимент люминесцентных ламп.

Миниатюрные атомные часы Deep Space - это линейные часы с ионными ловушками и ртутными ионами, разработанные для точной радионавигации в реальном времени в глубоком космосе.
Deep Space Atomic Clock (DSAC) в стадии разработки в Лаборатории реактивного движения использует ртуть в линейных ионной ловушке на основе часов. Новое использование ртути позволяет создавать очень компактные атомные часы с низким энергопотреблением, и поэтому они идеально подходят для космических зондов и миссий на Марс.
Ртуть, как тиомерсал, широко используется при изготовлении туши для ресниц. В 2008 году Миннесота стала первым штатом в Соединенных Штатах, который запретил намеренное добавление ртути в косметику, что установило более жесткие стандарты, чем федеральное правительство.
Исследование средней геометрической концентрации ртути в моче выявило ранее неизвестный источник воздействия (средства по уходу за кожей) неорганической ртути среди жителей Нью-Йорка. Биомониторинг населения также показал, что уровни концентрации ртути выше у потребителей морепродуктов и рыбной муки.
Молниеносный ртуть (II) - это первичное взрывчатое вещество, которое в основном используется в качестве капсюля для патронов в огнестрельном оружии.
 Однополюсный на одно направление ( SPST) ртутный переключатель.
Однополюсный на одно направление ( SPST) ртутный переключатель.  Манометр ртутный для измерения давления
Манометр ртутный для измерения давления Во многих исторических приложениях использовались особые физические свойства ртути, особенно как плотной жидкости и жидкого металла:
В других приложениях использовались химические свойства ртути:
Хлорид ртути (I) (также известный как каломель или хлорид ртути) используется в традиционной медицине в качестве мочегонного, местного дезинфицирующего средства и слабительного средства. Хлорид ртути (II) (также известный как хлорид ртути или коррозионный сублимат) когда-то использовался для лечения сифилиса (наряду с другими соединениями ртути), хотя он настолько токсичен, что иногда симптомы его токсичности путали с симптомами сифилиса. считается лечить. Он также используется как дезинфицирующее средство. Голубая масса, пилюля или сироп, в котором ртуть является основным ингредиентом, прописывалась на протяжении 19 века при многих состояниях, включая запоры, депрессию, деторождение и зубную боль. В начале 20-го века ртуть вводили детям ежегодно в качестве слабительного и деглистирующего средства, а также использовали в порошках для прорезывания зубов для младенцев. Ртутьсодержащий галогенид мербромин (иногда продаваемый как меркурохром) по-прежнему широко используется, но был запрещен в некоторых странах, таких как США.
| Опасности | |
|---|---|
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| Положения об опасности GHS | H330, H360D, H372, H410 |
| Меры предосторожности GHS | P201, P260, P273, P280, P304, P340, P310, P308, P313, P391, P403, P233 |
| NFPA 704 (огненный алмаз) |  2 0 0 2 0 0 |
| Часть серии по |
| Загрязнение |
|---|
 |
Загрязнение воздуха
|
| Биологическое загрязнение |
| Электромагнитное загрязнение |
| Естественное загрязнение |
Шумовое загрязнение
|
| Радиационное загрязнение |
| Загрязнение почвы |
| Загрязнение твердыми отходами |
| Загрязнение космоса |
| Тепловое загрязнение |
| Визуальное загрязнение |
Загрязнение воды
|
| Разное Списки Категории
|
|
|
Ртуть и большинство ее соединений чрезвычайно токсичны и требуют осторожного обращения; в случае разливов ртути (например, из некоторых термометров или люминесцентных ламп ) используются специальные процедуры очистки, чтобы избежать воздействия и локализовать разлив. Протоколы требуют физического слияния мелких капель на твердых поверхностях, объединения их в единый бассейн большего размера для более легкого удаления пипеткой или для осторожного выталкивания пролитой жидкости в одноразовый контейнер. Пылесосы и метлы вызывают большее рассеивание ртути, и их нельзя использовать. После этого мелкодисперсный порошок серы, цинка или другого порошка, который легко образует амальгаму (сплав) с ртутью при обычных температурах, разбрызгивается по поверхности, прежде чем он будет собран и должным образом утилизирован. Очистка пористых поверхностей и одежды неэффективна для удаления всех следов ртути, поэтому рекомендуется выбрасывать такие предметы, если они подвергаются воздействию ртути.
Ртуть может всасываться через кожу и слизистые оболочки, а пары ртути можно вдыхать, поэтому емкости с ртутью надежно закрываются, чтобы избежать разливов и испарений. Нагревание ртути или соединений ртути, которые могут разлагаться при нагревании, следует проводить при соответствующей вентиляции, чтобы свести к минимуму воздействие паров ртути. Наиболее токсичными формами ртути являются ее органические соединения, такие как диметилртуть и метилртуть. Ртуть может вызвать как хроническое, так и острое отравление.
 Количество атмосферной ртути, выпавшей на ледник Верхний Фремонт в Вайоминге за последние 270 лет
Количество атмосферной ртути, выпавшей на ледник Верхний Фремонт в Вайоминге за последние 270 лет Скорость доиндустриального осаждения ртути из атмосферы может составлять около 4 нг / (1 л льда). Хотя это можно считать естественным уровнем воздействия, региональные или глобальные источники оказывают значительное воздействие. Вулканические извержения могут увеличить атмосферный источник в 4–6 раз.
На естественные источники, такие как вулканы, приходится примерно половина выбросов ртути в атмосферу. Половину, созданную человеком, можно разделить на следующие приблизительные проценты:
Вышеуказанные проценты представляют собой оценки глобальных антропогенных выбросов ртути в 2000 году, за исключением сжигания биомассы, являющегося важным источником в некоторых регионах.
Недавнее атмосферное загрязнение атмосферным ртутью уличного городского воздуха составило 0,01–0,02 мкг / м 3. В исследовании 2001 года были измерены уровни ртути в 12 помещениях, выбранных для представления различных типов зданий, местоположений и возрастов в районе Нью-Йорка. Это исследование показало, что концентрация ртути значительно выше, чем на открытом воздухе, в диапазоне 0,0065–0,523 мкг / м 3. Среднее значение составляло 0,069 мкг / м 3.
Искусственные озера или водохранилища могут быть загрязнены ртутью из-за поглощения водой ртути из затопленных деревьев и почвы. Например, озеро Уиллистон в северной части Британской Колумбии, образовавшееся в результате перекрытия реки Пис в 1968 году, все еще достаточно загрязнено ртутью, поэтому нецелесообразно употреблять в пищу рыбу из озера. В вечномерзлых почвах ртуть накапливалась в результате атмосферных отложений, а таяние вечной мерзлоты в криосферных регионах также является механизмом выброса ртути в озера, реки и заболоченные земли.
Ртуть также попадает в окружающую среду в результате неправильной утилизации (например, захоронения, сжигания) определенных продуктов. К продуктам, содержащим ртуть, относятся: автомобильные детали, батареи, люминесцентные лампы, медицинские изделия, термометры и термостаты. Из-за проблем со здоровьем (см. Ниже) усилия по сокращению использования токсичных веществ сокращают или устраняют ртуть в таких продуктах. Например, количество ртути, продаваемой в термостатах в США, снизилось с 14,5 тонны в 2004 году до 3,9 тонны в 2007 году.
В большинстве термометров теперь используется пигментированный спирт вместо ртути. Ртутные термометры все еще иногда используются в медицине, потому что они более точны, чем спиртовые термометры, хотя оба обычно заменяются электронными термометрами и реже термометрами Galinstan. Ртутные термометры по-прежнему широко используются в некоторых научных целях из-за их большей точности и рабочего диапазона.
Исторически один из самых крупных выбросов был от завода Colex, завода по разделению изотопов лития в Ок-Ридже, штат Теннесси. Завод работал в 1950-1960-х годах. Записи неполны и неясны, но правительственные комиссии подсчитали, что около двух миллионов фунтов ртути не учтены.
Серьезной промышленной катастрофой стал сброс соединений ртути в залив Минамата в Японии. По оценкам, более 3000 человек пострадали от различных уродств, серьезных симптомов отравления ртутью или смерти от так называемой болезни Минамата.
Растение табака легко поглощает и накапливает тяжелые металлы, такие как ртуть из окружающей почвы в листы. Впоследствии они вдыхаются во время курения табака. Хотя ртуть входит в состав табачного дыма, исследования в значительной степени не смогли выявить существенной корреляции между курением и поглощением ртути людьми по сравнению с такими источниками, как профессиональное воздействие, потребление рыбы и пломбы из амальгамы.
Отложения в крупных городских и промышленных устьях действуют как важный сток для точечного источника и диффузного загрязнения ртутью внутри водосборов. Исследование прибрежных отложений в устье Темзы в 2015 году показало, что общее содержание ртути составляет от 0,01 до 12,07 мг / кг со средним значением 2,10 мг / кг и медианным значением 0,85 мг / кг (n = 351). Было показано, что самые высокие концентрации ртути наблюдаются в Лондоне и его окрестностях в сочетании с мелкозернистыми илами и высоким общим содержанием органического углерода. Сильное сродство ртути к отложениям, богатым углеродом, также наблюдалось в отложениях солончаков реки Мерси, в среднем от 2 до 5 мг / кг. Эти концентрации намного выше, чем те, которые показаны в отложениях ручья соленых болот в штате Нью-Джерси и мангровых зарослях Южного Китая, которые демонстрируют низкие концентрации ртути - около 0,2 мг / кг.
 Сотрудники Агентства по охране окружающей среды ликвидируют разлив ртути в жилых домах в 2004 году
Сотрудники Агентства по охране окружающей среды ликвидируют разлив ртути в жилых домах в 2004 году Из-за воздействия ртути на здоровье ее промышленное и коммерческое использование регулируется во многих странах. Всемирная организация здравоохранения, OSHA и NIOSH всего лакомство ртуть в качестве профессиональной опасности, и установили определенные лимиты воздействия. Выбросы и удаление ртути в окружающую среду регулируются в США в первую очередь Агентством по охране окружающей среды США.
Рыба и моллюски имеют естественную тенденцию концентрировать ртуть в своем организме, часто в форме метилртути, высокотоксичного органического соединения ртути. Виды рыб, занимающие высокие позиции в пищевой цепи, такие как акула, рыба-меч, королевская макрель, голубой тунец, тунец-альбакор и кафельник, содержат более высокие концентрации ртути, чем другие. Поскольку ртуть и метилртуть растворимы в жирах, они в основном накапливаются во внутренних органах, хотя они также обнаруживаются во всей мышечной ткани. Присутствие ртути в мышцах рыб можно изучить с помощью биопсии нелетальных мышц. Ртуть, присутствующая в добываемой рыбе, накапливается в хищнике, который их поедает. Поскольку рыба менее эффективно очищает, чем накапливает метилртуть, концентрация метилртути в тканях рыбы со временем увеличивается. Таким образом, виды, занимающие высокие позиции в пищевой цепи, накапливают в организме ртуть, которая может быть в десять раз выше, чем виды, которые они потребляют. Этот процесс называется биомагнификацией. Отравление ртутью произошло таким образом в Минамате, Япония, теперь оно называется болезнью Минамата.
Некоторые кремы для лица содержат опасные уровни ртути. Большинство из них содержат сравнительно нетоксичную неорганическую ртуть, но встречаются продукты, содержащие высокотоксичную органическую ртуть.
Токсические эффекты включают повреждение мозга, почек и легких. Отравление ртутью может привести к нескольким заболеваниям, включая акродинию (розовую болезнь), синдром Хантера-Рассела и болезнь Минаматы.
Симптомы обычно включают нарушение чувствительности (зрения, слуха, речи), нарушение чувствительности и нарушение координации. Тип и степень проявляемых симптомов зависят от конкретного токсина, дозы, а также метода и продолжительности воздействия. Исследования методом случай-контроль показали такие эффекты, как тремор, нарушение когнитивных способностей и нарушение сна у рабочих, хронически подвергающихся воздействию паров ртути даже при низких концентрациях в диапазоне 0,7–42 мкг / м 3. Исследование показало, что острое воздействие (4–8 часов) расчетных уровней элементарной ртути от 1,1 до 44 мг / м 3 приводит к боли в груди, одышке, кашлю, кровохарканью, нарушению легочной функции и признакам интерстициального пневмонита. Было показано, что острое воздействие паров ртути приводит к серьезным последствиям для центральной нервной системы, включая психотические реакции, характеризующиеся делирием, галлюцинациями и склонностью к суициду. Профессиональное воздействие привело к широким функциональным нарушениям, включая эретизм, раздражительность, возбудимость, чрезмерную застенчивость и бессонницу. При продолжительном воздействии развивается тонкий тремор, который может перерасти в сильные мышечные спазмы. Первоначально тремор поражает руки, а затем распространяется на веки, губы и язык. Длительное воздействие на низком уровне было связано с более тонкими симптомами эретизма, включая усталость, раздражительность, потерю памяти, яркие сны и депрессию.
Исследования по лечению отравления ртутью ограничены. Доступные в настоящее время препараты для лечения острого отравления ртутью включают хелаторы N-ацетил-D, L- пеницилламин (NAP), британский анти-люизит (BAL), 2,3-димеркапто-1-пропансульфоновую кислоту (DMPS) и димеркаптоянтарную кислоту (DMSA).. В одном небольшом исследовании с участием 11 рабочих-строителей, подвергшихся воздействию элементарной ртути, пациентов лечили DMSA и NAP. Хелатная терапия обоими препаратами привела к мобилизации небольшой части общей предполагаемой ртути в организме. DMSA смог увеличить выведение ртути в большей степени, чем NAP.
140 стран согласились в Минамате конвенции по ртути в Программе Организации Объединенных Наций по окружающей среде (ЮНЕП) для предотвращения выбросов. Конвенция подписана 10 октября 2013 года.
В Соединенных Штатах Агентство по охране окружающей среды отвечает за регулирование и борьбу с загрязнением ртутью. Несколько законов наделяют EPA такими полномочиями, включая Закон о чистом воздухе, Закон о чистой воде, Закон о сохранении и восстановлении ресурсов и Закон о безопасной питьевой воде. Кроме того, Закон об обращении с ртутьсодержащими и перезаряжаемыми батареями, принятый в 1996 году, постепенно исключает использование ртути в батареях и предусматривает эффективную и экономичную утилизацию многих типов использованных батарей. В 1995 году на долю Северной Америки приходилось примерно 11% общих глобальных антропогенных выбросов ртути.
Закон США о чистом воздухе, принятый в 1990 году, включил ртуть в список токсичных загрязнителей, которые необходимо контролировать в максимально возможной степени. Таким образом, предприятия, которые выбрасывают в окружающую среду высокие концентрации ртути, согласились установить технологии максимально достижимого контроля (ПДК). В марте 2005 года EPA обнародовало постановление, которое добавило электростанции в список источников, которые должны контролироваться, и ввело национальную систему ограничения выбросов и торговли. Штатам было дано до ноября 2006 года ввести более строгие меры контроля, но после судебного оспаривания со стороны нескольких штатов 8 февраля 2008 года федеральный апелляционный суд отменил постановления. Правило было сочтено недостаточным для защиты здоровья людей, живущих рядом с углями. с учетом негативных последствий, задокументированных в отчете об исследовании EPA для Конгресса за 1998 год. Однако более новые данные, опубликованные в 2015 году, показали, что после введения более строгих мер контроля ртуть резко упала, что указывает на то, что Закон о чистом воздухе оказал ожидаемое воздействие.
Агентство по охране окружающей среды объявило о новых правилах для угольных электростанций 22 декабря 2011 года. Цементные печи, сжигающие опасные отходы, соответствуют более жестким стандартам, чем стандартные установки для сжигания опасных отходов в Соединенных Штатах, и в результате являются непропорциональным источником загрязнения ртутью..
В Европейском союзе директива об ограничении использования определенных опасных веществ в электрическом и электронном оборудовании (см. RoHS ) запрещает использование ртути в определенных электрических и электронных продуктах и ограничивает количество ртути в других продуктах до уровня менее 1000 ppm. Существуют ограничения на концентрацию ртути в упаковке (предел составляет 100 ppm для суммы ртути, свинца, шестивалентного хрома и кадмия ) и батареях (предел составляет 5 ppm). В июле 2007 года Европейский Союз также запретил использование ртути в неэлектрических измерительных приборах, таких как термометры и барометры. Запрет распространяется только на новые устройства и содержит исключения для сектора здравоохранения и двухлетний льготный период для производителей барометров.
Норвегия ввела полный запрет на использование ртути при производстве и импорте / экспорте ртутных продуктов с 1 января 2008 года. В 2002 году было обнаружено, что несколько озер в Норвегии имеют плохое загрязнение ртутью, превышающее 1 мкг. / г ртути в их осадке. В 2008 году министр экологического развития Норвегии Эрик Сольхейм сказал: «Ртуть является одним из самых опасных экологических токсинов. Существуют удовлетворительные альтернативы ртути в продуктах, и поэтому уместно ввести запрет».
Продукты, содержащие ртуть, были запрещены в Швеции в 2009 году.
В 2008 году Дания также запретила стоматологическую ртутную амальгаму, за исключением пломбирования жевательных поверхностей коренных зубов постоянных (взрослых) зубов.