 | |
| Цезий | |
|---|---|
| Произношение | () |
| Альтернативное название | цезий (США, неофициально) |
| Внешний вид | бледное золото |
| Стандартный атомный вес A r, std (Cs) | 132.90545196 (6) |
| Цезий в периодической таблице | |
цезий (ИЮПАК правописание) (также п. ишется цезий в американском английском ) представляет собой химический элемент с символ Csи атомный номер 55. Это мягкий серебристо-золотой щелочной металл с температурным плавлением 28,5 ° C (83,3 ° F), что его одним из пятиэлементных металлов, которые являются жидкими при или около комнатная температура. Цезий имеет физические и химические свойства, аналогичные свойстваам рубидия и калия. Самый реактивный из всех металлов, он пирофор и реагирует с водой даже при -116 ° C (-177 ° F). Это наименьший электроотрицательный элемент со значением 0,79 по шкале Полинга. Он имеет только один стабильный изотоп, цезий-133. Цезий добывается в основном из поллуцита, тогда как радиоизотопы, особенно цезий-137, продукт деления, извлекаются из отходов, производимых ядерные реакторы. Немецкий химик Роберт Бунзен и физик Густав Кирхгоф открыли цезий в 1860 году с помощью недавно разработанного метода спектроскопии пламени. Первыми маломасштабными применениями цезия были «геттер » в электронных лампах и в фотоэлементах. В 1967 году, руководствуясь доказатель Эйнштейна, использовалась скорость света наиболее постоянным измерением во Вселенной, Международная система единиц использовала два конкретных подсчета волн из атмосферы . цезия-133 для совместного секунды и измерителя. С тех пор цезий широко используется в высокоточных атомных часах. . С 1990-х годов самым большим элементом был формиат цезия для буровые растворы, но он имеет ряд применений в производстве электроэнергии, в электронике и в химии. Радиоактивный изотоп цезия-137 имеет период полураспада около 30 лет и используется в медицине, приборах и гидрологии. Нерадиоактивные соединения цезия являются лишь умеренно умеренными токсичными, но склонность металла к взрывной реакции водой означает, что цезий считается опасным материалом, а радиоизотопы имеют значительную опасность для здоровья и окружающей среды. Содержание
Характеристики Физические свойства Цезий-133 высокой чистоты, хранящийся в аргоне. Цезий-133 высокой чистоты, хранящийся в аргоне.Цезий самым самым мягким (его твердость 0,2 по шкале Мооса). Это очень пластичный, бледный металл, который темнеет в определенных следовых количествах кислорода. В присутствии минерального масла (там, где его лучше всего хранить во время транспортировки), оно теряет свой металлический блеск и приобретает более тусклый серый вид. Он имеет точку плавления 28,5 ° C (83,3 ° F), что делает его одним из немногих элементарных металлов, которые являются жидкими при температуре около комнатной температуры. Ртуть - единственный стабильный элементарный металл с известной температурой плавления ниже, чем цезий. Кроме того, металл имеет довольно низкую точку кипения, 641 ° C (1186 ° F), самую низкую среди всех металлов, кроме ртути. Его соединения горят синим или фиолетовым цветом.  Кристаллы цезия (золотые) по сравнению с кристаллами рубидия (серебристые) Кристаллы цезия (золотые) по сравнению с кристаллами рубидия (серебристые) Цезий образует сплавы с другими щелочными металлами, золотом и ртутью (амальгамы ). При температурех ниже 650 ° C (1202 ° F) он не сплавляется с кобальтом, железом, молибденом, никелем, платина, тантал или вольфрам. Он образует четко интерметаллические соединения с сурьмой, галлием, индием и торием, которые светочувствительные. Он смешивается со всеми другими щелочными металлами (кроме лития); сплав с молярным распределением 41% цезия, 47% калия и 12% натрия имеет самую низкую температуру плавления среди всех известных металлических сплавов при - 78 ° С (- 108 ° F). Было изучено несколько амальгам: CsHg. 2- черный с пурпурным металлическим блеском, а CsHg - золотистого цвета, в том числе с металлическим блеском. Цезий имеет золотой цвет. от уменьшения частоты света, необходимого для возбуждения электронов щелочных металлов по мере того, как группа спускается. Для лития через рубидий эта частота находится в ультрафиолете, но для цезия она входит в сине-фиолетовый конец анода; словами, плазмонная частота щелочных металлов становится ниже от лития к цезию. Таким образом, цезий преимущественно пропускает и частично поглощает фиолетовый свет, в то время как другие цвета (более низкую частоту) отражаются; поэтому он выглядит желтоватым. Химические свойства Воспроизведение Добавление небольшого количества цезия в холодную воду является взрывоопасным. Воспроизведение Добавление небольшого количества цезия в холодную воду является взрывоопасным. Металлический цезий высокой реакционной способностью и очень пирофорным. Он самовоспламеняется на воздухе и вступает в реакцию с водой даже при низких температурах в большей степени, чем другие щелочные металлы (первая группа периодической таблицы ). Он вступает в реакцию со льдом при температуре до -116 ° C (-177 ° F). Из-за этой высокой реакционной способности металлический цезий классифицируется как опасный материал. Оно хранится и отправляется в сухих насыщенных углеводородах, таких как минеральное масло. С ним можно работать только в среде инертного газа, например, аргона. Однако взрыв цезий-вода часто бывает менее мощным, чем взрыв натрий -водяной с таким же происхождением натрия. Это связано с тем, что цезий мгновенно взрывается при контакте с водой, оставляя мало времени для накопления водорода. Цезий можно хранить в запаянных под вакуумом ампулах из боросиликатного . В количестве более 100 граммов (3,5 унции) цезий перевозится в герметично закрытых контейнерах из нержавеющей стали. Химический состав цезия аналогичен химическому составу других щелочных металлов, в частности рубидия, элемент выше цезия в периодической таблице. Как и ожидалось для щелочного металла, единственная степень общая окисления +1. Некоторые небольшие соединения имеют из-за того, что имеет более высокую атомную массу и является более электроположительным, чем другие (нерадиоактивные) щелочные металлы. Цезий - самый электроположительный химический элемент. Ион цезия также больше и менее «твердый», чем у более легких щелочных металлов. Соединения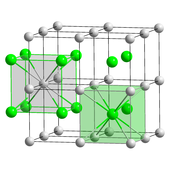 Шарообразная модель кубической кубической системы Cs и Cl в CsCl Шарообразная модель кубической кубической системы Cs и Cl в CsCl Основные соединения цезия содержат элементы в виде катиона Cs., который ионно связывается с широким спектром анионов. Одно заслуживающее внимание исключение - это анион цезида (Cs.), а другие - несколько субоксидов (см. Раздел об оксидах ниже). Соли Cs обычно бесцветны, если сам анион не окрашен. Многие из простых солей гигроскопичны, но менее гигроскопичны, чем соответствующие более легких щелочных металлов. фосфат, ацетат, карбонат, галогениды, оксид, нитрат и сульфатные соли растворимы в воде. Двойные соли часто менее растворимы, низкая растворимость сульфата цезия-алюминия используется при очистке Cs из руд. Двойная соль с сурьмой (например, CsSbCl. 4), висмутом, кадмием, медью, железом и свинец также плохо растворим. Гидроксид цезия (CsOH) гигроскопичен и сильно щелочной. Он быстро травит поверхность полупроводников, таких как кремний. CsOH ранее рассматривал химиками как «самое сильное основание», что отражает относительно слабое притяжение между большим ионом Cs и ОН; это действительно самое сильное основание Аррениуса, но ряды соединений, которые не растворяются в воде, такие как н-бутиллитий и 173>амид натрия, эти соединения более. A стехиометрическая смесь цезия и золота будет реагировать с образованием желтого аурида цезия (CsAu) при нагревании. Аурид-анион здесь ведет себя как псевдогалоген . Соединение бурно реагирует с водой, давая гидроксид цезия, металлическое золото и газообразный водород; в аммиаке он может реагировать с цезий-специфической ионообменной смолой с образованием аурида тетраметиламмония. Аналогичное соединение платины, красный платинид цезия (Cs 2 Pt), содержит ион платинида, который ведет себя как псевдо халькоген. КомплексыПодобный все катионы металлов, Cs образует комплексы с основаниями Льюиса в растворе. Из-за своего большого размера Cs обычно имеет координационные числа , превышающие 6, число, типичное для катионов щелочных металлов меньшего размера. Это различие проявляется в 8-повышенной CsCl. Это высокое координационное число и мягкость (склонность к образованию ковалентных связей) используются используемые для отделения Cs от других катионов при восстановлении ядерных отходов, где Cs необходимо отделять от больших количеств нерадиоактивного K. Галогениды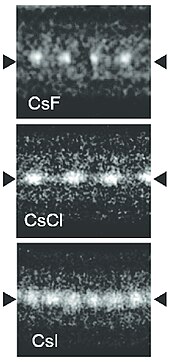 Проволоки одноатомного галогенида цезия, выращенные внутри двустенных углеродных нанотрубок (ПЭМ-изображение ). Проволоки одноатомного галогенида цезия, выращенные внутри двустенных углеродных нанотрубок (ПЭМ-изображение ).Фторид цезия (CsF) гигроскопичным белым твердым веществом, которое широко используется в фторорганической химии в источнике фторидных анионов., как и Na и Cl в хлориде натрия. Примечательно, что цезий и фтор имеют самую низкую и высокую электроотрицательность, соответственно, среди всех известных элементов. Цезий хлорид (CsCl) кристаллизу ется в простой кубической кристаллической системе. Этот структурный мотив также называется «структурой хлорида цезия». состоит из примитивной кубической решетки с двухатомным базисом, каждый с восьмикратной координацией ; атомы хлора лежат в узлах решетки на краях куба, а атомы цезия - в отверстиях в центре куба. Эта структура является общей с CsBr и CsI и многими другими соединениями, не содержащими Cs. Напротив, большинство других щелочных галогенидов имеют структуру хлорида натрия (NaCl). Структура CsCl предпочтительна, потому что Cs имеет ионный радиус 174 пм и Cl. 181 пм. Оксиды Cs. 11O. 3кластер Cs. 11O. 3кластер Более того, чем другие щелочные металлы, цезий образует многочисленные бинарные соединения с кислородом. Когда цезий горит на воздухе, эффективный продуктом является супероксид CsO. 2. «Нормальный» оксид цезия (Cs. 2O) образует желто-оранжевые гексагональные кристаллы и является единственным оксидом типа анти- CdCl. 2. Он испаряется при 250 ° C (482 ° F) и разлагается до металлической цезии и пероксида Cs. 2O. 2при температуре выше 400 ° C (752 ° F). Помимо супероксида и озонида CsO. 3, также были изучены несколько ярко окрашенных субоксидов. К ним защищаются Cs. 7O, Cs. 4O, Cs. 11O. 3, Cs. 3O (темно-зеленый), CsO, Cs. 3O. 2, а также Cs. 7O. 2. Последний можно нагреть в вакууме для образования Cs. 2O. Также существуют бинарные соединения с серой, селеном и теллуром. ИзотопыЦезий имеет 39 известных изотопы, в диапазоне массового числа (т. Е. Числа нуклонов в ядре) от 112 до 151. Некоторые из них синтезируются из более легких элементов в процессе медленного захвата нейтронов (S-процесс ) внутри старых звезд и с R-процесса во взрывах сверхновых. Единственным стабильным изотопом цезия является Cs с 78 нейтронами. Хотя он имеет большой ядерный спин (7/2 +), исследования ядерного магнитного резонанса может использовать этот изотоп на резонансной частоте 11,7 МГц.  Распад цезия -137 Распад цезия -137 Радиоактивный Cs имеет очень длительный период полураспада около 2,3 миллиона лет, самый длинный из всех радиоактивных изотопов цезия. Cs и Cs имеют период полураспада 30 и два года соответственно. Cs разлагается на короткоживущий Ba посредством бета-распада, а затем до нерадиоактивного бария, в то время как Cs превращается непосредственно в Ba. Изотопы с массовыми числами 129, 131, 132 и 136 имеют период полураспада от дня до двух недель, в то время как большинство других изотопов имеют период полураспада от нескольких секунд до долей секунды. Существует по крайней мере 21 метастабильный ядерный изомер. За исключением Cs (с периодом полураспада чуть менее 3 часов), все они очень нестабильны и распадаются с периодом полураспада несколько минут или меньше. Изотоп Cs является одним из длинных - живые продукты деления из урана, произведенные в ядерных реакторах. Этот выход продуктов деления снижается в большинстве реакторов, поскольку его предшественник, Xe, является мощным нейтронным ядром и часто превращается в стабильный Xe, прежде чем он сможет распасться на Cs. бета-распад от Cs до Ba - это сильное излучение гамма-излучения.Cs и Sr являются основными среднеактивными продуктами ядерного деления, а также основными источниками радиоактивности от отработавшего ядерного топлива после нескольких лет охлаждение, продолжающееся несколько сотен лет. Эти два изотопа являются крупнейшим источником остаточной радиоактивности в районе Чернобыльской катастрофы. Из-за низкой скорости захвата удаление Cs посредством захвата нейтронов невозможно, и единственное текущее решение - позволить ему распадаться с течением времени. Практически весь цезий, образующийся в результате ядерного деления, образуется от бета-распада изначально более богатых нейтронами продуктов деления, проходящих через различные изотопы йода и ксенон. Поскольку йод и ксенон летучие и могут диффундировать через ядерное топливо или воздух, радиоактивный цезий часто образуется далеко от исходного места деления. Во время испытаний ядерного оружия в 1950–1980-х годах Cs был выброшен в атмосферу и вернулся на поверхность земли как компонент радиоактивных осадков. Это готовый маркер движения почвы и наносов с тех времен. Происхождение Поллюцит, минерал цезия Поллюцит, минерал цезия Цезий является относительно редким элементом, в среднем 3 частей на миллионов в земной коре. Это 45-й элемент по распространенности и 36-й среди металлов. Тем не менее, его больше, чем таких элементов, как сурьма, кадмий, олово и вольфрам, и на два порядка больше. чем ртуть и серебро ; он на 3,3% больше, чем рубидий, с которым он связан химически. Из-за своего большого ионного радиуса цезий является одним из "несовместимых элементов ". Во время кристаллизации магмы цезий концентрируется в жидкой фазе и кристаллизуется последним. Следовательно, самые крупные месторождения цезия - это зона пегматит рудных тел, образованных этим процессом обогащения. Цезисий не заменяет калий так легко, как рубидий, минералы щелочного эвапорита сильвит (KCl) и карналлит (KMgCl. 3· 6H. 2O) может содержать только 0,002% цезия. Следовательно, цезий в нескольких минералах. Процентные количества цезия могут быть обнаружены в берилле (Be. 3Al. 2(SiO. 3). 6) и авогадрите ((K, Cs) BF. 4) до 15 мас.% Cs 2 O в связанном масле минерале пеццоттаите (Cs (Be. 2Li) Al. 2Si. 6O. 18), до 8,4.% Cs 2 O в редком минерале лондоните ((Cs, K) Al. 4Be. 4(B, Be). 12O. 28) и меньше в более распространенном родизите. Единственный экономически важный руда для цезия - это поллуцит Cs (AlSi. 2O. 6), который находится в нескольких местах по всему миру в зональных пегматитах, связанных с более коммерчески важными литиев минералами, лепидолит и петалит. Среди пегматитов большой размер зерна и сильное разделение приводят к получению высококачественных руды для добычи. Самая значительная и богатая в мире известная цезия является рудник Танко на озере Берник в Манитобе, Канада, где, по оценкам, содержат 350,000 метрических тонн руды поллуцита, репрес охват более двух третей мировой резервной базы. Хотя стехиометрическое содержание цезия в поллуците составляет 42,6%, чистые образцы поллуцита из этого месторождения содержат только около 34% цезия, в то время как среднее содержание составляет 24 мас.%. Промышленный поллуцит содержит более 19% цезия. Пегматитовое месторождение Бикита в Зимбабве добывается для получения петалита, но оно также содержит значительное количество поллуцита. Другой заметный источник поллуцита находится в пустыне Карибиб, Намибия. При нынешних темпах мировой добычи руды от 5 до 10 метрических тонн в год запасов хватит на тысячи лет. Производство Добыча и переработка поллуцитовой руды является селективным процессом и осуществляется в меньшем масштабе, чем для других металлов. Руда дробится, сортируется вручную, но обычно не концентрируется, а затем измельчается. Затем цезий извлекается из поллуцита в основном тремя методами: кислотным разложением, щелочным разложением и прямым восстановлением. При кислотном разложении силикатная порода растворяется с помощью сильных кислот, таких как соляная (HCl), серная (H. 2SO. 4), бромистоводородная (HBr) или фтористоводородная (HF) кислоты. Соляной кислотой образуется смесь растворимых хлоридов, и нерастворимые хлоридные двойные соли цезия осаждаются в виде хлорида цезия и сурьмы (Cs. 4SbCl. 7), хлорида иода цезия (Cs. 2ICl) или цезия. гексахлорцерат (Cs. 2(CeCl. 6)). После чистая осажденная двойная соль разлагается, а CsCl осаждается путем чистого испарения воды. Метод с использованием серной кислоты дает нерастворимую двойную соль непосредственно в виде цезии квасцы (CsAl (SO. 4). 2· 12H. 2O). компонент сульфата алюминия превращается в нерастворимый оксид алюминия путем обжига квасцов с углеродом, и полученный продукт выщелачивается водой с получением раствора Cs. 2SO. 4. Обжиг поллуцита с карбонатом кальция и хлоридом кальция дает нерастворимые силикаты кальция и растворимый хлорид цезия. Этот раствор можно упарить для получения хлорида цезия или превратить в квасцы цезия или карбонат цезия. Хотя это коммерчески нецелно, руду можно восстановить напрямую с помощью калия, натрия или кальция в вакууме. Большая часть добытого цезия (в виде солей) непосредственно превращается в формиат цезия (HCOOC) для таких применений, как бурение нефтяных скважин. Чтобы обеспечить развитие рынка, Cabot Corporation построила в 1997 году завод по производству формиата цезия на руднике Танко возле озера Берник в Манитобе с производительностью 12 000 баррелей (1900 м3) в год. Основными коммерческими соединениями цезия меньшего масштаба являются хлорид цезия и нитрат. . В качестве альтернативы металлический цезий может быть получен из очищенных соединений, полученные из руды. Хлорид цезия и другие галогениды цезия могут быть восстановлены при температуре от 700 до 800 ° C (от 1292 до 1472 ° F) с помощью кальция или бария и металлического цезия, полученного путем дистилляции. Таким же образом алюминат, карбонат или гидроксид могут быть восстановлены магнием. . Металл также можно выделить электролизом плавленого цианида цезия (CsCN). Исключительно чистый и не содержащий газов цезий может быть получен термическим разложением при температуре 390 ° C (734 ° F) азида цезия CsN. 3, может быть получен из водного сульфата цезия и азида бария. В условиях вакуума дихромат цезия может реагировать с цирконием для получения чистого металлического цезия без других газообразных продуктов.
Цена на цезий с чистотой 99,8% (металлическая основа) в 2009 году составляла около 10 долларов за грамм (280 долларов за унцию), но эти соединения значительно дешевле. История  Густав Кирхгоф (слева) и Роберт Бунзен (в центре) открыл цезий с помощью своего недавно изобретенного спектроскопа. Густав Кирхгоф (слева) и Роберт Бунзен (в центре) открыл цезий с помощью своего недавно изобретенного спектроскопа. В 1860 году Роберт Бунзен и Густав Кирхгоф представили цезий в минеральная вода из Дюркхайм, Германия. Из-за ярких синих линий в спектре излучения , они получили свое название от латинского слова caesius, что означает небесно-голубой. Цезий был первым первым, который был обнаружен с помощью спектроскопа, который был изобретен Бунзеном и Кирхгофом только годом ранее. Чтобы получить чистый образец цезия, 44000 литров (9700 имп. Галлон; 12000 галлонов США) минеральной воды необходимо было выпарить, чтобы получить 240 кг (530 фунтов) концентрированного раствора соли. щелочноземельные металлы осаждали либо в виде сульфатов, либо оксалатов, оставляя щелочной металл в растворе. После преобразования в нитраты и экстракции этанолом без смеси, не содержащейся натрия. Из этой смеси литий осаждали карбонатом аммония . Калий, рубидий и цезий образуют нерастворимые соли с платинохлористоводородной кислотой, но эти соли имеют небольшую разницу в растворимости в горячей воде, и менее растворимые гексахлороплатинаты цезия и рубидия ((Cs, Rb) 2 PtCl 6) были получены фракционная кристаллизация. После восстановления гексахлороплатината водородом цезий и рубидий были разделены по разнице в растворимости их карбонатов в спирте. В результате было получено 9,2 грамма (0,32 унции) хлорида рубидия и 7,3 грамма (0,26 унции) хлорида цезия из начальных 44000 литров минеральной воды. Из хлорида цезия оба ученых оценили атомный вес новый элемент в 123,35 (по сравнению с принятым в настоящее время значение 132,9). Они пытались получить элементарный цезий электролизом расплавленного хлорида цезия, но вместо металла они получили синее гомогенное вещество, которое «невооруженным глазом, ни под микроскопом не показало ни малейшего следа металлического вещества»; в результате они отнесли его к субхлориду (Cs. 2Cl). В действительности продукт, вероятно, был коллоидной смесью металла и хлорида цезия. Электролиз водного раствора хлорида с ртутным катодом дает амальгаму цезия, которая легко разлагается в водных условиях. В конечном итоге чистый металл выделен немецким хим во время работы над докторской диссертацией с Кекуле и Бунзеном. В 1882 году он произвел металлический цезий путем электролиза цианида цезия, избегая проблем с хлоридом. Исторически часто используемое использование цезия были исследования и разработки, прежде всего в химической и промышленности. электрические поля. Очень мало применений цезия существовало до 1920-х годов, когда он вошел в использование в радио электронных ламп, где он выполнял две функции; в качестве геттера он удалял избыток кислорода после изготовления, а в качестве покрытия на покрытии катоде он увеличивал электрическую проводимость. Цезий не считался промышленным металлом с высокими высокими до 1950-х годов. Применения нерадиоактивного цезия включают фотоэлементы, фотоумножители трубки, оптические компоненты инфракрасных спектрофотометров, катализаторы для различных воздействий, кристаллы для сцинтилляционных счетчиков, а в магнитогидродинамических генераторов энергии. Цезий также использовался и до сих пор используется в качестве источника положительных в масс-спектрометрии вторичных (SIMS). С 1967 года Международная система измерений основывает первую единицу времени, вторую, на свойствах цезия. Международная система (СИ) определяет секунду как продолжительность 9 192 631 770 циклов на мик-микроволновой част спектральной линии, создающей переход между двумя сверхтонкие уровни энергии основного состояния цезия-133. 13-я Генеральная конференция по мерам и весам 1967 г. определила секунду как: «продолжительность 9 192 631 770 циклов микроволнового света, поглощаемого или испускаемого сверхтонким переходом элементов цезия-133 в их основном состоянии, не нарушенном внешними полями. ". Приложения Разведка месторожденийНаибольшее современное использование нерадиоактивного цезия - это формиат цезия буровые растворы для Водные растворы формиата цезия (HCOOC), полученные реакцией гидроксида цезия с муравьиной кислотой, были разработаны в середине 1990-х годов для использования в качестве буровых скважин и жидкостей для заканчивания Буровой породы предназначенной для смазки бурового долота, вывода выбур на поверхность и поддержания давления на пласт во время бурения скважины позволяет установить контрольное оборудование после бурения, но до начала добычи, поддерживая давление. 139>Высокая плотность рассола формиата цезия (до 2,3 г / см, 19,2 фунта на галлон) в сочетании с Относительно безвредный характер соединений цезия снижает потребность в токсичных взвешенных твердых частицах высокой п лотности в буровом растворе - значительное технологическое, инженерное и экологическое преимущество. В отличие от компонентов многих других тяжелых жидкостей, формиат цезия относительно безвреден для окружающей среды. Солевой раствор формиата цезия можно смешивать с формиатами калия и натрия для уменьшения плотности жидкостей до плотности воды (1,0 г / см или 8,3 фунта на галлон). Кроме того, он поддается биологическому разложению и может быть переработан, что важно ввиду его высокой стоимости (около 4000 долларов за баррель в 2001 году). Формиаты щелочных металлов безопасны в обращении и не повреждают продуктивный пласт или забойные металлы, в отличие от агрессивных альтернативных растворов с высокой плотностью (например, растворы бромида цинка ZnBr. 2); они также требуют меньше очистки и сокращают затраты на утилизацию. Атомные часы Ансамбль атомных часов в Военно-морской обсерватории США Ансамбль атомных часов в Военно-морской обсерватории США  FOCS-1, атомные часы с непрерывным холодным цезиевым фонтаном в Швейцарии, начали работать в 2004 году с погрешностью в одну секунду за 30 миллионов лет FOCS-1, атомные часы с непрерывным холодным цезиевым фонтаном в Швейцарии, начали работать в 2004 году с погрешностью в одну секунду за 30 миллионов лет основанные на цезии атомные часы используют электромагнитные переходы в сверхтонкой структуре атомов цезия-133 как ориентир. Первые точные цезиевые часы были построены Луи Эссеном в 1955 году в Национальной физической лаборатории в Великобритании. Цезиевые часы улучшились за последние полвека и считаются «наиболее точной реализацией единицы измерения, которую человечество когда-либо достигло». Эти часы измеряют частоту с погрешностью от 2 до 3 частей из 10, что соответствует точности 2 наносекунды в день или одной секунды за 1,4 миллиона лет. Последние версии более точны, чем 1 часть из 10, примерно 1 секунда за 20 миллионов лет. Цезиевый эталон является основным эталоном для совместимых со стандартами измерений времени и частоты. Цезиевые часы регулируют синхронизацию сетей сотовой связи и Интернета. Единицы СИСекунда, символ s, является единицей измерения времени СИ. Он определяется путем принятия фиксированного числового значения частоты цезия Δν Cs, невозмущенной частоты сверхтонкого перехода в основное состояние атома цезия-133, равным 9192631770 при выражении в единицах Гц, что равно s. Электроэнергетика и электроникаЦезиевые пары термоэлектронные генераторы представляют собой маломощные устройства, преобразующие тепловую энергию в электрическую. В преобразователе с двумя электродами на вакуумных лампах цезий нейтрализует объемный заряд возле катода и усиливает ток. Цезий также важен благодаря своим фотоэмиссионным свойствам, преобразование света в поток электронов. Он используется в фотоэлементах, поскольку катоды на основе цезия, такие как интерметаллическое соединение K. 2CsSb, имеют низкое пороговое напряжение для эмиссии электронов. Ассортимент фотоэмиссионных устройств, использующих цезий, включает устройства оптического распознавания символов, трубки фотоумножителя и трубки видеокамеры. Тем не менее, германий, рубидий, селен, кремний, теллур и некоторые другие элементы могут заменить цезий в светочувствительных материалах. иодид цезия (CsI), бромид (CsBr) и кристаллы фторида цезия (CsF) используются для сцинтилляторов в сцинтилляционных счетчиках, широко используются в разведке полезных ископаемых и исследованиях физики частиц для обнаружения гамма и Рентгеновское излучение. Как тяжелый элемент, цезий обеспечивает хорошую способность с лучшим обнаружением. Соединения цезия могут обеспечивать более быстрый отклик (CsF) и быть менее гигроскопичными (CsI). Пары цезия используются во многих распространенных магнитометрах. Элемент используется в качестве внутреннего стандарта в спектрофотометрии. Как и другие щелочные металлы, цезий имеет большое сродство к кислороду и используется в качестве «геттера » в вакуумных трубках. Другие области применения металла включают высокоэнергетические лазеры, паровые лампы накаливания и паровые выпрямители. Центрифужные жидкостиВысокая плотность цезия ионов делает растворы хлорида цезия, сульфата цезия и трифторацетата цезия (Cs (O. 2CCF. 3)) полезными в молекулярной биологии для ультрацентрифугирования градиента плотности
| |