 Некоторые важные фторорганические соединения. A: фторметан. B: изофлуран. C: a CFC. D: и HFC. E: трифлиновая кислота. F: Тефлон. G: PFOS. H: фторурацил. I : флуоксетин
Некоторые важные фторорганические соединения. A: фторметан. B: изофлуран. C: a CFC. D: и HFC. E: трифлиновая кислота. F: Тефлон. G: PFOS. H: фторурацил. I : флуоксетин Фторорганическая химия описывает химию фторорганических соединений, органических соединений, содержащих связь углерод-фтор. Фторорганические соединения находят разнообразное применение: от масел и водоотталкивающих веществ до фармацевтических препаратов, хладагентов и реагентов в катализе. Помимо этих применений, некоторые фторорганические соединения являются загрязнителями из-за их вклада в истощение озонового слоя, глобальное потепление, биоаккумуляцию и токсичность. В области химии фторорганических соединений часто требуются специальные методы, связанные с обращением с фторирующими агентами.
Фтор имеет несколько отличий от всех других заместителей, встречающихся в органических молекулах. В результате физические и химические свойства фторорганических соединений могут отличаться от других галогенорганических соединений.
 10 см. Это вызывает очень слабые дисперсионные силы между полифторированными молекулами и является причиной часто наблюдаемого снижения температуры кипения при фторировании, а также одновременной гидрофобности и липофобности полифторированных соединений, в то время как другие пергалогенированные соединения соединения более липофильны.
10 см. Это вызывает очень слабые дисперсионные силы между полифторированными молекулами и является причиной часто наблюдаемого снижения температуры кипения при фторировании, а также одновременной гидрофобности и липофобности полифторированных соединений, в то время как другие пергалогенированные соединения соединения более липофильны.По сравнению с арилхлоридами и бромидами арилфториды образуют реактивы Гриньяра только неохотно. С другой стороны, арилфториды, например фтор анилины и фтор фенолы часто эффективно подвергаются нуклеофильному замещению.
Формально фторуглероды содержат только углерод и фтор. Иногда их называют перфторуглеродами. Это могут быть газы, жидкости, парафины или твердые вещества, в зависимости от их молекулярной массы. Простейшим фторуглеродом является газовый тетрафторметан (CF 4). Жидкости включают перфтороктан и перфтордекалин. В то время как фторуглероды с одинарными связями стабильны, ненасыщенные фторуглероды более реакционноспособны, особенно с тройными связями. Фторуглероды более химически и термически стабильны, чем углеводороды, что отражает относительную инертность связи C-F. Они также относительно липофобны. Из-за пониженных межмолекулярных ван-дер-ваальсовых взаимодействий соединения на основе фторуглеродов иногда используются в качестве смазочных материалов или являются очень летучими. Фторуглеродные жидкости используются в медицине в качестве переносчиков кислорода.
Структура фторорганических соединений может быть отличительной. Как показано ниже, перфторированные алифатические соединения имеют тенденцию отделяться от углеводородов. Этот эффект «подобное растворяется аналогично» связан с полезностью фторсодержащих фаз и использованием PFOA при переработке фторполимеров. В отличие от алифатических производных, перфторароматические производные имеют тенденцию к образованию смешанных фаз с нефторированными ароматическими соединениями в результате донорно-акцепторных взаимодействий между пи-системами.
 Разделение алкильных и перфторалкильных заместителей.
Разделение алкильных и перфторалкильных заместителей. 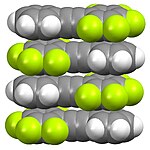 Упаковка в кристаллический пентафтортолан (C 6F5CCC 6H5), иллюстрирующая донорно-акцепторные взаимодействия между фторированным и нефторированным кольцами.
Упаковка в кристаллический пентафтортолан (C 6F5CCC 6H5), иллюстрирующая донорно-акцепторные взаимодействия между фторированным и нефторированным кольцами. Полимерные фторорганические соединения многочисленны и имеют коммерческое значение. Они варьируются от полностью фторированных видов, например ПТФЭ до частично фторированного, например поливинилиденфторид ([CH 2CF2]n) и полихлортрифторэтилен ([CFClCF 2]n). Фторполимерный политетрафторэтилен (ПТФЭ / тефлон) представляет собой твердое вещество.
Гидрофторуглероды (ГФУ), органические соединения, содержащие атомы фтора и водорода, являются наиболее распространенным типом фторорганических соединений. Они обычно используются в кондиционировании воздуха и в качестве хладагентов вместо более старых хлорфторуглеродов, таких как R-12 и гидрохлорфторуглеродов, таких как Р-21. Они не так вредят озоновому слою, как заменяемые ими соединения; однако они действительно способствуют глобальному потеплению. Их атмосферные концентрации и вклад в антропогенные выбросы парниковых газов быстро увеличиваются, вызывая международную озабоченность по поводу их радиационного воздействия.
Фторуглероды с небольшим количеством связей CF ведут себя аналогично исходным углеводородам., но их реакционная способность может быть существенно изменена. Например, как урацил, так и 5-фторурацил представляют собой бесцветные высокоплавкие кристаллические твердые вещества, но последний является сильнодействующим противораковым лекарственным средством. Использование связи C-F в фармацевтике основано на этой измененной реакционной способности. Некоторые лекарственные средства и агрохимикаты содержат только один фтористый центр или одну трифторметильную группу.
В отличие от других парниковых газов в Парижском соглашении, по гидрофторуглеродам ведутся другие международные переговоры.
В сентябре 2016 года так называемая Нью-Йоркская декларация призвала к глобальному сокращению использование ГФУ. 15 октября 2016 года из-за того, что эти химические вещества способствуют изменению климата, переговорщики из 197 стран, собравшиеся на саммите Программы Организации Объединенных Наций по окружающей среде в Кигали, Руанда, достигли юридически обязывающего соглашения. для поэтапного отказа от гидрофторуглеродов (ГФУ) в поправке к Монреальскому протоколу.
Как указано в этой статье, фтор-заместители приводят к реакционной способности, которая сильно отличается от классической органической химии. Первым примером является дифторкарбен, CF 2, который является синглетом, тогда как карбен (CH 2) имеет триплет основное состояние. Это различие является существенным, поскольку дифторкарбен является предшественником тетрафторэтилена.
Перфторированные соединения - это производные фторуглеродов, поскольку они по структуре тесно связаны с фторуглеродами. Однако они также обладают новыми атомами, такими как азот, йод, или ионными группами, такими как перфторированные карбоновые кислоты.
Фторорганические соединения получают различными способами, в зависимости от степени и региохимии искомого фторирования и природы предшественников. Прямое фторирование углеводородов с помощью F 2, часто разбавленного N 2, полезно для высокофторированных соединений:
Однако такие реакции часто являются неселективными и требуют осторожности, поскольку углеводороды могут неконтролируемо «гореть» в F. 2, аналогично горению углеводорода в O. 2. По этой причине были разработаны альтернативные методики фторирования. Обычно такие методы делятся на два класса.
Электрофильное фторирование основывается на источниках «F». Часто такие реагенты содержат связи N-F, например F-TEDA-BF 4. Асимметричное фторирование, при котором только один из двух возможных энантиомерных продуктов образуется из прохирального субстрата, зависит от реагентов электрофильного фторирования. Иллюстрацией этого подхода является приготовление предшественника противовоспалительных агентов:

Специализированный, но важный метод электрофильного фторирования включает электросинтез. Метод в основном используется для перфторирования, т.е. замены всех связей C – H связями C – F. Углеводород растворяют или суспендируют в жидком HF, и смесь электролизуют при 5–6 V с использованием анодов Ni . Впервые этот метод был продемонстрирован при получении перфторпиридина (C. 5F. 5N) из пиридина (C. 5H. 5N). Было описано несколько вариантов этого метода, включая использование расплавленного бифторида калия или органических растворителей.
Основной альтернативой электрофильному фторированию, естественно, является нуклеофильное фторирование с использованием реагентов, которые являются источниками «F», для нуклеофильного замещения обычно хлорида и бромида. Реакции метатезиса с использованием фторидов щелочных металлов являются простейшими.
Алкилмонофториды может быть получен из спиртов и реагента Ола (фторид пиридиния) или других фторирующих агентов.
При разложении тетрафторборатов арилдиазония в реакциях Сандмейера или Шимана используются фторбораты в качестве источников F.
Хотя фтороводород может показаться маловероятным нуклеофилом, он является наиболее распространенным источником фторида при синтезе фторорганических соединений. Такие реакции часто катализируются фторидами металлов, такими как трифторид хрома. 1,1,1,2-Тетрафторэтан, заменитель CFC, получают промышленным способом с использованием следующего подхода:
Обратите внимание, что это преобразование включает в себя два типа реакций: метатезис (замена Cl на F) и гидрофторирование алкена.
Агенты дезоксофторирования осуществить замену гидроксильной и карбонильной групп одним и двумя фторидами соответственно. Одним из таких реагентов, используемых для фторида для оксидного обмена в карбонильных соединениях, является тетрафторид серы :

Многие фторорганические соединения образуются из реагентов, доставляющих перфторалкильные и перфторарильные группы. (Трифторметил) триметилсилан, CF 3 Si (CH 3)3, используется, например, в качестве источника трифторметильной группы. Среди доступных фторированных строительных блоков CF 3 X (X = Br, I), C 6F5Br и C 3F7I. Эти частицы образуют реагенты Гриньяра, которые затем можно обрабатывать различными электрофилами.. Развитие фторсодержащих технологий (см. Ниже в разделе о растворителях) ведет к разработке реагентов для введения «фторсодержащих хвостов».
Особым, но важным применением подхода с использованием фторированных строительных блоков является синтез тетрафторэтилена, который производят в промышленных масштабах в промышленных масштабах посредством промежуточного соединения дифторкарбена. Процесс начинается с термического (600-800 ° C) дегидрохлорирования хлордифторметана :
Используется фтордихлорацетат натрия (CAS # 2837-90-3) для образования хлорфторкарбена для циклопропанирования.
Использование фторсодержащих радиофармпрепаратов в F- позитронно-эмиссионной томографии послужило стимулом для разработки новых методов формирования C – F связи. Из-за короткого периода полураспада F эти синтезы должны быть высокоэффективными, быстрыми и легкими. Иллюстрацией методов является получение глюкозы, модифицированной фтором, путем замещения трифлата меченым фторидным нуклеофилом:

Биологически синтезированные фторорганические соединения имеют были обнаружены у микроорганизмов и растений, но не у животных. Наиболее распространенным примером является фторацетат, который используется в качестве защиты растений от травоядных по меньшей мере на 40 растениях в Австралии, Бразилии и Африке. Другие биологически синтезированные органофторины включают ω-фтор жирные кислоты, фторацетон и 2-фторцитрат, которые, как полагают, все биосинтезируются биохимическими путями из промежуточного фторацетальдегида. Аденозилфторидсинтаза - это фермент, способный к биологическому синтезу связи углерод-фтор. Связи углерода и фтора, созданные человеком, обычно встречаются в фармацевтике и агрохимии, поскольку они добавляют стабильность углеродному каркасу; кроме того, относительно небольшой размер фтора удобен, поскольку фтор действует как приблизительный биоизостер группы гидроксильной. Введение углеродно-фторной связи в органические соединения является основной проблемой для медицинских химиков, использующих фторорганическую химию, поскольку углерод-фторная связь увеличивает вероятность получения успешного лекарства примерно в десять раз. По оценкам, 20% фармацевтических препаратов и 30–40% агрохимикатов составляют фторорганические соединения, в том числе некоторые из самых популярных лекарств. Примеры включают 5-фторурацил, флуоксетин (прозак), пароксетин (паксил), ципрофлоксацин (ципро), мефлохин и флуконазол.
Фторорганическая химия влияет на многие области повседневной жизни и технологий. Связь CF присутствует в фармацевтике, агрохимии, фторполимерах, хладагентах, поверхностно-активных веществах, анестетиках., масляные репелленты, катализаторы и гидрофобизаторы и другие.
Связь углерод-фтор обычно встречается в фармацевтических препаратах и агрохимикатах, поскольку она, как правило, метаболически стабильна, а фтор действует как биоизостер атом водорода. По оценкам, пятая часть фармацевтических препаратов содержит фтор, в том числе некоторые из самых популярных препаратов. Примеры включают 5-фторурацил, флунитразепам (рогипнол), флуоксетин (прозак), пароксетин (паксил), ципрофлоксацин (Cipro), мефлохин и флуконазол. Фторзамещенные простые эфиры являются летучими анестетиками, включая коммерческие продукты метоксифлуран, энфлуран, изофлуран, севофлуран и десфлуран. Фторуглеродные анестетики снижают опасность воспламенения с помощью диэтилового эфира и циклопропана. Перфторированные алканы используются в качестве кровезаменителей.
Фторуглероды также используются в качестве пропеллента для дозированных ингаляторов, используемых для введения некоторых лекарств от астмы. Текущее поколение пропеллента состоит из гидрофторалканов (HFA), которые пришли на смену ингаляторам на основе CFC. Ингаляторы с ХФУ были запрещены в 2008 году в рамках Монреальского протокола из-за экологических проблем с озоновым слоем. Пропеллентные ингаляторы HFA, такие как ProAir (сальбутамол ), не имеют общих версий по состоянию на октябрь 2014 года.
Фторсодержащие ПАВ с полифторированным «хвостом» и гидрофильная «голова», служат в качестве поверхностно-активных веществ, поскольку они концентрируются на границе раздела жидкость-воздух из-за своей липофобности. Фторсодержащие ПАВ имеют низкую поверхностную энергию и значительно меньшее поверхностное натяжение. Фторсодержащие ПАВ перфтороктансульфоновая кислота (ПФОС ) и перфтороктановая кислота (ПФОК ) являются двумя из наиболее изученных из-за их повсеместного распространения, токсичности и токсичности. и длительное время пребывания в организме человека и дикой природы.
Фторированные соединения часто проявляют отчетливые свойства растворимости. Дихлордифторметан и хлордифторметан были широко используемыми хладагентами. CFC обладают мощным озоноразрушающим потенциалом из-за гомолитического расщепления связей углерод-хлор; их использование в значительной степени запрещено Монреальским протоколом. Гидрофторуглероды (ГФУ), такие как тетрафторэтан, служат заменителями ХФУ, поскольку они не катализируют разрушение озона. Кислород проявляет высокую растворимость в перфторуглеродных соединениях, что еще раз отражается на их липофильности. Перфтордекалин был продемонстрирован как кровезаменитель, доставляющий кислород в легкие.
Растворитель 1,1,1,2-тетрафторэтан был использован для экстракции природных продуктов, таких как таксол, масло примулы вечерней и ванилин. 2,2,2-трифторэтанол представляет собой устойчивый к окислению полярный растворитель.
Развитие химии фторорганических соединений дало много ценных реагентов, выходящих за рамки химии фторорганических соединений. Трифликовая кислота (CF 3SO3H) и трифторуксусная кислота (CF 3CO2H) полезны в органическом синтезе. Их сильная кислотность объясняется электроотрицательностью трифторметильной группы, которая стабилизирует отрицательный заряд. Трифлатная группа (конъюгированное основание трифликовой кислоты) является хорошей уходящей группой в реакциях замещения.
Представляющие актуальный интерес в области «зеленой химии» высокофторированные заместители, например перфторгексил (C 6F13) придает молекулам отличительные свойства растворимости, что облегчает очистку продуктов в органическом синтезе. В этой области, описанной как «фторсодержащая химия », используется концепция подобного-растворяется-подобное в том смысле, что соединения, богатые фтором, растворяются преимущественно в богатых фтором растворителях. Из-за относительной инертности связи C-F такие фтористые фазы совместимы даже с агрессивными реагентами. Эта тема породила методы «фторсодержащего мечения и фторсодержащей защиты. Иллюстрацией фторсодержащей технологии является использование фторалкилзамещенных гидридов олова для восстановления, при этом продукты легко отделяются от отработанного оловянного реагента путем экстракции с использованием фторированных растворителей.>Гидрофобные фторированные ионные жидкости, такие как органические соли бистрифлимида или гексафторфосфата, могут образовывать фазы, нерастворимые как в воде, так и в органических растворителях, с образованием многофазные жидкости.
Фторорганические лиганды давно используются в металлоорганической и координационной химии. Одним из преимуществ F-содержащих лигандов является удобство F ЯМР-спектроскопии для мониторинга реакций. Фторорганические соединения могут служить в качестве «сигма-донорного лиганда», как проиллюстрировано производным титана (III) [(C 5Me5)2Ti (FC 6H5)] BPh 4. Однако чаще всего фторуглероды ub-заместители используются для увеличения льюисовской кислотности металлических центров. Первым примером является «Eufod », координационный комплекс европия (III), который содержит модифицированный перфторгептилом ацетилацетонат лиганд. Этот и родственные ему частицы используются в органическом синтезе и в качестве «реагентов сдвига» в ЯМР-спектроскопии.
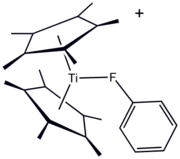 Структура [(C 5Me5)2Ti (FC 6H5)], координационного комплекса фторорганического лиганда.
Структура [(C 5Me5)2Ti (FC 6H5)], координационного комплекса фторорганического лиганда. В области, где совпадают координационная химия и материаловедение, фторирование органических лигандов используется для настройки свойств компонентных молекул. Например, степень и региохимия фторирования металлированных 2-фенилпиридиновых лигандов в Комплексы платины (II) значительно изменяют эмиссионные свойства комплексов.
Координационная химия фторорганических лигандов также включает фторсодержащие технологии. Например, трифенилфосфин был модифицирован путем присоединения перфторалкильных заместителей, которые обеспечивают растворимость в перфторгексане, а также в сверхкритическом диоксиде углерода. В качестве конкретного примера, [(C 8F17C3H6-4-C 6H4)3P.
Активная область металлоорганической химии охватывает расщепление C -F-связи реагентами на основе переходных металлов. Разработаны как стехиометрические, так и каталитические реакции, которые представляют интерес с точки зрения органического синтеза и ремедиации ксенохимических веществ. Активация связи CF классифицируется следующим образом: (i) окислительное присоединение фторуглерода, (ii) образование связи M – C с отщеплением HF, (iii) образование связи M – C с отщеплением фторсилана, (iv) гидродефторирование фторуглерода с образованием связи M – F, (v) нуклеофильная атака на фторуглерод и (vi) дефторирование фторуглерода ». Иллюстративной опосредованной металлами реакции активации CF является дефторирование фторгексана ди гидридом циркония, аналогом реагента Шварца :
Фторсодержащие соединения часто присутствуют в некоординирующих или слабо координирующих анионах. Оба тетракис (пентафторфенил) борат, B (C 6F5)4, и родственный тетракис [3,5-бис (трифторметил) фенил] борат, полезны в катализе Циглера-Натта и родственных ему Методологии полимеризации алкенов. Фторированные заместители делают анионы слабоосновными и повышают растворимость в слабощелочных растворителях, которые совместимы с сильными кислотами Льюиса.
Фторорганические соединения находят множество нишевых применений в материаловедение. Обладая низким коэффициентом трения , жидкие фторполимеры используются в качестве специальных смазочных материалов. На основе фторуглеродов смазки используются в сложных условиях. Типичные продукты включают Fomblin и Krytox, производимые Solvay Solexis и DuPont, соответственно. Некоторые смазочные материалы для огнестрельного оружия, такие как «Tetra Gun», содержат фторуглероды. Благодаря своей негорючести фторуглероды используются в пенах для тушения пожаров. Фторорганические соединения являются компонентами жидкокристаллических дисплеев. Полимерный аналог трифликовой кислоты, нафион, представляет собой твердую кислоту, которая используется в качестве мембраны в большинстве низкотемпературных топливных элементов. Бифункциональный мономер 4,4'-дифторбензофенон является предшественником полимеров класса PEEK.

В отличие от многих встречающихся в природе органических соединений, содержащих более тяжелые галогениды, хлорид, бромид и йодид, только небольшое количество биологически синтезированного фторуглерода облигации известны. Самым распространенным естественным фторорганическим соединением является фторацетат, токсин, обнаруженный в некоторых видах растений. Другие включают фторолеиновую кислоту, фторацетон, нуклеоцидин (4'-фуоро-5'-O-сульфамоиладенозин), фтортреонин и 2-фторцитрат. Некоторые из этих видов, вероятно, биосинтезируются из фторацетальдегида. фермент фториназа катализирует синтез 5'-фтор-5-дезоксиаденозина (см. Схему справа).
Фторорганическая химия началась в 1800-х годах с развитием органической химии. Первые фторорганические соединения были получены с использованием трифторида сурьмы в качестве источника F. Негорючесть и нетоксичность хлорфторуглеродов CCl 3 F и CCl 2F2привлекли внимание промышленности в 1920-х годах. 6 апреля 1938 года Рой Дж. Планкетт, молодой химик-исследователь, который работал в лаборатории Джексона DuPont в Дипуотер, Нью-Джерси, случайно обнаружил политетрафторэтилен (ПТФЭ). Последующие крупные разработки, особенно в США, основывались на опыте, накопленном в производстве гексафторида урана. Начиная с конца 1940-х годов был введен ряд методологий электрофильного фторирования, начиная с CoF 3. Было объявлено об электрохимическом фторировании («электрофторирование »), которое Джозеф Х. Саймонс разработал в 1930-х годах для получения высокостабильных перфторированных материалов, совместимых с гексафторидом урана. Эти новые методологии позволили синтезировать связи C-F без использования элементарного фтора и без использования метатетических методов.
В 1957 году была описана противораковая активность 5-фторурацила. В этом отчете был представлен один из первых примеров рационального дизайна лекарств. Это открытие вызвало всплеск интереса к фторированным фармацевтическим и агрохимическим препаратам. Открытие соединений благородных газов, например XeF 4 предоставил множество новых реагентов, начиная с начала 1960-х годов. В 1970-х годах фтордезоксиглюкоза была признана полезным реагентом для позитронно-эмиссионной томографии F . В работе, получившей Нобелевскую премию, было показано, что ХФУ способствуют разрушению атмосферного озона. Это открытие предупредило мир о негативных последствиях фторорганических соединений и послужило стимулом для разработки новых путей получения фторорганических соединений. В 2002 году было сообщено о первом ферменте, образующем связь CF, фториназа.
Лишь некоторые фторорганические соединения обладают высокой биологической активностью и высокой токсичностью, такие как фторацетат и перфторизобутен.
Некоторые фторорганические соединения представляют значительную опасность для здоровья и окружающей среды. ХФУ и ГХФУ (гидрохлорфторуглерод ) разрушают озоновый слой и являются сильнодействующими парниковыми газами. ГФУ являются сильнодействующими парниковыми газами и сталкиваются с призывами к более строгому международному регулированию и графикам поэтапного отказа в качестве быстрой меры по сокращению выбросов парниковых газов, как и перфторуглероды (ПФУ) и гексафторид серы (SF 6).
Из-за воздействия соединения на климат крупнейшие страны Большой двадцатки в 2013 году согласились поддержать инициативы по поэтапному отказу от использования ГХФУ. Они подтвердили роль Монреальского протокола и Рамочной конвенции Организации Объединенных Наций об изменении климата в глобальном учете и сокращении ГХФУ. США и Китай в то же время объявили о двустороннем соглашении с аналогичным эффектом.
Из-за прочности связи углерод-фтор многие синтетические фторуглероды и соединения на основе фторуглеродов стойкие в окружающей среде. Фторсодержащие ПАВ, такие как ПФОС и ПФОК, являются стойкими глобальными загрязнителями. ХФУ на основе фторуглеродов и тетрафторметан были обнаружены в изверженных и метаморфических породах. ПФОС является стойким органическим загрязнителем и может наносить вред здоровью дикой природы; Потенциальное воздействие ПФОК на здоровье человека изучается Научной группой C8.