| |||
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Пиридин | |||
| Системное название IUPAC Азабензол | |||
| Другие названия Азин. Азинин. 1-Азациклогекса-1,3,5-диен | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.003.464 | ||
| Номер EC |
| ||
| KEGG | |||
| PubChem CID | |||
| UNII | |||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химические формула | C5H5N | ||
| Молярная масса | 79,102 г · моль | ||
| Внешний вид | Бесцветная жидкость | ||
| Запах | Тошнота, рыбоподобность | ||
| Плотность | 0,9819 г / мл | ||
| Точка плавления | −41,6 ° C (- 42,9 ° F; 231,6 K) | ||
| Точка кипения | 115,2 ° C (239,4 ° F; 388,3 K) | ||
| Растворимость в воде | Смешиваемость | ||
| log P | 0,73 | ||
| Давление пара | 16 мм рт. ст. (20 ° C) | ||
| Конъюгированная кислота | Пиридиний | ||
| Показатель преломления (nD) | 1,5093 | ||
| Вязкость | 0,88 сП 25 ℃ | ||
| Дипольный момент | 2,2 D | ||
| Опасности | |||
| Паспорт безопасности | См.: страница данных | ||
| Классификация ЕС (DSD) (устарело) | Воспламеняющееся (F). Вредно (Xn) | ||
| R-фразы (устаревшие) | R20 R21 R22 R34 R36 R38 | ||
| NFPA 704 (пожар алмаз) |  3 2 0 3 2 0 | ||
| Температура вспышки | 21 ° C (70 ° F; 294 K) | ||
| Пределы взрываемости | 1,8–12,4% | ||
| Пороговое предельное значение (ПДК) | 5 ppm (TWA) | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LD50(средняя доза ) | 891 мг / кг (крыса, перорально). 1500 мг / кг (мышь, перорально). 1580 мг / кг (крыса, перорально) | ||
| LC50(средняя концентрация ) | 9000 ppm (крыса, 1 час) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимое) | TWA 5 частей на миллион (15 мг / м3) | ||
| REL (рекомендуется) | T WA 5 ppm (15 мг / м) | ||
| IDLH (Непосредственная опасность) | 1000 ppm | ||
| Родственные соединения | |||
| Родственные амины | Пиколин. Хинолин | ||
| Родственные соединения | Анилин. Пиримидин. Пиперидин | ||
| Страница дополнительных данных | |||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. д. | ||
| Термодинамические. данные | Фазовое поведение. твердое тело – жидкость – газ | ||
| Спектральные данные | UV, IR, ЯМР, MS | ||
| Если не указано иное, данные приведены для материалы в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Пиридин представляет собой основное гетероциклическое органическое соединение с химической формулой C5 H5 N. Он структурно связан с бензолом, с одной метиновой группой (= CH-), замененной на атом азота. Это легковоспламеняющаяся, слабощелочная, смешивающаяся с водой жидкость с характерным неприятным запахом рыбы. Пиридин бесцветен, но старые или загрязненные образцы могут иметь желтый цвет. Пиридиновое кольцо присутствует во многих важных соединениях, включая агрохимикаты, фармацевтические препараты и витамины. Исторически пиридин производился из каменноугольной смолы. Сегодня он синтезируется в масштабе около 20 000 тонн в год во всем мире.
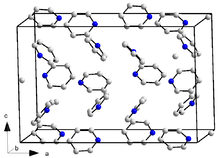 Кристаллическая структура пиридин
Кристаллическая структура пиридин . Молекулярный электрический дипольный момент составляет 2,2 дебаев. Пиридин является диамагнитным и имеет диамагнитную восприимчивость, равную -48,7 × 10 см · моль. Стандартная энтальпия образования составляет 100,2 кДж · моль в жидкой фазе и 140,4 кДж · моль в газовой фазе. При 25 ° C пиридин имеет вязкость 0,88 мПа / с и теплопроводность 0,166 Вт · м · К. энтальпия парообразования составляет 35,09 кДж · моль при точке кипения и нормальном давлении. энтальпия плавления составляет 8,28 кДж · моль при температуре плавления.
. Критическими параметрами пиридина являются давление 6,70 МПа, температура 620 К и объем 229 см · моль.. В диапазоне температур 340–426 ° C его давление пара p можно описать с помощью уравнения Антуана

где T - температура, A = 4,16272, B = 1371,358 K и C = −58,496 K.
Аналогично бензола, пиридиновое кольцо образует шестиугольник C 48 5 15 N. Локализация электронов в пиридине отражается в более короткой кольцевой связи C – N (137 пм для связи C – N в пиридине против 139 пм для связи C – C в бензоле), тогда как связи углерод-углерод в пиридиновом кольце имеют такую же длину 139 пм, что и в бензоле. Эти длины связей лежат между значениями одинарной и двойной связи и являются типичными для ароматических соединений.
Пиридин кристаллизуется в орторомбической кристаллической системе с пространственной группой Pna2 1 и параметрами решетки a = 1752 pm, b = 897 pm, c = 1135 pm, и 16 формульных единиц на элементарную ячейку (измерено при 153 K). Для сравнения, кристаллический бензол также является ромбическим, с пространственной группой Pbca, a = 729,2 пм, b = 947,1 пм, c = 674,2 пм (при 78 К), но количество молекул на ячейку составляет всего 4 Это различие частично связано с более низкой симметрией отдельной молекулы пиридина (C 2v против D 6h для бензола). Известен три гидрат (пиридин · 3H 2 O); он также кристаллизуется в орторомбической системе в пространственной группе Pbca, параметры решетки a = 1244 пм, b = 1783 пм, c = 679 пм и восемь формульных единиц на элементарную ячейку (измерено при 223 К).
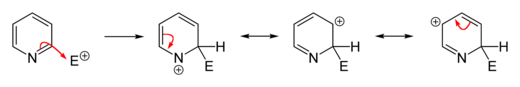
Спектр оптического поглощения пиридина в гексане содержит три полосы на длинах волн 195 нм (переход π → π *, молярная поглощающая способность ε = 7500 л · моль · см), 251 нм (π → π * переход, ε = 2000 л · моль · см) и 270 нм (n → π * переход, ε = 450 л · моль · см). Спектр H ядерного магнитного резонанса (ЯМР) пиридина содержит три сигнала с соотношением интегральных интенсивностей 2: 1: 2, которые соответствуют трем химически различным протонам в молекуле. Эти сигналы исходят от α-протонов (положения 2 и 6, химический сдвиг 8,5 м.д.), γ-протонов (положение 4, 7,5 м.д.) и β-протонов (положения 3 и 5, 7,1 м.д.). Углеродный аналог пиридина, бензол, имеет только один сигнал протона при 7,27 м.д. Большие химические сдвиги α- и γ-протонов по сравнению с бензолом являются результатом более низкой электронной плотности в α- и γ-положениях, что может быть получено из резонансных структур. Ситуация довольно похожа для спектров ЯМР 13С пиридина и бензола: пиридин показывает триплет при δ (α-C) = 150 м.д., δ (β-C) = 124 м.д. и δ (γ-C) = 136 м.д. тогда как бензол имеет единственную линию при 129 ppm. Все смены указаны для веществ, не содержащих растворителей. Пиридин обычно обнаруживают методами газовой хроматографии и масс-спектрометрии.
Из-за электроотрицательного азота в пиридиновом кольце молекула относительно электронодефицитна. Следовательно, он менее легко вступает в реакции электрофильного ароматического замещения, чем производные бензола. Соответственно, пиридин более склонен к нуклеофильному замещению, о чем свидетельствует легкость металлирования сильными металлоорганическими основаниями. По реакционной способности пиридин можно выделить три химические группы. Для электрофилов имеет место электрофильное замещение, когда пиридин проявляет ароматические свойства. С нуклеофилами пиридин реагирует в положениях 2 и 4 и, таким образом, ведет себя аналогично иминам и карбонилам. Реакция со многими кислотами Льюиса приводит к присоединению к атому азота пиридина, что аналогично реакционной способности третичных аминов. Способность пиридина и его производных окисляться с образованием оксидов амина (N-оксидов) также является характеристикой третичных аминов.
Азотный центр пиридина имеет основание неподеленная пара из электронов. Эта неподеленная пара не перекрывается с кольцом ароматической π-системы, следовательно, пиридин является основным, имеющим химические свойства, аналогичные свойствам третичных аминов. Протонирование дает пиридин, C 5H5NH. pKa сопряженной кислоты (катион пиридиния) составляет 5,25. Строения пиридина и пиридиния практически идентичны. Катион пиридиния изоэлектронен бензолу. Пиридиния п- толуолсульфонат (PPTS) представляет собой иллюстративную соль пиридиния; его получают обработкой пиридина п-толуолсульфоновой кислотой. Помимо протонирования, пиридин подвергается N-центрированному алкилированию, ацилированию и N-окислению.
 пиридина с его свободным электронная пара
пиридина с его свободным электронная пара Пиридин имеет сопряженную систему из шести π-электронов, которые делокализованы по кольцу. Молекула плоская и, таким образом, соответствует критериям Хюккеля для ароматических систем. В отличие от бензола, электронная плотность неравномерно распределена по кольцу, отражая отрицательный индуктивный эффект атома азота. По этой причине пиридин имеет дипольный момент и более слабую резонансную стабилизацию, чем бензол (энергия резонанса 117 кДж · моль в пиридине против 150 кДж · моль в бензоле).
Кольцевые атомы в молекуле пиридина sp-гибридизированы. Азот участвует в π-связывающей ароматической системе, используя свою негибридизированную p-орбиталь. Неподеленная пара находится на sp-орбитали, выступая наружу из кольца в той же плоскости, что и σ-связи. В результате неподеленная пара не вносит вклад в ароматическую систему, но существенно влияет на химические свойства пиридина, поскольку она легко поддерживает образование связи посредством электрофильной атаки. Однако из-за отделения неподеленной пары от ароматической кольцевой системы атом азота не может проявлять положительный мезомерный эффект.
Известно много аналогов пиридина, в которых N заменен другими гетероатомами (см. Рисунок ниже). Замещение одного C – H в пиридине вторым N дает диазин гетероциклы (C 4H4N2) с названиями пиридазин, пиримидин, и пиразин.
 длины и углы связей бензола, пиридина, фосфорина, арсабензола, стибабензола и бисмабензола длины и углы связей бензола, пиридина, фосфорина, арсабензола, стибабензола и бисмабензола |  атомных орбиталей в пиридине атомных орбиталей в пиридине |
 Резонансные структуры пиридина Резонансные структуры пиридина |  Атомные орбитали в протонированном пиридине Атомные орбитали в протонированном пиридине |
 Томас Андерсон
Томас Андерсон Неочищенный пиридин, несомненно, был получен ранними алхимиками путем нагревания костей животных и другого органического вещества, но самые ранние задокументированная ссылка приписывается шотландскому ученому Томасу Андерсону. В 1849 году Андерсон исследовал состав масла, полученного путем высокотемпературного нагревания костей животных. Среди других веществ он выделил из масла бесцветную жидкость с неприятным запахом, из которой два года спустя выделил чистый пиридин. Он описал его как хорошо растворимый в воде, легко растворимый в концентрированных кислотах и солях при нагревании и лишь слабо растворимый в маслах.
Из-за его воспламеняемости Андерсон назвал новое вещество пиридином после греческого : πῦρ (pyr), что означает огонь. Суффикс идин был добавлен в соответствии с химической номенклатурой, как в толуидин, для обозначения циклического соединения, содержащего атом азота.
Химическая структура пиридина была определена спустя десятилетия после его открытия. Вильгельм Кёрнер (1869) и Джеймс Дьюар (1871) предположили, что по аналогии между хинолином и нафталином структура пиридина является получено из бензола путем замены одного C – H звена на атом азота. Предположение Кёрнера и Дьюара позже было подтверждено в эксперименте, в котором пиридин восстанавливали до пиперидина с помощью натрия в этаноле. В 1876 году Уильям Рамзи соединил ацетилен и цианистый водород в пиридин в раскаленной железотрубной печи. Это был первый синтез гетероароматического соединения.
Первый крупный синтез производных пиридина был описан в 1881 году Артуром Рудольфом Ганцшем. Синтез пиридина Ганча обычно использует смесь 2: 1: 1 β- кетокислоты (часто ацетоацетат ), альдегида (часто формальдегид ) и аммиак или его соль в качестве донора азота. Сначала получают дважды гидрированный пиридин, который затем окисляют до соответствующего производного пиридина. Эмиль Кневенагель показал, что с помощью этого процесса можно получить асимметрично-замещенные производные пиридина.
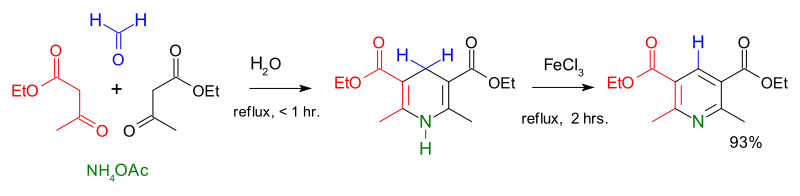 Синтез пиридина по Ганцу с ацетоацетатом, формальдегидом и ацетатом аммония и железом (III) хлорид в качестве окислителя.
Синтез пиридина по Ганцу с ацетоацетатом, формальдегидом и ацетатом аммония и железом (III) хлорид в качестве окислителя. Современные способы получения пиридина имеют низкий выход, и растущий спрос на новое соединение побуждает искать более эффективные пути. Прорыв произошел в 1924 году, когда русский химик Алексей Чичибабин изобрел реакцию синтеза пиридина, основанную на недорогих реагентах. Этот метод до сих пор используется для промышленного производства пиридина.
Пиридин в природе встречается редко, за исключением листьев и корней белладонны (Atropa belladonna ) и в зефире (Althaea officinalis ). Однако производные пиридина часто входят в состав биомолекул, таких как алкалоиды.
. В повседневной жизни следовые количества пиридина являются компонентами летучих органических соединений, которые образуются при обжиге и консервировании процессы, например в жареной курице сукияки, жареном кофе, картофельных чипсах и жареном беконе. Следы пиридина можно найти в сыре Бофор, вагинальных выделениях, черном чае, слюне людей, страдающих гингивитом и подсолнечный мед.
4-бромпиридин
2,2'- бипиридин

пиридин-2,6-дикарбоновая кислота (дипиколиновая кислота )

Общая форма пиридиния катион
Исторически пиридин извлекался из каменноугольной смолы или получался как побочный продукт при газификации угля. Этот процесс был трудоемким и неэффективным : каменноугольная смола содержит только около 0,1% пиридина, поэтому потребовалась многоступенчатая очистка, которая еще больше снизила выход. В настоящее время большая часть пиридина производится синтетически с использованием различных названных реакций, и основные из них обсуждаются ниже.
В 1989 году во всем мире было произведено 26 000 тонн пиридина. Среди 25 крупнейших предприятий по производству пиридина одиннадцать расположены в Европе (по состоянию на 1999 год). Основные производители пиридина к ним относятся Evonik Industries, Rütgers Chemicals, Jubilant Life Sciences, Imperial Chemical Industries и Koei Chemical. Производство пиридина значительно увеличилось в начале 2000-х, и только в материковом Китае годовая производственная мощность составила 30 000 тонн. Совместное американо-китайское предприятие Vertellus в настоящее время является мировым лидером в производстве пиридина.
Синтез пиридина чичибабина был описан в 1924 году и до сих пор используется в промышленность. В общем виде реакция может быть описана как реакция конденсации альдегидов, кетонов, α, β-ненасыщенных карбонильных соединений или любую комбинацию вышеперечисленного в аммиак или производные аммиака. В частности, незамещенный пиридин получают из формальдегида и ацетальдегида, которые являются недорогими и широко доступными. Во-первых, акролеин образуется при конденсации Кневенагеля из ацетальдегида и формальдегида. Затем акролеин конденсируют с ацетальдегидом и аммиаком с получением дигидропиридина, который окисляется с помощью твердотельного катализатора до пиридина. Этот процесс осуществляется в газовой фазе при 400–450 ° C. Продукт состоит из смеси пиридина, простых метилированных пиридинов (пиколинов и лутидинов ); его состав зависит от используемого катализатора и может быть адаптирован к потребностям производителя. Катализатор обычно представляет собой соль переходного металла, такую как фторид кадмия (II) или фторид марганца (II), но кобальт и таллий также могут быть использованы соединения. Восстановленный пиридин отделяется от побочных продуктов в многостадийном процессе.
 Образование акролеина из ацетальдегида и формальдегида
Образование акролеина из ацетальдегида и формальдегида 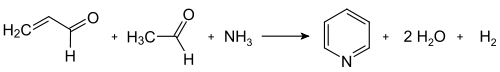 Конденсация пиридина из акролеина и ацетальдегида
Конденсация пиридина из акролеина и ацетальдегида Практическое применение традиционного синтеза пиридина Чичибабина ограничено его стабильно низким выходом обычно около 20%. Такой низкий выход вместе с высоким преобладанием побочных продуктов делает немодифицированные формы метода Чичибабина непопулярными.
Пиридин может быть получен деалкилированием алкилированных пиридинов, которые получаются как побочные продукты в синтезе других пиридинов. Окислительное деалкилирование проводят либо с использованием воздуха над катализатором оксид ванадия (V), либо путем деалкилирования паром на катализаторе на основе никеля, либо с помощью гидродеалкилирования с использованием серебра - или катализатор на основе платины. Выход пиридина может достигать 93% с использованием катализатора на основе никеля.
 Циклизация Беннемана
Циклизация Беннемана Тримеризация части молекулы нитрила и Две части ацетилена в пиридин называют циклизацией Беннемана . Эта модификация Reppe-синтеза может быть активирована либо нагреванием, либо светом. В то время как термическая активация требует высоких давлений и температур, фотоиндуцированное циклоприсоединение протекает в условиях окружающей среды с CoCp 2 (cod) (Cp = циклопентадиенил, cod = 1,5-циклооктадиен ) в качестве катализатора и может выполняться даже в воде. Таким способом можно получить ряд производных пиридина. При использовании ацетонитрила в качестве нитрила получается 2-метилпиридин, который можно деалкилировать до пиридина.
Синтез пиридина по Кронке обеспечивает довольно общий метод получения замещенных пиридинов с использованием самого пиридина в качестве реагента, который не включается в конечный продукт. Взаимодействие пиридина с α-бром сложными эфирами дает родственную пиридиниевую соль, в которой метиленовая группа является сильно кислой. Этот вид претерпевает присоединение типа Майкла к α, β-ненасыщенным карбонилам в присутствии ацетата аммония, чтобы претерпеть замыкание цикла и образование целевого замещенного пиридина, а также бромида пиридиния.

Перегруппировка Чамикиана-Денштедта влечет за собой расширение кольца пиррола с помощью дихлоркарбена до 3-хлорпиридина.

В Синтез Гаттерманна – Скиты, соль сложного эфира малоновой кислоты взаимодействует с дихлор метиламином.
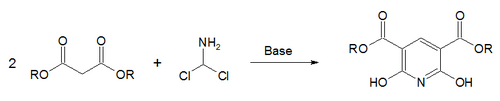
Другой метод - синтез пиридина Богера.
Пиридин также может быть получен декарбоксилированием никотиновая кислота с хромитом меди.
Некоторые производные пиридина играют важную роль в биологических системах. Хотя его биосинтез полностью не изучен, никотиновая кислота (витамин B 3) встречается в некоторых бактериях, грибах и млекопитающие. Млекопитающие синтезируют никотиновую кислоту путем окисления аминокислоты триптофана, где промежуточный продукт, анилин, образует производное пиридина, кинуренин. Напротив, бактерии Mycobacterium tuberculosis и Escherichia coli продуцируют никотиновую кислоту путем конденсации глицеральдегид-3-фосфата и аспарагиновой кислоты.
Несмотря на общие структурные и связывающие черты бензола и пиридина, их реакционная способность значительно различается. Напротив, по своей реакционной способности пиридин больше похож на нитробензол.
Из-за пониженной электронной плотности в ароматической системе электрофильные замещения подавляются в пиридине. и его производные. Алкилирование или ацилирование Фриделя – Крафтса обычно не работает для пиридина, потому что они приводят только к присоединению по атому азота. Замещения обычно происходят в 3-м положении, которое является наиболее богатым электронами атомом углерода в кольце и, следовательно, более восприимчивым к электрофильному присоединению.


Прямое нитрование пиридина происходит медленно. Производные пиридина, в которых атом азота экранирован стерически и / или электронно, могут быть получены нитрованием тетрафторборатом нитрония (NO 2BF4). Таким образом, 3-нитропиридин может быть получен путем синтеза 2,6-дибромпиридина с последующим дебромированием.
Сульфирование пиридина даже сложнее, чем нитрование. Однако можно получить пиридин-3-сульфоновую кислоту. Реакция с группой SO 3 также способствует добавлению серы к атому азота, особенно в присутствии катализатора сульфата ртути (II).
В отличие от медленное нитрование и сульфирование, бромирование и хлорирование пиридина протекают хорошо.

 Структура N-оксида пиридина
Структура N-оксида пиридина Окисление пиридина происходит при азоте с образованием пиридин-N-оксида. Окисление может быть достигнуто с помощью перкислоты :
Некоторые электрофильные замещения в пиридине эффективно осуществляются с использованием пиридин-N-оксида. с последующей деоксигенацией. Добавление кислорода подавляет дальнейшие реакции по атому азота и способствует замещению по 2- и 4-углеродным атомам. Затем атом кислорода можно удалить, например с использованием цинковой пыли.
В отличие от бензольного кольца пиридин эффективно поддерживает несколько нуклеофильных замен. Причина этого - относительно более низкая электронная плотность атомов углерода кольца. Эти реакции включают замещения с элиминированием иона гидрида и добавления с элиминированием с образованием промежуточной конфигурации арина и обычно протекают в 2- или 4-положении.



Многие нуклеофильные замещения легче происходят не с чистым пиридином, а с пиридином, модифицированным бромом, хлором, фтором или фрагментами сульфоновой кислоты, которые затем становятся уходящей группой. Таким образом, фтор является лучшей уходящей группой для замещения литийорганическими соединениями. Соединения для нуклеофильной атаки могут представлять собой алкоксиды, тиолаты, амины и аммиак (при повышенных давлениях).
Как правило, ион гидрида является плохо уходящей группой и происходит только в нескольких гетероциклических реакциях. Они включают реакцию Чичибабина, которая дает производные пиридина , аминированные по 2-положению. Здесь амид натрия используется в качестве нуклеофила, дающего 2-аминопиридин. Высвобождающийся в этой реакции гидрид-ион соединяется с протоном доступной аминогруппы, образуя молекулу водорода.
Аналогично бензолу, нуклеофильные замещения пиридина могут приводить к образованию промежуточных продуктов пиридина как гетеро арин. Для этой цели производные пиридина могут быть удалены с хорошими уходящими группами с использованием сильных оснований, таких как трет-бутоксид калия. Последующее присоединение нуклеофила к тройной связи имеет низкую селективность, и в результате получается смесь двух возможных аддуктов.
Пиридин поддерживает ряд радикальных реакций, которая используется при его димеризации до бипиридинов. Радикальная димеризация пиридина элементарным натрием или никелем Ренея избирательно дает 4,4'-бипиридин или 2,2'-бипиридин, которые являются важными реагентами-прекурсорами в химической промышленности. Одной из названных реакций с участием свободных радикалов является реакция Миниски. Он может производить 2-трет-бутилпиридин при взаимодействии пиридина с пивалиновой кислотой, нитратом серебра и аммонием в серной кислоте с выходом 97%.
 Добавки различных кислот Льюиса к пиридину
Добавки различных кислот Льюиса к пиридину кислоты Льюиса легко присоединяются к атому азота пиридина, образуя соли пиридиния. Реакция с алкилгалогенидами приводит к алкилированию атома азота. Это создает положительный заряд в кольце, который увеличивает реакционную способность пиридина как в отношении окисления, так и восстановления. Реакция Цинке используется для селективного введения радикалов в соединения пиридиния (она не имеет отношения к химическому элементу цинк ).
 Восстановление пиридина до пиперидина с помощью никеля Ренея
Восстановление пиридина до пиперидина с помощью никеля Ренея Пиперидин получают путем гидрирования пиридина с никелем <143 Катализатор на основе>-, кобальта или рутения при повышенных температурах. Гидрирование пиридина до пиперидина высвобождает 193,8 кДж · моль, что немного меньше энергии гидрирования бензола (205,3 кДж · моль).
Частично гидрированные производные получают в более мягких условиях. условия. Например, восстановление с помощью алюмогидрида лития дает смесь 1,4-дигидропиридина, 1,2-дигидропиридина и 2,5-дигидропиридина. Селективный синтез 1,4-дигидропиридина достигается в присутствии металлоорганических комплексов магния и цинка, а (Δ3,4) -тетрагидропиридин получают электрохимическим восстановлением пиридина <. 637>
Пиридин представляет собой основание Льюиса, отдающее свою пару электронов кислоте Льюиса. Его базовые свойства Льюиса обсуждаются в модели ECW. Его относительную донорную силу по отношению к ряду кислот по сравнению с другими основаниями Льюиса можно проиллюстрировать с помощью графиков C-B. Одним из примеров является комплекс триоксида серы и пиридина (точка плавления 175 ° C), который является агентом сульфатирования, используемым для преобразования спиртов в сложные эфиры сульфата. Пиридин- боран (C5H5NBH 3, точка плавления 10–11 ° C) является мягким восстановителем.
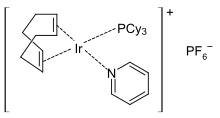 структура катализатора Крэбтри
структура катализатора Крэбтри Пиридиновые комплексы переходного металла многочисленны. Типичные октаэдрические комплексы имеют стехиометрию MCl 2 (py) 4 и MCl 3 (py) 3. Октаэдрические гомолептические комплексы типа M (py) 6 встречаются редко или имеют тенденцию к диссоциации пиридина. Известны многочисленные плоские квадратные комплексы, такие как катализатор Крэбтри. Замененный в ходе реакции пиридиновый лиганд восстанавливается после ее завершения.
η-координационный режим, как в η-бензольных комплексах, наблюдается только в пространственно обремененных производных, которые блокируют азотный центр.
В основном пиридин используется в качестве предшественника гербицидов паракват и дикват. Первая стадия синтеза инсектицида хлорпирифоса состоит из хлорирования пиридина. Пиридин также является исходным соединением для получения фунгицидов на основе пиритиона . цетилпиридиния и лаурилпиридиния, которые могут быть получены из пиридина с помощью реакции Цинке., используются как антисептик в продуктах для ухода за полостью рта и зубов. Пиридин легко подвергается действию алкилирующих агентов с образованием солей N-алкилпиридиния. Одним из примеров является хлорид цетилпиридиния.
 Синтез параквата
Синтез параквата Пиридин используется в качестве полярного, основного, низкоактивного растворителя, например, в конденсации Кневенагеля. Он особенно подходит для дегалогенирования, где он действует как основание реакции элиминирования и связывает полученный галогенид водорода с образованием соли пиридиния. При этерификации и ацилировании пиридин активирует галогениды или ангидриды карбоновой кислоты. Еще более активными в этих реакциях являются производные пиридина , 4-диметиламинопиридин (DMAP) и 4- (1-пирролидинил) пиридин. Пиридин также используется в качестве основы в реакциях конденсации.
 Реакция элиминирования с пиридином с образованием пиридиния
Реакция элиминирования с пиридином с образованием пиридиния Он также используется в текстильной промышленности для повышения сетевой емкости хлопка.
 Окисление спирта до альдегида с помощью реагента Коллинза.
Окисление спирта до альдегида с помощью реагента Коллинза.В качестве основания можно использовать пиридин в качестве реагента Карла Фишера, но его обычно заменяют альтернативами с более приятный запах, такой как имидазол.
хлорхромат пиридиния, дихромат пиридиния и реагент Коллинза (комплекс оксида хрома (VI) используются для окисления спиртов.
Пиридин добавляют к этанолу, чтобы сделать его непригодным для питья. В малых дозах пиридин добавляют к продукты, чтобы придать им горький вкус, и такое использование было одобрено Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США и по-прежнему считается безопасным агентством, даже несмотря на то, что внешнее лоббирование вынудило им запрещено использование пиридина в качестве синтетического ароматизатора в 2018 году. Порог обнаружения пиридина в растворах составляет примерно 1–3 м моль · л (79–237 мг · л).
Пиридин имеет температуру вспышки 17 ° C и, следовательно, легко воспламеняется. Температура воспламенения составляет 550 ° C, смеси 1,7–10,6 об.% Пиридина с воздухом взрывоопасны. Термическая модификация пиридина начинается при температуре выше 490 ° C, в результате образуется бипиридин (в основном 2,2'-бипиридин и в меньшей степени 2,3'-бипиридин и 2,4'-бипиридин), оксиды азота и оксид углерода. Пиридин легко растворяется в воде и наносит вред как животным, так и растениям в водных системах. Разрешенная предельно допустимая концентрация пиридина составляла 15–30 частей на миллион (ppm, или 15–30 мг · м в воздухе) в большинстве стран в 1990-х годах, но была снижена до 5 частей на миллион в 2000-х годах. Для сравнения: воздух в помещении, загрязненный табачным дымом, может содержать до 16 мкг · м пиридина, а одна сигарета - 21–32 мкг.
 Метаболизм пиридина
Метаболизм пиридина Пиридин вреден, если при вдыхании, проглатывании или всасывании через кожу. Эффекты острой пиридиновой интоксикации включают головокружение, головную боль, нарушение координации, тошноту, слюноотделение и потерю аппетита. Они могут прогрессировать в боль в животе, застой в легких и потерю сознания. Один человек умер после случайного проглатывания полстакана пиридина. Самая низкая известная летальная доза (LD Lo) при приеме внутрь пиридина человеком составляет 500 мг · кг. В высоких дозах пиридин оказывает наркотическое действие, а его концентрации паров выше 3600 ppm представляют опасность для здоровья. Пероральный LD50 у крыс составляет 891 мг · кг. Пиридин легко воспламеняется.
Оценки возможного канцерогенного агента показали, что у людей нет достаточных доказательств канцерогенности пиридина, хотя есть ограниченные доказательства канцерогенного воздействия на животных. Имеющиеся данные показывают, что «воздействие пиридина в питьевой воде привело к снижению подвижности сперматозоидов при всех уровнях доз у мышей и увеличению продолжительности эстрального цикла при самом высоком уровне дозы у крыс».
Пиридин также может иметь незначительные нейротоксическое, генотоксическое и кластогенное эффекты. Воздействие пиридина обычно приводит к его вдыханию и всасыванию в легких и желудочно-кишечном тракте, где он либо остается неизменным, либо метаболизируется. Основными продуктами метаболизма пиридина являются N-метилпиридиниягидроксид, который образован N-метилтрансферазами (например, пиридин N-метилтрансфераза ), а также N-оксидом пиридина и 2-, 3- и 4-гидроксипиридин, которые образуются под действием монооксигеназы. У человека пиридин метаболизируется только в гидроксид N-метилпиридиния. Пиридин легко разлагается бактериями до аммиака и двуокиси углерода. Незамещенное пиридиновое кольцо разлагается быстрее, чем пиколин, лутидин, хлорпиридин или аминопиридины, и было показано, что ряд разлагателей пиридина для перепроизводства рибофлавина в присутствии пиридина. Ионизируемые N-гетероциклические соединения, в том числе пиридин, взаимодействуют с поверхностями окружающей среды (такими как почвы и отложения) посредством множества pH-зависимых механизмов, включая разделение на органическое вещество почвы, обмен катионов и поверхностное комплексообразование. Такая адсорбция на поверхности снижает биодоступность пиридинов для микробных деструкторов и других организмов, тем самым замедляя скорость разложения и снижая экотоксичность.
Незначительные количества пиридина выбрасываются в окружающую среду в результате некоторых промышленных процессов, таких как производство стали, переработка горючего сланца, газификация угля, коксование и мусоросжигательные заводы. Атмосфера заводов по переработке горючего сланца может содержать пиридин в концентрациях до 13 мкг · м, а уровни 53 мкг · м были измерены в подземных водах поблизости от завода по газификации угля. Согласно исследованию Национального института охраны труда США, около 43000 американцев работают в контакте с пиридином.
Систематическое название пиридина в пределах номенклатура Ганча – Видмана, рекомендованная IUPAC, представляет собой азинин. Однако систематические названия простых соединений используются очень редко; вместо этого, гетероциклическая номенклатура следует исторически сложившимся общепринятым названиям. ИЮПАК не рекомендует использовать азинин / азин в пользу пиридина. Нумерация кольцевых атомов в пиридине начинается с азота (см. Инфобокс). Иногда используются распределение позиций по буквам греческого алфавита (α-γ) и шаблон замещения номенклатура, общая для гомоароматических систем (орто, мета, пара). Здесь α (орто), β (мета) и γ (пара) относятся к позиции 2, 3 и 4 соответственно. Систематическое название производных пиридина - пиридинил, в котором положению замещенного атома предшествует число. Однако историческое название пиридил поощряется IUPAC и используется вместо систематического названия. катионное производное, образованное добавлением электрофила к атому азота, называется пиридин.
| На Викискладе есть средства массовой информации, связанные с Пиридином. |