| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 1 H- пиррол | |||
| Другие названия | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| Ссылка на Beilstein | 1159 | ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.387 | ||
| Номер ЕС | |||
| Ссылка на Гмелин | 1705 | ||
| PubChem CID | |||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 1992, 1993 | ||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | C 4 H 5 N | ||
| Молярная масса | 67,091 г моль -1 | ||
| Плотность | 0,967 г см −3 | ||
| Температура плавления | -23 ° С (-9 ° F, 250 К) | ||
| Точка кипения | От 129 до 131 ° C (от 264 до 268 ° F, от 402 до 404 K) | ||
| Давление газа | 7 мм рт. Ст. При 23 ° C | ||
| Кислотность (p K a) | 16,5 (для протона NH) | ||
| Основность (p K b) | 13,6 (pKa 0,4 для CA ) | ||
| Магнитная восприимчивость (χ) | -47,6 10 −6 см 3 / моль | ||
| Вязкость | 0,001225 Па с | ||
| Термохимия | |||
| Теплоемкость ( C) | 1.903 Дж К −1 моль −1 | ||
| Std энтальпия формации (Δ F H ⦵298) | 108,2 кДж моль -1 (газ) | ||
| Std энтальпии сгорания (Δ с Н ⦵298) | 2242 кДж моль -1 | ||
| Опасности | |||
| Паспорт безопасности | Данные о химической безопасности | ||
| NFPA 704 (огненный алмаз) |  2 2 0 2 2 0 | ||
| точка возгорания | 33,33 ° С (91,99 ° F, 306,48 К) | ||
| самовоспламенения температуру | 550 ° С (1022 ° F, 823 К) | ||
| Пределы взрываемости | 3,1–14,8% | ||
| Родственные соединения | |||
| Родственные соединения | Phosphole, arsole, bismole, stibole | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
Пиррол представляет собой гетероциклическое ароматическое органическое соединение, пятичленное кольцо с формулой C 4 H 4 N H. Это бесцветная летучая жидкость, которая легко темнеет на воздухе. Замещенные производные также называют пирролами, например N- метилпиррол, C 4 H 4 NCH 3. Порфобилиноген, тризамещенный пиррол, является биосинтетическим предшественником многих природных продуктов, таких как гем.
Пирролов являются компонентами более сложных макроциклов, в том числе porphyrinogens и продукты, полученные из них, в том числе порфиринов из гема, в хлоринов, бактериохлоринов, и хлорофиллов.
Пиррол представляет собой бесцветную летучую жидкость, которая легко темнеет на воздухе и обычно очищается дистилляцией непосредственно перед использованием. Пиррол имеет ореховый запах. Пиррол представляет собой 5-членный ароматический гетероцикл, подобный фурану и тиофену. В отличие от фуран и тиофен, он имеет диполь, в котором положительный конец лежит на стороне гетероатом, с дипольным моментом 1,58 D. В CDCl 3 он имеет химические сдвиги 6,68 (H2, H5) и 6,22 (H3, H4). Пиррол является слабоосновным, с сопряженной кислотой p K a -3,8. Самый термодинамически стабильный катион пирроля (C 4 H 6 N +) образуется в результате протонирования в положении 2. Замена пиррола на алкильные заместители дает более основную молекулу - например, тетраметилпиррол имеет сопряженную кислоту p K a +3,7. Пиррол также является слабокислым в положении N – H с ap K a, равным 16,5. Как кислота Льюиса, связывающая водород, она классифицируется как твердая кислота, и в модели ECW ее кислотные параметры указаны как E A = 1,38 и C A = 0,68.
Пиррол был впервые обнаружен Ф. Ф. Рунге в 1834 году в составе каменноугольной смолы. В 1857 г. он был выделен из костного пиролизата. Его название происходит от греческого Пирра ( πυρρός, «красноватого огненный»), от реакции, используемой для его обнаружений-красного цвета, что придает древесину при увлажнении с соляной кислотой.
 Heme b
Heme b Сам по себе пиррол не встречается в природе, но многие его производные содержатся в различных кофакторах и натуральных продуктах. Общие, естественно, полученные молекулы, содержащие пирролы, включают витамин B 12, желчные пигменты, такие как билирубин и биливердин, и порфирины из гема, хлорофилл, хлорины, бактериохлорин, и porphyrinogens. Другие вторичные метаболиты, содержащие пиррол, включают PQQ, макалувамин M, рианодин, резинилам, ламелларин, продигиозин, мирмикарин и скептрин. Синтез пирролсодержащего гемина, синтезированный Гансом Фишером, был отмечен Нобелевской премией.
Пиррол входит в состав табачного дыма и может способствовать его токсическому действию.
Пиррола получают промышленно обработкой фурана с аммиаком в присутствии кислотных твердых катализаторов, как SiO 2 и Al 2 O 3.

Пиррол также может быть образован каталитическим дегидрированием пирролидина.
Описано несколько синтезов пиррольного кольца.
Синтез пиррола по Ганче представляет собой реакцию β-кетоэфиров (1) с аммиаком (или первичными аминами) и α-галогенкетонами (2) с образованием замещенных пирролов (3).

Синтез пиррола Knorr включает реакцию α-аминокетона или α-амино-β-кетоэфира с активированным метиленовым соединением. Способ включает реакцию с amp; alpha ; амино - кетон (1) и соединением, содержащим метиленовую группу amp; alpha ; к (связанный с атомом углерода, к следующему) в карбонильную группу (2).

В синтезе пиррола Паала-Кнорра 1,4-дикарбонильное соединение реагирует с аммиаком или первичным амином с образованием замещенного пиррола.

Реакция Ван Лойзена может быть использована для образования пирролов путем реакции тозилметилизоцианида (TosMIC) с еноном в присутствии основания при присоединении Михаэля. Затем в результате 5- эндоциклизации образуется 5-членное кольцо, которое реагирует с удалением тозильной группы. Последний шаг - таутомеризация до пиррола.
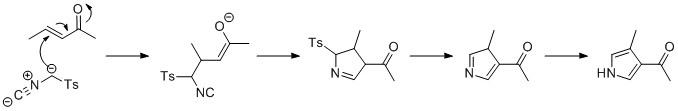
Синтез Бартона – Зарда протекает аналогично синтезу Ван Лойзена. An isocyanoacetate реагирует с nitroalkene в 1,4-присоединением, а затем 5 - эндо - Dig циклизации, устранение нитрогруппы, и таутомеризации.
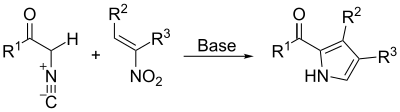
Исходные материалы в пиррола синтеза Robinson-Пилоты, названные по имени Гертруда и Роберт Робинсон и Oskar Пилоти, два эквивалентов альдегида и гидразина. Продукт представляет собой пиррол с заместителями в положениях 3 и 4. Альдегид реагирует с диамином с образованием промежуточного диимина (R – C = N – N = C – R). На втором этапе между ними происходит [3,3] -сигматропная перегруппировка. Добавление соляной кислоты приводит к замыканию цикла и потере аммиака с образованием пиррола. Механизм был разработан Robinsons.
В одной из модификаций пропиональдегид обрабатывают сначала гидразином, а затем бензоилхлоридом при высоких температурах и с помощью микроволнового излучения :
![Реакция Пилоти – Робинсона [22]](https://upload.wikimedia.org/wikipedia/commons/thumb/b/bd/Piloty-Robinson_reaction.png/400px-Piloty-Robinson_reaction.png)
Пирролы, содержащие несколько заместителей, получают в результате реакции мюнхнонов и алкинов. Механизм реакции включает 1,3-диполярное циклоприсоединение с последующей потерей углекислого газа в результате ретро - процесса Дильса-Альдера. Подобные реакции можно проводить с использованием азалактонов.

Пирролы могут быть получены катализируемой серебром циклизацией алкинов с изонитрилами, где R 2 представляет собой электроноакцепторную группу, а R 1 представляет собой алкан, арильную группу или сложный эфир. Также было замечено, что примеры дизамещенных алкинов образуют требуемый пиррол со значительным выходом. Предполагается, что реакция протекает через промежуточное соединение ацетилида серебра. Этот метод аналогичен азидно-алкиновой щелочной химии, используемой для образования азолов.
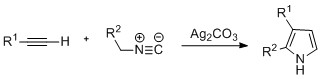
Один пути синтеза включает в пиррола с декарбоксилированием из муката аммония, солей аммония слизевой кислоты. Соль обычно нагревается в дистилляционной установке с глицерином в качестве растворителя.

Биосинтез пиррольных колец de novo начинается с аминолевулиновой кислоты (АЛК), которая синтезируется из глицина и сукцинил-КоА. АЛК-дегидратаза катализирует конденсацию двух молекул АЛК посредством кольцевого синтеза Кнорра с образованием порфобилиногена (PBG). Позднее он вступает в реакцию с образованием, например, макроциклов гема и хлорофилла.
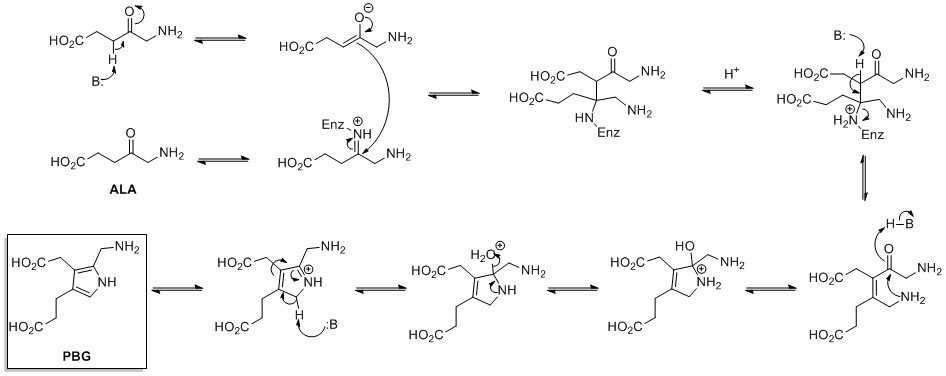
.
Пролин является биосинтетическим производным аминокислоты L - глутамата. Глутамат-5-полуальдегид сначала образуется глутамат-5-киназой (АТФ-зависимой) и глутамат-5-полуальдегиддегидрогеназой (которая требует НАДН или НАДФН). Затем он может либо спонтанно циклизоваться с образованием 1-пирролин-5-карбоновой кислоты, которая восстанавливается до пролина пирролин-5-карбоксилатредуктазой (с использованием NADH или NADPH), либо превращается в орнитин под действием орнитин аминотрансферазы с последующей циклизацией орнитинциклодезаминазой. с образованием пролина.
 Цвиттерионная структура обоих энантиомеров пролина: ( S) -пролин (слева) и ( R) -пролин
Цвиттерионная структура обоих энантиомеров пролина: ( S) -пролин (слева) и ( R) -пролин Пролин можно использовать в качестве предшественника ароматических пирролов во вторичных природных продуктах, например, в продигиозинах.
 Рисунок 1: Структура продигиозина 1 с выделением пиррольных колец A, B и C
Рисунок 1: Структура продигиозина 1 с выделением пиррольных колец A, B и C Биосинтез продигиозина включает конвергентное соединение трех колец пиррольного типа (обозначенных A, B и C на рисунке 1) из L-пролина, L-серина, L-метионина, пирувата и 2-октенала.
Кольцо A синтезируется из L-пролина через путь нерибосомальной пептид-синтазы (NRPS) (рисунок 2), где пирролидиновое кольцо пролина окисляется дважды через FAD + с образованием пиррольного кольца A.

Затем кольцо A расширяется по пути поликетидсинтазы, чтобы включить L-серин в кольцо B (рис. 3). Фрагмент кольца А переносится с пептидильного белка-носителя (PCP) на ацильный белок-носитель (ACP) посредством домена KS с последующим переносом на малонил-ACP посредством декарбоксилатной конденсации Клайзена. Затем этот фрагмент способен реагировать с замаскированным карбанионом, образованным в результате PLP-опосредованного декарбоксилирования L-серина, который циклизуется в реакции дегидратации с образованием второго пиррольного кольца. Затем это промежуточное соединение модифицируют метилированием (которое включает метильную группу из L-метионина на спирт в положении 6) и окислением первичного спирта до альдегида с образованием ядерных кольцевых структур AB.

Из-за своего ароматического характера пиррол трудно гидрогенизировать, с трудом реагирует как диен в реакциях Дильса-Альдера и не вступает в обычные реакции олефинов. Его реакционная способность аналогична реакционной способности бензола и анилина в том, что он легко алкилируется и ацилируется. В кислых условиях пирролы легко полимеризуются, и поэтому многие электрофильные реагенты, которые используются в химии бензола, неприменимы к пирролам. Напротив, замещенные пирролы (включая защищенные пирролы) использовались в широком диапазоне превращений.
Пирролы обычно реагируют с электрофилами в α-положении (C2 или C5) из-за наивысшей степени стабильности протонированного промежуточного соединения.

Пирролы легко реагируют с нитрующими (например, HNO 3 / Ac 2 O ), сульфирующими ( Py SO 3 ) и галогенирующими (например, NCS, NBS, Br 2, SO 2 Cl 2 и KI / H 2 O 2 ) агентами. Галогенирование обычно дает полигалогенированные пирролы, но можно проводить моногалогенирование. Как типично для электрофильных добавок к пирролам, галогенирование обычно происходит в положении 2, но также может происходить в положении 3 за счет силирования азота. Это полезный метод для дальнейшей функционализации, как правило, менее реактивного 3-положения.
Ацилирование обычно происходит во 2-м положении с помощью различных методов. Ацилирование ангидридами кислот и хлорангидридами может происходить без катализатора; альтернативно может использоваться кислота Льюиса. 2-Acylpyrroles также получены в результате реакции с нитрилами, с помощью реакции Губена-Hoesch. Пиррольные альдегиды могут быть образованы по реакции Вильсмайера – Хаака. N- Ацилирование простого пиррола не происходит.

Электрофильное алкилирование простого пиррола встречается редко. Было замечено алкилирование с образованием енонов по C2.
Протон NH в пирролах умеренно кислый с p K a 16,5. Пиррол можно депротонировать с помощью сильных оснований, таких как бутиллитий и гидрид натрия. Образующийся пирролид щелочного металла является нуклеофильным. Обработка этого конъюгированного основания электрофилом, таким как йодметан, дает N- метилпиррол. N- Металлический пиррол может реагировать с электрофилами в положениях N или C, в зависимости от координирующего металла. Больше ионных связей азот-металл (например, с Li, Na и K) и большее количество сольватирующих растворителей приводят к N- алкилированию. Нитрофильные металлы, такие как MgX, приводят к алкилированию по C (в основном C2) из-за более высокой степени координации с атомом азота. В случае N- замещенных пирролов металлирование атомов углерода происходит легче. Алкильные группы могут быть введены в виде электрофилов или путем реакций кросс-сочетания.
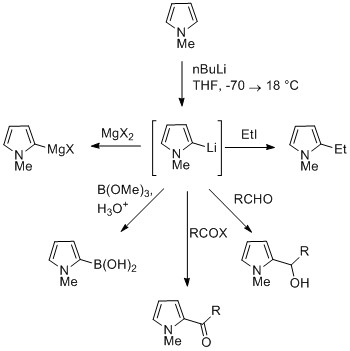
Замещение у C3 может быть достигнуто за счет использования N- замещенного 3-бромпиррола, который может быть синтезирован бромированием N- силилпиррола NBS.
Пирролы могут восстанавливаться до пирролидинов и пирролинов. Например, восстановление по Берчу сложных эфиров пиррола и амидов дает пирролины с региоселективностью, зависящей от положения электроноакцепторной группы.
Пирролы с N -замещением могут подвергаться реакциям циклоприсоединения, таким как [4 + 2] -, [2 + 2] - и [2 + 1] -циклизации. Циклизация Дильса-Альдера может происходить с пирролом, действующим как диен, особенно в присутствии электроноакцепторной группы на азоте. Винилпирролы также могут действовать как диены.
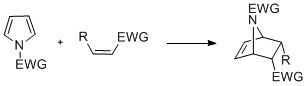
Пирролы могут реагировать с карбенами, такими как дихлоркарбен, в [2 + 1] -циклоприсоединении. С дихлоркарбеном образуется промежуточный дихлорциклопропан, который распадается с образованием 3-хлорпиридина (перегруппировка Чамикана-Денштедта).

Полипиррол имеет некоторую коммерческую ценность. N- Метилпиррол является предшественником N- метилпирролкарбоновой кислоты, строительного блока в фармацевтической химии. Пирролы также содержатся в нескольких лекарствах, включая аторвастатин, кеторолак и сунитиниб. Пирролы используются как светостойкие красные, алые и карминовые пигменты.
К структурным аналогам пиррола относятся:
Производные пиррола включают индол, производное с конденсированным бензольным кольцом.