| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Фуран | |||
| Систематическое название ИЮПАК 1,4-эпоксибута-1,3-диен 1-оксациклопента-2,4-диен | |||
| Другие имена Оксол Окса [5] аннулен 1,4- Эпокси -1,3-бутадиен 5-Оксациклопента-1,3-диен 5-Оксацикло-1,3-пентадиен Фурфуран Дивиниленоксид | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.390 | ||
| КЕГГ | |||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | С 4 Н 4 О | ||
| Молярная масса | 68,075 г моль -1 | ||
| Появление | Бесцветная летучая жидкость | ||
| Плотность | 0,936 г / мл | ||
| Температура плавления | -85,6 ° С (-122,1 ° F, 187,6 К) | ||
| Точка кипения | 31,3 ° С (88,3 ° F, 304,4 К) | ||
| Магнитная восприимчивость (χ) | -43,09 10 −6 см 3 / моль | ||
| Опасности | |||
| Паспорт безопасности | Pennakem | ||
| R-фразы (устаревшие) | R26 / 27/28, R45 | ||
| S-фразы (устаревшие) | S16, S37, S45, S28 | ||
| NFPA 704 (огненный алмаз) |  3 4 1 3 4 1 | ||
| точка возгорания | -36 ° С (-33 ° F, 237 К) | ||
| самовоспламенения температуру | 390 ° С (734 ° F, 663 К) | ||
| Пределы взрываемости | Нижняя: 2,3% Верхняя: 14,3% при 20 ° C | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LD 50 ( средняя доза ) | gt; 2 г / кг (крыса) | ||
| Родственные соединения | |||
| Родственные гетероциклы | Пиррол Тиофен | ||
| Родственные соединения | Тетрагидрофуран (THF) 2,5-Диметилфуран Бензофуран Дибензофуран | ||
| Состав | |||
| Группа точек | C 2v | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
Фуран - это гетероциклическое органическое соединение, состоящее из пятичленного ароматического кольца с четырьмя атомами углерода и одним атомом кислорода. Химические соединения, содержащие такие кольца, также называют фуранами.
Фуран - бесцветная, легковоспламеняющаяся, легколетучая жидкость с температурой кипения, близкой к комнатной. Он растворим в обычных органических растворителях, включая спирт, эфир и ацетон, и мало растворим в воде. Запах у него «сильный, эфирный, хлороформный ». Он токсичен и может быть канцерогенным для человека. Фуран используется в качестве отправной точки для других специальных химикатов.
Название «фуран» происходит от латинского furfur, что означает отруби. ( Фурфурол получают из отрубей.) Первым описанным производным фурана была 2-фурановая кислота, созданная Карлом Вильгельмом Шееле в 1780 году. Другое важное производное, фурфурол, было описано Иоганном Вольфгангом Доберейнером в 1831 году и охарактеризовано девятью годами позже Джоном Стенхаусом.. Сам фуран был впервые получен Генрихом Лимприхтом в 1870 году, хотя он назвал его «тетрафенол» (как если бы это был четырехуглеродный аналог фенола, C 6 H 6 O).
Промышленно фуран производится декарбонилированием фурфурола, катализируемым палладием, или окислением 1,3-бутадиена, катализируемым медью :

В лаборатории фуран можно получить из фурфурола окислением до 2-фурановой кислоты с последующим декарбоксилированием. Он также может быть получен непосредственно термическим разложением из пентозов отработанных материалов, а также целлюлозных твердых частицами, особенно сосновое дерево.
Синтез Собачонка-Бенари является классическим способом синтеза фуранов, хотя многие Синтезы были разработаны. Одним из простейших методов синтеза фуранов является реакция 1,4-дикетонов с пентоксидом фосфора (P 2 O 5) в синтезе Паала – Кнорра. Реакция образования тиофена 1,4-дикетонов с реактивом Лавессона также приводит к образованию фуранов в качестве побочных продуктов. Существует множество способов синтеза замещенных фуранов.
Фуран является ароматическим, потому что один из одиноких пар из электронов на атоме кислорода делокализован в кольцо, создавая 4 п +-ароматическую систему (см правила Хюккеля ), похожей на бензол. Из-за ароматичности молекула плоская и не имеет дискретных двойных связей. Другая неподеленная пара электронов атома кислорода проходит в плоскости плоской кольцевой системы. Зр 2 гибридизации, чтобы позволить одной из одиноких пар кислорода проживать в р орбитальных и, таким образом, чтобы позволить ему взаимодействовать в пределах системы П.
Из-за своей ароматичности поведение фурана совершенно не похоже на поведение более типичных гетероциклических эфиров, таких как тетрагидрофуран.

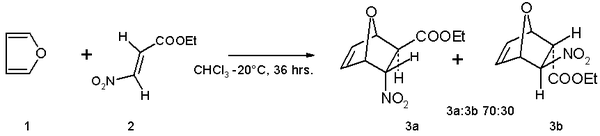
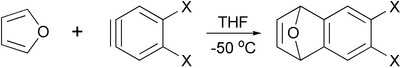
Фуран содержится в термически обработанных коммерческих пищевых продуктах и производится путем термического разложения натуральных компонентов пищи. Его можно найти в жареном кофе, растворимом кофе и обработанном детском питании. Исследования показали, что кофе, приготовленный в эспрессо мейкер и кофе из капсулы содержит больше фурана, чем из традиционных производителей капельного кофе, хотя они по- прежнему в безопасных пределах здоровья.
Воздействие фурана в дозах, примерно в 2000 раз превышающих прогнозируемый уровень воздействия на человека из пищевых продуктов, увеличивает риск гепатоцеллюлярных опухолей у крыс и мышей и опухолей желчных протоков у крыс. Поэтому фуран указан как возможный канцероген для человека.