В химии, орбитальная гибридизация (или гибридизация ) - это концепция смешивания атомных орбиталей в новые гибридные орбитали (с другими энергиями, формами и т.д., чем составляющие атомные орбитали), подходящие для спаривания электронов с образованием химических связей в теории валентных связей. Гибридные орбитали полезны для объяснения молекулярной геометрии и свойств атомных связей и симметрично расположены в пространстве.
Химик Линус Полинг впервые разработал теорию гибридизации в 1931 году, чтобы объяснить структуру простых молекул, таких как метан (CH 4) с использованием атомных орбиталей. Полинг указал, что атом углерода образует четыре связи, используя одну s и три p-орбитали, так что «можно было бы сделать вывод», что атом углерода образует три связи под прямым углом (используя p-орбитали) и четвертую более слабую связь, используя орбитали в произвольном направлении. В действительности, метан имеет четыре связи эквивалентной прочности, разделенных тетраэдрическим углом связи 109 ° 28 '(приблизительно 109,5 °). Полинг объяснил это предположением, что в присутствии четырех атомов водорода s- и p-орбитали образуют четыре эквивалентные комбинации или гибридные орбитали, каждая из которых обозначается sp, чтобы указать на ее состав, которые направлены вдоль четырех связей C-H. Эта концепция была разработана для таких простых химических систем, но позже этот подход был применен более широко, и сегодня он считается эффективной эвристикой для рационализации структур органических соединений. Это дает простую орбитальную картину, эквивалентную структурам Льюиса.
Теория гибридизации является неотъемлемой частью органической химии, одним из наиболее убедительных примеров является правила Болдуина. Для рисования механизмов реакции иногда требуется классическая связующая картина с двумя атомами, разделяющими два электрона. Теория гибридизации объясняет связывание алкенов и метана. Количество символов p или s, которое определяется в основном орбитальной гибридизацией, можно использовать для надежного прогнозирования молекулярных свойств, таких как кислотность или основность.
Орбитали являются модельным представлением поведение электронов внутри молекул. В случае простой гибридизации это приближение основано на атомных орбиталях, подобных тем, которые получены для атома водорода, единственного нейтрального атома, для которого уравнение Шредингера может быть решено точно. В более тяжелых атомах, таких как углерод, азот и кислород, в качестве атомных орбиталей используются 2s и 2p орбитали, аналогичные орбиталям в возбужденном состоянии для водорода.
Предполагается, что гибридные орбитали представляют собой смесь атомных орбиталей, наложенных друг на друга в различных пропорциях. Например, в метане гибридная орбиталь C, которая образует каждую связь углерод - водород, состоит из символа 25% s и символа 75% p и, таким образом, описывается как sp (читается как sp-three) гибридизированный. Квантовая механика описывает этот гибрид как sp волновую функцию формы N (s + √3pσ), где N - нормировочная константа (здесь 1/2) и pσ представляет собой апорбиталь, направленную вдоль оси CH с образованием сигма-связи . Отношение коэффициентов (обычно обозначаемое λ) в этом примере составляет √3. Поскольку электронная плотность, связанная с орбиталью, пропорциональна квадрату волновой функции, отношение p-символа к s-символу составляет λ = 3. Символ p или вес p-компонента равен Nλ = 3/4.
 Четыре sp-орбитали.
Четыре sp-орбитали. Гибридизация описывает связывание атомов с точки зрения атома. Для углерода с тетраэдрической координацией (например, метан CH4) углерод должен иметь 4 орбитали с правильной симметрией, чтобы связываться с 4 атомами водорода.
основное состояние углерода - конфигурация 1s 2s 2p или более легко читается:
| C | ↑ ↓ | ↑ ↓ | ↑ | ↑ | |
| 1s | 2s | 2p | 2p | 2p |
Атом углерода может использовать его две одиночно занятые орбитали p-типа с образованием двух ковалентных связей с двумя атомами водорода, с образованием синглетного метилена CH2, простейшего карбена. Атом углерода может также связываться с четырьмя атомами водорода посредством возбуждения (или продвижения) электрона с дважды занятой 2s-орбитали на пустую 2p-орбиталь, создавая четыре однократно занятые орбитали.
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1s | 2s | 2p | 2p | 2p |
Энергия, выделяемая при образовании двух дополнительных связей, больше, чем компенсирует требуемую энергию возбуждения, энергетически благоприятствуя образованию четырех связей C-H.
Квантово-механически, самая низкая энергия получается, если четыре связи эквивалентны, что требует, чтобы они образовывались из эквивалентных орбиталей на углероде. Можно получить набор из четырех эквивалентных орбиталей, которые являются линейными комбинациями волновых функций валентной оболочки (основные орбитали почти никогда не участвуют в связывании) s- и p-волновых функций, которые являются четырьмя sp-гибридами.
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1s | sp | sp | sp | sp |
В CH 4 четыре sp-гибридных орбитали перекрываются водородными 1s-орбиталями, что дает четыре σ ( сигма) связи (то есть четыре одинарные ковалентные связи) равной длины и прочности.
 переводится в
переводится в 
 Три sp-орбитали.
Три sp-орбитали.  Структура этена
Структура этена Другие соединения углерода и другие молекулы могут быть объяснены аналогичным образом. Например, этен (C2H4) имеет двойную связь между атомами углерода.
Для этой молекулы углерод sp гибридизуется, потому что для двойной связи между атомами углерода требуется одна π (pi) связь, и только три σ-связи образуются на атом углерода. При sp-гибридизации 2s-орбиталь смешивается только с двумя из трех доступных 2p-орбиталей, обычно обозначаемых 2p x и 2p y. Третья 2p-орбиталь (2p z) остается негибридизированной.
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1s | sp | sp | sp | 2p |
, образуя в общей сложности три sp-орбитали с одной оставшейся p-орбиталью. В этилене (этен ) два атома углерода образуют σ-связь, перекрывая одну sp-орбиталь от каждого атома углерода. Π-связь между атомами углерода, перпендикулярными плоскости молекулы, образована перекрытием 2p – 2p. Каждый атом углерода образует ковалентные связи C – H с двумя атомами водорода за счет s – sp перекрытия, все с валентными углами 120 °. Связи водород – углерод имеют одинаковую силу и длину, что согласуется с экспериментальными данными.
 Две sp-орбитали
Две sp-орбитали Химическая связь в соединениях, таких как алкины с тройными связями, объясняется sp-гибридизацией. В этой модели 2s-орбиталь смешана только с одной из трех p-орбиталей,
| C * | ↑ ↓ | ↑ | ↑ | ↑ | ↑ |
| 1s | sp | sp | 2p | 2p |
, что дает две sp-орбитали и две оставшиеся p-орбитали. Химическая связь в ацетилене (этине) (C 2H2) состоит из sp – sp перекрытия между двумя атомами углерода, образующими σ-связь, и двумя дополнительными π-связями, образованными p– р перекрытия. Каждый углерод также связывается с водородом в виде перекрытия σ s – sp под углом 180 °.
 Формы различных типов гибридных орбиталей
Формы различных типов гибридных орбиталей Гибридизация помогает объяснить форму молекулы, поскольку углы между связями примерно равны углам между гибридными орбитали. Это контрастирует с теорией отталкивания электронных пар валентных оболочек (VSEPR), которую можно использовать для предсказания геометрии молекул на основе эмпирических правил, а не на основе теорий валентных связей или орбиталей.
Поскольку валентные орбитали элементов основной группы - это одна s и три p-орбитали с соответствующим правилом октетов, sp-гибридизация используется для моделирования формы этих молекул.
| Координационное число | Форма | Гибридизация | Примеры |
|---|---|---|---|
| 2 | Линейная гибридизация | sp (180 °) | CO2 |
| 3 | Тригональная плоская гибридизация | sp (120 °) | BCl 3 |
| 4 | Тетраэдрическая | sp-гибридизация (109,5 °) | CCl 4 |
| Межглазничные углы |  | ||
Поскольку валентные орбитали переходных металлов - это пять d, один s и три p-орбитали с соответствующим правилом 18-электронов, spd-гибридизация используется для моделирования формы этих молекул. Эти молекулы имеют тенденцию иметь несколько форм, соответствующих одной и той же гибридизации из-за различных вовлеченных d-орбиталей. Квадратный плоский комплекс имеет одну незанятую p-орбиталь и, следовательно, имеет 16 валентных электронов.
| Координационное число | Форма | Гибридизация | Примеры |
|---|---|---|---|
| 4 | Квадратная планарная | spd гибридизация | PtCl 4 |
| 5 | Тригонально-бипирамидальная | spd-гибридизация | Fe (CO) 5 |
| Квадратная пирамидальная | MnCl 5 | ||
| 6 | Октаэдрическая | spd-гибридизация | Mo (CO) 6 |
| 7 | Пятиугольная бипирамидальная | spd-гибридизация | ZrF 7 |
| Закрытый восьмигранный | MoF 7 | ||
| Закрытый тригонально-призматический | TaF 7 | ||
| 8 | Квадратный антипризматический | spd гибридизация | ReF 8 |
| Додекаэдр | Mo (CN) 8 | ||
| Двуглавый тригонально-призматический | ZrF 8 | ||
| 9 | Трехшпиндельный тригонально-призматический | spd-гибридизация | ReH 9 |
| Квадратная антипризматическая |
В некоторых комплексах переходных металлов с низким числом d-электронов p-орбитали не заняты, и sd-гибридизация используется для смоделировать форму этих молекул.
| Координационное число | Форма | Гибридизация | Примеры |
|---|---|---|---|
| 3 | Тригонально-пирамидальная | sd-гибридизация (90 °) | CrO 3 |
| 4 | Тетраэдрическая | sd-гибридизация (70,5 °, 109,5 °) | TiCl 4 |
| 5 | Квадрат пирамидальная | sd-гибридизация (65.9 °, 114.1 °) | Ta (CH 3)5 |
| 6 | C3vТригонально-призматическая | sd-гибридизация (63.4 °, 116.6 °) | W (CH 3)6 |
| Межорбитальные углы |  | ||
В некоторых общих учебниках химии гибридизация представлена для основной группы с координационным числом 5 и выше с использованием схемы «расширенных октетов» с d-орбиталями, впервые предложенной Полингом. Однако в настоящее время такая схема считается некорректной в свете расчетов компьютерной химии.
| Координационное число | Форма | Гибридизация | Примеры |
|---|---|---|---|
| 5 | Тригонально-бипирамидальная | гибридизация spd | PF5 |
| 6 | Октаэдрическая | spd-гибридизация | SF6 |
| 7 | Пентагонально-бипирамидальная | spd-гибридизация | IF7 |
В 1990 году Эрик Альфред Магнуссон из Университета Нового Южного Уэльса опубликовал статью, окончательно исключающую роль d-орбитальной гибридизации в связывании в гипервалентных соединениях второго ряда (периода 3 ), положив конец спору и неразберихе. Отчасти путаница происходит из-за того, что d-функции важны в базисных наборах, используемых для описания этих соединений (или иначе возникают необоснованно высокие энергии и искаженная геометрия). Кроме того, вклад d-функции в волновую функцию молекулы велик. Эти факты были неправильно истолкованы как означающие, что d-орбитали должны участвовать в связывании.
В свете вычислительной химии, лучше было бы использовать сигма-связь резонанс в дополнение к гибридизации, что означает, что каждая резонансная структура имеет свою собственную схему гибридизации. Все резонансные структуры должны подчиняться правилу октетов.
| Координационное число | Резонансные структуры |
|---|---|
| 5 | Тригональные бипирамидальные |
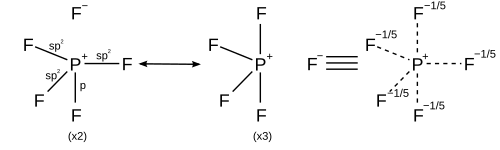 | |
| 6 | Октаэдрические |
 | |
| 7 | Пентагональные бипирамидальные |
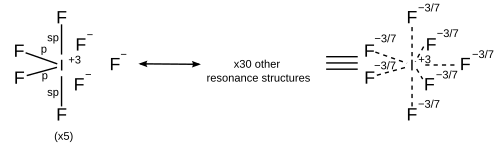 |
Хотя идеальные гибридные орбитали может быть полезным, в действительности для большинства облигаций требуются орбитали промежуточного характера. Это требует расширения для включения гибких весов атомных орбиталей каждого типа (s, p, d) и позволяет количественно описать образование связи, когда молекулярная геометрия отклоняется от идеальных валентных углов. Количество p-символа не ограничивается целыми значениями; то есть гибридизации, подобные sp, также легко описываются.
Гибридизация связанных орбиталей определяется правилом Бента : «Характер атома концентрируется на орбиталях, направленных к электроположительным заместителям».
Для молекул с неподеленными парами связывающие орбитали представляют собой изовалентные sp-гибриды. Например, две образующие связь гибридные орбитали кислорода в воде можно описать как sp, чтобы получить межглазничный угол 104,5 °. Это означает, что они имеют характер 20% s и характер 80% p и не подразумевают, что гибридная орбиталь образована из одной s и четырех p-орбиталей на кислороде, поскольку подоболочка 2p кислорода содержит только три p-орбитали. Формы молекул с неподеленными парами следующие:
В таких случаях есть два математически эквивалентных способа представления одиночных пар. Они могут быть представлены орбиталями сигма- и пи-симметрии, подобными теории молекулярных орбиталей, или эквивалентными орбиталями, подобными теории VSEPR.
Для гипервалентных молекул с неподеленными парами схема связывания может быть разделена на гипервалентный компонент и компонент, состоящий из гибридов изовалентных sp-связей. Гипервалентный компонент состоит из резонансных связей с использованием p-орбиталей. В таблице ниже показано, как каждая форма связана с двумя компонентами и их соответствующими описаниями.
| Количество гибридов с изовалентной связью (отмечено красным) | ||||
|---|---|---|---|---|
| Два | Один | – | ||
| Гипервалентный компонент | Линейная ось. (одна р-орбиталь) | Качели | Т-образный | Линейный |
 |  |  | ||
| Квадратный плоский экватор. (две p-орбитали) | Квадратный пирамидальный | Квадратный плоский | ||
 | 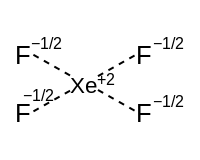 | |||
| Пятиугольный плоский экватор. (две p-орбитали) | Пятиугольная пирамидальная | Пятиугольная планарная | ||
 |  | |||
Для гибридизации s- и p-орбиталей с образованием эффективных sp-гибридов необходимо, чтобы они имели сопоставимую радиальную протяженность. В то время как 2p-орбитали в среднем менее чем на 10% больше, чем 2s, отчасти из-за отсутствия радиального узла на 2p-орбиталях, 3p-орбитали, которые имеют один радиальный узел, превышают 3s-орбитали на 20–33%. Разница в протяженности s- и p-орбиталей увеличивается вниз по группе. Гибридизацию атомов в химических связях можно проанализировать, рассматривая локализованные молекулярные орбитали, например, используя естественные локализованные молекулярные орбитали в схеме орбитали с естественными связями (NBO). В метане, CH 4 расчетное отношение p / s приблизительно равно 3, что соответствует "идеальной" sp-гибридизации, тогда как для силана SiH 4, отношение p / s ближе к 2. Аналогичная тенденция наблюдается для других элементов 2p. Замена водорода на фтор еще больше снижает отношение p / s. Элементы 2p демонстрируют почти идеальную гибридизацию с ортогональными гибридными орбиталями. Для более тяжелых блочных элементов p это предположение об ортогональности не может быть оправдано. Эти отклонения от идеальной гибридизации были названы дефектами гибридизации из-за Кутцельнигга.
Одно из заблуждений относительно орбитальной гибридизации состоит в том, что она неверно предсказывает ультрафиолетовые фотоэлектронные спектры многих молекул. Хотя это верно, если теорема Купманса применяется к локализованным гибридам, квантовая механика требует, чтобы (в данном случае ионизированная) волновая функция подчинялась симметрии молекулы, что подразумевает резонанс в валентной связи теория. Например, в метане ионизированные состояния (CH 4) могут быть построены из четырех резонансных структур, приписывающих выброшенный электрон каждой из четырех sp-орбиталей. Линейная комбинация этих четырех структур с сохранением количества структур приводит к трехкратно вырожденному состоянию T 2 и состоянию A 1. Разница в энергии между каждым ионизированным состоянием и основным состоянием будет энергией ионизации, которая дает два значения в соответствии с экспериментом.
Связующие орбитали, образованные из гибридных атомных орбиталей, можно рассматривать как локализованные молекулярные орбитали, которые могут быть сформированы из делокализованных орбиталей теории молекулярных орбиталей путем соответствующего математического преобразования. Для молекул в основном состоянии это преобразование орбиталей оставляет неизменной полную многоэлектронную волновую функцию. Гибридное орбитальное описание основного состояния, таким образом, эквивалентно делокализованному орбитальному описанию для полной энергии основного состояния и плотности электронов, а также геометрии молекулы, которая соответствует минимальному значению полной энергии.
Молекулы с множественными связями или множественными неподеленными парами могут иметь орбитали, представленные в терминах сигма- и пи-симметрии или эквивалентных орбиталей. Различные методы валентной связи используют одно из двух представлений, которые имеют математически эквивалентные полные многоэлектронные волновые функции и связаны посредством унитарного преобразования набора занятых молекулярных орбиталей.
Для множественных связей представление сигма-пи является преобладающим по сравнению с эквивалентным орбитальным (изогнутым соединением ) представлением. Напротив, для нескольких одиночных пар в большинстве учебников используется эквивалентное орбитальное представление. Однако представление сигма-пи также используется, например, Вайнхольдом и Ландисом в контексте орбиталей естественных связей, теории локализованных орбиталей, содержащей модернизированные аналоги классических (валентная связь / структура Льюиса) пар связей и одинокие пары. Для молекулы фтороводорода, например, две неподеленные пары F представляют собой по существу негибридизованные p-орбитали, а другая - sp-гидридную орбиталь. Аналогичное соображение применимо к воде (одна неподеленная пара О находится на чистой p-орбитали, другая - на гибридной sp-орбитали).