 . Сухой активированный никель Ренея . Сухой активированный никель Ренея | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| UNII | |
| Свойства | |
| Внешний вид | Светло-серый порошок |
| Опасности | |
| Пиктограммы GHS |    |
| Предупреждения об опасности GHS | H250, H317, H351, H372, H412 |
| Меры предосторожности GHS | P210, P273, P280, P302 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Никель Ренея, также называемый губчатым никелем, представляет собой мелкозернистое твердое вещество, состоящее в основном из никеля, производного из сплава никель - алюминий. Известно несколько сортов, большинство из которых являются серыми твердыми веществами. Некоторые из них пирофорны, большинство из них используется в виде устойчивых на воздухе суспензий. Никель Ренея используется в качестве реагента и катализатора в органической химии. Он был разработан в 1926 году американским инженером Мюрреем Рэни для гидрогенизации растительных масел.
Поскольку Raney является зарегистрированным товарным знаком W. R. Grace and Company, только продукты, произведенные ее подразделением Grace, правильно называются "никелем Ренея". Более общие термины «скелетный катализатор» или «катализатор из губчатого металла» могут относиться к катализаторам с физическими и химическими свойствами, аналогичными свойствам никеля Ренея. Однако, поскольку сама компания Grace не использует общих названий для поставляемых катализаторов, "Raney" может стать универсальным в соответствии с законом о товарных знаках США.
 Никель Ренея является пирофорный и требует осторожного обращения. Этот транспортный контейнер заполнен вермикулитом для защиты запечатанной бутылки внутри.
Никель Ренея является пирофорный и требует осторожного обращения. Этот транспортный контейнер заполнен вермикулитом для защиты запечатанной бутылки внутри. Сплав Ni – Al получают растворением никеля в расплавленном алюминии с последующим охлаждением («закалкой»). В зависимости от соотношения Ni: Al при закалке образуется ряд различных фаз. Во время процедуры гашения добавляются небольшие количества третьего металла, такого как цинк или хром, для повышения активности полученного катализатора. Этот третий металл называется «промотор ». Промотор превращает смесь из бинарного сплава в тройной, что может привести к различным свойствам закалки и выщелачивания во время активации.
В процессе активации сплав, обычно в виде мелкого порошка, обрабатывают концентрированным раствором гидроксида натрия. Упрощенная реакция выщелачивания дается следующим химическим уравнением :
Для образования алюмината натрия (Na [Al (OH) 4 ]) необходимо использовать растворы гидроксида натрия с высокой концентрацией, чтобы избежать образования гидроксид алюминия, который в противном случае выпал бы в осадок в виде байерита. Следовательно, используются растворы гидроксида натрия с концентрацией до 5 M.
Температура, используемая для выщелачивания сплава, оказывает заметное влияние на свойства катализатора. Обычно выщелачивание проводят при температуре от 70 до 100 ° C. Площадь поверхности никеля Ренея (и родственных катализаторов в целом) имеет тенденцию к уменьшению с увеличением температуры выщелачивания. Это происходит из-за структурных перестроек в сплаве, которые можно рассматривать как аналог спекания, когда связки сплава начинают слипаться друг с другом при более высоких температурах, что приводит к потере пористой структуры.
Во время процесса активации Al выщелачивается из фаз NiAl 3 и Ni 2Al3, которые присутствуют в сплаве, в то время как большая часть Ni остается в форме NiAl. Удаление Al из одних фаз, но не из других, известно как «селективное выщелачивание ». Было показано, что фаза NiAl обеспечивает структурную и термическую стабильность катализатора. В результате катализатор довольно устойчив к разложению («разрушению», обычно известному как «старение»). Это сопротивление позволяет хранить и повторно использовать никель Ренея в течение длительного периода; однако для лабораторного использования обычно предпочтительны свежие препараты. По этой причине коммерческий никель Ренея доступен как в «активной», так и в «неактивной» формах.
Перед хранением катализатор можно промыть дистиллированной водой при температуре окружающей среды для удаления оставшегося алюмината натрия. Бескислородная (дегазированная ) вода предпочтительна для хранения, чтобы предотвратить окисление катализатора, которое ускорит процесс его старения и приведет к снижению каталитической активности.
 Фазовая диаграмма системы Ni – Al, показывающая соответствующие фазы.
Фазовая диаграмма системы Ni – Al, показывающая соответствующие фазы.  СЭМ никелевого катализатора Ренея, на котором видны кристаллы размером 1-50 мкм.
СЭМ никелевого катализатора Ренея, на котором видны кристаллы размером 1-50 мкм.  Крупный план никеля Ренея. Внутри кристаллов видны небольшие трещины шириной приблизительно 1-100 нм, что приводит к увеличению площади поверхности.
Крупный план никеля Ренея. Внутри кристаллов видны небольшие трещины шириной приблизительно 1-100 нм, что приводит к увеличению площади поверхности. Макроскопически никель Ренея представляет собой мелкодисперсный серый порошок. Микроскопически каждая частица этого порошка представляет собой трехмерную меш с порами неправильного размера и формы, большая часть которых создается в процессе выщелачивания. Никель Ренея отличается термической и структурной стабильностью, а также большой поверхностью Брунауэра - Эмметта - Теллера (BET ). площадь. Эти свойства являются прямым результатом процесса активации и способствуют относительно высокой каталитической активности.
Площадь поверхности обычно определяется путем измерения БЭТ с использованием газа, который предпочтительно адсорбируется на металлических поверхностях, например водород. Используя этот тип измерения, было показано, что почти вся открытая площадь частицы катализатора содержит Ni на своей поверхности. Поскольку Ni является активным металлом катализатора, большая площадь поверхности Ni означает, что большая поверхность доступна для одновременного протекания реакций, что отражается в повышенной активности катализатора. Коммерчески доступный никель Ренея имеет среднюю площадь поверхности Ni 100 м на грамм катализатора.
Высокая каталитическая активность в сочетании с тем фактом, что водород абсорбируется в порах катализатора во время активации, делает никель Ренея полезным катализатором для многих реакций гидрирования. Его структурная и термическая стабильность (т.е.не разлагается при высоких температурах) позволяет использовать его в широком диапазоне условий реакции. Кроме того, растворимость никеля Ренея пренебрежимо мала в большинстве обычных лабораторных растворителей, за исключением минеральных кислот, таких как соляная кислота, а также его относительно высокая плотность (около 6,5 г / см3). облегчает его отделение от жидкой фазы после завершения реакции.
Никель Ренея используется в большом количестве промышленных процессов и в органическом синтезе из-за его стабильности и высокой каталитической активности при комнатной температуре.
Практический пример использования никеля Ренея в промышленности показан в следующей реакции, где бензол восстанавливается до циклогексана. Восстановление бензольного кольца очень трудно достичь другими химическими средствами, но его можно осуществить с помощью никеля Ренея. Вместо этого с аналогичным эффектом можно использовать другие гетерогенные катализаторы, например, использующие элементы платиновой группы , но они, как правило, более дороги в производстве, чем никель Ренея. Полученный таким образом циклогексан можно использовать в синтезе адипиновой кислоты, сырья, используемого в промышленном производстве полиамидов, таких как нейлон.
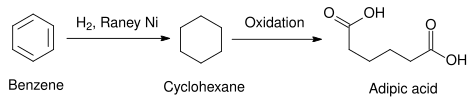 Бензол обычно восстанавливают до циклогексана с использованием Никель Ренея для производства нейлона.
Бензол обычно восстанавливают до циклогексана с использованием Никель Ренея для производства нейлона. Другие промышленные применения никеля Ренея включают преобразование:
Никель Ренея используется в органическом синтезе для десульфуризации. Например, тиоацетали будут восстановлены до углеводородов на последней стадии восстановления по Мозинго :
 Пример десульфурации тиоацеталей с использованием никеля Ренея
Пример десульфурации тиоацеталей с использованием никеля Ренея тиолов и сульфидов. может быть удален из алифатических, ароматических или гетероароматических соединений. Точно так же никель Ренея удаляет серу тиофена с получением насыщенного алкана.
 Восстановление тиофена никелем Ренея
Восстановление тиофена никелем Ренея Обычно используется при восстановлении соединений с кратными связями, таких как алкины, алкены, нитрилы, диены, ароматические углеводороды и карбонил -содержащие соединения. Кроме того, никель Ренея восстанавливает связи гетероатом-гетероатом, такие как гидразины, нитро группы и нитрозамины. Он также нашел применение в восстановительном алкилировании аминов и аминировании спиртов.
При восстановлении двойной связи углерод-углерод никель Ренея будет добавлять водород в соответствии с син модой.
 Никель Ренея легко воспламеняется.
Никель Ренея легко воспламеняется.  Никель металл классифицируется как «вредный».
Никель металл классифицируется как «вредный». Из-за большой площади поверхности и большого объема содержащегося в нем газообразного водорода сухой активированный никель Ренея является пирофорным материалом, с которым требуется обращаться в инертной атмосфере. Никель Ренея обычно поставляется в виде 50% суспензии в воде. Даже после реакции остаточный никель Ренея содержит значительное количество газообразного водорода и может самопроизвольно воспламениться при контакте с воздухом.
Кроме того, острое воздействие никеля Ренея может вызвать раздражение дыхательных путей и носовых полостей и вызвать фиброз легких при вдыхании. Проглатывание может вызвать судороги и кишечные расстройства. Он также может вызвать раздражение глаз и кожи. Хроническое воздействие может привести к пневмониту и другим признакам сенсибилизации к никелю, таким как кожная сыпь («никелевый зуд»).
| NFPA 704. огненный алмаз | |
|---|---|
 3 1 1 3 1 1 |
Никель также классифицируется как возможный человеческий канцероген IARC (Группа 2B, категория ЕС 3 ) и тератоген, в то время как вдыхание мелких частиц оксида алюминия связано с болезнью Шейвера.
Мюррей Рэйни, получив диплом инженера-механика в Университете Кентукки в 1909. В 1915 году он присоединился к Lookout Oil and Refining Company в Теннесси и отвечал за установку электролитических ячеек для производства водорода, который использовался в гидрогенизации растительного происхождения. масла. В то время в промышленности использовался никелевый катализатор, приготовленный из оксида никеля (II). Полагая, что могут быть произведены лучшие катализаторы, примерно в 1921 году он начал проводить независимые исследования, все еще работая в Lookout Oil. В 1924 году был получен сплав Ni / Si с соотношением 1: 1, который после обработки гидроксидом натрия оказался в пять раз более активным, чем лучший катализатор, используемый при гидрировании хлопкового масла. Патент на это открытие был выдан в декабре 1925 года.
Впоследствии Рэйни произвел сплав никель / алюминий 1: 1 по методике, аналогичной той, что использовалась для никель-кремниевого катализатора. Он обнаружил, что полученный катализатор был еще более активным, и подал заявку на патент в 1926 году. Сейчас это обычный состав сплава для современных никелевых катализаторов Ренея. Другие распространенные составы сплавов включают 21:29 Ni / Al и 3: 7 Ni / Al. И активность, и протоколы приготовления для этих катализаторов различаются.
После разработки никеля Ренея были рассмотрены другие системы сплавов с алюминием, из которых наиболее заметными являются медь, рутений и <277.>кобальт. Дальнейшие исследования показали, что добавление небольшого количества третьего металла к бинарному сплаву будет способствовать активности катализатора. Некоторыми широко используемыми промоторами являются цинк, молибден и хром. Альтернативный способ получения энантиоселективного никеля Ренея был разработан путем поверхностной адсорбции винной кислоты.