 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Амид натрия, азанид натрия | |
| Другие имена Содамид | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.064 |
| Номер ЕС |
|
| PubChem CID | |
| UNII | |
| Номер ООН | 1390 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | NaNH 2 |
| Молярная масса | 39,01 г моль |
| Внешний вид | Бесцветные кристаллы |
| Запах | аммиакоподобный |
| Плотность | 1,39 г см |
| Точка плавления | 210 ° C (410 ° F; 483 K) |
| Точка кипения | 400 ° C (752 ° F; 673 K) |
| Растворимость в воде | реагирует |
| Растворимость | 0,004 г / 100 мл (жидкий аммиак), реагирует в этаноле |
| Кислотность (pK a) | 38 (сопряженная кислота ) |
| Структура | |
| Кристаллическая структура | орторомбическая |
| Термохимия | |
| Теплоемкость (C) | 66,15 Дж / моль K |
| Станд. Молярный. энтропия (S 298) | 76,9 Дж / моль K |
| Стандартная энтальпия образования. (ΔfH298) | -118,8 кДж / моль |
| Свободная энергия Гиббса (ΔfG˚) | -59 кДж / моль |
| Опасности | |
| NFPA 704 (огненный алмаз) |  2 3 3 2 3 3 |
| Температура вспышки | 4,44 ° C (39,99 ° F; 277,59 K) |
| Самовоспламенение. температура | 450 ° C (842 ° F; 723 K) |
| Родственные соединения | |
| Другие анионы | бис (триметилсилил) амид натрия |
| Другие катионы | Амид лития. Амид калия |
| Родственные соединения | Аммиак |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Амид натрия, обычно называемый содамидом (систематическое название азанид натрия ), представляет собой неорганическое соединение с формулой NaNH 2. Это соль , состоящая из катиона натрия и аниона азанида. Это твердое вещество, опасно реактивное по отношению к воде, имеет белый цвет, но коммерческие образцы обычно имеют серый цвет из-за присутствия небольших количеств металлического железа в процессе производства. Такие примеси обычно не влияют на пригодность реагента . NaNH 2 проводит электричество в конденсированном состоянии, при этом его проводимость аналогична проводимости NaOH в аналогичном состоянии. NaNH 2 широко используется в качестве сильного основания в органическом синтезе.
Амид натрия может быть получают реакцией натрия с газообразным аммиаком, но обычно его получают реакцией в жидком аммиаке с использованием нитрата железа (III) в качестве катализатор. Реакция протекает быстрее всего при температуре кипения аммиака c. -33 ° С. электрид, [Na (NH 3)6] e, образуется как промежуточное соединение реакции.
NaNH 2 представляет собой солеподобный материал и, как таковой, кристаллизуется в виде бесконечного полимера. Геометрия натрия тетраэдрическая. В аммиаке NaNH 2 образует проводящие растворы, соответствующие присутствию ионов Na (NH 3)6и NH 2.
Амид натрия в основном используется в качестве сильного основание в органической химии, часто в жидком растворе аммиака. Это реагент выбора для сушки аммиака (жидкого или газообразного). Одним из основных преимуществ использования амида натрия является то, что он в основном функционирует как нуклеофил. При промышленном производстве индиго амид натрия является компонентом высокоосновной смеси, которая вызывает циклизацию N-фенилглицина. В результате реакции образуется аммиак, который обычно рециркулируют.
 Синтез Пфлегером красителя индиго.
Синтез Пфлегером красителя индиго..
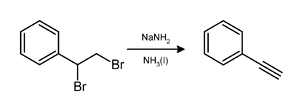
Sodi Амид um вызывает потерю двух эквивалентов бромистого водорода из вицинального дибромалкана с образованием тройной связи углерод-углерод, как при получении фенилацетилен. Обычно два эквивалента амида натрия дают желаемый алкин. Для получения концевых алкинов необходимы три эквивалента, поскольку концевой СН образовавшегося алкина протонирует эквивалентное количество основания.
Хлороводород и этанол также могут быть удалены таким образом, как при получении 1-этокси-1-бутина.
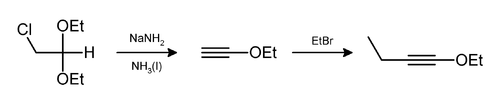
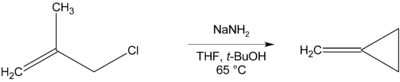
Где есть не является удаляемым β-водородом, могут образовываться циклические соединения, как при получении метиленциклопропана ниже.
Циклопропены, азиридины и циклобутаны может быть сформирован аналогичным образом.
Углеродные кислоты, которые могут быть депротонированы амидом натрия в жидком аммиаке, включают концевые алкины, метил кетоны, циклогексанон, фенилуксусная кислота и ее производные и дифенилметан. Ацетилацетон теряет два протона с образованием дианиона. Амид натрия также будет депротонировать индол и пиперидин.
. Однако он плохо растворим в других растворителях, кроме аммиака. Его использование было заменено соответствующими реагентами гидридом натрия, бис (триметилсилил) амидом натрия (NaHMDS) и диизопропиламидом лития (LDA).
Амид натрия бурно реагирует с вода с образованием аммиака и гидроксида натрия и будет гореть на воздухе с образованием оксидов натрия и диоксида азота.
В присутствии ограниченного количества воздуха и влаги, например, в плохо закрытом контейнере, могут образовываться взрывоопасные смеси пероксидов. Это сопровождается пожелтением или потемнением твердого вещества. Таким образом, амид натрия следует хранить в плотно закрытом контейнере в атмосфере инертного газа. Образцы амида натрия желтого или коричневого цвета представляют опасность взрыва.