A нитрил - любое органическое соединение, который имеет - C ≡N функциональную группу. Приставка циано - в промышленной литературе используется взаимозаменяемо с термином нитрил. Нитрилы обнаружены во многих полезных соединениях, включая метилцианоакрилат, используемый в суперклее, и нитрильный каучук, нитрилсодержащий полимер используются в безлатексных лабораторных и медицинских перчатках. Нитриловый каучук также широко используется в качестве автомобильных и других уплотнений, поскольку он устойчив к топливам и маслам. Органические соединения, содержащие несколько нитрильных групп, известны как цианоуглероды.
Неорганические соединения, содержащие группу -C≡N, называются не нитрилами, а цианидами. Хотя и нитрилы, и цианиды могут быть производными цианидных солей, большинство нитрилов не так токсичны.
Геометрия N − C − C линейна в нитрилах, что отражает sp-гибридизацию трехсвязанного углерода. Расстояние C-N короткое и составляет 1,16 Å, что соответствует тройной связи. Нитрилы полярны, на что указывают высокие дипольные моменты. Как жидкости, они имеют высокие относительные диэлектрические проницаемости, часто в пределах 30-х годов.
Первое соединение ряда гомологов нитрилов, нитрил муравьиной кислоты, цианистый водород было впервые синтезировано С. В. Шееле в 1782 г. В 1811 г. Дж. Л. Гей-Люссак смог приготовить очень токсичную и летучую чистую кислоту. Примерно в 1832 году бензонитрил, нитрил бензойной кислоты, был получен Фридрихом Велером и Юстусом фон Либихом, но из-за минимального выхода при синтезе не были определены ни физические, ни химические свойства, ни структура. В 1834 г. Теофил-Жюль Пелуз синтезировал пропионитрил, предположив, что это простой эфир пропионового спирта и синильной кислоты. Синтез бензонитрила Германом Фелингом в 1844 году путем нагревания бензоата аммония был первым методом, позволившим получить достаточно вещества для химических исследований. Фелинг определил структуру, сравнивая свои результаты с уже известным синтезом цианистого водорода путем нагревания формиата аммония . Он придумал название «нитрил» для вновь обнаруженного вещества, которое стало названием этой группы соединений.
В промышленности основными методами производства нитрилов являются аммоксидирование и гидроцианирование. Оба пути являются зелеными в том смысле, что они не генерируют стехиометрические количества солей.
В аммоксидировании, углеводород частично окисляется в присутствии аммиака. Это преобразование широко практикуется для акрилонитрила :
При производстве акрилонитрила побочным продуктом является ацетонитрил. В промышленном масштабе несколько производных бензонитрила, фталонитрила, а также изобутиронитрила получают аммоксидированием. Процесс катализируется оксидами металлов и предполагается, что он протекает через имин.
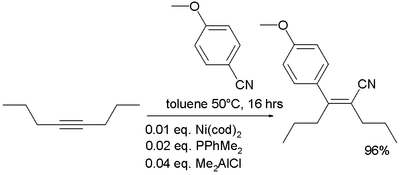
Гидроцианирование - это промышленный метод получения нитрилов из цианистого водорода и алкенов. Для процесса требуются гомогенные катализаторы. Примером гидроцианирования является получение адипонитрила, предшественника нейлона-6,6 из 1,3-бутадиена :
Две реакции метатезиса солей популярны для реакций лабораторного масштаба. В Кольбе синтез нитрила, алкилгалогениды подвергаются нуклеофильному алифатическому замещению щелочными металлами цианидами. Арилнитрилы получают в синтезе Розенмунда-фон Брауна.
 Синтез ароматических нитрилов через силилированные циангидрины
Синтез ароматических нитрилов через силилированные циангидрины циангидрины представляют собой особый класс нитрилов. Классически они образуются в результате присоединения цианидов щелочных металлов к альдегидам в реакции циангидрина.. Из-за полярности органического карбонила эта реакция не требует катализатора, в отличие от гидроцианирования алкенов. O-силилциангидрины образуются путем добавления триметилсилилцианида в Наличие катализатора (силилцианирование). Цианогидрины также получают реакциями трансциангидрина, начиная, например, с ацетонциангидрином в качестве источника HCN.
Нитрилы могут быть получены с помощью дегидратация первичных амидов. В присутствии и DBU, бензамид превращается в бензонитрил : другие реагенты, которые обычно используются для этой цели, включают P 4O10и SOCl 2.
При родственной дегидратации вторичные амиды дают нитрилы путем разложения амида фон Брауна. В этом случае разрывается одна связь C-N. Дегидратация альдоксимов (RCH = NOH) также дает нитрилы. Типичными реагентами для этого превращения являются триэтиламин / диоксид серы, цеолиты или сульфурилхлорид. Использование этого подхода заключается в синтезе в одной емкости нитрилов из альдегида с гидроксиламином в присутствии сульфата натрия.

Ароматические нитрилы часто получают в лаборатории из анилина с помощью соединений диазония. Это реакция Сандмейера. Для нее требуются цианиды переходных металлов.
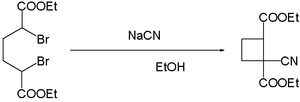
Нитрильные группы в органических соединениях могут претерпевать различные реакции в зависимости от реагентов или условий. Нитрильная группа может быть гидролизована, восстановлена или выброшена из молекулы в виде цианид-иона.
гидролиз нитрилов RCN проходит в отдельные стадии при кислотной или основной обработке с получением сначала карбоксамидов RC (= O) NH 2, а затем карбоновые кислоты RCOOH. Гидролиз нитрилов до карбоновых кислот эффективен. Для кислоты или основания сбалансированные уравнения имеют следующий вид:
Обратите внимание, что, строго говоря, эти реакции опосредуются (в отличие от катализируемых) кислотой или основанием, поскольку один эквивалент кислоты или основания расходуется с образованием аммониевой или карбоксилатной соли соответственно.
Кинетические исследования показывают, что константа скорости второго порядка для катализируемого гидроксид-ионами гидролиза ацетонитрила в ацетамид составляет 1,6 × 10 Мс, что меньше, чем гидролиз амида до карбоксилата (7,4 × 10 М с). Таким образом, основной путь гидролиза даст карбоксилат (или амид, загрязненный карбоксилатом). С другой стороны, реакции, катализируемые кислотой, требуют тщательного контроля температуры и соотношения реагентов, чтобы избежать образования полимеров, чему способствует экзотермический характер гидролиза. Классическая процедура превращения нитрила в соответствующий первичный амид требует добавления нитрила к холодной концентрированной серной кислоте. Дальнейшему превращению в карбоновую кислоту препятствуют низкая температура и низкая концентрация воды.
Два семейства ферментов катализируют гидролиз нитрилов. Нитрилазы гидролизуют нитрилы до карбоновых кислот:
Нитрилгидратазы являются металлоферменты, гидролизующие нитрилы до амидов.
Эти ферменты коммерчески используются для получения акриламида.
Нитрилы подвержены гидрированию на различных металлических катализаторах. В результате реакции может быть получен первичный амин (RCH 2NH2) или третичный амин ((RCH 2)3N), в зависимости от условий. При обычных органических восстановлениях нитрил восстанавливают обработкой литийалюмогидрид до амина. Восстановление до имина с последующим гидролизом до альдегида происходит в синтезе альдегида Стивена, в котором используется хлорид олова в кислоте.
Алкилнитрилы достаточно кислые, чтобы образовывать нитрильные анионы, которые алкилируют широкий спектр электрофилов. Ключом к исключительной нуклеофильности является небольшая стерическая потребность в блоке CN в сочетании с его индуктивной стабилизацией. Эти особенности делают нитрилы идеальными для создания новых углерод-углеродных связей в стерически сложных средах для использования в синтезе медицинской химии. Недавние разработки показали, что природа противоиона металла вызывает различные координация либо с нитрильным азотом, либо с Связанный нуклеофильный углерод, часто с глубокими различиями в реакционной способности и стереохимии.
Углеродный центр нитрила электрофильный, следовательно, он восприимчив к нуклеофильным реакции присоединения :
Нитрилы являются предшественниками перехода нитрильные комплексы металлов, являющиеся реагентами и катализаторами. Примеры включают [Cu (MeCN) 4] и PdCl 2 (PhCN) 2).
 Образец нитрильного комплекса PdCl 2 (PhCN) 2
Образец нитрильного комплекса PdCl 2 (PhCN) 2Цианамиды представляют собой N-цианамиды с общей структурой R 1R2N-CN, относящиеся к исходному неорганическому цианамиду.
Нитрилоксиды имеют общую структуру R-CNO.

Нитрилы встречаются в природе в разнообразных растительных и животных источниках. Более 120 нитрилов природного происхождения было выделено из наземных и морских источников. Нитрилы обычно встречаются во фруктовых косточках, особенно в миндале, и во время варки культур Brassica (таких как капуста, брюссельская капуста и цветная капуста), которые выделяют нитрилы в результате гидролиза. Мандельонитрил, циангидрин, получаемый при употреблении миндаля или некоторых фруктовых косточек, выделяет цианистый водород и отвечает за токсичность цианогенных гликозидов.
Более 30 нитрилсодержащих фармацевтических препаратов в настоящее время продаются по различным медицинским показаниям с более чем 20 дополнительными нитрилсодержащими препаратами, находящимися в стадии клинической разработки. Нитрильная группа довольно прочна и в большинстве случаев не метаболизируется быстро, но проходит через организм в неизменном виде. Типы фармацевтических препаратов, содержащих нитрилы, разнообразны: от вилдаглиптина, противодиабетического препарата, до анастрозола, который является золотым стандартом в лечении рака груди. Во многих случаях нитрил имитирует функциональность, присутствующую в субстратах для ферментов, тогда как в других случаях нитрил увеличивает растворимость в воде или снижает восприимчивость к окислительному метаболизму в печени. Функциональная группа нитрила содержится в нескольких лекарствах.

Структура перициазина, антипсихотика, изученного при лечении опиатной зависимости.

Структура циталопрама, антидепрессанта класса селективных ингибиторов обратного захвата серотонина (SSRI).
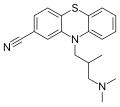
Структура циамемазина, антипсихотического препарата.

Структура фадрозола, ингибитора ароматазы для лечения рака груди.

Структура летрозола, перорального нестероидного ингибитора ароматазы для лечения некоторых видов рака молочной железы.