 | |||
| |||
| Имена | |||
|---|---|---|---|
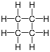
| Название ИЮПАК циклобутан | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 1900183 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.468 | ||
| Номер EC |
| ||
| Справочник Gmelin | 81684 | ||
| PubChem CID | |||
| UNII | |||
| Номер ООН | 2601 | ||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химическая формула | C4H8 | ||
| Молярная масса | 56,107 г / моль | ||
| Внешний вид | Бесцветный газ | ||
| Плотность | 0,720 г / см | ||
| Температура плавления | -91 ° C (-132 ° F; 182 K) | ||
| Точка кипения | 12,5 ° C (54,5 ° F; 285,6 K) | ||
| Опасности | |||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасно | ||
| Краткая характеристика опасности GHS | H220, H280 | ||
| Меры предосторожности GHS | P210, P377, P381, P403, P410 + 403 | ||
| NFPA 704 (огненный алмаз) |  4 1 0 4 1 0 | ||
| Родственные соединения | |||
| Родственные алкан | Бутан | ||
| Родственные соединения | Циклобутен ; Циклобутадиен ; Циклопропан ; Циклопентан | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на ink | |||
Циклобутан представляет собой циклоалкан и органическое соединение с формулой (CH 2)4. Циклобутан представляет собой бесцветный газ и коммерчески доступен как сжиженный газ. Производные циклобутана называются циклобутанами. Сам по себе циклобутан не имеет коммерческого или биологического значения, но более сложные производные важны в биологии и биотехнологии.
Углы связи между атомы углерода значительно напряжены и, как таковые, имеют более низкие энергии связи, чем соответствующие линейные или недеформированные углеводороды, например бутан или циклогексан. Таким образом, циклобутан нестабилен ab температура около 500 ° C.
Четыре атома углерода в циклобутане не компланарны; вместо этого кольцо обычно принимает сложенную или «сморщенную» форму . Один из атомов углерода образует угол 25 ° с плоскостью, образованной другими тремя атомами углерода. Таким образом уменьшаются некоторые из затмевающих взаимодействий. Внешность также известна как «бабочка». Эквивалентные складчатые конформации взаимопревращаются:

Несмотря на присущее им напряжение, мотив циклобутана действительно встречается в природе. Одним из необычных примеров является пентациклоанаммоксическая кислота, которая представляет собой ладдеран, состоящий из 5 конденсированных звеньев циклобутана. Расчетное напряжение в этом соединении в 3 раза выше, чем у циклобутана. Соединение обнаружено в бактериях, выполняющих процесс анаммокс, где оно образует часть плотной и очень плотной мембраны, которая, как считается, защищает организм от токсичных гидроксиламина и гидразина. при производстве азота и воды из ионов нитрита и аммиака. Некоторые родственные фенестраны также встречаются в природе.
Фотодимеры циклобутана (CPD) образуются в результате фотохимических реакций, которые приводят к сочетанию двойных связей C = C в пиримидины. Димеры тимина (димеры ТТ), образованные между двумя тиминами, являются наиболее распространенными из CPD. CPD легко репарируются ферментами эксцизионной репарации нуклеотидов. У большинства организмов они также могут быть восстановлены фотолиазами, семейством светозависимых ферментов. Xeroderma pigmentosum - это генетическое заболевание, при котором это повреждение не может быть исправлено, что приводит к изменению цвета кожи и опухолям, вызванным воздействием УФ-излучения.

Карбоплатин - популярное противоопухолевое средство., который является производным циклобутан-1,1-дикарбоновой кислоты.
Существует множество способов получения циклобутанов. Алкены димеризуются при облучении УФ-светом. 1,4-Дигалобутаны превращаются в циклобутаны при дегалогенировании восстанавливающими металлами.
Циклобутан был впервые синтезирован в 1907 году Джеймсом Брюсом и Ричардом Вилльштеттером путем гидрирования циклобутена в присутствии никеля.
| На Викискладе есть материалы, связанные с Циклобутаном. |