 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Циклоокта-1,5-диен | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| Сокращения | 1,5-ХПК |
| Ссылка на Beilstein | 2036542 1209288 ( Z, Z) |
| ChemSpider | |
| ECHA InfoCard | 100,003,552 |
| Номер ЕС | |
| MeSH | 1,5-циклооктадиен |
| PubChem CID | |
| Номер RTECS | |
| UNII | |
| Номер ООН | 2520 |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | С 8 Н 12 |
| Молярная масса | 108,184 г моль -1 |
| Появление | Бесцветная жидкость |
| Плотность | 0,882 г / мл |
| Температура плавления | −69 ° С; -92 ° F; 204 К |
| Точка кипения | 150 ° С; 302 ° F; 423 К |
| Давление газа | 910 Па |
| Показатель преломления ( n D) | 1,493 |
| Термохимия | |
| Теплоемкость ( C) | 198.9 Дж К −1 моль −1 |
| Стандартная мольная энтропия ( S | 250.0 Дж К −1 моль −1 |
| Std энтальпия формации (Δ F H ⦵298) | 21–27 кДж моль -1 |
| Std энтальпии сгорания (Δ с Н ⦵298) | −4,890 - −4,884 МДж моль −1 |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
| Формулировки опасности GHS | H226, H304, H315, H317, H319, H334 |
| Меры предосторожности GHS | Р261, Р280, Р301 + 310, P305 + 351 + 338, P331, P342 + 311 |
| точка возгорания | От 32 до 38 ° C (от 90 до 100 ° F; от 305 до 311 K) |
| самовоспламенения температуру | 222 ° С (432 ° F, 495 К) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
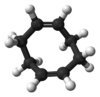
Циклоокта-1,5-диен представляет собой циклический углеводород с химической формулой C 8 H 12 ; в частности [- (CH 2) 2–CH = CH–] 2.
Имеются три конфигурационных изомера с этой структурой, которые отличаются расположением четырех одинарных связей C – C, примыкающих к двойным связям. Каждая пара одинарных связей может находиться на одной стороне ( цис, Z) или на противоположных сторонах ( транс, E) плоскости двойной связи; три возможности обозначаются цис, цис, транс, транс и цис, транс ; или ( Z, Z), ( E, E) и ( Z, E). (Из-за общей симметрии транс, цис имеет ту же конфигурацию, что и цис, транс.)
Обычно сокращенно COD, цис, цис- изомер этого диена является полезным предшественником других органических соединений и служит лигандом в металлоорганической химии. Это бесцветная жидкость с сильным запахом. 1,5-Циклооктадиен может быть получен димеризацией бутадиена в присутствии никелевого катализатора, побочным продуктом которого является винилциклогексен. В 2005 году было произведено около 10 000 тонн.
ХПК реагирует с бораном с образованием 9-борабицикло [3.3.1] нонана, широко известного как 9-BBN, реагента в органической химии, используемого в гидроборировании :

ХПК добавляет SCl 2 (или аналогичные реагенты) с получением 2,6-дихлор-9-тиабицикло [3.3.1] нонана:
![2,6-Дихлор-9-тиабицикло [3.3.1] нонан, синтез и реакции](https://upload.wikimedia.org/wikipedia/commons/thumb/a/ab/CODSCl2.png/450px-CODSCl2.png)
В результате дихлорид может быть дополнительно модифицирован в качестве ди азида или ди - циано - производный в нуклеофильном замещении помогшего anchimeric помощи.

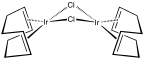
Комплекс Rh 2 (COD) 2 Cl 2.
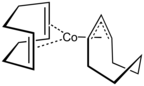
Со (1,5-циклооктадиен) (циклооктенил).

1,5-ХПК связывается с низковалентными металлами через обе алкеновые группы. Комплексы металл-ХПК привлекательны, потому что они достаточно стабильны для выделения, часто более устойчивы, чем родственные комплексы этилена. Стабильность комплексов ХПК объясняется хелатным эффектом. Лиганды COD легко заменяются другими лигандами, такими как фосфины.
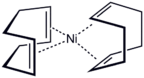
Ni (COD) 2 получают восстановлением безводного ацетилацетоната никеля в присутствии лиганда с использованием триэтилалюминия.
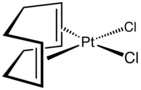
Родственная Pt (COD) 2 получается более окольным путем с участием циклооктатетраена дилития:
Сообщается об обширной работе по комплексам ХПК, многие из которых описаны в томах 25, 26 и 28 книги « Неорганические синтезы». Платиновый комплекс является предшественником 16-электронного комплекса этилена:
Комплексы ХПК полезны в качестве исходных материалов; Один примечательный пример - реакция:
Продукт Ni (CO) 4 очень токсичен, поэтому его выгодно генерировать в реакционном сосуде по мере необходимости. Другие низкая валентность комплексы металлов включают в себя ХПК димер циклооктадиен родий хлорид, циклооктадиен иридий хлорид димер и Fe (COD) (CO) 3, и катализатор Crabtree в.
Комплексы M (COD) 2 с никелем, палладием и платиной имеют тетраэдрическую геометрию, тогда как комплексы [M (COD) 2 ] + родия и иридия имеют плоскую квадратную форму.
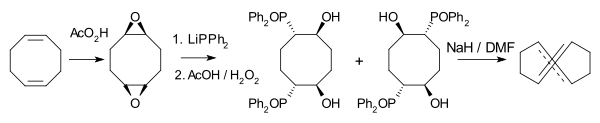 E, синтез E -COD (Stöckmann et al.2011)
E, синтез E -COD (Stöckmann et al.2011)Сильно напряженный транс, транс- изомер 1,5-циклооктадиена является известным соединением. ( Е, Е) -COD был впервые синтезирован Джорджа М. Whitesides и Arthur C. Коп в 1969 году фотоизомеризации из цис, цис - соединение. О другом синтезе (реакция двойного элиминирования из циклооктанового кольца) сообщил Рольф Хьюсген в 1987 году. Молекулярная конформация ( E, E) -COD скорее скрученная, чем подобная стулу. Соединение было исследовано как посредник химии щелчков.