стандартная энтальпия образования или стандартная теплота образования соединения представляет собой изменение энтальпии при образовании 1 моля вещества из составляющих его элементов, со всеми веществами в их стандартных состояниях. Стандартное значение давления p = 10 Па (= 100 кПа = 1 бар ) рекомендовано IUPAC, хотя до 1982 года значение 1,00 атм. (101,325 кПа). Стандартной температуры нет. Его символ - Δ f H. Верхний индекс Plimsoll на этом символе указывает, что процесс происходил в стандартных условиях при указанной температуре (обычно 25 ° C или 298,15 K). Стандартные состояния следующие:
Для Например, стандартная энтальпия образования диоксида углерода будет энтальпией следующей реакции при вышеуказанных условиях:
Все элементы записаны в своих стандартных состояниях, и образуется один моль продукта. Это верно для всех энтальпий образования.
Стандартная энтальпия образования измеряется в единицах энергии на количество вещества, обычно выражается в килоджоулях на моль (кДж моль), но также в килокалории на моль, джоуль на моль или килокалорию на грамм (любая комбинация этих единиц, соответствующая нормативам энергии на массу или количество).
Все элементы в их стандартных состояниях (кислород газ, твердый углерод в форме графита и т. Д.) Имеют стандартную энтальпию образование нуля, так как в их образовании нет никаких изменений.
Реакция пласта представляет собой процесс при постоянном давлении и постоянной температуре. Поскольку давление стандартной реакции образования фиксировано на уровне 1 бар, стандартная энтальпия образования или теплота реакции является функцией температуры. Для целей таблицы все стандартные энтальпии образования приведены для одной температуры: 298 K, представленной символом Δ fH. 298 K.
Для многих веществ реакция образования может рассматриваться как сумма ряд более простых реакций, реальных или вымышленных. энтальпию реакции затем можно проанализировать с применением закона Гесса, который гласит, что сумма изменений энтальпии для ряда отдельных стадий реакции равна изменению энтальпии всей реакции. Это верно, потому что энтальпия - это функция состояния , значение которой для всего процесса зависит только от начального и конечного состояний, а не от каких-либо промежуточных состояний. Примеры приведены в следующих разделах.
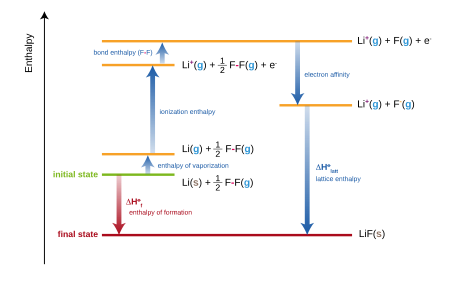 Стандартное изменение энтальпии образования на диаграмме Борна – Габера для фторида лития. ΔH latt соответствует U L в тексте. Стрелка вниз «сродство к электрону» показывает отрицательную величину –EA F, поскольку EA F обычно определяется как положительное.
Стандартное изменение энтальпии образования на диаграмме Борна – Габера для фторида лития. ΔH latt соответствует U L в тексте. Стрелка вниз «сродство к электрону» показывает отрицательную величину –EA F, поскольку EA F обычно определяется как положительное. Для ионных соединений стандартная энтальпия образование эквивалентно сумме нескольких членов, включенных в цикл Борна – Габера. Например, образование фторида лития,
можно рассматривать как сумму нескольких стадий, каждая из которых имеет свою энтальпию. (или энергия, приблизительно):
Сумма всех этих энтальпий дает стандартную энтальпию образования фторида лития.

На практике энтальпию образования фторида лития можно определить экспериментально, но энергию решетки нельзя измерить напрямую. Поэтому уравнение перестраивается, чтобы оценить энергию решетки:

Реакции образования большинства органических соединений являются гипотетическими. Например, углерод и водород не будут напрямую реагировать с образованием метана (CH 4), поэтому стандартную энтальпию образования нельзя измерить напрямую. Однако стандартную энтальпию сгорания легко измерить с помощью калориметрии с бомбой. Затем определяют стандартную энтальпию образования с использованием закона Гесса. Сжигание метана (CH 4 + 2 O 2 → CO 2 + 2 H 2 O) эквивалентно сумме гипотетическое разложение на элементы с последующим сгоранием элементов с образованием диоксида углерода и воды:
Применяя закон Гесса,
Решение для стандарта энтальпии образования,
Значение Δ f H (CH 4) определяется как -74,8 кДж / моль. Отрицательный знак показывает, что реакция, если бы она продолжалась, была бы экзотермической ; то есть метан энтальпически более устойчив, чем газообразный водород, и углерода.
Можно предсказать теплоту образования простых недеформированных органических соединений с помощью теплоты образования группы ad дитивность метод.
Стандартное изменение энтальпии любой реакции может быть рассчитано из стандартных энтальпий образования реагентов и продуктов с использованием закона Гесса. Данная реакция рассматривается как разложение всех реагентов на элементы в их стандартных состояниях с последующим образованием всех продуктов. В этом случае теплота реакции равна минус сумме стандартных энтальпий образования реагентов (каждая из которых умножается на соответствующий стехиометрический коэффициент ν) плюс сумма стандартных энтальпий образования продуктов (каждая также умножается на соответствующую стехиометрическую величину). коэффициент), как показано в уравнении ниже:
Если стандартная энтальпия продуктов меньше стандартной энтальпии реагентов, стандартная энтальпия реакции отрицательна. Это означает, что реакция экзотермическая. Обратное также верно; стандартная энтальпия реакции положительна для эндотермической реакции. Этот расчет подразумевает неявное предположение о идеальном растворе между реагентами и продуктами, где энтальпия смешения равна нулю.
Например, для сжигания метана, CH 4 + 2 O 2 → CO 2 + 2 H 2 O:
Однако O 2 - элемент в его стандартном состоянии, так что Δ f H (O 2) = 0, а теплота реакции упрощена до
, которое представляет собой уравнение для энтальпии сгорания в предыдущем разделе Δ comb H.
Термохимические свойства выбранных веществ при 298 K и 1 атм
| Виды | Фаза | Химическая формула | ΔfH / (кДж / моль) |
|---|---|---|---|
| Алюминий | |||
| Алюминий | Твердый | Al | 0 |
| Хлорид алюминия | Твердый | AlCl 3 | -705,63 |
| Оксид алюминия | Твердый | Al2O3 | -1675,5 |
| Алюминий гидроксид | твердое вещество | Al (OH) 3 | -1277 |
| сульфат алюминия | твердое вещество | Al2(SO 4)3 | -3440 |
| аммиак (гидроксид аммония) | Водный | NH3(NH4OH) | -80,8 |
| Аммиак | Газ | NH3 | -46,1 |
| Нитрат аммония | Твердый | NH4NO3 | -365,6 |
| Барий | |||
| Хлорид бария | Твердый | BaCl 2 | -858,6 |
| Карбонат бария | Твердый | BaCO 3 | -1213 |
| Гидроксид бария | Твердый | Ba (OH) 2 | -944,7 |
| Барий оксид | Твердый | BaO | -548,1 |
| Сульфат бария | Твердый | BaSO 4 | -1473,2 |
| Бериллий | |||
| Бериллий | Твердый | Be | 0 |
| Гидроксид бериллия | Твердый | Be (OH) 2 | -902,9999 |
| Оксид бериллия | Твердый | BeO | -609,4 (25) |
| Бор | |||
| Треххлористый бор | Твердый | BCl 3 | -402,96 |
| Бром | |||
| Бром | Жидкий | Br2 | 0 |
| Бромид-ион | Водный | Br | −121 |
| Бром | Газ | Br | 111,884 |
| Бром | Газ | Br2 | 30,91 |
| Бром трифторид | газ | BrF 3 | -255,60 |
| бромистый водород | газ | HBr | -36,29 |
| кадмий | |||
| кадмий | Твердый | Cd | 0 |
| Оксид кадмия | Твердый | CdO | -258 |
| Гидроксид кадмия | Твердый | Cd (OH) 2 | -561 |
| Сульфид кадмия | Твердый | CdS | -162 |
| Сульфат кадмия | Твердый | CdSO 4 | −935 |
| Кальций | |||
| Кальций | Твердый | Ca | 0 |
| Кальций | Газ | Ca | 178,2 |
| Ион кальция (II) | Газ | Ca | 1925,90 |
| Карбид кальция | Твердый | CaC 2 | -59,8 |
| Кальций карбонат (Кальцит ) | Твердый | CaCO 3 | -1206,9 |
| Хлорид кальция | Твердый | CaCl 2 | -795,8 |
| Кальций хлорид | водный | CaCl 2 | -877,3 |
| фосфат кальция | твердое вещество | Ca3(PO 4)2 | -4132 |
| фторид кальция | твердое вещество | CaF 2 | −1219,6 |
| гидрид кальция | твердое вещество | CaH 2 | −186,2 |
| гидроксид кальция | твердое вещество | Ca (OH) 2 | -986,09 |
| гидроксид кальция | водный | Ca (OH) 2 | -1002,82 |
| оксид кальция | твердый | CaO | -635,09 |
| Сульфат кальция | Твердый | CaSO 4 | -1434,52 |
| Сульфид кальция | Твердый | CaS | -482,4 |
| Волластонит | Твердый | CaSiO 3 | −1630 |
| Цезий | |||
| Цезий | Твердый | Cs | 0 |
| Цезий | Газ | Cs | 76,50 |
| Цезий | Жидкий | Cs | 2,09 |
| Ca ион эзия (I) | Газ | Cs | 457,964 |
| Хлорид цезия | Твердый | CsCl | -443,04 |
| Углерод | |||
| Углерод (Графит ) | Твердый | C | 0 |
| Углерод (Алмаз ) | Твердый | C | 1,9 |
| Углерод | Газ | C | 716,67 |
| Двуокись углерода | Газ | CO2 | -393,509 |
| Дисульфид углерода | Жидкость | CS2 | 89,41 |
| Дисульфид углерода | Газ | CS2 | 116,7 |
| Окись углерода | Газ | CO | -110,525 |
| Карбонилхлорид (Фосген ) | Газ | COCl 2 | -218,8 |
| Двуокись углерода (неионизированная) | Водный | CO2(водный) | -419,26 |
| Бикарбонат ион | Водный | HCO 3 | -689,93 |
| Карбонат ион | Водный | CO3 | -675,23 |
| Хлор | |||
| Одноатомный хлор | Газ | Cl | 121,7 |
| Хлорид ион | Водный | Cl | -167,2 |
| Хлор | Газ | Cl2 | 0 |
| Хром | |||
| Хром | Твердый | Cr | 0 |
| Медь | |||
| Медь | Твердый | Cu | 0 |
| Оксид меди (II) | Твердый | CuO | -155,2 |
| Сульфат меди (II) | Водный | CuSO 4 | -769,98 |
| Фтор | |||
| Фтор | Газ | F2 | 0 |
| Водород | |||
| Одноатомный водород | Газ | H | 218 |
| Водород | Газ | H2 | 0 |
| Вода | Газ | H2O | −241,818 |
| Вода | Жидкость | H2O | −285,8 |
| Ион водорода | Водный | H | 0 |
| Ион гидроксида | Водный | OH | -230 |
| Пероксид водорода | Жидкость | H2O2 | -187,8 |
| Фосфорная кислота | Жидкость | H3PO4 | -1288 |
| Цианистый водород | Газ | HCN | 130,5 |
| Бромистый водород | Жидкость | HBr | -36,3 |
| Хлористый водород | Газ | HCl | -92,30 |
| Хлороводород | Водный | HCl | -167,2 |
| Фтористый водород | Газ | HF | -273,3 |
| Йодоводород | Газ | HI | 26,5 |
| Йод | |||
| Йод | Твердый | I2 | 0 |
| Йод | Газ | I2 | 62,438 |
| Йод | Водный | I2 | 23 |
| Йодид ион | Водный | I | -55 |
| Железо | |||
| Железо | Твердое | Fe | 0 |
| Карбид железа (Цементит ) | Твердый | Fe3C | 5,4 |
| Карбонат железа (II) (Сидерит ) | Твердый | FeCO 3 | -750,6 |
| Хлорид железа (III) | Твердый | FeCl 3 | -399,4 |
| Оксид железа (II) (Вюстит ) | Твердый | FeO | -272 |
| Оксид железа (II, III) (Магнетит ) | Твердый | Fe3O4 | −1118,4 |
| Оксид железа (III) (Гематит ) | Твердый | Fe2O3 | - 824,2 |
| Сульфат железа (II) | Твердый | FeSO 4 | -929 |
| Сульфат железа (III) | Твердый | Fe2(SO 4)3 | -2583 |
| Сульфид железа (II) | Твердый | FeS | -102 |
| Пирит | Твердый | FeS 2 | -178 |
| Свинец | |||
| Свинец | Твердый | Pb | 0 |
| Диоксид свинца | Твердый | PbO 2 | −277 |
| Сульфид свинца | Твердый | PbS | -100 |
| Сульфат свинца | Твердый | PbSO 4 | -920 |
| Нитрат свинца (II) | Твердый | Pb (NO 3)2 | -452 |
| Сульфат свинца (II) | Твердый | PbSO 4 | -920 |
| Литий | |||
| Фторид лития | Твердый | LiF | -616,93 |
| Магний | |||
| Магнезия ium | Твердый | Mg | 0 |
| Ион магния | Водный | Mg | -466,85 |
| Карбонат магния | Твердый | MgCO 3 | -1095,797 |
| Хлорид магния | Твердый | MgCl 2 | -641,8 |
| Гидроксид магния | Твердый | Mg (OH) 2 | -924,54 |
| Гидроксид магния | Водный | Mg (OH) 2 | -926,8 |
| Оксид магния | Твердый | MgO | -601,6 |
| Сульфат магния | Твердый | MgSO 4 | −1278,2 |
| Марганец | |||
| Марганец | Твердый | Mn | 0 |
| Оксид марганца (II) | Твердый | MnO | -384,9 |
| Оксид марганца (IV) | Твердый | MnO 2 | -519,7 |
| Оксид марганца (III) | Твердый | Mn2O3 | - 971 |
| оксид марганца (II, III) | твердый | Mn3O4 | -1387 |
| перманганат | водный | MnO. 4 | -543 |
| ртуть | |||
| ртуть (II) оксид (красный) | Твердый | HgO | -90,83 |
| Сульфид ртути (красный, киноварь ) | Твердый | HgS | -58,2 |
| Азот | |||
| Азот | Газ | N2 | 0 |
| Аммон ia | Водный | NH3 | -80,8 |
| Аммиак | Газ | NH3 | -45,90 |
| Хлорид аммония | Твердый | NH4Cl | -314,55 |
| Двуокись азота | Газ | NO2 | 33,2 |
| Закись азота | Газ | N2O | 82,05 |
| Оксид азота | Газ | NO | 90,29 |
| Двуокись азота | Газ | N2O4 | 9,16 |
| Пятиокись азота | Твердое вещество | N2O5 | -43,1 |
| Пятиокись азота | Газ | N2O5 | 11,3 |
| Азотная кислота | Водная | HNO 3 | −207 |
| Кислород | |||
| Одноатомный кислород | Газ | O | 249 |
| Кислород | Газ | O2 | 0 |
| Озон | Газ | O3 | 143 |
| Фосфор | |||
| Белый фосфор | Твердый | P4 | 0 |
| Красный фосфор | Твердый | P | -17,4 |
| Черный фосфор | Твердый | P | -39,3 |
| Треххлористый фосфор | Жидкость | PCl 3 | −319,7 |
| Трихлорид фосфора | Газ | PCl 3 | −278 |
| Пентахлорид фосфора | Твердое вещество | PCl 5 | -440 |
| Пентахлорид фосфора | Газ | PCl 5 | -321 |
| Пятиокись фосфора | Твердый | P2O5 | -1505,5 |
| Калий | |||
| Бром калия de | Твердый | KBr | -392,2 |
| Карбонат калия | Твердый | K2CO3 | -1150 |
| Хлорат калия | Твердый | KClO 3 | -391,4 |
| Хлорид калия | Твердый | KCl | -436,68 |
| Фторид калия | Твердый | KF | −562,6 |
| оксид калия | твердое вещество | K2O | −363 |
| перхлорат калия | твердое вещество | KClO 4 | −430,12 |
| кремний | |||
| кремний | газ | Si | 368,2 |
| Карбид кремния | Твердый | SiC | -74,4, -71,5 |
| Тетрахлорид кремния | Жидкость | SiCl 4 | -640,1 |
| Кремнезем (Кварц ) | Твердый | SiO 2 | -910,86 |
| Серебро | |||
| Бромид серебра | Твердый | AgBr | -99,5 |
| Хлорид серебра | Твердый | AgCl | -127,01 |
| Иодид серебра | Твердый | AgI | -62,4 |
| Оксид серебра | Твердый | Ag2O | -31,1 |
| Сульфид серебра | Твердый | Ag2S | -31,8 |
| Натрий | |||
| Натрий | Твердое вещество | Na | 0 |
| Натрий | Газ | Na | 107,5 |
| Натрий b икарбонат | твердое вещество | NaHCO 3 | -950,8 |
| карбонат натрия | твердое вещество | Na2CO3 | -1130,77 |
| хлорид натрия | водный | NaCl | -407,27 |
| хлорид натрия | твердый | NaCl | -411,12 |
| хлорид натрия | жидкий | NaCl | -385,92 |
| хлорид натрия | газ | NaCl | -181,42 |
| хлорат натрия | твердое вещество | NaClO 3 | -365,4 |
| Фторид натрия | Твердый | NaF | -569,0 |
| Гидроксид натрия | Водный | NaOH | -469,15 |
| Натрий гидроксид | твердое вещество | NaOH | -425,93 |
| гипохлорит натрия | твердое вещество | NaOCl | -347,1 |
| нитрат натрия | Водный | NaNO 3 | -446,2 |
| Нитрат натрия | Твердый | NaNO 3 | -424,8 |
| Оксид натрия | Твердый | Na2O | -414,2 |
| Сера | |||
| Сера (моноклинная) | Твердая | S8 | 0,3 |
| Сера (ромбическая) | Твердая | S8 | 0 |
| Сероводород | Газ | H2S | -20,63 |
| Диоксид серы | Газ | SO2 | -29 6,84 |
| Триоксид серы | Газ | SO3 | -395,7 |
| Серная кислота | Жидкость | H2SO4 | -814 |
| Олово | |||
| Титан | |||
| Титан | Газ | Ti | 468 |
| Тетрахлорид титана | Газ | TiCl 4 | −763,2 |
| Тетрахлорид титана | Жидкость | TiCl 4 | - 804,2 |
| Диоксид титана | Твердый | TiO 2 | -944,7 |
| Цинк | |||
| Цинк | Газ | Zn | 130,7 |
| Хлорид цинка | Твердый | ZnCl 2 | -415,1 |
| Оксид цинка | Твердый | ZnO | -348,0 |
| Сульфат цинка | Твердое вещество | ZnSO 4 | -980,14 |
| Формула | Название | ΔfH / (ккал / моль) | ΔfH / (кДж / моль) |
|---|---|---|---|
| Прямая цепь | |||
| CH4 | Метан | −17,9 | −74,9 |
| C2H6 | Этан | −20,0 | -83,7 |
| C2H4 | Этилен | 12,5 | 52,5 |
| C2H2 | Ацетилен | 54,2 | 226,8 |
| C3H8 | Пропан | −25,0 | -104,6 |
| C4H10 | n-Бутан | -30,0 | -125,5 |
| C5H12 | n-Пентан | -35,1 | -146,9 |
| C6H14 | n-Гексан | -40,0 | -167,4 |
| C7H16 | n-Гептан | -44,9 | -187,9 |
| C8H18 | n-Октан | -49,8 | -208,4 |
| C9H20 | n-Нонан | -54,8 | -229,3 |
| C10H22 | n-Декан | -59,6 | -249,4 |
| C4Разветвленные изомеры алканов | |||
| C4H10 | Изобутан (метилпропан) | -32,1 | -134,3 |
| C5Разветвленные изомеры алканов | |||
| C5H12 | Неопентан ( диметилпропан) | −40,1 | −167,8 |
| C5H12 | Изопентан (метилбутан) | −36,9 | −154,4 |
| C6Алкановые разветвленные изомеры | |||
| C6H14 | 2,2-диметилбутан | -44,5 | -186,2 |
| C6H14 | 2,3-диметилбутан | -42,5 | -177,8 |
| C6H14 | 2 -Метилпентан (изогексан) | -41,8 | -174,9 |
| C6H14 | 3-Метилпентан | -41,1 | -172,0 |
| C7Разветвленные изомеры алкана | |||
| C7H16 | 2,2-Диметилпентан | -49,2 | -205,9 |
| C7H16 | 2,2,3-Триметилбутан | -49,0 | -205,0 |
| C7H16 | 3,3- Диметилпентан | -48,1 | -201,3 |
| C7H16 | 2,3-Диметилпентан | -47,3 | -197,9 |
| C7H16 | 2,4-Диметилпентан | -48,2 | −201,7 |
| C7H16 | 2-Метилгексан | -46,5 | −194,6 |
| C7H16 | 3- Метилгексан | -45,7 | - 191,2 |
| C7H16 | 3-этилпентан | -45,3 | -189,5 |
| C8Разветвленные изомеры алкана | |||
| C8H18 | 2,3-диметилгексан | -55,1 | -230,5 |
| C8H18 | 2,2,3,3-Тетраметилбутан | -53,9 | -225,5 |
| C8H18 | -53,7 | -224,7 | |
| C8H18 | 2,2,4-Триметилпентан (изооктан) | −53,5 | −223,8 |
| C8H18 | 2,5- Диметилгексан | −53,2 | −222,6 |
| C8H18 | −52,6 | - 220,1 | |
| C8H18 | −52,6 | −220,1 | |
| C8H18 | −52,4 | −219,2 | |
| C8H18 | 2,3,4-Триметилпентан | −51,9 | −217,1 |
| C8H18 | 2,3,3-Триметилпентан | −51,7 | −216,3 |
| C8H18 | 2-Метилгептан | −51,5 | −215,5 |
| C8H18 | -51,4 | −215,1 | |
| C8H18 | −50,9 | −213,0 | |
| C8H18 | −50,4 | −210,9 | |
| C8H18 | 3- Метилгептан | −60,3 | −252,5 |
| C8H18 | ? | ? | |
| C8H18 | ? | ? | |
| C9Алкановые разветвленные изомеры (выбранные) | |||
| C9H20 | -57,8 | -241,8 | |
| C9H20 | -56,7 | -237,2 | |
| C9H20 | -56,6 | -236,8 | |
| C9H20 | -56,4 | -236,0 | |
| C9H20 | 3,3- Диэтилпентан | -55,7 | -233,0 |
| Виды | Фаза | Химическая формула | ΔfH / (кДж / моль) |
|---|---|---|---|
| Ацетон | Жидкость | C3H6O | -248,4 |
| Бензол | Жидкость | C6H6 | 48,95 |
| Бензойная кислота | Твердое вещество | C7H6O2 | -385,2 |
| Тетрахлорид углерода | Жидкость | CCl 4 | -135,4 |
| Тетрахлорид углерода | Газ | CCl 4 | -95,98 |
| Этанол | Жидкость | C2H5OH | −277,0 |
| этанол | газ | C2H5OH | −235,3 |
| глюкоза | твердое вещество | C6H12O6 | −1271 |
| изопропанол | газ | C3H7OH | −318,1 |
| Метанол (метиловый спирт) | Жидкость | CH3OH | -238,4 |
| Метанол (метиловый спирт) | Газ | CH3OH | -201,0 |
| (Биодизель ) | Газ | C19H34O2 | -356,3 |
| Сахароза | Твердое вещество | C12H22O11 | -2226,1 |
| Трихлорметан (Хлороформ ) | Жидкость | CHCl 3 | -134,47 |
| Трихлорметан (Хлороформ ) | Газ | CHCl 3 | -103,18 |
| Винилхлорид | Твердое | C2H3Cl | -94,12 |