| |||
| Названия | |||
|---|---|---|---|
| Предпочтительное название IUPAC Анилин | |||
| Систематическое название IUPAC Бензоламин | |||
| Другие названия Фениламин. Аминобензол. Бензамин | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| 3DMet | |||
| Ссылка Beilstein | 605631 | ||
| ЧЭБИ | |||
| ChEMBL |
| ||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.491 | ||
| Номер EC |
| ||
| Справочник Гмелина | 2796 | ||
| KEGG | |||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1547 | ||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКА
| |||
| Свойства | |||
| Химическая формула | C6H7N | ||
| Молярная масса | 93,129 г · моль | ||
| Внешний вид | От бесцветной до желтой жидкости | ||
| Плотность | 1,0297 г / мл | ||
| Температура плавления | -6,3 ° C (20,7 ° F; 266,8 K) | ||
| Температура кипения | 184,13 ° C (363,43 ° F; 457,28 K) | ||
| Растворимость в воде | 3,6 г / 100 мл при 20 ° C | ||
| Давление пара | 0,6 мм рт. (20 ° C) | ||
| Кислотность (pK a) |
| ||
| Магнитная восприимчивость (χ) | -62,95 · 10 см / моль | ||
| Вязкость | 3,71 сП (3,71 мПа · с при 25 ° C) | ||
| Термохимия | |||
| Стандартная энтальпия. горения (ΔcH298) | -3394 кДж / mol | ||
| Опасности | |||
| Основные опасности | потенциальный профессиональный канцероген | ||
| Паспорт безопасности | См.: страница данных | ||
| пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасно | ||
| Краткая характеристика опасности GHS | H301, H311, H317, H318, H331, H341, H351, H372, H400 | ||
| Меры предосторожности GHS | P201, P202, P260, P261, P264, P270, P271, P272, P273, P280, P281, P301 + 310, P302 + 352, P304 + 340, P305 + 351 + 338, P308 + 313, P310, P311, P312, P314, P321, P322, P330, P333 + 313, P361 | ||
| NFPA 704 (огонь алмаз) |  2 3 0 2 3 0 | ||
| Температура вспышки | 70 ° C (158 ° F; 343 K) | ||
| Самовоспламенение. температура | 770 ° C (1420 ° F; 1040 K) | ||
| Пределы взрываемости | 1,3–11% | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LDLo(самый низкий опубликованный ) | 195 мг / кг (собака, перорально). 250 мг / кг (крыса, перорально). 464 мг / кг (мышь, перорально). 440 мг / кг (крыса, перорально). 400 мг / кг (морская свинка, перорально) | ||
| LC50(средняя концентрация ) | 175 частей на миллион (мышь, 7 часов) | ||
| LCLo(самая низкая опубликованная ) | 250 частей на миллион (крыса, 4 часа). 180 ppm (кошка, 8 ч) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимое) | TWA 5 ppm (19 мг / м) [кожа ] | ||
| REL (рекомендуется) | Ca [потенциальный профессиональный канцероген] | ||
| IDLH (непосредственная опасность) | 100 ppm | ||
| Родственные соединения | |||
| Родственные ароматические амины | 1-Нафтиламин. 2-Нафтиламин | ||
| Родственные соединения | Фенилгидразин. Нитрозобензол. Нитробензол | ||
| Страница дополнительных данных | |||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. Д. | ||
| Термодинамические. данные | Фазовое поведение. твердое тело – жидкость – газ | ||
| Спектральные данные | UV, IR, ЯМР, MS | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Анилин представляет собой органическое соединение с формулой C6H5NH2. Состоящий из фенильной группы, присоединенной к аминогруппе, анилин представляет собой простейший ароматический амин. Это промышленно значимый товарный химикат, а также универсальный исходный материал для тонкого химического синтеза. Его основное применение - производство прекурсоров полиуретана, красителей и других промышленных химикатов. Как и большинство летучих аминов, он имеет запах тухлой рыбы. Он легко воспламеняется, горит с дымным пламенем, характерным для ароматических соединений.
С химической точки зрения он считается богатым электронами производным бензола и, как следствие, быстро реагирует в реакциях электрофильного ароматического замещения. Точно так же он также склонен к окислению: в то время как свежеочищенный анилин представляет собой почти бесцветное масло, воздействие воздуха приводит к постепенному потемнению образца (до желтого или красного цвета) из-за образования сильно окрашенных окисленных примесей. Анилин можно диазотировать с получением соли диазония , которая затем может подвергаться различным реакциям нуклеофильного замещения.
Как и другие амины, анилин является основанием (pK aH = 4,6) и нуклеофилом, хотя он является более слабым основанием и более бедным нуклеофилом, чем структурно схожие алифатические амины.
Анилин представляет собой слегка пирамидальную молекулу с гибридизацией азота где-то между sp и sp. В результате неподеленная пара азота оказывается на sp-гибридной орбитали с высоким значением p. Аминогруппа в анилине более плоская (т.е. это «более мелкая пирамида»), чем в алифатическом амине, из-за конъюгации неподеленной пары с арильным заместителем. Наблюдаемая геометрия отражает компромисс между двумя конкурирующими факторами: 1) стабилизация N неподеленной пары на орбитали со значительным s-характером способствует пирамидализации (орбитали с s-характером имеют меньшую энергию), а 2) делокализация неподеленная пара в арильном кольце способствует планарности (неподеленная пара в чистой p-орбитали дает наилучшее перекрытие с орбиталями π-системы бензольного кольца).
В соответствии с этими факторами замещенные анилины с электронодонорными функциями группы более пирамидализированы, тогда как группы с электроноакцепторными группами более плоские. В исходном анилине неподеленная пара имеет приблизительно 12% s-признак, соответствующий sp-гибридизации. (Для сравнения, алкиламины обычно имеют неподеленные пары на орбиталях, близких к sp.)
Угол пирамидализации между связью C – N и биссектрисой угла H – N – H составляет 142,5 °. (Для сравнения, в более сильно пирамидном метиламине это значение составляет ~ 125 °, в то время как плоский азот, подобный азоту формамида, имеет угол 180 °.) Расстояние C-N также соответственно короче. В анилине длина связи C − N составляет 1,41 Å по сравнению с 1,47 Å для циклогексиламина, что указывает на частичную π-связь между N и C.
Промышленное производство анилина включает два шага. Сначала бензол подвергается нитрованию концентрированной смесью азотной кислоты и серной кислоты при температуре от 50 до 60 ° C с получением нитробензол. Затем нитробензол гидрируют (обычно при 200–300 ° C) в присутствии металлических катализаторов :
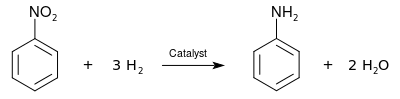
Восстановление нитробензола до анилина впервые было выполнено Николаем Зининым в 1842 г. с использованием неорганического сульфида в качестве восстановителя (реакция Зинина ). Восстановление нитробензола до анилина также проводилось как часть восстановлений Антуаном Бешаном в 1854 году с использованием железа в качестве восстановителя (восстановление Бешана ).
Анилин альтернативно можно получить из аммиака и фенола, полученного кумольным процессом.
В коммерции различают три марки анилина: анилиновое масло для синего, которое является чистым анилин; анилиновое масло для красного цвета, смесь эквимолекулярных количеств анилина и орто- и пара-толуидинов ; и анилиновое масло для сафранина, которое содержит анилин и орто- толуидин и получено из дистиллята (échappés) сплава фуксина.
Известно много аналогов анилина, в которых фенильная группа дополнительно замещена. К ним относятся толуидины, ксилидины, хлоранилины, аминобензойные кислоты, нитроанилины и многие другие. Их часто получают нитрованием замещенных ароматических соединений с последующим восстановлением. Например, этот подход используется для превращения толуола в толуидины и хлорбензола в 4-хлоранилин. В качестве альтернативы, используя подходы сочетания Бухвальда-Хартвига или реакции Ульмана, арилгалогениды можно оживить водным или газообразным аммиаком.
Химический состав анилина богат, потому что это соединение было дешево доступно в течение многих лет. Ниже приведены некоторые классы его реакций.
Окисление анилина было тщательно изучено и может приводить к реакциям, локализованным на азоте, или, чаще, к образованию новых связей C-N. В щелочном растворе образуется азобензол, тогда как мышьяковая кислота дает фиолетово-окрашивающее вещество виоланилин. Хромовая кислота превращает его в хинон, тогда как хлораты в присутствии некоторых металлических солей (особенно ванадия ) дают анилиновый черный. Соляная кислота и хлорат калия дают хлоранил. перманганат калия в нейтральном растворе окисляет его до нитробензола ; в щелочном растворе к азобензолу, аммиаку и щавелевой кислоте ; в растворе кислоты до анилинового черного. Хлорноватистая кислота дает 4-аминофенол и пара-амино дифениламин. Окисление персульфатом дает различные полианилины. Эти полимеры обладают богатыми окислительно-восстановительными и кислотно-основными свойствами.
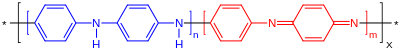 Полианилины могут образовываться при окислении анилина.
Полианилины могут образовываться при окислении анилина. .
Как и фенолы, производные анилина очень чувствительны к реакциям электрофильного замещения. Его высокая реакционная способность отражает то, что это енамин, который усиливает электронодонорную способность кольца. Например, реакция анилина с серной кислотой при 180 ° C дает сульфаниловую кислоту, H 2NC6H4SO3H.
Если к анилину добавляется бромная вода, бромная вода обесцвечивается и белый осадок 2,4,6-триброманилина становится сформирован. Для образования монозамещенного продукта требуется защита ацетилхлоридом:
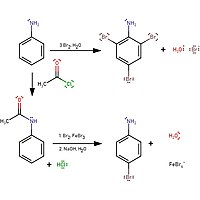 Анилин может реагировать с бромом даже при комнатной температуре в воде. Ацетилхлорид добавляют для предотвращения трибромирования.
Анилин может реагировать с бромом даже при комнатной температуре в воде. Ацетилхлорид добавляют для предотвращения трибромирования. Реакция с образованием 4-броманилина заключается в защите амина с помощью ацетилхлорида, а затем в обратном гидролизе с преобразованием анилина.
Самая крупномасштабная промышленная реакция анилина включает его алкилирование формальдегидом. Показано идеализированное уравнение:
Полученный диамин является предшественником 4,4'-MDI. и родственные диизоцианаты.
Анилин представляет собой слабое основание. Ароматические амины, такие как анилин, обычно являются гораздо более слабыми основаниями, чем алифатические амины. Анилин реагирует с сильными кислотами с образованием иона анилиния (или фениламмония) (C 6H5-NH 3).
Традиционно слабую основность анилина приписывают комбинации индуктивных Эффект от более электроотрицательного sp-углерода и резонансных эффектов, поскольку неподеленная пара на азоте частично делокализована в пи-систему бензольного кольца. (см. рисунок ниже):
 Электрон азота был делокализован в кольце. поэтому анилин менее основной, чем большинство аминов.
Электрон азота был делокализован в кольце. поэтому анилин менее основной, чем большинство аминов. В таком анализе не учитывается сольватация. Анилин, например, более щелочной, чем аммиак в газовой фазе, но в десять тысяч раз меньше в водном растворе.
Анилин реагирует с ацилхлоридами, такими как ацетилхлорид, с образованием амидов. Амиды, образованные из анилина, иногда являются называемые анилидами, например, CH 3 -CO-NH-C 6H5представляет собой ацетанилид. При высоких температурах анилин и карбоксил c кислоты реагируют с образованием анилидов.
N-метилирование анилина метанолом при повышенных температурах над кислотными катализаторами дает N-метиланилин и диметиланилин :
N-Метиланилин и диметиланилин бесцветны жидкости с точками кипения 193–195 ° C и 192 ° C соответственно. Эти производные очень важны в цветной промышленности. Анилин непосредственно соединяется с алкилйодидами с образованием вторичных и третичных аминов.
Кипячение с сероуглеродом дает сульфокарбанилид (дифенил тиомочевина ) (CS (NHC 6H5)2), который может разлагаться на фенил изотиоцианат (C6H5CNS) и трифенил гуанидин (C6H5N = C (NHC 6H5)2).
Анилин и его замещенные в кольцо производные реагируют с азотистой кислотой с образованием солей диазония. С помощью этих промежуточных соединений анилин можно легко превратить в -ОН, -CN, или галогенид посредством реакций Зандмейера. Эта соль диазония также может реагировать с NaNO 2 и фенолом с образованием красителя, известного как бензолазофенол, в процессе, называемом сочетание. Реакция превращения первичного ароматического амина в диазониевую соль называется диазотизацией. В этой реакции первичный ароматический амин реагирует с нитрилом натрия и 2 молями HCl, который известен как Ice cold m Смесь, потому что используется температура 0,5 ° C, и она образует соль бензолдиазония в качестве основного продукта, а также воду и хлорид натрия.
Он реагирует с нитробензолом с образованием феназина в реакции Воля-Ауэ. Гидрирование дает циклогексиламин.
Будучи стандартным реагентом в лабораториях, анилин используется во многих нишевых реакциях. Его ацетат используется в тесте с ацетатом анилина для углеводов, в котором пентозы идентифицируются путем преобразования в фурфурол. Он используется для окрашивания нейронной РНК синим в окрашивании по Нисслю.
Наибольшее применение анилин используется для получения метилендианилина и родственных соединений путем конденсации с формальдегидом. Диамины конденсируются с фосгеном с образованием метилендифенилдиизоцианата, предшественника уретановых полимеров.
 Большая часть анилина расходуется на производство метилендианилина, a прекурсор полиуретанов.
Большая часть анилина расходуется на производство метилендианилина, a прекурсор полиуретанов.Другие применения включают химикаты для обработки каучука (9%), гербициды (2%), а также красители и пигменты (2%). В качестве добавок к каучуку производные анилина, такие как фенилендиамины и дифениламин, являются антиоксидантами. Иллюстративным препаратом, полученным из анилина, является парацетамол (ацетаминофен, тайленол ). Основное применение анилина в красильной промышленности - это предшественник индиго, синего цвета синих джинсов.
 кек красителя индиго, который получают из анилина.
кек красителя индиго, который получают из анилина. Анилин также используется в меньшем масштабе при производстве собственно проводящего полимера полианилина.
Некоторые ранние американские ракеты, такие как Aerobee и WAC капрал использовал смесь анилина и фурфурилового спирта в качестве топлива с азотной кислотой в качестве окислителя. Комбинация - гиперголик, воспламеняющаяся при контакте топлива и окислителя. Он также плотный и может храниться в течение длительного времени.
Впервые анилин был выделен в 1826 году Отто Унвердорбеном деструктивной перегонкой индиго. Он назвал его Кристаллин. В 1834 году Фридлиб Рунге выделил из каменноугольной смолы вещество, которое приобрело красивый синий цвет при обработке хлоридом извести. Он назвал его кианолом или цианолом. В 1840 году Карл Юлиус Фриче (1808–1871) обработал индиго едким калием и получил масло, которое он назвал анилином в честь растения, дающего индиго, анил (Indigofera суффрутикоза ) В 1842 г. Николай Николаевич Зинин восстановил нитробензол и получил основание, которое назвал бензидамом. В 1843 году Август Вильгельм фон Хофманн показал, что это все те же вещества, впоследствии известные как фениламин или анилин.
В 1856 году, пытаясь синтезировать хинин, ученик фон Хофмана Уильям Генри Перкин открыл мовеин и вошел в промышленность, выпустив первый коммерческий синтетический краситель. Затем последовали другие анилиновые красители, такие как фуксин, сафранин и индулин. На момент открытия мовена анилин был дорогим. Вскоре после этого, применяя метод, описанный в 1854 году Антуаном Бешаном, он был приготовлен «тоннами». Сокращение по Бешану способствовало развитию крупной красильной промышленности в Германии. Сегодня название BASF, первоначально Badische Anilin- und Soda-Fabrik (английский: Baden Aniline and Soda Factory), ныне крупнейшего поставщика химикатов, перекликается с наследие индустрии синтетических красок, построенное на анилиновых красителях и расширенное с помощью родственных азокрасителей. Первым азокрасителем был желтый анилин.
В конце 19 века производные анилина, такие как ацетанилид и фенацетин, появились как болеутоляющие препараты с их подавляющими сердечную побочными эффектами часто нейтрализуются с помощью кофеина. В течение первого десятилетия 20-го века, пытаясь модифицировать синтетические красители для лечения африканской сонной болезни, Пол Эрлих - который ввел термин химиотерапия для своего волшебная пуля подход к медицине - потерпел неудачу и переключился на модификацию атоксила Бешана, первого органического мышьяка, и случайно получил лечение сифилиса - сальварсан - первое успешное химиотерапевтическое средство. Микроорганизм-мишень сальварсана, еще не признанный бактерией, все еще считался паразитом, и медицинские бактериологи, полагая, что бактерии не восприимчивы к химиотерапевтическому подходу, упустили из виду Александр Флеминг ' s отчет 1928 г. о влиянии пенициллина.
В 1932 г. Bayer искал медицинские применения своих красителей. Герхард Домагк идентифицировал как антибактериальный красный азокраситель, представленный в 1935 году в качестве первого антибактериального препарата, пронтозил, вскоре обнаруженный в Институте Пастера быть пролекарством, разложенным in vivo до сульфаниламида - бесцветного промежуточного соединения для многих, очень цветостойких азокрасителей - уже с просроченным патент, синтезированный в 1908 году в Вене исследователем Полем Гельмо для его докторских исследований. К 1940-м годам было произведено более 500 родственных сульфамидных препаратов. Лекарства, пользующиеся большим спросом во время Второй мировой войны (1939–45), эти первые чудодейственные препараты, химиотерапия с широкой эффективностью, двигали американскую фармацевтическую промышленность. В 1939 году в Оксфордском университете в поисках альтернативы сульфамидным препаратам Говард Флори разработал пенициллин Флеминга в первый системный антибиотик, пенициллин G. (Грамицидин, разработанный Рене Дубос в Рокфеллеровском институте в 1939 году, был первым антибиотиком, но его токсичность ограничивала его местное применение.) После Второй мировой войны Корнелиус П. Роадс представил химиотерапевтический подход к лечению рака.
В 1940-х и начале 1950-х годов анилин использовался с азотная кислота или тетроксид диазота в качестве ракетного топлива для малых ракет и Aerobee. Два компонента топлива гиперголичны, вызывая бурную реакцию при контакте. Позже анилин был заменен на гидразин.
Анилин токсичен при вдыхании паров, проглатывании или чрескожной абсорбции. IARC относит его к группе 3 (не классифицируемой по его канцерогенности для человека) из-за ограниченности и противоречивости имеющихся данных. Раннее производство анилина привело к увеличению числа случаев рака мочевого пузыря, но эти эффекты теперь приписываются нафтиламинам, а не анилинам.
Анилин считается одной из возможных причин леса dieback.
Существует множество методов обнаружения анилина.
| Посмотрите анилин в Викисловаре, бесплатном словаре. |
| Викискладе есть медиафайлы, связанные с анилином. |