 Трехмерная модель этилена, простейшего алкена.
Трехмерная модель этилена, простейшего алкена. В химии, алкен - это углеводород, содержащий углерод –углерод двойную связь.
Этот термин часто используется как синоним олефин, то есть любой углеводород, содержащий одну или несколько двойных связей. Однако IUPAC рекомендует использовать название «алкен» только для ациклических углеводородов с одной двойной связью; алкадиен, алкатриен и т.д. или полиен для ациклических углеводородов с двумя или более двойными связями; циклоалкен, циклоалкадиен и т.д. для циклических соединений; и «олефин» для общего класса - циклический или ациклический, с одной или несколькими двойными связями.
Ациклические алкены только с одной двойной связью и без других функциональных групп (также известные как моно-ены ) образуют гомологичный ряд из углеводородов с общей формулой C nH 2n, где n равно 2 или более (то есть два атома водорода меньше, чем соответствующий алкан ). Когда n равно четырем или более, имеется несколько изомеров с этой формулой, различающихся положением и конформацией двойной связи.
Алкены обычно представляют собой бесцветные аполярные соединения, отчасти похожие на алканы, но более реакционные. Первые несколько членов этого ряда - это газы или жидкости при комнатной температуре. Простейший алкен, этилен (C2H4) (или «этен» в номенклатуре ИЮПАК ) - это органическое соединение, производимое в самых крупных промышленных масштабах.
Ароматический соединения часто изображаются как циклические алкены, но их структура и свойства достаточно различны, чтобы не классифицировать их как алкены или олефины. Углеводороды с двумя перекрывающимися двойными связями (C = C = C) называются алленами после простейшего такого соединения, а углеводороды с тремя или более перекрывающимися связями (C = C = C = C, C = C = C = C = C и т. Д.) Называются кумуленами. Некоторые авторы не считают аллены и кумулены «алкенами».
Алкены, содержащие четыре или более атомов углерода, могут образовывать различные структурные изомеры. Некоторые алкены также являются изомерами циклоалканов. Структурные изомеры ациклических алкенов только с одной двойной связью:
Многие из этих молекул проявляют цис-транс-изомерию. Также могут быть хиральные атомы углерода, особенно внутри более крупных молекул (от C 5). Число потенциальных изомеров быстро увеличивается с добавлением дополнительных атомов углерода.
 Этилен (этен), пи-связь показана зеленым.
Этилен (этен), пи-связь показана зеленым. Подобно одинарной ковалентной связи, двойные связи могут быть описаны в термины перекрывающихся атомных орбиталей, за исключением того, что, в отличие от одинарной связи (которая состоит из одинарной сигма-связи ), углерод-углеродная двойная связь состоит из одной сигма-связи и одна пи-облигация. Эта двойная связь прочнее одинарной ковалентной связи (611 kJ /моль для C = C по сравнению с 347 кДж / моль для C – C), а также короче, со средним значением длина облигации 1,33 ангстрёмов (133 pm ).
Каждый углерод двойной связи использует свои три sp гибридные орбитали для образования сигма-связей с тремя атомами (другим углеродом и двумя атомами водорода). Негибридизированные атомные орбитали 2p, которые лежат перпендикулярно плоскости, созданной осями трех гибридных орбиталей sp², объединяются, образуя связь пи. Эта связь лежит вне главной оси C – C, причем половина связи находится на одной стороне молекулы, а половина - на другой. При силе 65 ккал / моль пи-связь значительно слабее сигма-связи.
Вращение вокруг двойной связи углерод-углерод ограничено, потому что это требует энергетических затрат, чтобы нарушить выравнивание p-орбиталей на двух атомах углерода. Как следствие, замещенные алкены могут существовать в виде одного из двух изомеров, называемых цис- или транс-изомерами. Более сложные алкены могут быть названы с помощью обозначения E – Z для молекул с тремя или четырьмя различными заместителями (боковые группы). Например, изомеров бутена две метильные группы (Z) -бут-2 -ена (также известные как цис-2-бутен) появляются на одной стороне двойная связь, а в (E) -бут-2-ене (также известном как транс-2-бутен) метильные группы появляются с противоположных сторон. Эти два изомера бутена обладают разными свойствами.
Скручивание на двугранный угол 90 ° между двумя группами на атомах углерода требует меньше энергии, чем прочность связи пи, и связь все еще сохраняется. Атомы углерода двойной связи становятся пирамидальными, что позволяет сохранить некоторое выравнивание p-орбиты и, следовательно, пи-связь. Две другие присоединенные группы остаются под большим двугранным углом. Это противоречит распространенному в учебниках утверждению, что два атома углерода сохраняют свою планарную природу при скручивании, и в этом случае p-орбитали повернутся достаточно далеко друг от друга, чтобы не поддерживать пи-связь. В алкене, закрученном на 90 °, p-орбитали смещены только на 42 °, а энергия деформации составляет всего около 40 ккал / моль. Напротив, полностью разорванная пи-связь имеет энергетическую стоимость около 65 ккал / моль.
Некоторые пирамидные алкены стабильны. Например, транс- циклооктен представляет собой стабильный деформированный алкен, и смещение орбиты составляет всего 19 °, несмотря на наличие значительного двугранного угла, равного 137 ° (плоская система имеет двугранный угол 180 °) и степень пирамидализации 18 °. Даже транс- циклогептен стабилен при низких температурах.
Как предсказано моделью VSEPR пары электронов отталкивания молекулярная геометрия алкенов включает валентные углы вокруг каждого углерода в двойной связи около 120 °. Угол может изменяться из-за стерической деформации, вносимой несвязанными взаимодействиями между функциональными группами, присоединенными к атомам углерода двойной связи. Например, валентный угол C – C – C в пропилене составляет 123,9 °.
Для мостиковых алкенов, правило Бредта гласит, что двойная связь не может возникнуть на мостиковой кольцевой системе, если кольца не достаточно большие. Следуя Фосетту и определив S как общее количество атомов, не являющихся мостами в кольцах, бициклические системы требуют S ≥ 7 для стабильности, а трициклические системы требуют S ≥ 11.
Многие из По физическим свойствам алкены и алканы схожи: они бесцветны, неполярны и горючие. физическое состояние зависит от молекулярной массы : как и соответствующие насыщенные углеводороды, простейшие алкены (этилен, пропилен и бутен ) представляют собой газы при комнатной температуре. Линейные алкены, содержащие приблизительно от пяти до шестнадцати атомов углерода, являются жидкостями, а высшие алкены - воскообразными твердыми веществами. Температура плавления твердых веществ также увеличивается с увеличением молекулярной массы.
Алкены обычно имеют более сильный запах, чем соответствующие им алканы. У этилена сладкий и затхлый запах. Связывание иона меди с олефином в обонятельном рецепторе млекопитающих MOR244-3 связано с запахом алкенов (а также тиолов). Известно, что напряженные алкены, в частности, такие как норборнен и транс-циклооктен, имеют сильный неприятный запах, что согласуется с более сильными π-комплексами, которые они образуют с ионами металлов, включая медь.
Алкены являются относительно стабильными соединениями, но обладают большей реакционной способностью, чем алканы, либо из-за реакционной способности пи-связи углерод-углерод, либо из-за присутствия аллила CH центры. Большинство реакций алкенов включает присоединения к этой пи-связи с образованием новых одинарных связей. Алкены служат сырьем для нефтехимической промышленности, потому что они могут участвовать в большом количестве реакций, особенно в полимеризации и алкилировании.
Алкены реагируют во многих реакциях присоединения, которые происходят при раскрытии двойной связи. Большинство этих реакций присоединения следуют механизму электрофильного присоединения. Примерами являются гидрогалогенирование, галогенирование, образование галогидрина, оксимеркурация, гидроборирование, добавление дихлоркарбена, реакция Симмонса-Смита, каталитическое гидрирование, эпоксидирование, радикальная полимеризация и гидроксилирование.
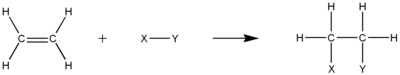
Гидрогенизация алкенов дает соответствующие алканы. Иногда реакцию проводят под давлением и при повышенной температуре. Металлический катализатор требуется почти всегда. Обычные промышленные катализаторы основаны на платине, никеле и палладии. Широкомасштабное применение - производство маржерина.
Помимо добавления H-H через двойную связь, могут быть добавлены многие другие H-X. Эти процессы часто имеют большое коммерческое значение. Одним из примеров является добавление H-SiR 3, то есть гидросилилирование. Эта реакция используется для получения кремнийорганических соединений. Другой реакцией является гидроцианирование, добавление H-CN по двойной связи.
Гидратация, добавление воды по двойной связи алкенов, дает спирты. Реакция катализируется фосфорной кислотой или серной кислотой. Эту реакцию проводят в промышленном масштабе для получения синтетического этанола.
Алкены также могут быть превращены в спирты с помощью реакции оксимеркурации-демеркурации, реакции гидроборирования-окисления или гидратации Мукаямы.
При электрофильном галогенировании добавление элементарного брома или хлора к алкенам дает вицинальный дибром- и дихлоралканы (1,2-дигалогениды или этилен дигалогениды) соответственно. Обесцвечивание раствора брома в воде является аналитическим тестом на присутствие алкенов:
Связанные реакции также используются в качестве количественных показателей ненасыщенности, выражаемой как бромное число и йодное число соединения или смеси.
Гидрогалогенирование - это добавление галогенидов водорода, таких как HCl или HI, к алкенам с получением соответствующие галогеналканы :
Если два атома углерода в двойной связи связаны с другим числом атомов водорода галоген находится преимущественно у углерода с меньшим количеством водородных заместителей. Эта закономерность известна как правило Марковникова. Использование радикальных инициаторов или других соединений может привести к противоположному результату продукта. Бромистоводородная кислота, в частности, склонна к образованию радикалов в присутствии различных примесей или даже атмосферного кислорода, что приводит к обратному результату Марковникова:
Алкены реагируют с водой и галогенами с образованием галогидринов посредством реакции присоединения. Встречаются марковниковская региохимия и антистереохимия.
Алкены реагируют с перкарбоновыми кислотами и даже пероксидом водорода с образованием эпоксидов :
Для этилена эпоксидирование проводят в очень большом промышленном масштабе. В этом коммерческом способе используется кислород в присутствии катализаторов:
Алкены реагируют с озоном, что приводит к разрыву двойной связи. Процесс называется озонолизом. Часто процедура реакции включает мягкий восстановитель, такой как диметилсульфид (SMe 2):
При обработке горячим концентрированный подкисленный раствор KMnO 4, алкены представляют собой расщепленные кетоны и / или карбоновые кислоты. Стехиометрия реакции зависит от условий. Эта реакция и озонолиз могут быть использованы для определения положения двойной связи в неизвестном алкене.
Окисление может быть остановлено на мочи диоле, а не при полном расщеплении алкена с помощью тетроксида осмия или других окислителей:
Эта реакция называется дигидроксилированием.
В присутствии подходящего фотосенсибилизатора, такого как метиленовый синий и свет, алкены могут вступать в реакцию с химически активными формами кислорода, генерируемыми фотосенсибилизатор, такой как гидроксильные радикалы, синглетный кислород или ион супероксида. Реакции возбужденного сенсибилизатора могут включать перенос электрона или водорода, обычно с восстанавливающим субстратом (реакция типа I) или взаимодействие с кислородом (реакция типа II). Этими различными альтернативными процессами и реакциями можно управлять путем выбора конкретных условий реакции, что позволяет получить широкий спектр продуктов. Типичным примером является [4 + 2] - циклоприсоединение синглетного кислорода с диеном, таким как циклопентадиен, с образованием эндопероксида :
![Generation of singlet oxygen and its [4+2]-cycloaddition with cyclopentadiene](http://upload.wikimedia.org/wikipedia/commons/thumb/1/12/4%2B2_cycloaddition_cyclopentadiene_O2.svg/350px-4%2B2_cycloaddition_cyclopentadiene_O2.svg.png)
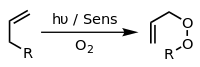
другого Примером является реакция Шенкена, в которой синглетный кислород реагирует с аллильной структурой с образованием транспонированного аллила пероксида :
Полимеризация алкенов. представляет собой реакцию, в результате которой получают полимеры, имеющие высокую промышленную ценность при большой экономии, такие как пластмассы полиэтилен и полипропилен. Полимеры из алкеновых мономеров обычно называются полиолефинами или, в редких случаях, полиалкенами. Полимер из альфа-олефинов называется полиальфаолефином (PAO). Полимеризация может протекать либо по свободному радикальному, либо по ионному механизму, превращая двойную связь в одинарную и образуя одинарные связи для соединения других мономеров. Полимеризация сопряженных диенов, таких как бута-1,3-диен или изопрен (2-метилбута-1,3-диен) приводит в основном к 1,4-присоединению с возможным некоторым 1,2-присоединением диенового мономера к растущей полимерной цепи.
 Структура бис (циклооктадиен) никеля (0), комплекс металл-алкен
Структура бис (циклооктадиен) никеля (0), комплекс металл-алкенАлкены являются лигандами в переходе комплексы алкенов металлов. Два углеродных центра связываются с металлом с помощью пи- и пи * -орбиталей C – C. Моно- и диолефины часто используются в качестве лигандов в стабильных комплексах. Циклооктадиен и норборнадиен являются популярными хелатирующими агентами, и даже сам этилен иногда используется в качестве лиганда, например, в соли Цейса. Кроме того, комплексы металл-алкен являются промежуточными продуктами во многих катализируемых металлами реакциях, включая гидрирование, гидроформилирование и полимеризацию.
| Название реакции | Продукт | Комментарий |
|---|---|---|
| Гидрирование | алканов | добавление водорода |
| алкенов | гидрометаллирование / внедрение / бета-элиминирование металлическим катализатором | |
| Реакция присоединения галогена | 1,2-дигалогенид | электрофильное присоединение галогенов |
| Гидрогалогенирование (Марковников ) | галогеналканы | добавление галогеноводородных кислот |
| антимарковниковское гидрогалогенирование | галогеналканы | свободные радикалы, опосредованные присоединением галогеноводородных кислот |
| гидроаминирование | аминов | присоединение связи N – H через двойную связь C – C |
| гидроформилирование | альдегидов | промышленный процесс, добавление CO и H 2 |
| гидрокарбоксилирование и Реакция Коха | карбоновая кислота | промышленный процесс, добавление CO и H 2 O. |
| Карбоалкоксилирование | сложного эфира | промышленный процесс, добавление CO и спирт. |
| алкилирование | сложный эфир | промышленный процесс: алкеналкила соединение карбоновой кислоты с катализатором кремневольфрамовой кислотой. |
| бисгидроксилирование Шарплесса | диолы | окисление, реагент: четырехокись осмия, хиральный лиганд |
| цис-гидроксилирование Вудворда | диолы | окисление, реагенты: йод, ацетат серебра |
| Озонолиз | альдегиды или кетоны | реагент: озон |
| метатезис олефинов | алкены | два алкена перегруппируются с образованием двух новых алкенов |
| реакция Дильса – Альдера | циклогексены | циклоприсоединение с диеном |
| реакция Паусона – Ханда | циклопентеноны | циклоприсоединение с алкином и CO |
| гидроборирование – окисление | спирты | реагенты: боран, затем пероксид |
| оксимеркурация-восстановление | спирты | электрофильное добавление ацетата ртути, затем восстановление |
| реакция Принса | 1,3-диолы | электрофильное присоединение с альдегидом или кетоном |
| реакция Патерно – Бюхи | оксетаны | фотохимическая реакция с альдегидом или кетоном |
| эпоксидирование | эпоксид | электрофильное присоединение пероксида |
| Циклопропанат ион | циклопропаны | добавление карбенов или карбеноидов |
| гидроацилирование | кетонов | окислительное присоединение / восстановительное элиминирование металлическим катализатором |
| гидрофосфинирование | фосфины |
Алкены получают путем крекинга углеводородов . Сырье - это в основном компоненты конденсата природного газа (в основном этан и пропан) в США и на Ближнем Востоке и нафта в Европе и Азии. Алканы распадаются при высоких температурах, часто в присутствии цеолитного катализатора , с образованием смеси преимущественно алифатических алкенов и алканов с более низкой молекулярной массой. Смесь зависит от сырья и температуры и разделяется фракционной перегонкой. Это в основном используется для производства небольших алкенов (до шести атомов углерода).
С этим связано каталитическое дегидрирование, при котором алкан теряет водород при высоких температурах с образованием соответствующего алкена. Это противоположно каталитическому гидрированию алкенов.

Этот процесс также известен как преобразование. Оба процесса являются эндотермическими и направляются к алкену при высоких температурах за счет энтропии.
Каталитический синтез высших α-алкенов (типа RCH = CH 2) также может быть достигнут взаимодействием этилена с металлоорганическим соединением триэтилалюминий в присутствии никеля, кобальта или платины.
Один из основных методов синтеза алкенов в лаборатории - это комнатное удаление алкилгалогенидов, спиртов и подобных соединений. Наиболее распространенным является β-устранение по механизму E2 или E1, но известны также α-исключения.
Механизм E2 обеспечивает более надежный метод β-элиминирования, чем E1, для большинства синтезов алкенов. Большинство случаев удаления E2 начинается с алкилгалогенида или сложного эфира алкилсульфоновой кислоты (такого как тозилат или трифлат ). Когда используют алкилгалогенид, реакция называется дегидрогалогенированием. Для несимметричных продуктов, как правило, преобладают более замещенные алкены (с меньшим количеством атомов водорода, присоединенными к C = C) (см. правило Зайцева ). Двумя распространенными методами реакций элиминирования являются дегидрогалогенирование алкилгалогенидов и дегидратация спиртов. Типичный пример показан ниже; обратите внимание, что если возможно, H является анти-уходящей группой, даже если это приводит к менее стабильному Z-изомеру.
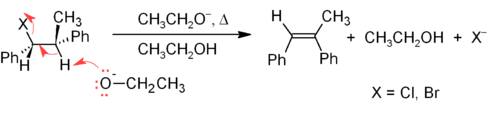
Алкены могут быть синтезированы из спиртов посредством дегидратации, в этом случае теряется вода. через механизм E1. Например, при дегидратации этанола получается этилен:
Спирт также может быть преобразован в лучшую уходящую группу (например, ксантат ), чтобы обеспечить более мягкое син-устранение, такое как устранение Чугаева и удаление Грико. Связанные реакции включают отщепление β-галогенэфирами (синтез олефинов Бора ) и сложными эфирами (пиролиз сложного эфира ).
Алкены могут быть получены косвенно из алкил аминов. Амин или аммиак не являются подходящей уходящей группой, поэтому амин сначала либо алкилируют (как в элиминировании Хофмана ), либо окисляют до оксида амина ( реакция Копа ), чтобы обеспечить плавное удаление. Реакция Коупа представляет собой син-элиминирование, которое происходит при 150 ° C или ниже, например:

Элиминирование Хофмана необычно тем, что менее замещенный (не Сайцефф ) алкен обычно является основным продуктом..
Алкены образуются из α-галоген сульфонов в реакции Рамберга – Бэклунда через трехчленное кольцевое промежуточное соединение сульфона.
Другой важный метод синтеза алкена включает создание новой двойной углерод-углеродной связи путем сочетания карбонильного соединения (такого как альдегид или кетон ) до эквивалента карбаниона. Такие реакции иногда называют олефинациями. Наиболее известным из этих методов является реакция Виттига, но известны и другие родственные методы, в том числе реакция Хорнера – Уодсворта – Эммонса.
Реакция Виттига включает реакцию альдегида или кетона. с реагентом Виттига (или фосфораном) типа Ph 3 P = CHR для получения алкена и Ph3P = O. Реагент Виттига легко получить из трифенилфосфина и алкилгалогенида. Реакция является довольно общей, и допускаются многие функциональные группы, даже сложные эфиры, как в этом примере:

Связано с реакцией Виттига олефинирование Петерсона, в котором вместо фосфорана используются реагенты на основе кремния.. Эта реакция позволяет выбрать E- или Z-продукты. Если желателен Е-продукт, другой альтернативой является олефинирование Джулиа, в котором используется карбанион, образованный из фенил сульфона. Олефинирование Такаи на основе хроморганического промежуточного соединения также обеспечивает получение Е-продуктов. Соединение титана, реагент Теббе, полезно для синтеза метиленовых соединений; в этом случае вступают в реакцию даже сложные эфиры и амиды.
Пара кетонов или альдегидов может быть деоксигенирована с образованием алкена. Симметричные алкены могут быть получены путем сочетания одного альдегида или кетона с самим собой, используя восстановление металла титан (реакция МакМурри ). Если необходимо связать разные кетоны, требуется более сложный метод, такой как реакция Бартона – Келлогга.
Отдельный кетон также может быть преобразован в соответствующий алкен через его тозилгидразон, используя метоксид натрия (реакция Бэмфорда – Стивенса ) или алкиллитий (реакция Шапиро ).
Рений- и молибденсодержащий гетерогенный катализ используются в этом процессе, который коммерчески используется для взаимного превращения этилена и 2-бутен в пропилен:
Катализируемое переходным металлом гидровинилирование - еще один важный процесс синтеза алкена, начинающийся с самого алкена. Он включает присоединение водорода и винильной группы (или алкенильной группы) через двойную связь.
Восстановление алкинов является полезным методом стереоселективного синтеза двузамещенных алкенов. Если требуется цис-алкен, обычно используется гидрирование в присутствии катализатора Линдлара (гетерогенный катализатор, состоящий из палладия, нанесенного на карбонат кальция и обработанного различными формами свинца)., хотя гидроборирование с последующим гидролизом обеспечивает альтернативный подход. Восстановление алкина металлическим натрием в жидком аммиаке дает транс-алкен.
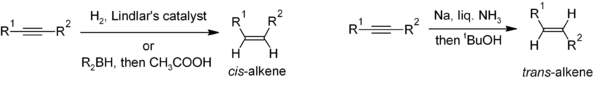
Для получения мультизамещенных алкенов карбометаллирование алкинов может привести к большое разнообразие производных алкена.
Алкены могут быть синтезированы из других алкенов с помощью реакций перегруппировки. Помимо метатезиса олефинов (описанного выше), можно использовать многие перициклические реакции, такие как еновая реакция и перегруппировка Коупа..
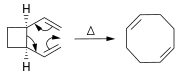
В реакции Дильса-Альдера производное циклогексена получают из диена и реакционноспособного или электронодефицитного алкена.
Хотя номенклатура широко не соблюдается, согласно ИЮПАК, алкен представляет собой ациклический углеводород только с одной двойной связью между атомами углерода. Олефины включают в себя более крупный набор циклических и ациклических алкенов, а также диенов и полиенов.
Чтобы сформировать корень названий IUPAC для алкенов с прямой цепью, измените инфикс -ан- родитель -en-. Например, CH3-CH 3- это алкан этАН. Таким образом, имя CH2= CH 2- ethENe.
Для алкенов с прямой цепью с 4 или более атомами углерода это название не полностью идентифицирует соединение. Для этих случаев и для разветвленных ациклических алкенов применяются следующие правила:
Положение двойного bond часто вставляется перед названием цепочки (например, «2-пентен», а не перед суффиксом («пент-2-ен»).
Позиции указывать не обязательно, если они уникальны. Обратите внимание, что двойная связь может означать другую нумерацию цепей, чем та, которая используется для соответствующего алкана: (H. 3C). 3C – CH. 2–CH. 3означает «2,2-диметилпентан», тогда как (H. 3C). 3C – CH = CH. 2представляет собой «3,3-диметил-1-пентен».
Более сложный r Улы применяются для полиенов и циклоалкенов.
 Обозначение замещенных гекс-1-енов
Обозначение замещенных гекс-1-енов Если двойная связь ациклического моноена не является первой связью в цепи, название, построенное выше, все еще не полностью идентифицирует соединение из-за цис-транс-изомерии. Затем необходимо указать, находятся ли две одинарные связи C – C, смежные с двойной связью, на одной стороне ее плоскости или на противоположных сторонах. Для моноалкенов конфигурация часто обозначается префиксом цис- (от латинского «на этой стороне»]] или транс- («поперек», «на другой стороне») перед названием, соответственно; как в цис-2-пентене или транс-2-бутене.
 Разница между цис- и транс-изомерами
Разница между цис- и транс-изомерами В более общем смысле, цис-транс-изомерия будет существовать, если каждый из двух атомов углерода в двойном Связь имеет два разных атома или группы, прикрепленные к ней. Учитывая эти случаи, IUPAC рекомендует более общую нотацию EZ вместо цис- и транс-префиксов. Эта нотация учитывает группу с наивысшим CIP приоритет в каждом из двух атомов углерода. Если эти две группы находятся на противоположных сторонах плоскости двойной связи, конфигурация помечается буквой E (от немецкого entgegen, означающего «противоположный»); если они с той же стороны он помечен Z (от немецкого zusammen, «вместе»). Этому обозначению можно обучить мнемоникой «Z означает 'on ze zame zide'».
 Разница между E и Z изомеры
Разница между E и Z изомеры IUPAC распознает два названия углеводородных групп, содержащих двойные связи углерод-углерод: винильная группа и аллильная группа.

| Найдите алкен в Викисловаре, бесплатном словаре. |
| Викицитатник содержит цитаты, относящиеся к: Алкен |
.