Ароматические соединения - это те химические соединения (чаще всего органические ), которые содержат одно или несколько колец с пи-электронами делокализованы вокруг них. В отличие от соединений, которые проявляют ароматичность, алифатические соединения лишены этой делокализации. Термин «ароматический» был присвоен до открытия физического механизма, определяющего ароматичность, и относился просто к тому факту, что многие такие соединения имеют сладкий или приятный запах; однако не все ароматические соединения имеют сладкий запах, и не все соединения со сладким запахом являются ароматическими. Ароматические углеводороды или арены - это ароматические органические соединения, содержащие только атомы углерода и водорода. Конфигурация шести атомов углерода в ароматических соединениях называется «бензольным кольцом» после простого ароматического соединения бензол или фенильной группой, когда она является частью более крупного соединения.
Не все ароматические соединения имеют бензольную основу; ароматичность может также проявляться в гетероаренах, которые следуют правилу Хюккеля (для моноциклических колец: когда число его π-электронов равно 4n + 2, где n = 0, 1, 2, 3,...). В этих соединениях по меньшей мере один атом углерода заменен одним из гетероатомов кислорода, азота или серы. Примерами небензольных соединений с ароматическими свойствами являются фуран, гетероциклическое соединение с пятичленным кольцом, которое включает один атом кислорода, и пиридин, гетероциклическое соединение с шестичленным - членное кольцо, содержащее один атом азота.
 Бензол
Бензол Бензол, C 6H6, является наименее сложным ароматическим углеводородом, и он был первым, названным так. Природу его связи впервые осознал Август Кекуле в 19 веке. Каждый атом углерода в гексагональном цикле имеет четыре общих электрона. Один идет к атому водорода, и по одному к каждому из двух соседних атомов углерода. Это оставляет один электрон делиться с одним из двух соседних атомов углерода, таким образом создавая двойную связь с одним углеродом и оставляя одинарную связь с другим, поэтому некоторые представления молекулы бензола изображают ее в виде шестиугольника с чередующимися одинарными и двойные связи.
Другие изображения структуры изображают шестиугольник с кругом внутри, чтобы указать, что шесть электронов плавают по делокализованным молекулярным орбиталям размером с само кольцо. Это представляет собой эквивалентную природу шести углерод-углеродных связей всего порядка связи 1,5; эквивалентность объясняется резонансными формами. Электроны визуализируются плавающими над и под кольцом, а генерируемые ими электромагнитные поля действуют, чтобы кольцо оставалось плоским.
Общие свойства ароматических углеводородов:
Символ круга для обозначения ароматичности был введен сэром Робертом Робинсоном и его учеником Джеймс Армит в 1925 году и популяризировал, начиная с 1959 года, учебником Моррисона и Бойда по органической химии. Правильное использование символа обсуждается: в некоторых публикациях он используется для любой циклической π-системы, в то время как другие используют его только для тех π-систем, которые подчиняются правилу Хюккеля. Дженсен утверждает, что в соответствии с первоначальным предложением Робинсона использование символа круга должно быть ограничено моноциклическими 6 π-электронными системами. Таким образом, символ круга для шестицентровой шестиэлектронной связи можно сравнить с символом Y для трехцентровой двухэлектронной связи.
Реакция, которая формирует ареновое соединение из ненасыщенного или частично ненасыщенного циклического предшественника называется просто ароматизацией. Существует множество лабораторных методов органического синтеза аренов из предшественников, не являющихся аренами. Многие методы основаны на реакциях циклоприсоединения. Тримеризация алкинов описывает [2 + 2 + 2] циклизацию трех алкинов, в реакции Дёца реагентами являются алкин, монооксид углерода и комплекс карбена хрома. Реакции Дильса – Альдера алкинов с пироном или циклопентадиеноном с выделением двуокиси углерода или окиси углерода также образуются ареновые соединения. В циклизации Бергмана реагентами являются енин плюс донор водорода.
Другой набор методов - это ароматизация циклогексанов и других алифатических колец: реагенты - это катализаторы, используемые в гидрировании, такие как платина, палладий и никель (обратное гидрирование), хиноны и элементы сера и селен.
Ароматические кольцевые системы участвуют во многих органических реакциях.
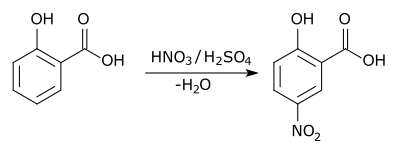
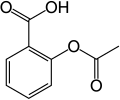
При ароматическом замещении один заместитель в ареновом кольце, обычно водород, заменяется другим заместителем. Двумя основными типами являются электрофильное ароматическое замещение, когда активный реагент является электрофилом, и нуклеофильное ароматическое замещение, когда реагент является нуклеофилом. В радикально-нуклеофильном ароматическом замещении активный реагент представляет собой радикал. Примером электрофильного ароматического замещения является нитрование салициловой кислоты :
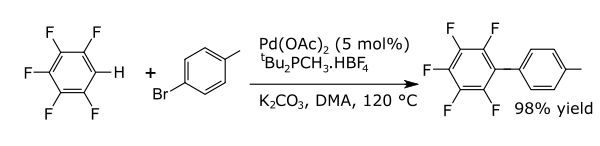
В реакциях связывания металл катализирует связывание между двумя формальными радикальными фрагментами. Обычные реакции сочетания с аренами приводят к образованию новых углерод-углеродных связей, например, алкиларенов, виниларенов, бирарилов, новых углерод-азотных связей (анилины) или нового углерода. –Кислородные связи (арилоксисоединения). Примером является прямое арилирование перфторбензолов
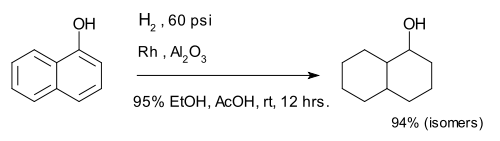
Гидрирование аренов с образованием насыщенных колец. Соединение 1-нафтол полностью восстанавливается до смеси декалин -ол изомеров.
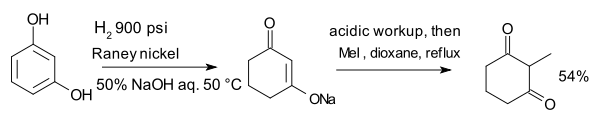
Соединение резорцин, гидрированное с помощью Ренея. никель в присутствии водного гидроксида натрия образует енолят, который алкилируется метилиодидом до 2-метил-1,3-циклогександиона:
Реакции циклоприсоединения встречаются нечасто. Необычная термическая реакционная способность аренов Дильса – Альдера может быть обнаружена в реакции Вагнера-Яурегга. Другие реакции фотохимического циклоприсоединения с алкенами протекают через эксимеры.
В реакциях деароматизации ароматичность реагента навсегда теряется.
Производные бензола имеют от одного до шести заместителей, присоединенных к центральному бензольному ядру. Примерами бензольных соединений только с одним заместителем являются фенол, который несет гидроксильную группу, и толуол с метильной группой. Когда в кольце присутствует более одного заместителя, их пространственное соотношение становится важным, для чего разрабатываются схемы замещения арена орто, мета и пара. Например, для крезола существует три изомера, потому что метильная группа и гидроксильная группа могут быть расположены рядом друг с другом (орто), одно положение удалено друг от друга (мета) или две позиции удалены друг от друга (п.). Ксиленол имеет две метильные группы в дополнение к гидроксильной группе, и для этой структуры существует 6 изомеров.







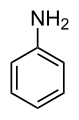




Ареновое кольцо обладает способностью стабилизировать заряды. Это видно, например, в феноле (C 6H5–OH), который является кислым у гидроксила (OH), поскольку заряд этого кислорода (алкоксид -O) частично делокализован в бензольное кольцо.
Другой моноциклический ароматический углеводород включает Циклотетрадекагептаен или Циклооктадеканонаен.
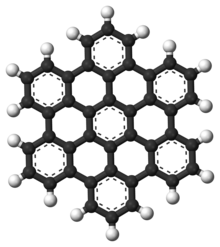 Гексабензокоронен <46c>большой поли ароматический углеводород.
Гексабензокоронен <46c>большой поли ароматический углеводород. Полициклические ароматические углеводороды (ПАУ) - это ароматические углеводороды, которые состоят из конденсированных ароматических колец и не содержат гетероатомов или не содержат заместители. Нафталин представляет собой простейший пример ПАУ. ПАУ встречаются в месторождениях нефти, угля и смолы и образуются как побочные продукты сгорания топлива (будь то ископаемое топливо или биомасса). Как загрязнители, они вызывают озабоченность, поскольку некоторые соединения определены как канцерогенные, мутагенные и тератогенные. ПАУ также содержатся в приготовленной пище. Исследования показали, что высокие уровни ПАУ обнаруживаются, например, в мясе, приготовленном при высоких температурах, таких как жарка на гриле или барбекю, и в копченой рыбе.
Они также обнаруживаются в межзвездной среде, в кометах и в метеоритах и являются молекулой-кандидатом на роль основы для самых ранних форм жизни. В графене мотив PAH расширен на большие 2D-листы.