 Гидрирование этена на твердой каталитической поверхности (1) Адсорбция (2) Реакция (3) Десорбция
Гидрирование этена на твердой каталитической поверхности (1) Адсорбция (2) Реакция (3) Десорбция В химии гетерогенный катализ - это катализ, где фаза катализаторов отличается от фазы реагентов или продукты. В отличие от гомогенного катализа, где реагенты, продукты и катализатор находятся в одной фазе. Фаза различает не только твердые, жидкие и газовые компоненты, но также и несмешивающиеся смеси (например, нефть и вода ) или в любом месте, где присутствует интерфейс. Катализаторы полезны, потому что они увеличивают скорость реакции, не расходясь сами по себе, и поэтому их можно использовать повторно.
Гетерогенный катализ обычно включает твердофазные катализаторы и газофазные реагенты. В этом случае на поверхности катализатора происходит цикл молекулярной адсорбции, реакции и десорбции. Термодинамика, массоперенос и теплопередача влияют на скорость (кинетику) реакции.
Гетерогенный катализ очень важен, поскольку он обеспечивает более быстрое крупномасштабное производство и селективное образование продукта. Примерно 35% мирового ВВП находится под влиянием катализа. Производство 90% химикатов (по объему) обеспечивается твердыми катализаторами. Химическая и энергетическая промышленность в значительной степени полагаются на гетерогенный катализ. Например, в процессе Хабера-Боша используются катализаторы на основе металлов в синтезе аммиака, важного компонента удобрений; В 2016 году было произведено 144 миллиона тонн аммиака.
Адсорбция - важный этап гетерогенного катализа. Адсорбция - это процесс, при котором молекула в газовой (или растворной) фазе (адсорбат) связывается с твердыми (или жидкими) поверхностными атомами (адсорбентом). Обратной стороной адсорбции является десорбция, отделение адсорбата от адсорбента. В реакции, которой способствует гетерогенный катализ, катализатор является адсорбентом, а реагенты - адсорбатом.
Различают два типа адсорбции: физисорбция, слабосвязанная адсорбция и хемосорбция, прочносвязанная адсорбция. Многие процессы гетерогенного катализа находятся между двумя крайностями. Модель Леннарда-Джонса обеспечивает базовую основу для предсказания молекулярных взаимодействий как функции разделения атомов.
При физической сорбции молекула притягивается к поверхностным атомам через силы Ван дер Ваальса. К ним относятся диполь-дипольные взаимодействия, индуцированные дипольные взаимодействия и дисперсионные силы Лондона. Обратите внимание, что между адсорбатом и адсорбентом не образуются химические связи, и их электронные состояния остаются относительно неизменными. Типичные энергии для физической адсорбции составляют от 3 до 10 ккал / моль. В гетерогенном катализе, когда молекула реагента физадсорбируется на катализаторе, обычно говорят, что она находится в состоянии предшественника, промежуточном энергетическом состоянии перед хемосорбцией, при более прочно связанной адсорбции. Из состояния-предшественника молекула может подвергаться хемосорбции, десорбции или миграции по поверхности. Природа состояния предшественника может влиять на кинетику реакции.
Когда молекула приближается достаточно близко к поверхностным атомам, так что их электронные облака перекрываются, может происходить хемосорбция. При хемосорбции адсорбат и адсорбент разделяют электроны, что означает образование химических связей. Типичные энергии хемосорбции находятся в диапазоне от 20 до 100 ккал / моль. Два случая хемосорбции:
 Координата реакции. (A) Некатализируемые (B) Катализированные (C) Катализируемые дискретными промежуточными продуктами (переходные состояния)
Координата реакции. (A) Некатализируемые (B) Катализированные (C) Катализируемые дискретными промежуточными продуктами (переходные состояния) Большинство реакций на поверхности металлов протекает путем распространения цепи, при котором каталитические промежуточные продукты циклически образуются и расходуются. Два основных механизма поверхностных реакций можно описать для A + B → C.
Наиболее гетерогенно катализируемые реакции описываются моделью Ленгмюра-Хиншелвуда.
При гетерогенном катализе реагенты диффундируют из основной жидкой фазы к адсорбции на поверхности катализатора. Сайт адсорбции не всегда является активным сайтом катализатора, поэтому молекулы реагента должны мигрировать по поверхности к активному центру. В активном центре молекулы реагента будут реагировать с образованием молекулы (-ов) продукта, следуя более энергетически легкому пути через каталитические промежуточные соединения (см. Рисунок справа). Затем молекулы продукта десорбируются с поверхности и диффундируют. Сам катализатор остается нетронутым и свободен для проведения дальнейших реакций. Явления переноса, такие как тепломассоперенос, также играют роль в наблюдаемой скорости реакции.
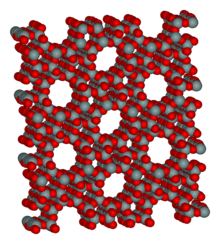 Структура цеолита. Обычный материал носителя катализатора в гидрокрекинге. Также действует как катализатор при алкилировании и изомеризации углеводородов.
Структура цеолита. Обычный материал носителя катализатора в гидрокрекинге. Также действует как катализатор при алкилировании и изомеризации углеводородов. Катализаторы не активны по отношению к реагентам по всей своей поверхности; только определенные участки обладают каталитической активностью, называемые активными центрами. Площадь поверхности твердого катализатора сильно влияет на количество доступных активных центров. В промышленной практике твердые катализаторы часто бывают пористыми для увеличения площади поверхности, обычно достигающей 50–400 м / г. Некоторые мезопористые силикаты, такие как MCM-41, имеют площадь поверхности более 1000 м 2 / г. Пористые материалы экономически эффективны из-за их высокого отношения площади поверхности к массе и повышенной каталитической активности.
Во многих случаях твердый катализатор диспергируют на материале носителя для увеличения площади поверхности (увеличения числа активных центров) и обеспечения стабильности. Обычно носители катализатора представляют собой инертные материалы с высокой температурой плавления, но они также могут сами быть каталитическими. Большинство носителей катализаторов являются пористыми (часто на основе углерода, диоксида кремния, цеолита или оксида алюминия) и выбираются из-за их высокого отношения площади поверхности к массе. Для данной реакции необходимо выбирать пористые носители, чтобы реагенты и продукты могли входить в материал и выходить из него.
Часто вещества намеренно добавляют к исходному сырью реакции или к катализатору, чтобы повлиять на каталитическую активность, селективность и / или стабильность. Эти соединения называются промоторами. Например, оксид алюминия (Al 2O3) добавляется во время синтеза аммиака для обеспечения большей стабильности за счет замедления процессов спекания на Fe-катализаторе.
Принцип Сабатье можно рассматривать как один из краеугольных камней современной теории катализа.. Принцип Сабатье гласит, что взаимодействие между поверхностью и адсорбатами должно быть оптимальным: не слишком слабым, чтобы быть инертным по отношению к реагентам, и не слишком сильным, чтобы отравить поверхность и избежать десорбции продуктов. Утверждение о том, что взаимодействие поверхности с адсорбатом должно быть оптимальным, носит качественный характер. Обычно количество адсорбатов и переходных состояний, связанных с химической реакцией, велико, поэтому оптимальный должен быть найден в многомерном пространстве. Разработка катализатора в таком многомерном пространстве не является вычислительно жизнеспособной задачей. Кроме того, такой процесс оптимизации был бы далеко не интуитивно понятным. Соотношения масштабирования используются для уменьшения размерности пространства конструкции катализатора. Такие отношения представляют собой корреляции между энергиями связи адсорбатов (или между энергиями связи адсорбатов и переходными состояниями, также известными как отношения ВОБ ), которые «достаточно похожи», например масштабирование ОН по сравнению с ООН. Применение масштабных соотношений к задачам конструкции катализатора значительно снижает размерность пространства (иногда до 1 или 2). Можно также использовать микрокинетическое моделирование, основанное на таких масштабных соотношениях, чтобы учесть кинетику, связанную с адсорбцией, реакцией и десорбцией молекул при определенных условиях давления или температуры. Такое моделирование затем приводит к хорошо известным вулканическим сюжетам, на которых оптимум, качественно описанный принципом Сабатье, называется «вершиной вулкана». Масштабные соотношения могут использоваться не только для связи энергетики радикальных поверхностно-адсорбированных групп (например, O *, OH *), но также для связи энергий молекул с закрытой оболочкой между собой или с аналогичными адсорбатами радикалов. В последнее время перед исследователями каталитических наук стоит задача «разорвать» отношения масштабирования. Корреляции, которые проявляются в соотношениях масштабирования, ограничивают пространство конструкции катализатора, не позволяя достичь «вершины вулкана». Нарушение отношений масштабирования может относиться либо к проектированию поверхностей или мотивов, которые не следуют соотношению масштабирования, либо к тем, которые следуют другому соотношению масштабирования (чем обычное соотношение для связанных адсорбатов) в правильном направлении: такое, которое может приблизить нас к вершина вулкана реактивности. Помимо изучения каталитической реакционной способности, масштабные соотношения могут использоваться для изучения и отбора материалов на селективность по отношению к конкретному продукту. Существуют особые комбинации энергий связывания, которые отдают предпочтение определенным продуктам по сравнению с другими. Иногда набор энергий связывания, которые могут изменить селективность по отношению к конкретному продукту, «масштабируется» друг с другом, таким образом, чтобы улучшить селективность, необходимо нарушить некоторые соотношения масштабирования; Примером этого является масштабирование между энергиями окислительной активации метана и метанола, что приводит к недостаточной селективности при прямом превращении метана в метанол.
Деактивация катализатора определяется как потеря в каталитической активности и / или селективности с течением времени.
Вещества, снижающие скорость реакции, называются ядами . Яды хемосорбируются на поверхности катализатора и уменьшают количество доступных активных центров для связывания молекул реагента. Обычные яды включают элементы групп V, VI и VII (например, S, O, P, Cl), некоторые токсичные металлы (например, As, Pb) и адсорбирующие вещества с множественными связями (например, CO, ненасыщенные углеводороды). Например, сера нарушает производство метанола, отравляя катализатор Cu / ZnO. Вещества, увеличивающие скорость реакции, называются промоторами . Например, присутствие щелочных металлов в синтезе аммиака увеличивает скорость диссоциации N 2.
Присутствие ядов и промоторов может изменить энергию активации стадии ограничения скорости и повлиять на селективность катализатора к образованию определенных продуктов. В зависимости от количества вещество может быть благоприятным или неблагоприятным для химического процесса. Например, при производстве этилена небольшое количество хемосорбированного хлора будет действовать как промотор, улучшая селективность Ag-катализатора по отношению к этилену по сравнению с CO 2, в то время как слишком много хлора будет действовать как яд.
Другие механизмы дезактивации катализатора включают:
В промышленности дезактивация катализатора обходится в миллиарды долларов каждый год из-за остановки процесса и замены катализатора.
В промышленности многие конструктивные параметры должны рассматриваться, включая конструкцию реактора. Обычные реакторы для гетерогенного катализа включают периодические, непрерывные и реакторы с псевдоожиженным слоем, в то время как более современные установки включают неподвижный слой, микроканальные и многофункциональные реакторы. Другими переменными, которые следует учитывать, являются размеры реактора, площадь поверхности, тип катализатора, носитель катализатора, а также рабочие условия реактора, такие как температура, давление и концентрации реагентов.
Некоторые крупномасштабные промышленные процессы, включающие гетерогенные катализаторы, перечислены ниже.
| Процесс | Реагенты, продукты (несбалансированные) | Катализатор | Комментарий |
|---|---|---|---|
| Синтез серной кислоты (Контактный процесс ) | SO2+ O 2, SO 3 | оксиды ванадия | Гидратация SO 3 дает H 2SO4 |
| Синтез аммиака (процесс Габера-Боша ) | N2+ H 2, NH 3 | оксиды железа на оксиде алюминия (Al 2O3) | потребляет 1% мировой энергетический бюджет |
| Синтез азотной кислоты (процесс Оствальда ) | NH3+ O 2, HNO 3 | Pt-Rh марля без подложки | Прямые маршруты из N 2 неэкономичны |
| Производство водорода с помощью парового риформинга | CH4+ H 2 O, H 2 + CO 2 | Никель или K 2O | Более экологичные пути к H 2 путем расщепления воды активно ищутся |
| синтез оксида этилена | C2H4+ O 2, C 2H4O | серебро на оксиде алюминия со многими промоторами | Плохо применимо к другим алкенам |
| Hydrog en цианидный синтез (окисление Андруссова ) | NH3+ O 2 + CH 4, HCN | Pt-Rh | Связанные процесс аммоксидирования превращает углеводороды в нитрилы |
| полимеризация олефинов полимеризация Циглера-Натта | пропилен, полипропилен | TiCl 3 на MgCl 2 | Существует множество вариантов, включая некоторые гомогенные примеры |
| Обессеривание нефти (гидродесульфуризация ) | H2+ R 2 S (идеализированная сероорганическая примесь), RH + H 2S | Mo -Co на оксид алюминия | Производит углеводороды с низким содержанием серы, сера извлекается с помощью процесса Клауса |
 Блок-схема процесса, иллюстрирующая использование катализа в синтезе аммиака (NH 3)
Блок-схема процесса, иллюстрирующая использование катализа в синтезе аммиака (NH 3)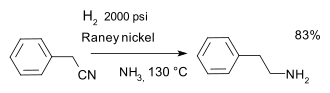 Гидрирование нитрила
Гидрирование нитрилаХотя большинство гетерогенных катализаторов являются твердыми, есть несколько вариантов, имеющих практическое значение. В случае двух несмешивающихся растворов (жидкостей) один несет катализатор, а другой - реагент. Эта установка является основой двухфазного катализа, применяемого при промышленном производстве бутиральдегида гидроформилированием пропилена.
| Реагирующие фазы | Приведенные примеры | Комментарий |
|---|---|---|
| твердое вещество + раствор | гидрирование жирных кислот с никелем | , используемым для производства маргарина |
| несмешивающихся жидких фаз | гидроформилирования катализатора в водной фазе пропена | ; реагенты и продукты в основном в неводной фазе |