A реакция присоединения галогена - это простая органическая реакция, в которой молекула галогена добавляется к двойная связь углерод-углерод функциональной группы алкен .
Общая химическая формула реакции присоединения галогена:
(X представляет галогены бром или хлор, и в этом случае растворителем может быть CH2Cl2 или CCl 4 ). Продукт представляет собой вицинальный дигалогенид.
Этот тип реакции представляет собой галогенирование и электрофильное присоединение.
Механизм реакции бромирования алкена можно описать следующим образом. На первой стадии реакции молекула брома приближается к богатой электронами алкену двойной связи углерод-углерод. Атом брома, расположенный ближе к связи, приобретает частичный положительный заряд, поскольку его электроны отталкиваются электронами двойной связи.
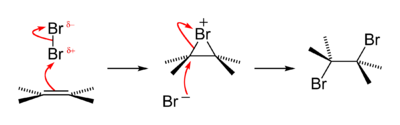 |  |
| Присоединение брома к механизму реакции алкена | Ион бромида атакует антисвязывающую молекулярную орбиталь C – Br σ * иона бромония |
В это время атом электрофильный и атакованы пи-электронами алкена [углерод-углеродная двойная связь]. Он на мгновение образует одинарную сигма-связь с обоими задействованными атомами углерода. Связывание брома в этом промежуточном продукте является особенным, из-за его относительно большого размера по сравнению с углеродом ион бромида способен взаимодействовать с обоими атомами углерода, которые однажды разделяет π-связь, образуя трехчленное кольцо. Бромид-ион приобретает положительный формальный заряд. В этот момент ион галогена называется «ионом бромония » или «ионом хлорония соответственно.
Когда первый атом брома атакует π-связь углерод-углерод , он оставляет после себя один из своих электронов с другим бромом, с которым он был связан в Br 2. Этот другой атом теперь является отрицательным анионом бромида и притягивается небольшим положительным зарядом на атомах углерода. Он блокируется от нуклеофильной атаки на одной стороне углеродной цепи первым атомом брома и может атаковать только с другой стороны. Когда он атакует и образует связь с одним из атомов углерода, связь между первым атомом брома и другими атомами углерода разрывается, оставляя каждый атом углерода с галогеновым заместителем.
Таким образом, два галогена складываются в режиме анти-присоединения, и когда алкен является частью цикла, дибромид принимает транс-конфигурацию. Для максимального перекрытия молекулярной орбитали C – Br σ * , разрывающей связь (НСМО, показано справа красным) и неподеленной пары нуклеофила (X) (HOMO, показан справа внизу зеленым), X должен атаковать ион бромония сзади, на углероде.
Этот механизм реакции был предложен Робертсом и Кимбаллом в 1937 году. Этим они объяснили наблюдаемые стереоспецифические транс-добавления при бромировании малеиновой кислоты и фумаровой кислоты. Малеиновая кислота с цис-двойной связью образует дибромид в виде смеси энантиомеров :
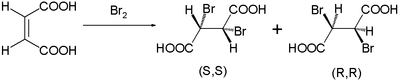
, в то время как транс-изомер фумаровая кислота образует одно мезосоединение :

Реакция даже стереоспецифична в алкенах с двумя объемными трет-бутил группы в цис-положении, как в соединении цис-ди-трет-бутилэтилен. Несмотря на стерическое отталкивание, присутствующее в ионе хлорония, единственный образующийся продукт - это антиаддукт.
В альтернативной схеме реакции, изображенной ниже, реакционноспособный промежуточный продукт представляет собой β-бромокарбокатион или β-бромокарбониевый ион с одним из атомов углерода подлинным карбокатион.

Для реакций, протекающих по этому механизму, стереоспецифичность не ожидается и действительно не обнаруживается.
Робертс и Кимбалл в 1937 году уже учли тот факт, что бромирование с ионом малеат приводило к цис-присоединению, вызванному отталкиванием между отрицательно заряженными анионами карбоновой кислоты, более сильным, чем образование иона галония. В алкенах, таких как анетолы и стильбены, заместители способны стабилизировать карбокатион, отдавая электроны за счет иона галония.
Ионы галония можно идентифицировать по средствами ЯМР-спектроскопии. В 1967 году группа Джорджа А. Ола получила ЯМР-спектры ионов тетраметилэтиленбромония путем растворения 2,3-дибром-2,3-диметилбутана в магической кислоте при -60 ° C. С другой стороны, спектр соответствующего соединения фтора согласовывался с быстро уравновешивающейся парой β-фторкарбокатионов.