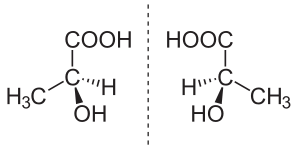 (S) - (+) - молочная кислота (слева) и (R) - (-) - молочная кислота (справа) являются несуществующими зеркальными отображениями друг друга.
(S) - (+) - молочная кислота (слева) и (R) - (-) - молочная кислота (справа) являются несуществующими зеркальными отображениями друг друга. В химии, энантиомер (; от греч. ἐνάντιος (enántios) «противоположный» и μέρος (méros) «часть») (также называемый оптическим изомером, антиподом или оптическим антиподом) является одним из двух стереоизомеров, которые являются зеркальными изображениями. друг друга, которые не могут быть совмещены (не идентичны), так же как левая и правая руки являются зеркальными отображениями друг друга, которые не могут казаться идентичными просто путем переориентации. Одиночный хиральный атом или аналогичный структурный элемент в соединении приводит к тому, что это соединение имеет две возможные структуры, которые не могут быть совмещены, каждая из которых является зеркальным отображением другой. Каждый член пары называется энантиоморфом (энантио = противоположность; морф = форма); структурное свойство называется энантиомерией. Наличие нескольких хиральных элементов в данном соединении увеличивает количество возможных геометрических форм, хотя все еще могут быть пары идеального зеркального отображения.
Образец химического вещества считается энантиочистым (также называемым энантиомерно чистым), если он имеет в пределах обнаружения молекулы только одной хиральности.
При наличии в симметричной среде энантиомеры имеют идентичные химические и физические свойства, за исключением их способности вращать плоскость - поляризованный свет (+/-) на равные количества, но в противоположных направлениях (хотя поляризованный свет можно рассматривать как асимметричную среду). Таким образом, такие соединения описываются как оптически активные со специальными терминами для каждого энантиомера в зависимости от направления: правовращающее соединение вращает свет по часовой стрелке (+), тогда как левовращающее соединение вращает свет против часовой стрелки (-). Смесь равного количества обоих энантиомеров называется рацемической смесью или рацематом. В рацемической смеси количеству положительного вращения точно противодействует равное количество отрицательного вращения, поэтому чистое вращение равно нулю (смесь не является оптически активной). Для всех намерений и целей пары энантиомеров имеют одинаковую свободную энергию Гиббса. Однако теоретическая физика предсказывает, что из-за нарушения четности слабой ядерной силы (единственной силы в природе, которая может «отличать левое от правого»), на самом деле существует небольшая разница в энергия между энантиомерами (порядка 10 эВ или 10 кДж / моль или меньше) из-за механизма слабого нейтрального тока. Эта разница в энергии намного меньше, чем изменения энергии, вызванные даже тривиальным изменением молекулярной конформации, и слишком мала, чтобы ее можно было измерить с помощью современных технологий, и поэтому химически несущественна.
Члены энантиомера часто вступают в различные химические реакции с другими энантиомерные вещества. Поскольку многие биологические молекулы являются энантиомерами, иногда наблюдается заметная разница в действии двух энантиомеров на биологические организмы. В лекарствах, например, часто только один из энантиомеров лекарства отвечает за желаемые физиологические эффекты, в то время как другой энантиомер менее активен, неактивен или иногда даже вызывает побочные эффекты. Благодаря этому открытию, лекарства, состоящие только из одного энантиомера («энантиопер»), могут быть разработаны, чтобы улучшить действие лекарства, а иногда и устранить некоторые побочные эффекты. Примером может служить эзопиклон (Lunesta), который представляет собой всего лишь единственный энантиомер более старого рацемического препарата под названием зопиклон. Один энантиомер отвечает за все желаемые эффекты, в то время как другой энантиомер, по-видимому, неактивен, поэтому доза эзопиклона составляет половину дозы зопиклона.
При химическом синтезе энантиомерных веществ неэнантиомерные предшественники неизбежно образуют рацемические смеси. В отсутствие эффективного энантиомерного окружения (предшественник, хиральный катализатор или кинетическое разрешение ) разделение рацемической смеси на ее энантиомерные компоненты невозможно, хотя некоторые рацемические смеси самопроизвольно кристаллизуются в форме рацемического конгломерата, в котором кристаллы энантиомеров физически разделены и могут быть разделены механически (например, энантиомеры винной кислоты, кристаллизованные энантиомеры которых были разделены пинцетом Пастером ). Однако большинство рацематов кристаллизуются в кристаллы, содержащие оба энантиомера в соотношении 1: 1 и образующие правильную решетку.
Система R / S является важной системой номенклатуры, используемой для обозначения различных энантиомеров. Другая система основана на префиксных обозначениях оптической активности: (+) - и (-) - или d- и l-. Латинские слова, обозначающие левый, - это laevus и зловещий, а слово, обозначающее право, - dexter (или rectus в смысле правильного или добродетельного). Английское слово right является родственным от rectus. Это источник обозначений L / D и S / R, а также использование префиксов levo- и dextro- в общих именах.
Префикс ent- в химическом названии может быть используется для обозначения химического вещества, которое является энантиомером того, что указано в названии.
 проекция Фишера мезо-винной кислоты
проекция Фишера мезо-винной кислоты Асимметричный атом углерода - это атом углерода, который имеет связи с четырьмя разными атомами или группами, так что эти связи могут быть расположены двумя разными способами, которые не могут быть совмещены. Большинство соединений, которые содержат один или несколько асимметричных атомов углерода (или другого элемента с тетраэдрической геометрией), демонстрируют энантиомерию, но это не всегда так. Соединения, которые содержат два или более асимметричных атома углерода, но имеют плоскость симметрии относительно всей молекулы, известны как мезосоединения. Мезосоединение не имеет стереоизомера, отражающего зеркальное отображение, поскольку оно является его собственным зеркальным отображением (т.е. оно и его зеркальное отображение являются одной и той же молекулой). Например, мезо винная кислота (показана справа) имеет два асимметричных атома углерода, но не проявляет энантиомерию, потому что каждая из двух половин молекулы равна и противоположна другой и, таким образом, может накладываться друг на друга. на его геометрическом зеркальном отображении. И наоборот, существуют формы хиральности, которые не требуют отдельных асимметричных атомов. Фактически, существует четыре различных типа хиральности: центральная, осевая, плоская и спиральная. Наличие энантиомера благодаря асимметричному атому углерода представляет собой наиболее распространенный тип центральной хиральности. Другие три типа хиральности не связаны с асимметричными атомами углерода, и даже центральная хиральность не требует, чтобы центр хиральности располагался у атома углерода или любого другого атома. Следовательно, хотя наличие асимметричного атома углерода является удобной характеристикой, которую нужно искать при определении того, будет ли молекула иметь энантиомер, его недостаточно и не нужно в качестве критерия.
В качестве строгого критерия молекула является хиральной и, следовательно, будет обладать энантиомером, если и только если она принадлежит к одной из хиральных точечных групп: C n, D n, T, O и I. Однако, как предостережение, энантиомеры не обязательно могут быть выделены, если существует доступный путь рацемизации при данной температуре и времени. Например, амины с тремя различными заместителями являются хиральными, но за исключением нескольких нетипичных случаев (например, замещенные N-хлоразиридины), они быстро планаризуются и инвертируются («зонтичная инверсия») при комнатной температуре, что приводит к рацемизации. Если рацемизация происходит достаточно быстро, молекулу часто можно рассматривать как ахиральную усредненную структуру.
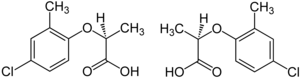 Структуры двух энантиомерных форм (S слева, R справа) мекопроп
Структуры двух энантиомерных форм (S слева, R справа) мекопроп  Энантиомеры циталопрама. Вверху находится (R) -циталопрам, а внизу - (S) -циталопрам.
Энантиомеры циталопрама. Вверху находится (R) -циталопрам, а внизу - (S) -циталопрам.. Примером такого энантиомера является седатив талидомид, который продавался в в ряде стран мира с 1957 по 1961 год. Он был изъят с рынка, когда было обнаружено, что он вызывает врожденные дефекты. Один энантиомер вызвал желаемый седативный эффект, тогда как другой, неизбежно присутствующий в равных количествах, вызвал врожденные дефекты.
гербицид мекопроп представляет собой рацемическую смесь с (R) - (+) - энантиомер («Мекопроп-П», «Дуплосан KV»), обладающий гербицидной активностью.
Другим примером являются антидепрессанты эсциталопрам и циталопрам.. Циталопрам представляет собой рацемат [смесь (S) -циталопрама и (R) -циталопрама, 1: 1]; эсциталопрам [(S) -циталопрам] представляет собой чистый энантиомер. Дозировки эсциталопрама обычно составляют 1/2 дозировки циталопрама.
Существуют две основные стратегии получения энантиочистых соединений. Первый известен как хиральное разрешение. Этот метод включает получение соединения в рацемической форме и разделение его на его изомеры. В своей новаторской работе Луи Пастер смог выделить изомеры винной кислоты, потому что они кристаллизуются из раствора в виде кристаллов, каждый с разной симметрией. Менее распространенным методом является самодиспропорционирование энантиомера.
. Вторая стратегия - асимметричный синтез: использование различных методик для получения желаемого соединения с высоким энантиомерным избытком. Охватываемые методы включают использование хиральных исходных материалов (синтез хирального пула ), использование хиральных вспомогательных веществ и и применение асимметричной индукции. Использование ферментов (биокатализ ) также может дать желаемое соединение.
представляет собой синтез одного энантиомера из молекулы рацемического предшественника с использованием обоих энантиомеров. Таким образом, два энантиомера реагента образуют один энантиомер продукта.
Достижения в области промышленных химических процессов сделали для производителей фармацевтической продукции экономически выгодным принимать лекарства, которые первоначально продавались как рацемическая смесь, и продавать индивидуальные энантиомеры. В некоторых случаях энантиомеры действительно имеют разные эффекты. В других случаях клиническая польза для пациента может отсутствовать. В некоторых юрисдикциях одноэнантиомерные лекарства могут быть запатентованы отдельно от рацемической смеси. Возможно, активен только один из энантиомеров. Или может оказаться, что оба активны, и в этом случае разделение смеси не дает объективных преимуществ, но увеличивает патентоспособность лекарства.
Квазиэнантиомеры представляют собой молекулярные разновидности, которые не строго энантиомеры, но ведут себя так, как если бы они были. Квазиэнантиомеры имеют параллельное применение кинетическое разрешение.