Гидратации Mukaiyama представляет собой органическая реакцию с участием формального добавления эквивалента воды поперек олефина под действием каталитического бис (ацетилацетонат) кобальт (II), комплекс, фенилсилан и атмосферный кислород с получением спирта с Марковниковым селективностью.
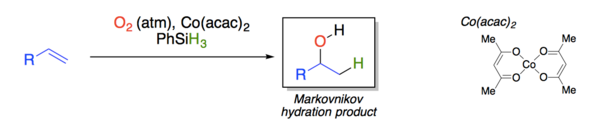
Реакция была разработана Теруаки Мукаяма из Mitsui Petrochemical Industries, Ltd. Ее открытие было основано на предыдущей работе по селективной гидратации олефинов, катализируемой комплексами кобальта с лигандами основания Шиффа и лигандами порфирина. Благодаря своей хемоселективности (толерантность к другим функциональным группам) и мягким условиям реакции (протекание на воздухе при комнатной температуре) гидратация Мукаяма стала ценным инструментом в химическом синтезе.
В своей первоначальной публикации Мукаяма предположил, что реакция протекает через посредство аддукта перекиси кобальта. Реакция обмена металлов между гидросиланом и аддуктом пероксида кобальта приводит к силилпероксиду, который превращается в спирт при восстановлении, предположительно под действием кобальтового катализатора.

Исследования Нодзимы и его коллег, изучающие механизм катализируемого кобальтом перекисного окисления алкенов, подтверждают промежуточную роль гидрида металла, который непосредственно реагирует с алкеном с образованием временной кобальт-алкильной связи. Гомолиз генерирует углерод-центрированный радикал, который непосредственно реагирует с кислородом и впоследствии улавливается разновидностью кобальта (II) с образованием того же аддукта кобальта и пероксида, как это было предложено Мукаяма. Обмен металла с гидросиланом дает продукт перекиси силила, а дальнейшее восстановление (посредством гомолиза кислородно-кислородной связи) приводит к получению спирта. Использование силанового восстановителя позволяет проводить эту реакцию без нагрева. Авторы также отмечают, в соответствии с предыдущими исследованиями, что добавление трет- бутилгидропероксида может увеличить скорость менее реагирующих субстратов. Такое увеличение скорости, вероятно, связано с окислением кобальта (II) до комплекса алкилпероксокобальта (III), который впоследствии участвует в быстром обмене металла с гидросиланом с образованием активного гидрида кобальта (III).

Важно отметить, что изложенный выше механизм резко контрастирует с предыдущими механистическими предложениями, которые предполагают, что комплекс кобальт-перокси вставляется непосредственно в алкены. Вышеупомянутое исследование, проведенное Нодзимой и его коллегами, не согласилось с этим предложением из-за трех наблюдений: 1) промежуточная связь гидрида кобальта, наблюдаемая с помощью 1 H ЯМР 2) склонность алкенов подвергаться автоокислению до α, β-ненасыщенных кетонов или аллиловых спиртов. когда та же реакция протекает в отсутствие гидросилана 3) преобладающий способ разложения разновидностей алкилпероксокобальта (III) на алкокси или алкилперокси радикал по механизму Габера-Вейсса.
В недавнем обзоре, проведенном Шенви и соавторами, было высказано предположение, что гидратация Мукаямы осуществляется по тем же принципам, что и перенос атома водорода гидрида металла (MH HAT), что было объяснено Джеком Халперном и Джеком Р. Нортоном в их исследованиях гидрирования антраценов синтез-газом и Co 2. (CO) 8 и химический состав имитатора витамина B 12 соответственно.
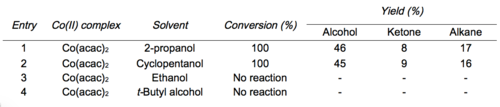
Ямада исследовал влияние различных растворителей и лигандов бета-дикетоната кобальта на выход и распределение продуктов реакции.

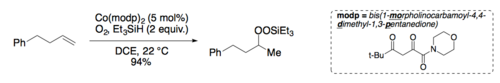
Мукаяма и Исаяма разработали условия для выделения промежуточного силилпероксида. Обработка промежуточного силилпероксида 1 каплей концентрированной HCl в метаноле приводит к гидропероксидному продукту.
И Мукаяма, и Магнус описывают условия реакции гидроксилирования α-енона с использованием Mn (dpm) x в присутствии кислорода и фенилсилана. Асимметричный вариант был описан Ямадой и соавторами.

Дейл Богер и его коллеги использовали вариант гидратации Мукаямы с использованием катализатора оксалата железа (Fe 2 ox 3 • 6H 2 O) в присутствии воздуха для полного синтеза винбластина и родственных аналогов.
Группа Эрика Каррейры разработала методы гидрогидразинирования олефинов, катализируемые как кобальтом, так и марганцем.
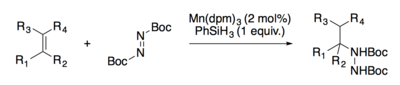
И Каррейра, и Богер разработали реакции гидроазидирования.
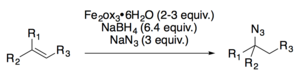
Гидратация Мукаямы или ее варианты были представлены в синтезе (±) -гарсубеллина A, стигмалона, винбластина, (±) -кортистатина A, (±) -лахадинина B, уабагенина, пектенотоксина -2, (±) -индоксамицина B., триходерматид А, (+) - омфадиол и многие другие натуральные продукты.
На следующей диаграмме проиллюстрировано применение гидратации Мукаямы в полном синтезе (±) -гарсубеллина А:

Реакция гидратации катализируется Co (acac) 2 (acac = 2,4-пентандионато, более известное как ацетилацетонато) и проводится в присутствии кислорода воздуха и фенилсилана. При использовании изопропанола в качестве растворителя выход составляет 73%.