Циклопропанирование относится к любому химическому процессу, при котором образуются кольца циклопропана. Это важный процесс в современной химии, так как многие полезные соединения имеют этот мотив; например, пиретроиды и ряд хинолоновых антибиотиков (ципрофлоксацин, спарфлоксацин и т. д.). Однако высокое содержание кольцевого штамма , присутствующее в циклопропанах, затрудняет их получение и обычно требует использования высокореактивных частиц, таких как карбены, илиды и . карбанионы. Многие реакции протекают по хелетропной манере.
 Структура природных инсектицидов пиретрин I, R = CH 3 и пиретрин II, R = CO 2CH3.
Структура природных инсектицидов пиретрин I, R = CH 3 и пиретрин II, R = CO 2CH3.Существует несколько методов превращения алкенов в циклопропановые кольца с использованием реагентов типа карбен. Поскольку сами карбены обладают высокой реакционной способностью, они обычно используются в стабилизированной форме, называемой карбеноидом.
В реакции Симмонса – Смита реакционноспособный карбеноид представляет собой йодметилцинк иодид, который обычно образуется в результате реакции между дииодметаном и парой цинк-медь. Были разработаны модификации, включающие более дешевые альтернативы, такие как дибромметан или диазометан и йодид цинка. Реакционную способность системы также можно увеличить, заменив пару цинк-медь на диэтилцинк. Известны асимметричные версии.

Некоторые диазосоединения, такие как диазометан, могут реагировать с олефинами с образованием циклопропанов в двухстадийном режиме. Первый этап включает 1,3-диполярное циклоприсоединение с образованием пиразолина, который затем подвергается денитрогенизации либо фотохимическим, либо термическим разложением, чтобы дать циклопропан. Термический путь, который часто использует КОН и платину в качестве катализаторов, также известен как синтез циклопропана Кишнера в честь русского химика Николая Кишнера и также может быть выполнено с использованием гидразина и α, β-ненасыщенных карбонильных соединений. Механизм разложения был предметом нескольких исследований и остается несколько спорным, хотя в целом считается, что он происходит через бирадикальные виды. С точки зрения зеленой химии этот метод превосходит другие циклопропанирование на основе карбена; поскольку в нем не используются металлы или галогенированные реагенты, а в качестве побочного продукта образуется только N 2. Однако реакция может быть опасной, поскольку следовые количества непрореагировавших диазосоединений могут взорваться во время термической перегруппировки пиразолина.

Метилфенилдиазоацетат и многие родственные диазопроизводные являются предшественниками донорно-акцепторных карбенов, которые можно использовать для циклопропанирования или для вставки в связи CH органических субстраты. Эти реакции катализируются тетраацетатом диродия или, что более эффектно, родственными хиральными производными.
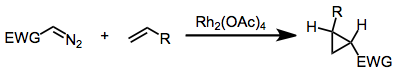
Свободные карбены могут быть использованы для реакций циклопропанирования, однако возможности для этого ограничены, так как немногие из них могут быть удобно получены, и почти все они нестабильны (см.: димеризация карбена ). Исключением являются дигалогенкарбены, такие как дихлоркарбен или дифторкарбен, которые достаточно стабильны и будут реагировать с образованием геминальных дигалоциклопропанов. Эти соединения затем можно использовать для образования алленов посредством перегруппировки Скаттебёля.

Реакция расширения кольца Бюхнера также включает образование стабилизированного карбена. Циклопропанирование также стереоспецифично, поскольку добавление карбена и карбеноидов к алкенам является формой хелетропной реакции, при этом добавление происходит по типу syn. Например, дибромокарбен и цис-2-бутен дают цис-2,3-диметил-1,1-дибромциклопропан, тогда как транс-изомер дает исключительно трансциклопропан.
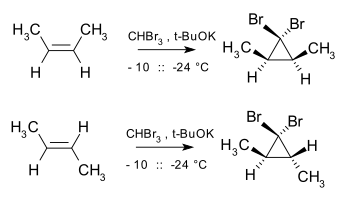
Циклопропаны могут быть получены с использованием серы илид в реакции Джонсона – Кори – Чайковского, однако этот процесс в значительной степени ограничен использованием на бедных электронами олефинах, особенно α, β-ненасыщенные карбонильные соединения.
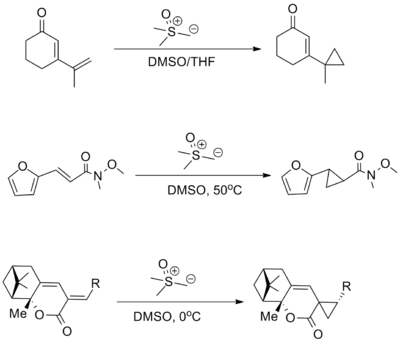
Циклопропаны могут быть получены различными реакциями внутримолекулярной циклизации. Простым методом является использование первичных галогеналканов, содержащих соответственно расположенные электроноакцепторные группы. Обработка сильным основанием приведет к образованию карбаниона, который будет циклизоваться по типу 3-экзо-тригона со смещением галогенида. Примеры включают образование циклопропилцианида и циклопропилацетилена. Этот механизм также составляет основу перегруппировки Фаворского.
Родственным процессом является циклизация 1,3 -дибромпропан через соединение Вюрца. Он был использован для первого синтеза циклопропана Августом Фройндом в 1881 году. Первоначально эта реакция проводилась с использованием натрия, однако выход можно улучшить, заменив его на цинк.
 Структура U-106305, производного циклопропановой жирной кислоты с шестью циклопропановыми кольцами, выделенного из S treptomyces sp.
Структура U-106305, производного циклопропановой жирной кислоты с шестью циклопропановыми кольцами, выделенного из S treptomyces sp. Хотя циклопропаны относительно редки в биохимии, многие пути циклопропанирования были идентифицированы в природе. Наиболее распространенные пути включают реакции замыкания кольца карбокатионов в терпеноидах. Циклопропановые жирные кислоты являются производными от воздействия S-аденозилметионина (SAM) на ненасыщенные жирные кислоты. Предшественник гормона этилен, 1-аминоциклопропан-1-карбоновая кислота получается непосредственно из SMM посредством внутримолекулярного нуклеофильного замещения группы SMe 2 после конденсации. с пиридоксальфосфатом. Прямой перенос карбена от диазоэфиров к олефинам также был достигнут посредством биокатализа in vitro с использованием модифицированных вариантов фермента цитохрома P450 из Bacillus megaterium, которые были оптимизированы с помощью направленной эволюции.