 | |
 | |
| Названия | |
|---|---|
| Название IUPAC Хлорид цезия | |
| Другие названия Хлорид цезия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.728 |
| Номер EC |
|
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химическая формула | CsCl |
| Молярная масса | 168,36 г / моль |
| Внешний вид | белое твердое вещество. гигроскопично |
| Плотность | 3,988 г / см |
| Плавление точка | 646 ° C (1195 ° F; 919 K) |
| Температура кипения | 1297 ° C (2367 ° F; 1570 K) |
| Растворимость в воде | 1910 г / л (25 ° C) |
| Растворимость | растворим в этаноле |
| Ширина запрещенной зоны | 8,35 эВ (80 K) |
| Магнитная восприимчивость (χ) | -56,7 · 10 см / моль |
| Показатель преломления (nD) | 1,712 (0,3 мкм). 1,640 (0,59 мкм). 1,631 (0,75 мкм). 1,626 (1 мкм). 1,616 (5 мкм). 1,563 (20 мкм) |
| Структура | |
| Кристаллическая структура | CsCl, cP2 |
| Пространственная группа | Pm3m, No. 221 |
| Постоянная решетки | a = 0,4119 нм |
| Объем решетки (В) | 0,0699 нм |
| Формула единицы (Z) | 1 |
| Координационная геометрия | Кубическая (Cs). Кубическая (Cl) |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
| Опасность GHS заявления | H302, H341, H361, H373 |
| Меры предосторожности GHS | P201, P202, P260, P264, P270, P281, P301 + 312, P308 + 313, P314, P330, P405, P501 |
| Летальная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 2600 мг / кг (перорально, крыса) |
| Родственные соединения | |
| Другие анионы | Фторид цезия. Бромид цезия. Иодид цезия. |
| Другие катионы | Хлорид лития. Хлорид натрия. Хлорид калия. Хлорид рубидия. |
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
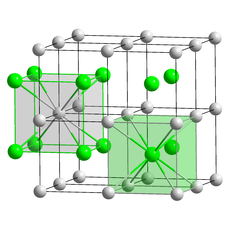
хлорид цезия или хлорид цезия представляет собой неорганическое соединение формулы Cs Cl. Эта бесцветная соль является важным источником ионов цезия для различных нишевых применений. Его кристаллическая структура образует основной структурный тип, в котором каждый ион цезия координируется 8 ионами хлора. Хлорид цезия растворяется в воде. CsCl при нагревании переходит в структуру NaCl. Хлорид цезия встречается в природе в виде примесей в карналлите (до 0,002%), сильвите и каините. Ежегодно во всем мире производится менее 20 тонн CsCl, в основном из цезийсодержащего минерала поллуцита.
. Хлорид цезия широко используется в качестве лекарственной структуры в изопикническом центрифугировании для разделения различных типы ДНК. Это реагент в аналитической химии, где он используется для идентификации ионов по цвету и морфологии осадка. Обогащенный радиоизотопами, такими как CsCl или CsCl, хлорид цезия используется в ядерной медицине, таких как лечение рака и диагностика инфаркта миокарда.. Другая форма лечения рака была изучена с использованием обычного нерадиоактивного CsCl. В то время как обычный хлорид цезия имеет довольно низкую токсичность для людей и животных, радиоактивная форма легко загрязняет окружающую среду из-за высокой растворимости CsCl в воде. Распространение порошка CsCl из 93-граммового контейнера в 1987 году в Гоянии, Бразилия, привело к одной из самых ужасных аварий, связанных с разливом радиации, в результате чего четыре человека погибли и пострадали более 100 000 человек.
В структуре хлорида цезия используется примитивная кубическая решетка с двухатомной основой, где оба атома имеют восьмикратную координацию. Атомы хлора лежат в точках решетки на краях куба, а атомы цезия - в отверстиях в центре кубов. Эта структура является общей с CsBr и CsI и многими бинарными металлическими сплавами. Напротив, другие щелочные галогениды имеют структуру хлорида натрия (каменная соль). Когда оба иона близки по размеру (ионный радиус Cs 174 пм для этого координационного числа, Cl 181 пм), структура CsCl принимается, когда они различны (ионный радиус Na 102 пм, Cl 181 пм) принята структура хлорида натрия. При нагревании до температуры выше 445 ° C нормальная структура хлорида цезия (α-CsCl) преобразуется в форму β-CsCl со структурой каменной соли (пространственная группа Fm3m). Структура каменной соли также наблюдается в условиях окружающей среды в нанометровых пленках CsCl, выращенных на подложках из слюды, LiF, KBr и NaCl.
Хлорид цезия бесцветен в виде крупных кристаллов и белого цвета при растирании. Он легко растворяется в воде, максимальная растворимость увеличивается с 1865 г / л при 20 ° C до 2705 г / л при 100 ° C. Кристаллы очень гигроскопичны и постепенно разрушаются в условиях окружающей среды. Хлорид цезия не образует гидратов.
| Т (° C) | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| S (мас.%) | 61,83 | 63,48 | 64,96 | 65,64 | 66,29 | 67,50 | 68,60 | 69,61 | 70,54 | 71,40 | 72,21 | 72,96 |
В отличие от хлорид натрия и хлорид калия, хлорид цезия легко растворяется в концентрированной соляной кислоте. Хлорид цезия также имеет относительно высокую растворимость в муравьиной кислоте (1077 г / л при 18 ° C) и гидразине ; средняя растворимость в метаноле (31,7 г / л при 25 ° C) и низкая растворимость в этаноле (7,6 г / л при 25 ° C), диоксид серы (2,95 г / л при 25 ° C), аммиак (3,8 г / л при 0 ° C), ацетон (0,004% при 18 ° C), ацетонитрил (0,083 г / л при 18 ° C), этилацетаты и другие сложные простые эфиры, бутанон, ацетофенон, пиридин и хлорбензол.
Несмотря на широкую запрещенную зону, составляющую около 8,35 эВ при 80 K, хлорид цезия слабо проводит электричество, и проводимость не электронная, а ионная. Электропроводность имеет значение порядка 10 См / см при 300 ° C. Это происходит за счет скачков вакансий в решетке ближайших соседей, и подвижность вакансий Cl намного выше, чем вакансий Cs. Проводимость увеличивается с температурой примерно до 450 ° C, при этом энергия активации изменяется от 0,6 до 1,3 эВ при примерно 260 ° C. Затем она резко падает на два порядка из-за фазового перехода из фазы α-CsCl в фазу β-CsCl. Проводимость также подавляется приложением давления (уменьшение примерно в 10 раз при 0,4 ГПа), которое снижает подвижность вакансий в решетке.
| Концентрация,. мас.% | Плотность,. кг / л | Концентрация,. моль / л | показатель преломления. (при 589 нм) | Понижение точки замерзания, ° С относительно воды | Вязкость,. 10 Па · с |
|---|---|---|---|---|---|
| 0,5 | – | 0,030 | 1,3334 | 0,10 | 1.000 |
| 1.0 | 1.0059 | 0,060 | 1,3337 | 0,20 | 0,997 |
| 2,0 | 1,0137 | 0,120 | 1,3345 | 0,40 | 0,992 |
| 3,0 | 0,182 | 1,3353 | 0,61 | 0,988 | |
| 4,0 | 1,0296 | 0,245 | 1,3361 | 0,81 | 0,984 |
| 5,0 | 0,308 | 1,3369 | 1,02 | 0,980 | |
| 6,0 | 1,0461 | 0,373 | 1,3377 | 1,22 | 0,977 |
| 7,0 | 0,438 | 1,3386 | 1,43 | 0,974 | |
| 8,0 | 1,0629 | 0,505 | 1,3394 | 1,64 | 0,971 |
| 9,0 | 0,573 | 1,3403 | 1,85 | 0,969 | |
| 10,0 | 1,0804 | 0,641 | 1,3412 | 2,06 | 0,966 |
| 12,0 | 1,0983 | 0,782 | 1,3430 | 2,51 | 0,961 |
| 14,0 | 1,1168 | 0,928 | 1,3448 | 2,97 | 0,955 |
| 16,0 | 1,1358 | 1,079 | 1,3468 | 3,46 | 0,950 |
| 18,0 | 1,1555 | 1,235 | 1,3487 | 3,96 | 0,945 |
| 20,0 | 1,1758 | 1,397 | 1,3507 | 4,49 | 0,939 |
| 22,0 | 1,1968 | 1,564 | 1,3528 | – | 0,934 |
| 24,0 | 1,2185 | 1,737 | 1,3550 | – | 0,930 |
| 26,0 | 1,917 | 1,3572 | – | 0,926 | |
| 28,0 | 2,103 | 1,3594 | – | 0,924 | |
| 30,0 | 1,2882 | 2,296 | 1,3617 | – | 0,922 |
| 32,0 | 2,497 | 1,3641 | – | 0,922 | |
| 34,0 | 2,705 | 1,3666 | – | 0,924 | |
| 36,0 | 2,921 | 1,3691 | – | 0,926 | |
| 38,0 | 3,146 | 1,3717 | – | 0,930 | |
| 40,0 | 1,4225 | 3,380 | 1,3744 | – | 0,934 |
| 42,0 | 3,624 | 1,3771 | – | 0,940 | |
| 44,0 | 3,877 | 1,3800 | – | 0,947 | |
| 46,0 | 4,142 | 1,3829 | – | 0,956 | |
| 48,0 | 4,418 | 1,3860 | – | 0,967 | |
| 50,0 | 1,5858 | 4,706 | 1,3892 | – | 0,981 |
| 60,0 | 1,7886 | 6,368 | 1,4076 | – | 1,120 |
| 64,0 | 7,163 | 1,4167 | – | 1,238 |
Хлорид цезия полностью диссоциирует при растворении в воде, и катионы Cs сольватируются в разбавленном растворе. CsCl превращается в сульфат цезия при нагревании в концентрированной серной кислоте или нагревании с гидросульфатом цезия при 550–700 ° C:
Хлорид цезия образует множество двойных солей с другими хлоридами. Примеры включают 2CsCl · BaCl 2, 2CsCl · CuCl 2, CsCl · 2CuCl и CsCl·LiCl, а с межгалогенными соединениями:
![{\displaystyle {\ce {CsCl + ICl3 ->Cs [ICl4]}}}]( https://wikimedia.org/api/rest_v1/media/math/render/svg/6b106856bd4fcba7764e52dc61de8ec0049b4a3e )
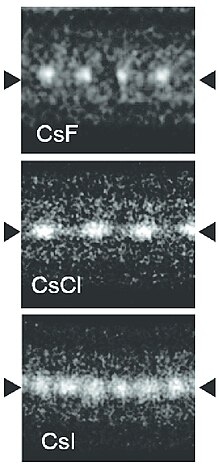 Одноатомные галогенидные провода цезия, выращенные внутри двустенных углеродные нанотрубки.
Одноатомные галогенидные провода цезия, выращенные внутри двустенных углеродные нанотрубки.Хлорид цезия встречается в природе в качестве примеси в галогенидных минералах карналлите (KMgCl 3 · 6H 2 O с содержанием CsCl до 0,002%), сильвит (KCl) и каинит (MgSO 4 · KCl · 3H 2 O), а также в минеральных водах. вода курорта Бад-Дюркхайм, которая использовалась для выделения цезия, содержала около 0,17 мг / л CsCl. Ни один из этих минералов не имеет коммерческого значения.
В промышленных масштабах производят CsCl из минерала поллуцит, который измельчают и обрабатывают соляной кислотой при повышенной температуре. Экстракт обрабатывают хлоридом сурьмы, монохлоридом йода или хлоридом церия (IV) с получением плохо растворимой двойной соли, например:
Обработка двойной соли сероводородом дает CsCl:
CsCl высокой чистоты также получают из перекристаллизованного ![{\ displaystyle {\ ce {Cs [ICl2]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/179cfcb1c479f90128c3ac48e2906b3f844d8781)
![{\ displaystyle {\ ce {Cs [ICl4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7ae265895d0004997e064fbc7fa581ef0db7a2c4)
![{\displaystyle {\ce {Cs[ICl2] ->{CsCl} + ICl}}}]( https: / /wikimedia.org/api/rest_v1/media/math/render/svg/7824fed40e3efe7816a0e91633974ab54eb1aa87)
Ежегодно производилось около 20 тонн соединений цезия, в основном из CsCl. 1970-е и 2000-е годы во всем мире. Хлорид цезия, обогащенный цезием-137 на лучевая терапия производится на единственном предприятии Маяк в Уральском регионе России и продается на международном уровне через дилера в Великобритании. Соль синтезируется при 200 ° C из-за ее гигроскопичности и запечатывается в стальном контейнере в форме гильзы, который затем помещается в другой стальной корпус. Герметизация необходима для защиты соли от влаги.
В лаборатории CsCl может быть получен путем обработки гидроксида цезия, карбоната, бикарбонат цезия или сульфид цезия с соляной кислотой:
Хлорид цезия является основным прекурсором металлического цезия при высокотемпературном восстановлении:
Подобная реакция - нагревание CsCl с кальцием в вакууме в присутствии фосфора - была впервые описана в 1905 году французским химиком М.Л. Хакспиллом и до сих пор используется в промышленности..
Гидроксид цезия получают электролизом водного раствора хлорида цезия:
Хлорид цезия широко используется в центрифугировании в методике, известной как изопикническое центрифугирование. Центростремительные и диффузионные силы создают градиент плотности, который позволяет разделить смеси на основе их молекулярной плотности. Этот метод позволяет разделить ДНК разной плотности (например, фрагменты ДНК с различным содержанием A-T или G-C). Для этого применения требуется раствор с высокой плотностью и при этом относительно низкой вязкостью, и CsCl подходит для него из-за его высокой растворимости в воде, высокой плотности из-за большой массы Cs, а также низкой вязкости и высокой стабильности растворов CsCl.
Хлорид цезия редко используется в органической химии. Он может действовать как реагент катализатора межфазного переноса в выбранных реакциях. Одна из этих реакций - синтез производных глутаминовой кислоты
![{\displaystyle \overbrace {\ce {CH2=CHCOOCH3}} ^{\text{Methyl acrylate}}+{\ce {ArCH=N-CH(CH3)-COOC(CH3)3->[{\ ce {TBAB, \ CsCl, \ K2CO3}} ] [{\ ce {CPME, \ 0 ^ {\ circ} C}}] {ArCH = NC (C2H4COOCH3) (CH3) -COOC (CH3) 3}}}}]( https://wikimedia.org/api/rest_v1/media/math/render/svg/5f20c83eb7669c6266c0cc534608d0b13cef0f5a )
где TBAB представляет собой тетрабутиламмонийбромид (CPME представляет собой метиловый эфир метилового эфира) и CPME представляет собой метиловый эфир растворитель).
Другой реакцией является замещение тетранитрометана
где ДМФ представляет собой диметилформамид (растворитель).
Хлорид цезия - это реагент в традиционной аналитической химии, используемый для обнаружения неорганических ионов по цвету и морфологии осадков. Количественное измерение концентрации некоторых из этих ионов, например Mg с помощью масс-спектрометрии с индуктивно связанной плазмой используется для оценки жесткости воды.
| Ион | Сопутствующие реагенты | Остаток | Морфология | Предел обнаружения (мкг) |
|---|---|---|---|---|
| AsO 3 | KI | Cs2[AsI 5 ] или Cs 3 [AsI 6] | Красные шестиугольники | 0,01 |
| Au | AgCl, HCl | Cs2Ag [AuCl 6] | Серо-черные кресты, четырех- и шестилучевые звезды | 0,01 |
| Au | NH4SCN | Cs [Au (SCN) 4] | Оранжево-желтые иглы | 0,4 |
| Bi | KI, HCl | Cs2[BiI 5 ] или 2,5H 2O | Красные шестиугольники | 0,13 |
| Cu | (CH 3 COO) 2 Pb, CH 3 COOH, KNO 2 | Cs2Pb [Cu (NO 2)6] | Маленькие черные кубики | 0,01 |
| In | — | Cs3[InCl 6] | Малые октаэдры | 0,02 |
| [IrCl 6] | — | Cs2[IrCl 6] | Маленькие темно-красные октаэдры | – |
| Mg | Na2HPO 4 | CsMgPO 4 или 6H 2O | Маленькие тетраэдры | – |
| Pb | KI | Cs [PbI 3] | Желто-зеленые иглы | 0,01 |
| Pd | NaBr | Cs2[PdBr 4] | Темно-красные иглы и призмы | – |
| [ReCl 4] | — | Cs [ReCl 4] | Темно-красные ромбы, бипирамиды | 0,2 |
| [ReCl 6] | — | Cs2[ReCl 6] | S желто-зеленые октаэдры | 0,5 |
| ReO 4 | — | CsReO 4 | Тетрагональные бипирамиды | 0,13 |
| Rh | KNO 2 | Cs3[Rh (NO 2)6] | Желтые кубики | 0,1 |
| Ru | — | Cs3[RuCl 6] | Розовые иглы | – |
| [RuCl 6] | — | Cs2[RuCl 6] | Маленькие темно-красные кристаллы | 0,8 |
| Sb | — | Cs2[SbCl 5 ] · nH 2O | Шестиугольники | 0,16 |
| Sb | NaI | ![{\ displaystyle {\ ce {Cs [SbI4] }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/78c190f0fcfde2966d052ab2d73b0e938953df43) или или ![{\ displaystyle {\ ce {Cs2 [SbI5]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1eb7ac284505510c341e93e2c1743311fb4e25b6) | Красные шестиугольники | 0,1 |
| Sn | — | Cs2[SnCl 6] | Маленькие октаэдры | 0,2 |
| TeO 3 | HCl | Cs2[TeCl 6] | Светло-желтые октаэдры | 0,3 |
| Tl | NaI | ![{\ displaystyle {\ ce {Cs [TlI4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d3c1830f454449a2bcdcf18f352984bf51997de0) | Оранжево-красные шестиугольники или прямоугольники | 0,06 |
Он также используется для обнаружения следующих ионов:
| Ион | Сопутствующие реагенты | Обнаружение | Предел обнаружения (мкг / мл) |
|---|---|---|---|
| Al | K2SO4 | Бесцветные кристаллы образуются в нейтральной среде после испарения | 0,01 |
| Ga | KHSO 4 | Бесцветные кристаллы образуются при нагревании | 0,5 |
| Cr | KHSO 4 | Бледно-фиолетовый криста Осаждается в слабокислой среде | 0,06 |
Американское онкологическое общество заявляет, что «имеющиеся научные данные не подтверждают утверждения о том, что нерадиоактивные добавки хлорида цезия оказывают какое-либо влияние на опухоли ». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов предупредило о рисках безопасности, включая значительную сердечную токсичность и смерть, связанные с использованием хлорида цезия в натуропатической медицине. и радиография
хлорид цезия, состоящий из радиоизотопов, таких как CsCl и CsCl, используется в ядерной медицине, включая лечение рака (брахитерапия ) и диагностика инфаркта миокарда. При производстве радиоактивных источников обычно выбирают химическую форму радиоизотопа, которая не будет легко рассеиваться в окружающей среде в случае аварии. Например, радиотермические генераторы (РИТЭГи) часто используют титанат стронция, который нерастворим в воде. Однако для источников телетерапии радиоактивная плотность (Ci в данном объеме) должна быть очень высокой, что невозможно с известными нерастворимыми соединениями цезия. Контейнер радиоактивного хлорида цезия в форме наперстка является активным источником.
Хлорид цезия используется при изготовлении электропроводящих стекол и экранов электронно-лучевых трубок. CsCl вместе с инертными газами используется в эксимерных лампах и эксимерных лазерах. Другие применения включают активацию электродов при сварке; производство минеральной воды, пива и буровых растворов ; и жаропрочные припои. Высококачественные монокристаллы CsCl имеют широкий диапазон прозрачности от УФ до инфракрасного излучения и поэтому использовались для изготовления кювет, призм и окон в оптических спектрометрах; это использование было прекращено с разработкой менее гигроскопичных материалов.
CsCl является мощным ингибитором каналов HCN, которые переносят h-ток в возбудимых клетках, таких как нейроны. Следовательно, он может быть полезен в экспериментах по электрофизиологии в неврологии.
Хлорид цезия имеет низкую токсичность для человека и животных. Его средняя летальная доза (LD 50) для мышей составляет 2300 мг на килограмм веса тела для перорального введения и 910 мг / кг для внутривенной инъекции. Легкая токсичность CsCl связана с его способностью снижать концентрацию калия в организме и частично замещать его в биохимических процессах. Однако прием в больших количествах может вызвать значительный дисбаланс калия и привести к гипокалиемии, аритмии и острой остановке сердца. Однако порошок хлорида цезия может раздражать слизистые оболочки и вызывать астму.
. Из-за его высокой растворимости в воде хлорид цезия очень подвижен и может даже диффундировать через бетон. Это недостаток его радиоактивной формы, который требует поиска более стабильных радиоизотопных материалов. Коммерческие источники радиоактивного хлорида цезия надежно закрыты двойным стальным корпусом. Однако во время аварии в Гоянии в Бразилии такой источник, содержащий около 93 граммов CsCl, был украден из заброшенной больницы и взломан двумя мусорщиками. Голубое свечение, излучаемое в темноте радиоактивным хлоридом цезия, привлекло воров и их родственников, которые не подозревали о связанных с этим опасностях, и рассыпали порошок. Это привело к одной из самых тяжелых аварий с разливом радиации, в которой 4 человека умерли в течение месяца после облучения, у 20 были обнаружены признаки лучевой болезни, 249 человек были заражены радиоактивным хлоридом цезия и около тысячи получили доза, превышающая годовое количество радиационного фона. Более 110 000 человек переполнили местные больницы, а несколько городских кварталов пришлось снести в ходе уборочных работ. В первые дни заражения у нескольких человек были расстройства желудка и тошнота из-за лучевой болезни, но только через несколько дней один человек связал симптомы с порошком и принес властям образец.
| На Викискладе есть средства массовой информации, связанные с хлоридом цезия. |
.