 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Нитрат меди (II) | |
| Другие названия Нитрат меди | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.019.853 |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| CompTox Dashboard ( EPA) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химические формула | Cu (NO 3)2 |
| Молярная масса | 187,5558 г / моль (безводный). 241,60 г / моль (тригидрат). 232,591 г / моль (гемипентагидрат) |
| Внешний вид | синие кристаллы. гигроскопичны |
| Плотность | 3,05 г / см (безводный). 2,32 г / см (тригидрат). 2,07 г / см (гексагидрат) |
| Температура плавления | 114 ° C (237 ° F; 387 K) (безводный, разлагается). 114,5 ° C (тригидрат). 26,4 ° C (гексагидрат, разлагается) |
| Точка кипения | 170 ° C (338 ° F; 443 K) (тригидрат, разлагается) |
| Растворимость в воде | тригидрат:. 381 г / 100 мл (40 ° C). 666 г / 100 мл (80 ° C). гексагидрат:. 243,7 г / 100 мл (80 ° C) |
| Растворимость | гидраты, хорошо растворимые в этаноле, аммиаке, воде ; не растворим в этилацетате |
| Магнитная восприимчивость (χ) | + 1570,0 · 10 см / моль (~ 3H 2 O) |
| Структура | |
| Кристаллическая структура | орторомбический (безводный). ромбоэдрический (гидраты) |
| Опасности | |
| Основные опасности | Раздражитель, окислитель |
| Паспорт безопасности | Cu (NO 3)2· 3H 2O |
| NFPA 704 (огненный алмаз) |  0 1 3 OX 0 1 3 OX |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимый) | TWA 1 мг / м (как Cu) |
| REL (рекомендуется) | TWA 1 мг / м (как Cu) |
| IDLH (Непосредственная опасность) | TWA 100 мг / м (как Cu) |
| Родственные соединения | |
| Другие анионы | Сульфат меди (II). Хлорид меди (II) |
| Прочие катионы | Нитрат никеля (II). Нитрат цинка |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Нитрат меди (II), Cu (NO3 )2представляет собой неорганическое соединение, которое образует голубое кристаллическое твердое вещество. Безводный c Верхний нитрат образует темно-сине-зеленые кристаллы и сублимирует в вакууме при 150-200 ° C. Нитрат меди также представлен в виде пяти различных гидратов, наиболее распространенными из которых являются гемипентагидрат и тригидрат. Эти материалы чаще встречаются в торговле, чем в лаборатории.
 Водный раствор нитрата меди (II).
Водный раствор нитрата меди (II). Гидратированный нитрат меди можно получить путем гидратации безводного материала или путем обработки металлическая медь с водным раствором нитрата серебра или концентрированной азотной кислотой :
Безводная Cu (NO 3)2образуется, когда металлическая медь обрабатывается N2O4 :
Попытка дегидратации любого из гидратированных нитратов меди (II) путем нагревания вместо этого дает оксиды, а не Cu (NO 3)2. При 80 ° C гидраты превращаются в «основной нитрат меди» (Cu 2 (NO 3) (OH) 3), который превращается в CuO при 180 ° C.Используя эту реакционную способность, нитрат меди может быть sed для получения азотной кислоты путем нагревания ее до разложения и пропускания паров непосредственно в воду. Этот метод аналогичен последнему шагу в процессе Оствальда. Уравнения следующие:
Природные основные нитраты меди включают редкие минералы гергардтит и руаит, оба являются полиморфными модификациями Cu 2 (NO 3) (OH) 3 вещество.
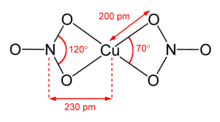
Безводный нитрат меди (II) имеет кристаллизован в двух свободных -сольватных полиморфах. α- и β-Cu (NO 3)2представляют собой полностью трехмерные координационные полимерные сети. Альфа-форма имеет только одно окружение Cu, с [ 4 + 1], но бета-форма имеет два разных медных центра, один с [4 + 1], а другой - квадратный. Сольват нитрометана также имеет «[4+ 1] координацию» с четырьмя короткими Cu-O связи примерно 200 пм и одна более длинная связь в 240 пм. Это координационные полимеры с бесконечными цепочками центров меди (II) и нитратных групп. В газовой фазе нитрат меди (II) имеет два бидентата нитратные лиганды (см. изображение вверху справа). Таким образом, испарение твердого вещества влечет за собой «крекинг » с образованием молекулы нитрата меди (II).
Сообщалось о пяти гидратах : моногидрат (Cu (NO 3)2·H2O), сесквигидрат (Cu (NO 3)2· 1,5H 2 O), гемипентагидрат (Cu (NO 3)2· 2,5H 2 O), тригидрат (Cu (NO 3)2· 3H 2 O), и гексагидрат ([Cu (H 2O)6] (NO 3)2). Гексагидрат интересен тем, что все расстояния Cu-O равны, не обнаруживая обычного эффекта Яна - Искажение упора, которое в остальном характерно для октаэдрических комплексов Cu (II). Это отсутствие эффекта объясняется сильной водородной связью, которая ограничивает эластичность связей Cu-O.
Нитрат меди (II) находит множество применений, главным из которых является его преобразование в оксид меди (II), который используется в качестве катализатора для различных процессов в органической химии. Его растворы используются в текстильных изделиях и полировальных средствах для других металлов. Нитраты меди содержатся в некоторых пиротехнике. Это o Часто используется в школьных лабораториях для демонстрации химических реакций гальванических элементов. Он входит в состав некоторых керамических глазурей и металлических патин.
Нитрат меди в сочетании с уксусным ангидридом является эффективным реагентом для нитрования ароматических соединений, известных как Нитрование Менке в честь голландского химика, открывшего, что нитраты металлов являются эффективными реагентами для нитрования. Гидратированный нитрат меди, адсорбированный на глине, дает реагент под названием «Claycop». Полученная глина синего цвета используется в виде суспензии, например, для окисления тиолов до дисульфидов. Claycop также используется для преобразования дитиоацеталей в карбонилы. Соответствующий реагент на основе монтмориллонита оказался полезным для нитрования ароматических соединений.
| На Викискладе есть материалы, относящиеся к нитрату меди (II). |
| HNO 3 | He | ||||||||||||||||
| LiNO 3 | Be (NO 3)2 | B (NO. 3). 4 | RONO 2 | NO. 3. NH4NO3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3)2 | Al (NO 3)3 | Si | P | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3)2 | Sc (NO 3)3 | Ti (NO 3)4 | VO (NO 3)3 | Cr (NO 3)3 | Mn (NO 3)2 | . Fe (NO 3)3 | Co (NO 3)2. Co (NO 3)3 | Ni (NO 3)2 | CuNO 3. Cu ( NO 3)2 | Zn (NO 3)2 | Ga (NO 3)3 | Ge | As | Se | Br | Kr |
| RbNO 3 | Sr (NO 3)2 | Y (NO 3)3 | Zr (NO 3)4 | Nb | Mo | Tc | Pd (NO 3)2. | AgNO 3. | Cd ( NO 3)2 | In | Sn | Te | I | Xe (NO 3)2 | |||
| CsNO 3 | Ba (NO 3)2 | Hf | Ta | W | Re | Os | Ir | . | Hg2(NO 3)2. Hg (NO 3)2 | . Tl (NO 3)3 | Pb (NO 3)2 | Bi (NO 3)3. BiO (NO 3) | At | Rn | |||
| Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||
| Ce (NO 3)3. Ce (NO 3)4 | Nd (NO 3)3 | Eu (NO 3)3 | Gd (NO 3)3 | Tb (NO 3)3 | |||||||||||||
| Th (NO 3)4 | UO2(NO 3)2 | Bk | Cf | Es | Fm | Md | № | Lr | |||||||||