 Добавление нуклеофильного конъюгата
Добавление нуклеофильного конъюгата Добавление нуклеофильного конъюгата - это тип органической реакции. Обычные нуклеофильные добавки или 1,2-нуклеофильные добавки в основном относятся к присоединениям к карбонильным соединениям. Простые алкеновые соединения не показывают реакционной способности 1,2 из-за отсутствия полярности, если алкен не активирован специальными заместителями. С α, β-ненасыщенными карбонильными соединениями, такими как циклогексенон, из резонансных структур можно сделать вывод, что положение β является электрофильным сайтом, который может реагировать с нуклеофилом.. Отрицательный заряд в этих структурах хранится в виде алкоксид- аниона. Такое нуклеофильное присоединение называется присоединением нуклеофильного конъюгата или 1,4-нуклеофильным присоединением. Наиболее важными активными алкенами являются упомянутые выше сопряженные карбонилы и акрилонитрилы.
Добавление конъюгата является винилогичным аналогом прямого нуклеофильного добавления. A Нуклеофильные вступает в реакцию с amp; alpha ;, amp; beta; ненасыщенным карбонильным соединением в положении бета. Отрицательный заряд, переносимый нуклеофилом, теперь делокализован в алкоксид-анионе и α- карбанионе углерода за счет резонанса. Протонирование через кето-енольную таутомерию приводит к насыщенному карбонильному соединению. При вицинальной дифункциональности протон заменяется другим электрофилом.
Добавление конъюгата эффективно при образовании новых углерод-углеродных связей с помощью металлоорганических реагентов, таких как реакция иодистого цинка с метилвинилкетоном.
![(4R ', 5R') - 5- (5-Этил-2,2-диметил- [1,3] диоксолан-4-ил) -пентан-2-он](https://upload.wikimedia.org/wikipedia/commons/7/7b/Conjugateadditionexample.png)
Примером асимметричного синтеза путем присоединения конъюгата является синтез (R) -3-фенилциклогексанона из циклогексенона, фенилбороновой кислоты, родиевого катализатора acac и хирального лиганда BINAP.

В другом примере асимметрического синтеза amp; alpha ;, β-ненасыщенный карбонильное соединение первое взаимодействует с хиральным имидазолидиноном катализатором и хиральными вспомогательным реагентом к иминию соединению в Алкилимино-де-оксо-bisubstitution, который затем вступает в реакцию энантиоселективный с фураном нуклеофилом. Непосредственным продуктом реакции является нуклеофильный енамин, и реакция каскадируется с отрывом хлора от хлорированного хинона. После удаления аминного катализатора кетон эффективно функционализируется нуклеофилом и электрофилом с соотношением син: анти 8: 1 и 97% энантиомерным избытком.
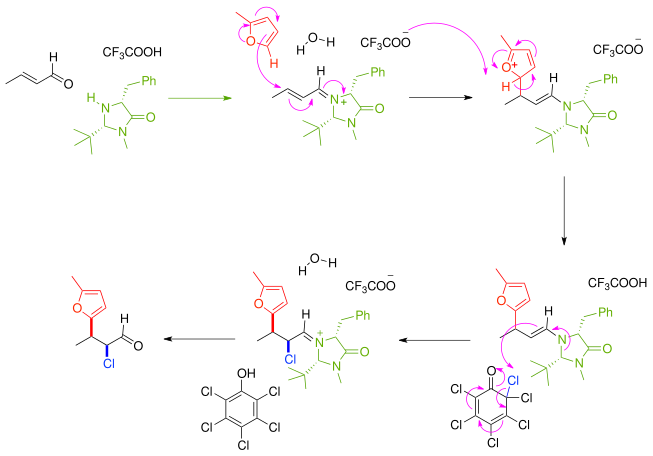
Этот принцип также применяется при энантиоселективном многокомпонентном домино- конъюгированном добавлении нуклеофильных тиолов, таких как бензилмеркаптан и электрофильный DEAD.

Подходящие растворимые акцепторы Михаэля токсичны, потому что они алкилируют ДНК путем присоединения конъюгата. Такая модификация вызывает мутации, которые являются цитотоксическими и канцерогенными. Однако глутатион также может реагировать с ними, и, например, с ними реагирует диметилфумарат.