 Медный гальванический станок для нанесения слоев ПП
Медный гальванический станок для нанесения слоев ПП Гальваника - это общее название процессов, которые создают покрытие из металла на твердой подложке посредством восстановления катионов этого металла с помощью постоянный электрический ток. Покрываемая часть действует как катод (отрицательный электрод ) электролитической ячейки ; электролит представляет собой раствор соли соли металла, на который наносится покрытие; и анод (положительный электрод) обычно представляет собой блок из этого металла или некоторого инертного проводящего материала. Ток подается от внешнего источника питания..
Гальваника широко используется в промышленности и декоративном искусстве для улучшения качества поверхности объектов, например устойчивости к истиранию и коррозия, смазывающая способность, отражательная способность, электрическая проводимость или внешний вид. Его также можно использовать для увеличения толщины деталей меньшего размера или изношенных деталей или для изготовления металлических пластин сложной формы - процесс, называемый гальванопластикой. Он также используется для очистки металлов, таких как медь.
. Термин «гальваника» также может иногда использоваться для процессов, в которых используется электрический ток для достижения окисления анионов на твердую подложку, как при образовании хлорида серебра на серебряной проволоке для изготовления электродов из серебра / хлорида серебра.
Электрополировка, процесс, при котором для удаления катионы металлов с поверхности металлического предмета можно рассматривать как противоположность гальванизации.
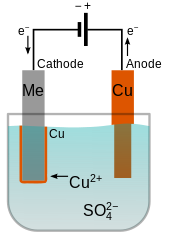 Упрощенная диаграмма гальванического покрытия меди (оранжевый) на конусе Дуктивный объект (катод, «Я», серый). Электролит представляет собой раствор сульфата меди CuSO. 4. Медный анод используется для пополнения электролита катионами меди Cu. по мере того, как они наносятся на катод.
Упрощенная диаграмма гальванического покрытия меди (оранжевый) на конусе Дуктивный объект (катод, «Я», серый). Электролит представляет собой раствор сульфата меди CuSO. 4. Медный анод используется для пополнения электролита катионами меди Cu. по мере того, как они наносятся на катод. Электролит должен содержать положительные ионы (катионы) осаждаемого металла. Эти катионы восстанавливаются на катоде до металла в нулевом валентном состоянии. Например, электролитом для меднения может быть раствор сульфата меди (II), который диссоциирует на катионы Cu и анионы SO. 4. На катоде Cu восстанавливается до металлической меди за счет получения двух электронов.
Когда анод изготовлен из металла покрытия, там может происходить обратная реакция, превращающая его в растворенные катионы. Например, медь окисляется на аноде до Cu, теряя два электрона. В этом случае скорость растворения анода будет равна скорости нанесения покрытия на катод, и, таким образом, ионы в ванне электролита будут постоянно пополняться анодом. Конечным результатом является эффективный перенос металла от анодного источника к катоду.
Вместо этого анод может быть изготовлен из материала, который сопротивляется электрохимическому окислению, такого как свинец или углерод. Кислород, перекись водорода или некоторые другие побочные продукты затем образуются на аноде. В этом случае ионы металла, подлежащего нанесению покрытия, должны периодически пополняться в ванне по мере их извлечения из раствора.
Покрытие чаще всего представляет собой отдельный металлический элемент, а не сплав. Однако некоторые сплавы могут быть подвергнуты электроосаждению, в частности, латунь и припой. Гальванические «сплавы» не являются настоящими сплавами, то есть твердыми растворами, а скорее дискретными крошечными кристаллами покрываемых металлов. В случае плакированного припоя иногда считается необходимым иметь «настоящий сплав», и плакированный припой плавится, чтобы позволить олову и свинцу объединиться с образованием настоящего сплава. Настоящий сплав более устойчив к коррозии, чем сплав с покрытием.
Многие ванны для нанесения покрытия содержат цианиды других металлов (например, цианид калия ) в дополнение к цианидам осаждаемого металла. Эти свободные цианиды способствуют коррозии анода, помогают поддерживать постоянный уровень ионов металлов и повышают проводимость. Кроме того, для увеличения проводимости могут быть добавлены неметаллические химические вещества, такие как карбонаты и фосфаты.
Если гальваника на определенных участках подложки нежелательна, применяются ограничители для предотвращения контакта ванны с подложкой. Типичные защитные покрытия включают ленту, фольгу, лаки и воски.
. Способность покрытия равномерно покрывать поверхность называется отбрасывающей силой; чем выше метательная сила, тем более однородное покрытие.
Первоначально можно использовать специальное покрытие, называемое ударом или вспышкой, для образования очень тонкого (обычно толщиной менее 0,1 мкм)) покрытие с высоким качеством и хорошей адгезией к основанию. Это служит основой для последующих процессов нанесения покрытия. Для удара используется высокая плотность тока и ванна с низкой концентрацией ионов. Этот процесс медленный, поэтому после получения желаемой толщины покрытия используются более эффективные способы нанесения покрытия.
Ударный метод также используется в сочетании с нанесением покрытия на различные металлы. Если желательно нанести один тип покрытия на металл для улучшения коррозионной стойкости, но этот металл по своей природе имеет плохую адгезию к подложке, сначала можно нанести удар, совместимый с обоими. Одним из примеров такой ситуации является плохая адгезия электролитического никеля к цинковым сплавам, и в этом случае используется медный стержень, который хорошо сцепляется с обоими.
Электрохимическое осаждение обычно используется для выращивания металлов и проводящих оксидов металлов из-за следующих преимуществ: толщину и морфологию наноструктуры можно точно контролировать, регулируя электрохимические параметры; относительно однородные и компактные отложения могут быть синтезированы в структурах на основе темплатов; получаются более высокие скорости осаждения; а оборудование недорогое из-за отсутствия требований ни к высокому вакууму, ни к высокой температуре реакции.
Процесс импульсного гальванического покрытия или импульсного электроосаждения (PED) включает быстрое чередование электрического потенциала или тока между двумя разными значениями, в результате чего получается серия импульсов одинаковой амплитуды, длительности и полярности, разделенных нулевым током. Изменяя амплитуду и ширину импульса, можно изменить состав и толщину осажденной пленки.
Экспериментальные параметры импульсного гальванического покрытия обычно состоят из пикового тока / потенциала, рабочего цикла, частоты и эффективного тока / потенциала. Пиковый ток / потенциал - это максимальное значение тока или потенциала гальваники. Рабочий цикл - это эффективная часть времени в течение определенного периода гальваники с приложенным током или потенциалом. Эффективный ток / потенциал рассчитывается путем умножения рабочего цикла на пиковое значение тока или потенциала. Импульсное гальваническое покрытие может помочь улучшить качество гальванической пленки и снять внутреннее напряжение, возникающее во время быстрого осаждения. Комбинация короткого рабочего цикла и высокой частоты может уменьшить поверхностные трещины. Однако для поддержания постоянного эффективного тока или потенциала может потребоваться высокопроизводительный источник питания, обеспечивающий высокий пиковый ток / потенциал и быстрое переключение. Другой распространенной проблемой импульсного гальванического покрытия является то, что анодный материал может быть покрыт и загрязнен во время обратного гальванического покрытия, особенно из-за дорогостоящего инертного электрода, такого как платина.
. Другие факторы, которые могут повлиять на импульсное гальваническое покрытие, включают температуру, анод -катодный зазор и перемешивание. Иногда импульсное гальваническое покрытие может выполняться в нагретой гальванической ванне для увеличения скорости осаждения, поскольку скорость почти всех химических реакций экспоненциально возрастает с температурой в соответствии с законом Аррениуса. Зазор между анодом и катодом связан с распределением тока между анодом и катодом. Небольшое отношение площади зазора к площади образца может вызвать неравномерное распределение тока и повлиять на топологию поверхности образца с покрытием. Перемешивание может увеличить скорость переноса / диффузии ионов металла из объема раствора к поверхности электрода. Настройки перемешивания различаются для разных процессов гальваники металла.
Тесно связанным процессом является гальваническое покрытие щеткой, при котором локализованные области или целые предметы покрываются щеткой, пропитанной раствором для гальваники. Кисть, как правило, представляет собой корпус из нержавеющей стали, обернутый абсорбирующей тканью материалом, который удерживает раствор для нанесения покрытия и предотвращает прямой контакт с покрываемым элементом, соединяется с анодом . источника питания низкого напряжения постоянного тока, и элемент, который необходимо покрыть, подсоединен к катоду. Оператор окунает кисть в раствор для покрытия, затем наносит его на предмет, непрерывно перемещая щетку, чтобы равномерно распределить материал покрытия.
Щеточное гальваническое покрытие имеет несколько преимуществ по сравнению с покрытием резервуаров, включая портативность, способность наносить покрытие на предметы, которые по какой-то причине не могут быть покрыты резервуаром (одним из применений было покрытие участков очень больших декоративных опорных колонн при реставрации здания), низкие требования к маскировке или ее отсутствие и сравнительно низкие требования к объему раствора для нанесения покрытия. Недостатки по сравнению с металлизацией резервуара могут включать большее участие оператора (покрытие резервуара часто может выполняться с минимальным вниманием) и невозможность достичь такой большой толщины листа.
Твердый хром является одним из наиболее распространенных материалов покрытия, используемых для твердого покрытия и гальваники, благодаря своей прочности, устойчивости и гладкой поверхности. Однако хром очень опасен в своем шестивалентном состоянии. При вдыхании или употреблении содержащийся в воздухе Cr [JT2] связан с раком легких и вызывает повреждение горла, рта и носа.
Это связано с тем, что в шестивалентном состоянии хром обладает канцерогенными и тератогенными свойствами, что оказывает мутагенное действие на клетки.
Ежегодно 558 000 технических специалистов в США подвергаются воздействию шестивалентного хрома на рабочем месте, при этом те, кто работает в гальванической, сварочной и лакокрасочной промышленности, подвергаются наибольшему риску из-за повышенного воздействия высоких уровней соединений Cr.
Из-за опасностей, связанных с шестивалентным хромом, поиск более безопасных и экологически чистых альтернатив был основным двигателем исследований щеточного гальванического покрытия в последнее десятилетие. Одной из разработанных альтернатив является композиты с металлической матрицей (MMC). MMC предлагает уникальные превосходные характеристики для металлических покрытий, включая твердость, износостойкость и защиту от окисления при высоких температурах. Эта альтернатива хрому MMC включает в себя и.
Этот метод гальваники является одним из наиболее часто используемых в промышленности для большого количества небольших объектов. Объекты помещаются в бочкообразную непроводящую клетку, а затем погружаются в химическую ванну, содержащую взвешенные атомы металла, который должен быть нанесен на них. Затем ствол вращается, и электрические токи проходят через различные части ствола, замыкая цепи, когда они касаются друг друга. В результате получается очень однородный и эффективный процесс нанесения покрытия, хотя отделка конечных продуктов, вероятно, будет страдать от истирания во время процесса нанесения покрытия. Он не подходит для декоративных или точно спроектированных предметов.
Чистота важна для успешного гальванического покрытия, поскольку молекулярные слои масла могут предотвратить адгезию покрытия. ASTM B322 - стандартное руководство по очистке металлов перед нанесением гальванических покрытий. Очистка включает очистку растворителем, очистку горячим щелочным моющим средством, электроочистку, кислотную обработку и т. Д. Наиболее распространенным промышленным тестом на чистоту является испытание на разрыв воды, при котором поверхность тщательно ополаскивается и удерживается в вертикальном положении. Гидрофобные загрязнители, такие как масла, заставляют воду рассыпаться и рассыпаться, позволяя воде быстро стекать. Идеально чистые металлические поверхности гидрофильны и будут удерживать непрерывный слой воды, который не скатывается и не стекает. ASTM F22 описывает версию этого теста. Этот тест не обнаруживает гидрофильных загрязнителей, но гальваника может легко их вытеснить, поскольку растворы на водной основе. Поверхностно-активные вещества, такие как мыло, снижают чувствительность теста и должны быть тщательно смыты.
Гальваника изменяет химические, физические и механические свойства детали. Примером химического изменения может служить покрытие никелем, улучшающее коррозионную стойкость. Примером физического изменения является изменение внешнего вида. Примером механического изменения является изменение прочности на разрыв или поверхностной твердости, что является обязательным атрибутом в инструментальной промышленности. Гальваническое покрытие кислотным золотом нижележащих медных или никелированных цепей снижает контактное сопротивление, а также твердость поверхности. Покрытые медью участки из мягкой стали действуют как маска, если упрочнение таких участков нежелательно. Луженая сталь хромируется, чтобы предотвратить потускнение поверхности из-за окисления олова.
Гальваническое или химическое нанесение покрытия может использоваться как способ сделать металлическую деталь радиоактивной с помощью водного раствора, приготовленного из концентратов никель– фосфор, которые содержат радиоактивные гипофосфит P ионы.
Существует ряд альтернативных способов получения металлических покрытий на твердых субстратах, которые не включают электролитическое восстановление:
 Парфянская батарея
Парфянская батарея  Луиджи Валентино Бругнателли
Луиджи Валентино Бругнателли  Борис Якоби разработал гальванику, электротипирование и гальванопластическую скульптуру в России
Борис Якоби разработал гальванику, электротипирование и гальванопластическую скульптуру в России Считается, что первые гальванические покрытия были сделаны в эпоху Парфянской империи. Вильгельм Кёниг был ассистентом в Национальном музее Ирака в 1930-х годах наблюдал ряд очень тонких серебряных предметов из древнего Ирака, покрытых очень тонкими слоями золота, и предположил, что они были гальваническими. Он подтвердил свою идею, объяснив парфянскую батарею, которая была обнаружена в 1938 году возле метрополии Ктесифон, столицы парфян (150 г. до н.э. - 223 г. н.э.) и Сасанидские (224–650 гг. Н.э.) империи Персии. однако неопровержимые доказательства использования парфянских батарей являются предметом споров среди исследователей.
Современная электрохимия была изобретена итальянским химиком Луиджи Валентино Бругнателли в 1805 году. Бругнателли использовал свои коллега Алессандро Вольта изобрел пятью годами ранее гальваническую батарею для облегчения первого электроосаждения. Изобретения Бругнателли были запрещены Французской академией наук и не стали использоваться в общей промышленности в течение следующих тридцати лет. К 1839 году ученые из Британии и России независимо друг от друга разработали процессы осаждения металлов, аналогичные методам Бругнателли, для гальванического покрытия медью пластин печатного станка .
 Гальванопластическая скульптура на ул. Исаакиевский собор в Санкт-Петербурге
Гальванопластическая скульптура на ул. Исаакиевский собор в Санкт-Петербурге Борис Якоби в России не только заново открыл гальванопластику, но и разработал гальванопластику и гальванопластическую скульптуру. Гальванопластика быстро вошла в моду в России, и такие люди, как изобретатель Петр Багратион, ученый Генрих Ленц и писатель-фантаст Владимир Одоевский, внесли свой вклад в дальнейшее развитие технологии. технологии. Среди наиболее громких случаев применения гальваники в России середины XIX века были гигантские гальванопластические скульптуры Св. Исаакиевский собор в Санкт-Петербурге и позолоченный купол Храма Христа Спасителя в Москве, самая высокая православная церковь в мире.
 Никелирование
Никелирование Вскоре после Джон Райт из Бирмингема Англия обнаружила, что цианистый калий является подходящим электролит для гальваники золота и серебра. Сподвижники Райта, Джордж Элкингтон и Генри Элкингтон, получили первые патенты на гальванику в 1840 году. Эти двое затем основали гальваническую промышленность в Бирмингеме, откуда она распространилась по всему миру. Электрический генератор Вулрича 1844 года, ныне находящийся в Thinktank, Бирмингемский музей науки, - это самый ранний электрический генератор, использовавшийся в промышленности. Он использовался Элкингтоном.
Norddeutsche Affinerie в Гамбурге был первым современным гальваническим заводом, начавшим производство в 1876 году.
Как наука о Электрохимия выросла, стала понятна ее связь с гальваникой и были разработаны другие виды недекоративной гальваники металлов. Промышленное гальваническое покрытие никеля, латуни, олова и цинка было разработано к 1850-м годам. Гальванические ванны и оборудование, основанные на патентах Elkingtons, были увеличены для размещения покрытия многочисленных крупномасштабных объектов и для конкретных производственных и инженерных приложений.
Гальваническая промышленность получила большой импульс с появлением в конце 19 века электрических генераторов. При наличии более высоких токов металлические компоненты машин, оборудование и автомобильные детали, требующие защиты от коррозии и улучшенных свойств износа, а также лучшего внешнего вида, могут обрабатываться в больших объемах.
Две мировые войны и растущая авиационная промышленность дали толчок к дальнейшим разработкам и усовершенствованиям, включая такие процессы, как твердое хромирование, бронзовый сплав гальваника, сульфаматное никелирование и множество других процессов гальваники. Гальваническое оборудование превратилось из деревянных резервуаров с гудроном с ручным приводом в автоматизированное оборудование, способное обрабатывать тысячи килограммов в час деталей.
Одним из первых проектов американского физика Ричарда Фейнмана была разработка технологии гальванического нанесения металла на пластик. Фейнман превратил оригинальную идею своего друга в успешное изобретение, позволив своему работодателю (и другу) сдержать коммерческие обещания, которые он дал, но не смог бы выполнить иначе.
 Раствор цинка, испытанный в ячейке Халла
Раствор цинка, испытанный в ячейке Халла  Ячейка Харинга – Блюма
Ячейка Харинга – Блюма Ячейка Халла - это тип испытательной ячейки, используемой для качественной проверки состояния гальванической ванны. Он позволяет оптимизировать диапазон плотности тока, оптимизировать концентрацию добавок, распознавать эффекты примесей и указывать способность к выбросу макроэлементов. Ячейка Халла воспроизводит гальваническую ванну в лабораторных масштабах. Он заполнен образцом гальванического раствора, соответствующий анод подключен к выпрямителю . «Работу» заменяют испытательной панелью с ячейками корпуса, на которую будет нанесено покрытие, чтобы показать «здоровье» ванны.
Ячейка Корпуса представляет собой контейнер трапециевидной формы, вмещающий 267 мл раствора. Такая форма позволяет размещать испытательную панель под углом к аноду. В результате осаждение наносится при различной плотности тока, которую можно измерить линейкой корпуса. Объем раствора позволяет количественно оптимизировать концентрацию добавки: добавление 1 грамма к 267 мл эквивалентно 0,5 унции / галлон в гальваническом резервуаре.
Харинга-Блюма Ячейка используется для определения макро-метательной способности гальванической ванны. Ячейка состоит из двух параллельных катодов с фиксированным анодом посередине. Катоды находятся на расстоянии от анода в соотношении 1: 5. Бросковая мощность макроса рассчитывается из толщины покрытия на двух катодах, когда постоянный ток пропускается в течение определенного периода времени. Ячейка изготовлена из плексигласа или стекла.