 | |
| Имена | |
|---|---|
| Название IUPAC Медь (I) йодид | |
| Другие названия Йодид меди, маршит | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.795 |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химические формула | CuI |
| Молярная масса | 190,45 г / моль |
| Внешний вид | Порошок цвета от белого до коричневого |
| Запах | без запаха |
| Плотность | 5,67 г / см |
| Точка плавления | 606 ° C (1123 ° F; 879 K) |
| Точка кипения | 1290 ° C (2350 ° F; 1560 K) (разлагается) |
| Растворимость в воде | 0,000042 г / 100 мл |
| произведение растворимости (Ksp) | 1 x 10 |
| Растворимость | растворим в растворах аммиака и йодида. нерастворим в разбавленных кислотах |
| Давление пара | 10 мм рт. Ст. (656 ° C) |
| Магнитная восприимчивость (χ) | -63,0 · 10 см / моль |
| Показатель преломления (nD) | 2,346 |
| Структура | |
| Кристаллическая структура | цинковая обманка |
| Координационная геометрия | Тетраэдрические анионы и катионы |
| Опасности | |
| Паспорт безопасности | Sigma Aldrich |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H302, H315, H319, H335, H400, H410 |
| Меры предосторожности GHS | P261, P273, P305 + 351 + 338, P501 |
| NFPA 704 (огненный алмаз) |  1 1 0 1 1 0 |
| Температура вспышки | Невоспламеняющийся |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимо) | TWA 1 мг / м (как Cu) |
| REL (рекомендуется) | TWA 1 мг / м (как Cu) |
| IDLH (Непосредственная опасность) | TWA 100 мг / м (как Cu) |
| Родственные соединения | |
| Другие анионы | |
| Прочие катионы | йодид серебра |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на информационные панели | |
Иодид меди (I) - это неорганическое соединение формулы CuI. Он также известен как йодид меди . Его можно использовать в различных областях, от органического синтеза до затравки облаков.
Чистый йодид меди (I) имеет белый цвет, но его образцы часто желтовато-коричневого цвета или даже, если встречаются в природе, как редкие минерал маршит, красновато-коричневый, но такой цвет обусловлен наличием примесей. Обычно образцы йодидсодержащих соединений обесцвечиваются из-за легкого аэробного окисления иодид-аниона до молекулярного йода.
Медь (I) йодид, как и большинство бинарных (содержащих только два элемента) металлов галогениды, представляет собой неорганический полимер. Он имеет богатую фазовую диаграмму, что означает, что он существует в нескольких кристаллических формах. Он имеет структуру цинковой обманки при температуре ниже 390 ° C (γ-CuI), структуру вюрцита при температуре от 390 до 440 ° C (β-CuI) и каменную соль . структура при температуре выше 440 ° C (α-CuI). Ионы имеют тетраэдрическую координацию в структуре цинковой обманки или вюрцита с расстоянием Cu-I 2,338 Å. Бромид меди (I) и хлорид меди (I) также трансформируются из структуры цинковой обманки в структуру вюрцита при 405 и 435 ° C соответственно. Следовательно, чем больше длина связи галогенид меди, тем ниже должна быть температура, чтобы изменить структуру от структуры цинковой обманки к структуре вюрцита. Межатомные расстояния в бромиде меди (I) и хлориде меди (I) составляют 2,173 и 2,051 Å соответственно.
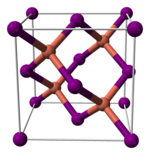 | 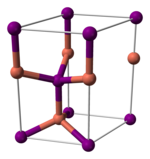 |  |
Иодид меди (I) можно получить путем нагревания йода и меди в концентрированной иодоводородной кислоте, HI. Однако в лаборатории иодид меди (I) получают простым смешиванием водного раствора иодида калия и растворимой соли меди (II), такой как сульфат меди.
CuI 2 быстро разлагается до иодида меди (I) с выделением I 2.
Эта реакция была использована в качестве средства анализа образцов меди (II), так как выделившийся I 2 можно анализировать окислительно-восстановительным титрованием. Сама по себе реакция может выглядеть довольно странно, поскольку при использовании практического правила для протекающей окислительно-восстановительной реакции, E окислитель - E восстановитель>0, эта реакция не проходит.. Количество ниже нуля, поэтому реакция не должна продолжаться. Но константа равновесия реакции равна 1,38 * 10. При использовании довольно умеренных концентратов 0,1 моль / л как для йодида, так и для Cu, концентрация Cu рассчитывается как 3 * 10. Как следствие, произведение концентраций намного превышает произведение растворимости, поэтому йодид меди (I) выпадает в осадок. Процесс осаждения снижает концентрацию меди (I), обеспечивая энтропийную движущую силу в соответствии с принципом Ле Шателье и позволяя протекать окислительно-восстановительной реакции.
CuI плохо растворяется в воде (0,00042 г / л при 25 ° C), но растворяется в присутствии NaI или KI с образованием линейного аниона [CuI 2 ]. При разбавлении таких растворов водой переосаждается CuI. Этот процесс растворения-осаждения используется для очистки CuI с получением бесцветных образцов.
Иодид меди (I) может быть растворен в ацетонитриле, давая раствор различных комплексных соединений. После кристаллизации можно выделить молекулярные или полимерные соединения. Растворение также наблюдается, когда используется раствор соответствующего комплексообразователя в ацетоне или хлороформе. Например, можно использовать тиомочевину и ее производные. Твердые вещества, которые кристаллизуются из этих растворов, состоят из гибридных неорганических цепей.
CuI имеет несколько применений:
| На Викискладе есть материалы, связанные с йодидом меди (I). |