| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Тиомочевина | |||
| Другие названия Тиокарбамид | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 605327 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.000.494 | ||
| Справочник Gmelin | 1604 | ||
| KEGG | |||
| PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2811 | ||
| Панель управления CompTox (EPA) | |||
InChI
| |||
| SMILES | |||
| >C (= S) (N) N | |||
| Свойства | |||
| Химическая формула | CH4N2S | ||
| Молярная масса | 76,12 г / моль | ||
| Внешний вид | белое твердое вещество | ||
| Плотность | 1,405 г / мл | ||
| Температура плавления | 182 ° C (360 ° F; 455 K) | ||
| Растворимость в воде | 142 г / л (25 ° C) | ||
| Магнитная восприимчивость (χ) | -4,24 × 10 см / моль | ||
| Опасности | |||
| EU классификация (DSD) (устаревшая) | Carc. Кошка. 3. Репр. Кошка. 3. Вредно (Xn). Опасно для окружающей среды (N) | ||
| R-фразы (устаревшие) | R22, R40, R51 / 53, R63 | ||
| S-фразы (устаревший) | (S2), S36 / 37, S61 | ||
| NFPA 704 (огненный алмаз) |  1 3 0 1 3 0 | ||
| Родственные соединения | |||
| Родственные соединения | Мочевина | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Тиомочевина () - это сероорганическое соединение с формулой S C (N H 2)2. Это структурно аналогичен мочевине, за исключением того, что атом кислорода заменен атомом серы, но свойства мочевины и тиомочевины значительно различаются. Тиомочевина является реагентом в органический синтез. «Тиомочевины» относятся к широкому классу соединений с общей структурой (RRN) (RRN) C = S. Тиомочевины относятся к тиоамидам, например RC (S) NR 2, где R представляет собой метил, этил и т.д.
 Ген Основная химическая структура тиомочевины
Ген Основная химическая структура тиомочевины Тиомочевина - это плоская молекула. Расстояние связи C = S составляет 1,71 Å. Расстояние C-N составляет в среднем 1,33 Å. На ослабление связи C-S за счет пи-связи C-N указывает короткая связь C = S в тиобензофеноне, которая составляет 1,63 Å.
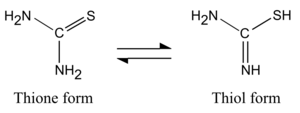
Тиомочевина существует в двух таутомерных формах, из которых тионовая форма преобладает в водных растворах. константа равновесия была рассчитана, как K eq равно 1,04 × 10. Форма тиола, которая также известна как изотиомочевина, может встречаться в замещенных соединениях, таких как соли изотиоурония 34.
Мировое годовое производство тиомочевины составляет около 10 000 тонн. Около 40% производится в Германии, еще 40% в Китае и 20% в Японии. Тиомочевина может быть произведена из тиоцианата аммония, но чаще ее получают реакцией сероводорода с цианамидом кальция в присутствии диоксида углерода..
Тиомочевина как таковая имеет несколько применений. В основном он потребляется в качестве предшественника диоксида тиомочевины, который является обычным восстановителем в текстильной промышленности.
Другие промышленные применения тиомочевины включают производство пламени. смолы-замедлители и ускорители вулканизации .
Тиомочевина используется в качестве вспомогательного вещества в диазобумаге, светочувствительной фотокопировальной бумаге и почти во всех других типах копировальной бумаги.
Он также используется для тонирования серебряно-желатиновых фотопринтов.
Тиомочевина используется в процессах яркого и полублестящего гальванического покрытия Клифтона-Филлипса и Бивера. Он также используется в растворе с хлоридом олова (II) в качестве раствора для химического лужения для меди печатных плат.
Материал имеет необычное свойство превращаться в аммоний. тиоцианат при нагревании выше 130 ° C. При охлаждении соль аммония снова превращается в тиомочевину.
Тиомочевина восстанавливает пероксиды до соответствующих диолов. Промежуточным продуктом реакции является нестабильный эндопероксид.

. Тиомочевина также используется в восстановительной обработке озонолиза с получением карбонильных соединений. Диметилсульфид также является эффективным реагентом для этой реакции, но он очень летуч (температура кипения 37 ° C) и имеет неприятный запах, тогда как тиомочевина не имеет запаха и обычно нелетучая (что отражает ее полярность).

Тиомочевина используется в качестве источника сульфида, например, для превращения алкилгалогенидов в тиолы. В реакции используется высокая нуклеофильность серного центра и легкий гидролиз промежуточного соединения изотиоурониевой соли :
В этом примере этан-1,2-дитиол получают из 1, 2-дибромэтан :
Как и другие тиоамиды, тиомочевина может служить источником сульфида при реакция с ионами металлов. Например, сульфид ртути образуется при обработке солей ртути в водном растворе тиомочевиной:
Эти реакции сульфидирования, которые применялись для синтеза многих сульфидов металлов, требуют воды и, как правило, некоторого нагревания.
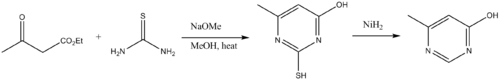
Тиомочевины являются строительными блоками для производных пиримидина. Таким образом, тиомочевины конденсируются с β-дикарбонильными соединениями. Аминогруппа тиомочевины сначала конденсируется с карбонилом с последующей циклизацией и таутомеризацией. Обессеривание дает пиримидин.
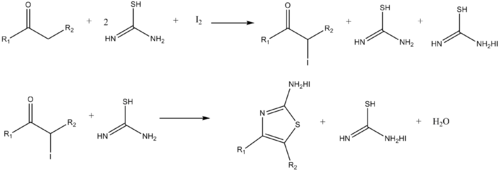
Аналогичным образом аминотиазолы могут быть синтезированы реакцией α-галоген кетонов и тиомочевины.
Фармацевтические препараты тиобарбитуровой кислоты и сульфатиазола получают с использованием тиомочевина. 4-амино-3-гидразино-5-меркапто-1,2,4-триазол получают реакцией тиомочевины и гидразина.
Согласно этикетке на потребительском продукте, жидкое чистящее средство для серебра TarnX содержит тиомочевину, моющее средство и сульфаминовую кислоту. выщелачивающий агент для выщелачивания золота и серебра может быть создан путем избирательного окисления тиомочевины, минуя стадии использования цианида и плавления.
LD50 для тиомочевины является 125 мг / кг для крыс (перорально).