В биохимии, фенолы природного происхождения относятся к фенолу функциональная группа, которая содержится в натуральных продуктах. Фенольные соединения вырабатываются растениями и микроорганизмами. Организмы иногда синтезируют фенольные соединения в ответ на экологическое давление, такое как нападение патогенов и насекомых, УФ-излучение и ранения. Поскольку они присутствуют в пище, потребляемой в рационе человека, и в растениях, используемых в традиционной медицине нескольких культур, их роль в здоровье человека и болезнях является предметом исследования. Некоторые фенолы обладают бактерицидным действием и используются при приготовлении дезинфицирующих средств.
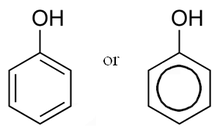 Фенол - простейший из фенолов.
Фенол - простейший из фенолов.  Химическая структура салициловой кислоты, активного метаболита аспирина.
Химическая структура салициловой кислоты, активного метаболита аспирина.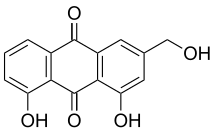 Химическая структура алоэ эмодин, дифенол.
Химическая структура алоэ эмодин, дифенол.  Кверцетин, типичный флавоноид, представляет собой полифенол.
Кверцетин, типичный флавоноид, представляет собой полифенол.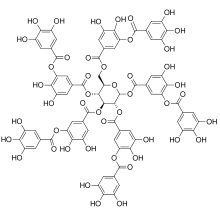 Дубильная кислота, типичный полифенол неопределенной структуры.
Дубильная кислота, типичный полифенол неопределенной структуры. 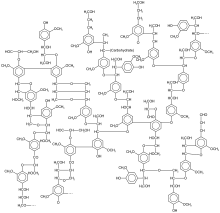 Лигнин составляет около 25% от состава древесины. Обратите внимание, что эта структура повторяется много раз в каждой молекуле лигнина.
Лигнин составляет около 25% от состава древесины. Обратите внимание, что эта структура повторяется много раз в каждой молекуле лигнина. Могут применяться различные схемы классификации. Обычно используемая схема основана на количестве атомов углерода и была разработана Джеффри Харборном и Симмондсом в 1964 году и опубликована в 1980 году:
| Число атомов углерода | Основной скелет | Число фенольных циклов | Класс | Примеры | ||||
|---|---|---|---|---|---|---|---|---|
| 6 | C6 | 1 | Простые фенолы, Бензохиноны | Катехол, гидрохинон, 2,6-диметоксибензохинон | ||||
| 7 | C6-C1 | 1 | Фенольные кислоты, Фенольные альдегиды | Галловая, салициловая кислоты | ||||
| 8 | C6-C2 | 1 | Ацетофеноны, производные тирозина, Фенилуксусные кислоты | 3-Ацетил-6-метоксибензальдегид, Тирозол, п-гидроксифенилуксусная кислота, гомогентизиновая кислота | ||||
| 9 | C6-C3 | 1 | гидроксикоричная кислота, фенилпропены, кумарины, изокумарины, Хромоны | Кофеиновая, феруловая кислоты, миристицин, эвгенол, умбеллиферон, эскулетин, евгенин | ||||
| 10 | C6-C4 | 1 | нафтохиноны | юглон, плюмбагин | ||||
| 13 | C6-C1-C6 | 2 | ксантоноиды | мангиферин>14 | C6-C2-C6 | 2 | Стилбеноиды, Антрахиноны | Ресвератрол, Эмодин |
| 15 | C6-C3-C6 | 2 | Халконоиды, Флавоноиды, Изофлавоноиды, Неофлавоноиды | Кверцетин, цианидин, Генистеин | ||||
| 16 | C6-C4-C6 | 2 | Галогенированные фенольные соединения водорослей | , | ||||
| 18 | (C6-C3)2 | 2 | Лигнаны, Неолигнаны | Пинорезинол, Эусидерин | ||||
| 30 | (C6-C3-C6)2 | 4 | Бифлавоноиды | Аментофлавон | ||||
| многие | (C6-C3)n,. (C6)n,. (C6-C3-C6)n | n>12 | Лигнины,. Катехоловые меланины,. Флаволаны (Конденсированные танины ),. Полифенольные белки,. Полифенолы | Малиновый эллагитаннин,. Дубильная кислота |
Не в этой классификации Харборна C 6-C7-C6диарилгептаноиды.
Их также можно классифицировать по в основе их количество фенольных групп. Поэтому их можно назвать простыми фенолами или монофенолами с одной фенольной группой или ди (би), три- и олигофенолами с двумя, тремя или несколькими фенольными группами соответственно.
Разнообразное семейство природных фенолов - это флавоноиды, которые включают несколько тысяч соединений, среди которых флавонолы, флавоны, флаван. -3ol (катехины), флаваноны, антоцианидины и изофлавоноиды.
Фенольные звенья могут быть димеризованы или подвергнуты дальнейшей полимеризации, создавая новый класс полифенолов.. Например, эллаговая кислота представляет собой димер галловой кислоты и образует класс эллагитаннинов, или катехин и галлокатехин могут объединяться с образованием красного соединения теафлавин, процесс, который также приводит к большому классу коричневых теарубигинов в чае.
Два природных фенола из двух разных категорий, например флавоноид и лигнан, могут объединяться с образованием гибридного класса, такого как флавонолигнаны.
Номенклатура полимеров :
| Базовая единица: |  |  |  |
|---|---|---|---|
| Класс / Полимер: | Гидролизуемые танины | Флавоноид, Конденсированные танины |
Растения из рода Humulus и Cannabis продуцируют терпенофенольные метаболиты, соединения, которые являются меротерпенами. Фенольные липиды давно являются алифатическими цепи, связанные с фенольным фрагментом.
Многие природные фенолы хиральны. Примером таких молекул является катехин. Кавикулярин является необычным макроциклом, поскольку он был первым соединением, выделенным из природы, проявляющим оптическую активность из-за наличия планарной хиральности и аксиальной хиральности.
Природные фенолы обладают оптическими свойствами, характерными для бензола, например поглощение около 270 нм. Согласно правилам Вудворда, батохромные сдвиги также часто происходят, что свидетельствует о наличии делокализованных π-электронов, возникающих в результате конъюгации между бензолом и винилами
Поскольку молекулы с более высокими уровнями конъюгации подвергаются этому явлению батохромного сдвига, часть видимого спектра поглощается. Длины волн, оставшиеся в процессе (обычно в красной части спектра), воссоздают цвет конкретного вещества. Ацилирование коричными кислотами антоцианидинов изменило тональность цвета (угол оттенка CIE Lab ) до пурпурного.
. Вот серия УФ видимых спектров молекулы, классифицированные слева направо в соответствии с их уровнем конъюгации:
 УФ-видимый спектр галловой кислоты, с лямбда макс около 270 нм. УФ-видимый спектр галловой кислоты, с лямбда макс около 270 нм. |  УФ-видимый спектр феруловая кислота, с макс. лямбда при 321 и плечом при 278 нм. УФ-видимый спектр феруловая кислота, с макс. лямбда при 321 и плечом при 278 нм. |  УФ-видимый спектр кверцетина с макс. лямбда при 369 нм. УФ-видимый спектр кверцетина с макс. лямбда при 369 нм. |  УФ-видимый спектр цианидин-3-O-глюкозид (хризантемин), с лямбда макс при 518 нм. УФ-видимый спектр цианидин-3-O-глюкозид (хризантемин), с лямбда макс при 518 нм. |
 Химическая структура галловой кислоты, фенольной кислоты. Химическая структура галловой кислоты, фенольной кислоты. | 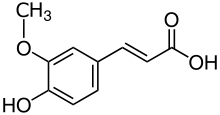 Химическая структура феруловая кислота, гидроксикоричная кислота. Химическая структура феруловая кислота, гидроксикоричная кислота. |  Химическая структура кверцетина, флавонола. Химическая структура кверцетина, флавонола. | 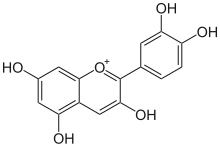 Химическая структура цианидина, антоцианидина. Химическая структура цианидина, антоцианидина. |
Картина поглощения отвечает за красный цвет антоцианов, может дополнять зеленый цвет c хлорофилл в фотосинтетически активных тканях, таких как молодые листья Quercus coccifera.
 Хроматограммы, показывающие окисление димера проантоцианидина B2. В окисленном образце появились новые пики.
Хроматограммы, показывающие окисление димера проантоцианидина B2. В окисленном образце появились новые пики. Природные фенолы являются реакционноспособными видами по отношению к окислению, в частности, сложная смесь фенольных соединений, например, содержащихся в пищевых продуктах, может подвергаться автоокисление в процессе старения. Простые природные фенолы могут приводить к образованию процианидинов B-типа в винах или модельных растворах. Это коррелирует с неферментативным потемнением изменением цвета, характерным для этого процесса. Это явление можно наблюдать в таких пищевых продуктах, как морковное пюре.
потемнение, связанное с окислением фенольных соединений, также рассматривается как причина гибели клеток каллусов, образованных в культурах in vitro. Эти фенольные соединения происходят как из тканей эксплантата, так и из его секретов.
| Каннабиноиды | активные компоненты каннабиса |
| Капсаицин | острое соединение перца чили |
| Карвакрол | найден в, например, орегано ; антимикробное и нейропротекторное вещество |
| Крезол | , обнаруженное в каменноугольной смоле и креозот |
| эстрадиол | эстроген - гормоны |
| эвгенол | основной компонент эфирное масло из гвоздики |
| Галловая кислота | , обнаруженная в галлах |
| Гуаякол | (2-метоксифенол) - имеет дымный аромат, и содержится в жареном кофе, виски и дыме |
| Метилсалицилат | основной составляющей эфирного масла винтергрин |
| кетон малины | соединение с интенсивным малиновым запахом |
| салициловая кислота | соединение-предшественник аспирина (химический синтез используется в производстве) |
| Серотонин / дофамин / адреналин / норадреналин | природные нейротрансмиттеры |
| Тимол | (2-изопропил-5- метилфенол) - содержится в тимьяне ; антисептик, который используется в жидкости для полоскания рта |
| тирозин | аминокислота |
| сезамол | природное соединение, обнаруженное в семенах кунжута |
| фенол | исходное соединение, используемое в качестве дезинфицирующего средства и для химического синтеза |
| бисфенол A | и другие бисфенолы, полученные из кетонов и фенола / крезола |
| BHT | (бутилированный гидрокситолуол) - жирорастворимый антиоксидант и пищевая добавка |
| 4-нонилфенол | продукт распада детергентов и ноноксинол-9 |
| ортофенилфенол | a фунгицид, используемый для восковой обработки цитрусовых |
| пикриновая кислота | (тринитрофенол) - взрывчатое вещество |
| фенолфталеин | индикатор pH |
| Ксиленол | , используемый в антисептических и дезинфицирующих средствах |
Фенолы образуются тремя разными путями биосинтеза: (i) шикимат / хоризмат или сукцинилбензоатный путь, который производит производные фенилпропаноидов (C6 –C3); (ii) ацетат / малонатный или поликетидный путь, который продуцирует фенилпропаноиды с удлиненными боковыми цепями, включая большую группу флавоноидов (C6 – C3 – C6) и некоторые хиноны; и (iii) ацетатно-мевалонатный путь, который дает ароматические терпеноиды, в основном монотерпены, в результате реакций дегидрирования. Ароматическая аминокислота фенилаланин, синтезируемая по пути шикимовой кислоты, является обычным предшественником фенолсодержащих аминокислот и фенольных соединений.
В растениях фенольные звенья этерифицированы или метилированы и подвергаются конъюгации, что означает, что природные фенолы в основном находятся в форма гликозида вместо формы агликона.
В оливковом масле тирозол образует сложные эфиры с жирными кислотами. В ржи алкилрезорцины представляют собой фенольные липиды.
В некоторых ацетилированиях участвуют терпены, например гераниол. Эти молекулы называются меротерпенами (химическое соединение, имеющее частичную структуру терпеноида).
Метилирование может происходить путем образования связи простого эфира на гидроксильных группах с образованием О-метилированных полифенолов. В случае O-метилированного флавона танжеритина все пять гидроксилов метилированы, не оставляя свободных гидроксилов фенольной группы. Метилирование также может происходить непосредственно на углероде бензольного кольца, как в случае пориола, C-метилированного флавоноида.
Грибок белой гнили Phanerochaete chrysosporium может удалять до 80% фенольных соединений из сточных вод коксования.
Танины используются в кожевенной промышленности.
Некоторые природные фенолы могут использоваться в качестве биопестицидов. Фуранофлавоноиды, такие как каранджин или ротеноиды, используются в качестве акарицида или инсектицида.
Энологические дубильные вещества являются важными элементами в аромат вина.
Некоторые фенолы продаются как диетические добавки. Фенолы были исследованы как лекарства. Например, Crofelemer (USAN, торговое название Fulyzaq) - это разрабатываемый препарат для лечения диареи, связанной с лекарствами против ВИЧ. Кроме того, были изготовлены производные фенольного соединения комбретастатин A-4, противораковой молекулы, включающей атомы азота или галогенов для повышения эффективности лечения.
Экстракция фенола - это технология обработки, используемая для получения фенолов в качестве сырья, соединений или добавок для промышленной обработки древесины и химической промышленности.
Экстракция может выполняться с использованием различных растворителей. Существует риск того, что полифенолоксидаза (PPO) ухудшит содержание фенолов в образце, поэтому необходимо использовать ингибиторы PPO, такие как калий дитионит (K2S2O4) или провести эксперимент с использованием жидкого азота или прокипятить образец в течение нескольких секунд (бланширование ), чтобы инактивировать фермент. Дальнейшее фракционирование экстракта может быть достигнуто с использованием колонок для твердофазной экстракции и может привести к выделению индивидуальных соединений.
Извлечение природных фенолов из остатков биомассы является частью биопереработки.
pKa фенольных соединений может быть рассчитано по времени удерживания в жидкостной хроматографии..
В исследованиях по оценке антиоксидантной способности можно использовать электрохимические методы.
Обнаружение может быть выполнено с помощью рекомбинантных люминесцентных бактерий сенсоры.
Фенольное профилирование может быть достигнуто с помощью жидкостной хроматографии-масс-спектрометрии (ЖХ / МС).
Метод для Количественное определение содержания фенола - это объемное титрование. Окислитель, перманганат, используется для окисления стандартных концентраций стандартных растворов с получением стандартной кривой . Затем содержание неизвестных фенолов выражается в эквиваленте соответствующего стандарта.
Некоторые методы количественного определения общего содержания фенолов основаны на колориметрических измерениях. Общее количество фенолов (или антиоксидантный эффект) можно измерить с помощью реакции Фолина-Чокальте. Результаты обычно выражаются в эквивалентах галловой кислоты (GAE). Тест с хлоридом железа (FeCl 3) также является колориметрическим тестом.
Ламейсон и Карнет разработали тест для определения общего содержания флавоноидов в образце (метод AlCI 3). После надлежащего смешивания образца и реагента смесь инкубируют в течение 10 минут при температуре окружающей среды и определяют оптическую плотность раствора при 440 нм. Содержание флавоноидов выражается в мг / г кверцетина.
Результаты количественного анализа, полученные с помощью детектора с диодной матрицей -связанного ВЭЖХ, обычно даются как относительные, а не абсолютные значения, так как отсутствуют коммерчески доступные стандарты для каждой фенольной молекулы. Этот метод также можно сочетать с масс-спектрометрией (например, HPLC – DAD– ESI / MS) для более точной идентификации молекул .
Другие тесты измеряют антиоксидантную способность фракции. В некоторых используется катион-радикал 2,2'-азино-бис (3-этилбензотиазолин-6-сульфоновая кислота) (ABTS ), который реагирует с большинством антиоксидантов, включая фенольные соединения, тиолы и витамин С. Во время этой реакции синий катион-радикал ABTS превращается обратно в свою бесцветную нейтральную форму. За реакцией можно следить спектрофотометрически. Этот анализ часто называют анализом эквивалентной антиоксидантной способности Trolox (TEAC). Реакционная способность различных протестированных антиоксидантов сравнивается с реакционной способностью Trolox, который является аналогом витамина E.
Другие анализы антиоксидантной способности, в которых Trolox используется в качестве стандарта, включают дифенилпикрилгидразил (DPPH), способность поглощения радикалов кислорода (ORAC), способность восстановления железа анализ плазмы (FRAP) или ингибирование катализируемого медью in vitro окисления человеческих липопротеинов низкой плотности.
Также существует анализ клеточной антиоксидантной активности (CAA). Дихлорфлуоресцин - это зонд, который захватывается клетками и легко окисляется до флуоресцентного дихлорфлуоресцеина (DCF). Метод измеряет способность соединений предотвращать образование DCF пероксильными радикалами, генерируемыми 2,2'-азобис (2-амидинопропан) дигидрохлорид (ABAP), в клетках гепатокарциномы HepG2 человека..
Другие методы включают бутилированный гидрокситолуол (BHT), бутилированный гидроксианизол (BHA), метод Rancimat (оценка прогоркания жира). 843>Модели in vivo
Личинки модельного животного Galleria mellonella, также называемые восковые черви, могут быть использованы для проверки антиоксидантного действия отдельных молекул с использованием борной кислоты в пище, чтобы вызвать индуцированный окислительный стресс. Содержание малонового диальдегида, индикатора окислительного стресса, и активности антиоксидантных ферментов супероксиддисмутазы, каталазы, глутатион-S-трансферазы и глутатионпероксидазу можно контролировать. Про фенолоксидазу также можно выделить из насекомого.
Фенольные биосинтетические и метаболические пути и ферменты могут быть изучены с помощью трансгенеза генов. Регуляторный ген Arabidopsis для продукции антоцианина пигмента 1 (AtPAP1) может быть экспрессирован в других видах растений.
Найдены фенолы в мире природы, особенно в царстве растений.
Orobol может быть обнаружена в Streptomyces neyagawaensis (актинобактерии). Фенольные соединения можно найти в cyanobacterium Arthrospira maxima, используемых в пищевой добавке Spirulina. Три цианобактерии Microcystis aeruginosa, Cylindrospermopsis raciborskii и Oscillatoria sp. являются предметом исследования естественного производства бутилированного гидрокситолуола (BHT), антиоксиданта, пищевой добавки и промышленного химического вещества.
Proteobacterium Pseudomonas fluorescens продуцирует флороглюцин, флороглюцинкарбоновую кислоту и диацетилфлорглюцин. Другим примером фенольных соединений, продуцируемых протеобактериями, является 3,5-дигидрокси-4-изопропил-транс-стильбен, бактериальный стильбеноид, продуцируемый бактериальными симбионтами Photorhabdus нематод Heterorhabditis.
Фенольные кислоты могут быть обнаружены у грибов базидиомицетов видов. Например, протокатеховая кислота и пирокатехол содержатся в Agaricus bisporus, а также в других фенилированных веществах, таких как фенилуксусная и фенилпировиноградная кислоты.. Другие соединения, такие как атроментин и телефорная кислота, также могут быть выделены из грибов класса Agaricomycetes. Оробол, изофлавон, может быть выделен из Aspergillus niger.
Ароматические спирты (пример: тирозол ) производятся дрожжи Candida albicans. Они также встречаются в пиве. Эти молекулы являются чувствительными к кворуму соединениями для Saccharomyces cerevisiae.
Дегидрогеназа арил-спирта использует ароматический спирт и НАД для производства ароматического альдегида, НАДН и Н.
Арилалкогольдегидрогеназа (НАДФ +) использует ароматический спирт и НАДФ для производства ароматического альдегида, НАДФН и Н.
арилдиалкилфосфатазы (также известной как фосфорорганическая гидролаза, фосфотриэстераза и параоксон гидролаза) использует арилдиалкилфосфат и H 2 O для получения диалкилфосфата и арилового спирта.
Гирофорная кислота, депсид и орцинол обнаружены в лишайнике.
зеленая водоросль Botryococcus braunii является объектом исследования естественного производства бутилированного гидрокситолуола (BHT), антиоксиданта, пищевой добавки и промышленного химический.
Фенольные кислоты, такие как протокатеховая, п-гидроксибензойная, 2,3-дигидроксибензойная, хлорогеновая, ванильная, кофейная, п-кумаровая и салициловая кислота, коричная кислота и гидроксибензальдегиды, такие как п- гидроксибензальдегид, 3,4-дигидроксибензальдегид, ванилин были выделены из in vitro культуры пресноводных зеленых водорослей Spongiochloris spongiosa.
Флоротанины, для экземпляр эккол, встречаются в бурых водорослях. Видаленолон содержится в тропических красных водорослях Vidalia sp.
Фенольные соединения в основном встречаются в сосудистых растениях (трахеофиты), например, Lycopodiophyta (ликоподы), Pteridophyta (папоротники и хвощи), покрытосеменных (цветковые растения или Magnoliophyta) и голосеменные (хвойные, саговники, гинкго и Gnetales ).
папоротники, соединения, такие как кемпферол и его глюкозид, могут быть выделены из метанольного экстракта листьев Phegopteris connectilis или кемпферол- 3-O-рутинозид, известный флавоноидный гликозид с горьким вкусом, может быть выделен из корневищ Selliguea Fei. гипогалловая кислота, кофейная кислота, пеонифлорин и может быть выделен из пресноводного папоротника Salvinia Molesta.
У хвойных пород (Pinophyta) фенольные соединения хранятся в полифенольные клетки паренхимы, ткань, изобилующая флоэмой всех хвойных деревьев.
водное растение Myriophyllum spicatum производит эллаговая, галловая и пирогалловая кислоты и (+) - катехин.
Алкилрезорцинах можно найти в злаки.
2,4-бис (4-гидроксибензил) фенол представляет собой фенольное соединение, обнаруженное в орхидеях Gastrodia elata и Galeola faberi.
Фенолы также можно найти в несосудистых наземных растениях (мохообразных ). Дигидростильбеноиды и могут быть обнаружены в печеночниках (Marchantiophyta ), например, макроциклы кавикуикулин и риккардин C. Хотя лигнин отсутствует в мхах (Bryophyta) и роголистниках (Anthocerotophyta), некоторые фенольные соединения можно найти в этих двух таксонах. Например, розмариновая кислота и 3'-O-β-D-глюкозид розмариновой кислоты могут быть обнаружены в роголистнике Anthoceros agrestis.
Было показано, что отверждение белкового компонента кутикулы насекомых происходит из-за дубильного действия агента, продуцируемого окислением фенольного вещества, образующего склеротин. При аналогичном закаливании таракана ootheca рассматриваемым фенольным веществом является 3: 4-дигидроксибензойная кислота (протокатеховая кислота ).
Ацетосирингон продуцируется самцом листового клопа () Leptoglossus phyllopus ) и используется в его системе связи. Гуаякол вырабатывается в кишечнике пустынной саранчи, Schistocerca gregaria, путем разложения растительного материала. кишечная бактерия Pantoea agglomerans. Гуаякол - один из основных компонентов феромонов, вызывающих скопление саранчи. Орцинол был обнаружен в «токсичном клее» видов муравьев Camponotus saundersi. Rhynchophorus ferrugineus (красный пальмовый долгоносик) использует 2-метокси-4-винилфенол для передачи химических сигналов (феромоны ). Другие простые и сложные фенолы могут быть обнаружены у эусоциальных муравьев (таких как Crematogaster ) в качестве компонентов яда.
У слонов-самок два вида фунтов 3-этилфенола и 2-этил-4,5-диметилфенола были обнаружены в образцах мочи. Исследование секреции височных желез показало наличие фенола, м-крезола и п-крезола (4-метилфенола) во время муст в самцы слонов.
п-крезол и о-крезол также являются компонентами человеческого пота. Пара-крезол также является основным компонентом запаха свиньи.
4-этилфенол, 1,2-дигидроксибензол, 3-гидроксиацетофенон, 4-метил-1,2-дигидроксибензол, 4-метоксиацетофенон, 5-метоксисалициловая кислота, салицилальдегид и 3 -гидроксибензойная кислота входят в состав кастореума, экссудата касторовых мешочков зрелого североамериканского бобра (Castor canadensis ) и европейского бобра (Castor fiber ), используемые в парфюмерии.
В некоторых случаях природные фенолы присутствуют в растительной листве, чтобы препятствовать травоядности, например, в случае ядовитого дуба западного.
В почвах предполагается, что большее количество фенолов выделяется из разлагающейся опада растений, а не через какое-либо естественное растительное сообщество. Разложение отмершего растительного материала вызывает медленное окисление сложных органических соединений лигнин -подобных гумус или распад на более простые формы (сахара и аминосахары, алифатические и фенольные органические кислоты), которые далее трансформируются в микробную биомассу (микробный гумус) или реорганизуются и далее окисляются в гуминовые ассоциации (фульвовая и гуминовая кислоты), которые связываются с глинистыми минералами и гидроксиды металлов. О способности растений поглощать гуминовые вещества из корневой системы и метаболизировать их ведутся долгие споры. В настоящее время существует консенсус в отношении того, что гумус играет гормональную роль, а не просто роль питания в физиологии растений.
В почве растворимые фенолы сталкиваются с четырьмя разными судьбами. Они могут быть разложены и минерализованы как источник углерода гетеротрофными микроорганизмами ; они могут быть преобразованы в нерастворимые и трудно поддающиеся лечению гуминовые вещества в результате реакций полимеризации и конденсации (с участием почвенных организмов); они могут адсорбироваться глинистыми минералами или образовывать хелаты с ионами алюминия или железа; или они могут оставаться в растворенной форме, выщелачиваться просачивающейся водой и, наконец, покидать экосистему в составе растворенного органического углерода (DOC).
Выщелачивание - это процесс, при котором катионы, такие как железо (Fe) и алюминий (Al), а также органические вещества удаляются из подстилки и переносятся вниз, в почву. Этот процесс известен как оподзоление и особенно интенсивен в бореальных лесах и лесах с прохладным умеренным климатом, которые в основном состоят из хвойных сосен, опада которых богата фенольными соединениями и фульвокислотой.
Фенольные соединения могут действовать как защитные агенты, ингибиторы, природные токсические вещества для животных и пестициды против вторгающихся организмов, то есть травоядных, нематод, насекомых-фитофагов, а также грибковых и бактериальных патогенов. Запах и пигментация, создаваемые другими фенольными соединениями, могут привлекать симбиотических микробов, опылителей и животных, разносящих плоды.
Летучие фенольные соединения содержатся в растительной смоле, где они могут привлекать благодетелей, таких как паразитоидов или хищников травоядных, нападающих на растение.
У видов водорослей Alaria marginata действуют фенольные соединения. как химическая защита от травоядных. Среди тропических видов Sargassum и Turbinaria, которые часто предпочитают травоядные рыбы и ехиноиды, встречается относительно низкий уровень фенольных соединений и дубильных веществ. Морские аллелохимические вещества обычно присутствуют в большем количестве и разнообразии в тропических регионах, чем в регионах с умеренным климатом. Сообщается, что фенольные морские водоросли являются очевидным исключением из этой биогеографической тенденции. Высокие концентрации фенолов встречаются у видов бурых водорослей (отряды Dictyotales и Fucales ) как из умеренных, так и из тропических регионов, что указывает на то, что широта сама по себе не является разумным предиктором растения. концентрации фенола.
В винограде Vitis vinifera транс- ресвератрол представляет собой фитоалексин, вырабатываемый против роста грибковых патогенов, таких как Botrytis cinerea и дельта-виниферин - еще один фитоалексин виноградной лозы , продуцируемый после грибковой инфекции Plasmopara viticola. Пиносилвин представляет собой преинфекционный стильбеноид токсин (т.е. синтезированный до заражения), в отличие от фитоалексинов, которые синтезируются во время инфекции. Он присутствует в сердцевине Pinaceae. Это фунгитоксин, защищающий древесину от грибковой инфекции.
Сакуранетин - это флаванон, тип флавоноида. Его можно найти в Polymnia fruticosa и рис, где он действует как фитоалексин против прорастания спор Pyricularia oryzae. В Sorghum ген SbF3'H2, кодирующий флавоноид-3'-гидроксилазу, по-видимому, экспрессируется в фитоалексинах патоген -специфических 3-дезоксиантоцианидин синтез, например, во взаимодействиях сорго - Colletotrichum.
6-Метоксимеллеин представляет собой дигидроизокумарин и фитоалексин, индуцированные в ломтиках моркови с помощью УФ-C, что обеспечивает устойчивость к Botrytis cinerea и другим микроорганизмам.
Danielone - это фитоалексин, обнаруженный в папайя плод. Это соединение показало высокую противогрибковую активность против Colletotrichum gloesporioides, патогенного гриба папайи.
Стилбены продуцируются в Eucalyptus sideroxylon в случае атак патогенов. Такие соединения могут быть включены в гиперчувствительный ответ растений. Высокий уровень фенольных соединений в некоторых лесах может объяснить их естественную сохранность против гниения.
В растениях VirA представляет собой протеин-гистидинкиназу, которая распознает определенные сахара и фенольные соединения. Эти соединения обычно обнаруживаются в поврежденных растениях, и в результате VirA используется Agrobacterium tumefaciens для определения местонахождения потенциальных организмов-хозяев для заражения.
Природные фенолы могут участвовать в аллелопатические взаимодействия, например, в почве или в воде. Juglone является примером такой молекулы, ингибирующей рост других видов растений вокруг ореховых деревьев. Водное сосудистое растение Myriophyllum spicatum производит эллаговую, галловую и пирогалловую кислоты и (+) - катехин, аллелопатические фенольные соединения, ингибирующие рост сине-зеленой водоросли Microcystis aeruginosa.
Фенолы, и в частности флавоноиды и изофлавоноиды, могут быть вовлечены в эндомикоризы <68
Ацетосирингон был наиболее известен своим участием в распознавании патогенов растений, особенно своей ролью в качестве сигнала, привлекающего и трансформирующего уникальные онкогенные бактерии из рода Agrobacterium. Ген virA на плазмиде Ti в геноме Agrobacterium tumefaciens и Agrobacterium rhizogenes используется этими почвенными бактериями для заражения растений посредством кодирования рецептора. для ацетосирингона и других фенольных фитохимических веществ, выделяемых ранами растений. Это соединение также обеспечивает более высокую эффективность трансформации растений в процедурах трансформации, опосредованных A. tumefaciens, и поэтому имеет важное значение в биотехнологии растений.
Известные источники природных фенолов в питание человека включает ягоды, чай, пиво, оливковое масло, шоколад или какао, кофе, гранаты, попкорн, йерба мате, фрукты и на фруктовой основе напитки (включая сидр, вино и уксус ) и овощи. Травы и специи, орехи (грецкие орехи, арахис) и водоросли также потенциально важны для обеспечения некоторых природных фенолов.
Природные фенолы также могут быть найдены в жирных матрицах, таких как оливковое масло. Нефильтрованное оливковое масло имеет более высокий уровень фенолов или полярных фенолов, которые образуют сложный фенол- белковый комплекс.
Было показано, что фенольные соединения при использовании в напитках, таких как чернослив, улучшают цвет и сенсорные компоненты, например, смягчают горечь.
Некоторые сторонники органического земледелия утверждают, что органически выращенный картофель, апельсины и листовые овощи содержат больше фенольных соединений, и эти может обеспечивать антиоксидантную защиту от болезни сердца и рака. Однако данных о существенных различиях между органическими продуктами питания и обычными продуктами питания недостаточно, чтобы утверждать, что органические продукты питания безопаснее или полезнее обычных продуктов питания.
У животных и людей после приема внутрь природные фенолы становятся частью метаболизма ксенобиотиков. В последующих реакциях фазы II эти активированные метаболиты конъюгированы с заряженными частицами, такими как глутатион, сульфат, глицин или глюкуроновая кислота. Эти реакции катализируются большой группой трансфераз с широкой специфичностью. UGT1A6 представляет собой ген человека, кодирующий фенол-UDP-глюкуронозилтрансферазу, активную по отношению к простым фенолам. Фермент, кодируемый геном UGT1A8, обладает глюкуронидазной активностью со многими субстратами, включая кумарины, антрахиноны и флавоны.