Биохимия или биологическая химия, это исследование химических процессов внутри живых организмов и в них отношении. Биохимические процессы усложняют жизнь.
Преобразование глюкозы в полезную формулы энергии, называемую АТФ (аденозинтрифосфат) дыхание - один из видов важнейшего биологического процесса. Изучение биохимии показывает множество химических процессов, которые превращают глюкозу в углекислый газ и воду.
Субдисциплина биологии и химии, биохимия может быть разделена на три области: структурная биология, энзимология и метаболизм. За десятилетия 20-го века последние десятилетия биохимия успешно жизннила процессы с помощью этих объяс трех дисциплин. Почти все области наук о жизни раскрываются и развиваются с помощью биохимической методологии и исследований. Биохимия фокусируется на понимании основы химической структуры, которая позволяет вызвать процессы, происходящие в живых клетках между клетками, что, в свою очередь, в степени степени связано с пониманием тканей и органы, а также структура и функции организма.
Биохимия связывает с молекулярной биологией, которая является изучением молекулярной механизмами биологических явлений.
Большая часть биохимии имеет дело со структурами, функции и взаимодействиями биологических макромолекул, таких как белки, нуклеиновые кислоты, углеводы и липиды. Они имеют функции, связанные с жизнью. Химический состав клетки также зависит от местных молекул и Ном. Это могут быть неорганические (например, вода и ионы металлов ) или органические (например, аминокислоты, которые используются для алгоритмов белков ). Механизмы, используемые клетками для получения энергии из окружающей среды посредством химических методов, известны как метаболизм. Результаты биохимии применяются в основном в медицине, питании и сельском хозяйстве. В медицине биохимики исследуют причины и излечивают из болезней. Изучение питания изучает, как поддерживать здоровье и хорошее самочувствие, а также эффекты недостаточности питания. В сельском хозяйстве биохимики исследуют почву и удобрения. Улучшение выращивания сельскохозяйственных культур, хранения урожая и борьба с вредителями также являются целями.
 Герти Кори и Карл Кори получили Нобелевскую премию в 1947 году за открытие цикла Кори в RPMI.
Герти Кори и Карл Кори получили Нобелевскую премию в 1947 году за открытие цикла Кори в RPMI. В самом широком смысле биохимию можно рассматривать как исследование компонентов и состав живых существ и того, как они объединяются, чтобы стать жизнью. Таким образом, в этом смысле история биохимии может восходить к древним грекам. Внимание уделяется биохимии как особая научная дисциплина зародилась в 19 веке или раньше, в зависимости от того, на каком аспекте биохимии уделяется внимание. Некоторые утверждали, что начало ферментации, диастазы (теперь называемого амилазой ) в 1833 году Ансельмом Пайеном., в то время как другие считали, что Эдуард Бухнер проявал сложный биохимический процесс спиртовое брожение в бесклеточных экстрактах в 1897 году, как рождение биохимии. Некоторые могут также указать ее начало на влиятельную работу 1842 года Юстуса фон Либиха, Химия животных или Органическая химия в ее приложениях в качестве физиологии и патологии, которые представили химическую теорию метаболизма, или даже раньше, исследования 18 века по ферментации и дыханию, выполненные Антуаном Лавуазье. Многие другие пионеры в этой области, которые помогли раскрыть сложные слои биохимии, были объявлены основателями современной биохимии. Эмиль Фишер, изучавший химию белков, и Ф. Гоуленд Хопкинс, изучавший ферменты и динамическую природу биохимии, представляет собой два примера ранних биохимиков.
Сам термин «биохимия» произошел от комбинации биологии и химия. В 1877 году Феликс Хоппе-Зейлер использовал термин («биохимия» на немецком языке) как синоним физиологической химии в предисловии к первому выпуску Zeitschrift für Physiologische Chemie (Journal физиологической химии), где он выступал за создание институтов, посвященных этой области исследований. Немецкий химик Карл Нойберг, однако часто упоминается как автор этого слова в 1903 году, в то время как некоторые приписывают его Францу Хофмайстеру.
 преобразовать ДНК (1D65 )
преобразовать ДНК (1D65 ). Когда-то считалось, что жизнь и ее материалы обладают некоторыми характеристиками или субстанциями (называемыми «жизненным принципом »), отличными от любых свойств неживой материи, и было, что только живые существа могут Затем в 1828 г. Фридрих Велер опубликовал статью о синтезе мочевины, доказав, что органическое соединение может быть искусственно. С тех пор биохимия продвинулась вперед, особенно с середины 20-го века, с развитием новых методов, таких как хроматография, дифракция рентгеновских лучей, двухполяризационная интерферометрия, ЯМР-спектроскопия, радиоизотопное мечение, электронная микроскопия и мо лекулярная динамика моделирования. T Эти методы позволили открыть и детально проанализировать многие молекулы и метаболические пути клетки, такие как гликолиз и цикл Кребса (цикл лимонной кислоты) и привел к пониманию биохимии на молекулярном уровне.
Другим важным историческим событием в биохимии является открытие гена и его роль в передаче информации в клетке. В 1950-е годы Джеймс Д. Уотт, Фрэнсис Крик, Розалинда Франклин и Морис Уилкинс сыграли важную роль в структуре структуры ДНК и предложили ее связь с генетической передачей информации. В 1958 году Джордж Бидл и Эдвард Тейтум получили Нобелевскую премию показывать работу с грибами, что один ген производит один фермент. В 1988 году Колин Вилы был первым человеком, осужденным за преступлениями , ДНК привело к развитию судебной медицины. Совсем недавно Эндрю З. Файер и Крейг С. Мелло получили Нобелевскую премию 2006 года за открытие роли РНК-интерференции (РНКи ), в подавлении экспрессии гена.
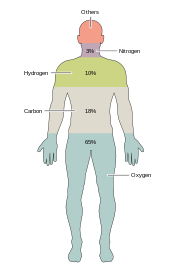 Основные элементы, из которых состоит человеческое тело, показаны от наиболее распространенных основных распространенных
Основные элементы, из которых состоит человеческое тело, показаны от наиболее распространенных основных распространенных Около двух десятков химических элементов необходимы для различных видов биологической жизни. Большинство редких элементов на Земле не нужны жизни (исключение составляют селен и йод ), в то время как некоторые общие элементы (алюминий и титан ) не используются. У организмов есть общие потребности в элементах, но есть несколько различных между растениями и животными. Например, морские водоросли используют бром, а наземные растения и животные, похоже, не нуждаются в нем. натрий требуется всем животным, некоторым растениям - нет. Растениям нужны бор и бор и , но животным может не потребоваться (или потребоваться сверхмалые количества).
Всего шесть элементов - углерод, водород, азот, кислород, кальций и фосфор - составляют почти 99% массы живых клеток, включая клетки человеческого тела (полный список см. В состав человеческого тела ). В дополнение к шести основным элементам, которые составляют большую часть человеческого тела, людям требуется меньшее количество, возможно, еще 18.
Четыре основных класса молекул в биохимии (часто называемые биомолекулы) ) представьте собой углеводы, липиды, белки и нуклеиновые кислоты. Многие биологические молекулы представляют собой полимерами : в этой терминологии мономеры представляют собой относительно небольшие макромолекулы, которые связаны вместе с большими макромолекул, известные как полимеры. Когда мономеры соединяются вместе для синтеза биологического полимера, они подвергаются процедуре, называемому дегидратационным синтезом. Различные макромолекулы могут находиться в более крупных комплексов, часто необходимые для биологической активности.
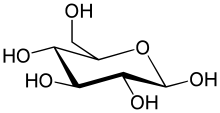 Глюкоза, моносахарид
Глюкоза, моносахарид  Молекула сахарозы (глюкоза + фруктоза ), дисахарид
Молекула сахарозы (глюкоза + фруктоза ), дисахарид  амилоза, полисахарид, состоящий из нескольких тысяч глюкозных
амилоза, полисахарид, состоящий из нескольких тысяч глюкозных Две основные функции углеводов - хранение энергии и обеспечение структуры. Один из распространенных сахаров, известный как глюкоза, является углеводом, но не все углеводы являются сахарами. На Земле больше углеводов, чем любой другой известный тип биомолекул; они используются для хранения энергии и генетической информации, а также играют важную роль в межклеточных взаимодействиях и коммуникации.
Простейшим типом углеводов моносахарид, среди других свойств содержит формула, водород и кислород, в основном в составе 1: 2: 1 (обобщенная формула C nH2nOn, где n равно не менее 3). Глюкоза (C6H12O6) - один из важнейших углеводов; другие включают фруктозу (C6H12O6), сахар, обычно связанный со сладким вкусом фруктов и дезирибозой (C5H10O4), компонент ДНК. Моносахарид может переключаться между ациклической (с открытой цепью) формой и циклической формой. Форму с открытой цепью можно превратить кольцо из атомов углерода, соединенного мостиком атома, образованного из карбонильной группы одного конца и гидроксильной группы еще один. Циклическая молекула имеет полуацетальную или гемикетальную группу, в зависимости от того, была ли линейная форма альдозой или кетозой.
в этих циклических формах. кольцо обычно имеет 5 или 6 атомов. Эти формы называются фуранозами и пиранозами соответственно - по аналогии с фураном и пираном, простейшими соединениями с одним и тем же углерод-кислородом. кольцо (хотя в них отсутствуют двойные молекулы углерода этих двух молекул). Например, альдогексоза глюкоза может образовывать полуацетальную связь между гидроксилом на углероде 1 и кислородом на углероде 4, давая молекулу с 5-членным кольцом, называемую глюкофуранозой. Такая же реакция может происходить между атомами углерода 1 и 5 с молекулы с 6-членным кольцом, называемой глюкопиранозой. Циклические формы с 7-атомным кольцом, называемые гептозами, встречаются редко.
Два моносахарида могут быть соединены гликозидной или простой эфирной связью в дисахарид посредством реакции дегидратации во время при этом выделяется молекула воды. Обратная реакция, в которой гликозидная связь дисахарида разрывается на два моносахарида, называется гидролизом. Наиболее известным дисахаридом является сахароза или обычный сахар, который состоит из молекулы глюкозы и молекулы фруктозы, соединенных вместе. Другой важный дисахарид - это лактоза, обнаруженный в молоке, состоящий из молекулы глюкозы и молекулы галактозы. Лактоза может гидролизоваться лактазой, и дефицит этого фермента приводит к непереносимости лактозы.
Когда соединяются несколько (от трех до шести) моносахаридов, это называется олигосахаридом (олиго - означает « немногие »). Эти молекулы обычно используются в качестве маркеров и сигналов, а также имеют некоторые другие применения. Многие моносахариды, соединенные вместе, образуют полисахарид. Они могут быть соединены вместе в одну длинную линейную цепь или могут быть разветвленными. Двумя наиболее распространенными полисахаридами являются целлюлоза и гликоген, оба состоящие из повторяющихся мономеров глюкозы . Целлюлоза является важным компонентом клеточных стенок , а гликоген используется как форма хранения энергии у животных.
Сахар может характеризоваться наличием восстанавливающих или невосстанавливающих концов. восстанавливающий конец углевода представляет собой атом углерода, который может находиться в равновесии с альдегидом с открытой цепью (альдозой ) или кетоформой (кетозой ). Если соединение мономеров происходит у такого атома углерода, свободная гидроксильная группа формы пиранозы или фуранозы заменяется на боковую цепь ОН другого сахара, давая полный ацеталь. Это предотвращает раскрытие цепи до альдегидной или кето формы и делает модифицированный остаток невосстанавливающим. Лактоза содержит восстанавливающий конец своей глюкозной составляющей, тогда как галактозная составляющая образует полный ацеталь с С4-ОН группой глюкозы. Сахароза не имеет восстанавливающего конца из-за полного образования ацеталя между альдегидным углеродом глюкозы (C1) и кетоуглеродом фруктозы (C2).
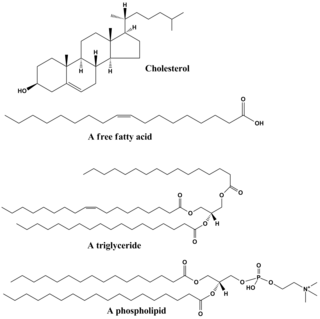 Структуры некоторых распространенных липидов. Вверху находятся холестерин и олеиновая кислота. Средняя структура представляет собой триглицерид , состоящий из цепей олеоила, стеароила и пальмитоила, прикрепленных к основной цепи глицерина.. Внизу - обычный фосфолипид, фосфатидилхолин.
Структуры некоторых распространенных липидов. Вверху находятся холестерин и олеиновая кислота. Средняя структура представляет собой триглицерид , состоящий из цепей олеоила, стеароила и пальмитоила, прикрепленных к основной цепи глицерина.. Внизу - обычный фосфолипид, фосфатидилхолин.Липиды содержат разнообразный диапазон молекул и в некоторой степени являются ловушкой для относительно воды. -нерастворимые или неполярные соединения биологического происхождения, включая воски, жирные кислоты, производные жирные кислоты фосфолипиды, сфинголипиды, гликолипиды и терпеноиды (например, ретиноиды и стероиды ). Некоторые липиды представляют собой линейные алифатические молекулы с открытой цепью, тогда как другие имеют кольцевую структуру. Некоторые из них являются ароматическими (с циклической [кольцевой] и планарной [плоской] структурой), а другие - нет. Некоторые из них гибкие, а другие жесткие.
Липиды обычно состоят из одной молекулы глины с другими молекулами. В триглицеридах, основной группе основных липидов, есть одна молекула глицерина и три жирных кислот. В этом случае жирные кислоты считаются мономером и могут быть насыщенными (без двойных связей в углеродной цепи) или ненасыщенными (одной или несколькими двойными связями в углеродной цепи).
Большинство липидов некоторые полярные характеристики в дополнение к тому, что они в степени неполярны. В общем, основная часть их структуры неполярна или гидрофобна («водобоязненная»), что означает, что она плохо взаимодействует с полярными элементами, такими как вода. Другая часть их структуры является полярной или гидрофильной («водолюбивой») и будет тенденцию ассоциироваться с полярными растворителями, такими как вода. Это делает их амфифильными молекулами (имеющими как гидрофобные, так и гидрофильные части). В случае холестерина полярная группа представляет собой простой –ОН (гидроксил или спирт). В случае фосфолипидов полярные группы значительно больше и более полярны, как описано ниже.
Липиды - неотъемлемая часть нашего ежедневного рациона. Большинство масел и молочных продуктов, которые мы используем для приготовления и еды, таких как масло, сыр, топленое масло и т. Д., состоят из жиров. Растительные масла богаты различными полиненасыщенными жирными кислотами (ПНЖК). Липидсодержащие продукты перевариваются в организме и расщепляются на жирные кислоты и глицерин, являющиеся конечными продуктами распада жиров и липидов. Липиды, особенно фосфолипиды, также используются в различных фармацевтических продуктах либо в качестве совместных солюбилизаторов (например, в парентеральных инфузиях), либо в качестве компонентов носителя лекарственного средства ( например, в липосоме или трансферсоме ).
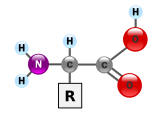 Общая структура α-аминокислоты с группой амино слева и карбоксильной группой справа.
Общая структура α-аминокислоты с группой амино слева и карбоксильной группой справа. Белки представляют собой очень большие молекулы, макробиополимеры, состоящие из мономеров, называемых аминокислотами. Аминокислота состоит из альфа-атома углерода, присоединенного к группе амино, –NH 2, группе карбоновой кислоты, –COOH (хотя они существуют как - NH 3 и –COO в физиологических условиях), простой атом водорода и боковая цепь, обычно обозначаемая как «–R». Боковая цепь «R» различна для каждой аминокислоты, из которых 20 стандартных. Именно эта группа «R» делает каждую аминокислоту различной, и свойства боковых цепей сильно влияют на общую трехмерную конформацию белка. Некоторые аминокислоты выполняют функции сами по себе или в модифицированной форме; например, глутамат функционирует как важный нейромедиатор. Аминокислоты могут быть соединены посредством пептидной связи. В этом синтезе с дегидратацией удаляется молекула воды, и пептидная связь связывает азот аминогруппы одной аминокислоты с углеродом группы карбоновой кислоты другой. Полученная молекула называется дипептидом, а короткие отрезки аминокислот (обычно менее тридцати) называются пептидами или полипептидами. Более длинные отрезки заслуживают названия белков. Например, важный сывороточный белок альбумин крови содержит 585 аминокислотных остатков.
 Общие аминокислоты (1) в нейтральной форме, (2) в том виде, в каком они существуют физиологически, и (3) соединены вместе в виде дипептида.
Общие аминокислоты (1) в нейтральной форме, (2) в том виде, в каком они существуют физиологически, и (3) соединены вместе в виде дипептида.  Схема гемоглобина. Красная и синяя ленты представляют белок глобин ; зеленые структуры - это группы гема.
Схема гемоглобина. Красная и синяя ленты представляют белок глобин ; зеленые структуры - это группы гема. Белки могут выполнять структурные и / или функциональные роли. Например, движения белков актина и миозина в конечном итоге ответственны за сокращение скелетных мышц. Одним из свойств многих белков является то, что они специфически связываются с определенной молекулой или классом молекул - они могут быть чрезвычайно избирательными в том, что они связывают. Антитела представляют собой пример белков, которые прикрепляются к одному конкретному типу молекулы. Антитела состоят изтяжелых и легких цепей. Две тяжелые цепи связаны с легкими цепями посредством дисульфидных связей между их аминокислотами. Антитела специфические за счет вариаций, основанных на различиях в N-концевом домене.
иммуноферментный анализ (ELISA), который использует антитела, одним из самых чувствительных тестов современной медицины. использует для обнаружения различных биомолекул. Однако, вероятно, наиболее важными белками являются ферменты . Практически каждая реакция в живой клетке требует, чтобы фермент активировал энергию реакции. Эти молекулы распознают молекулы реагентов, называемые субстратами ; затем они катализируют реакцию между собой. Уменьшая энергию активации, фермент ускоряет эту реакцию в 10 или более раз; реакция, на спонтанное завершение которой обычно уходит более 3000 лет, с ферментом может занять менее секунды. Сам фермент не расходуется в процессе и может катализировать ту же реакцию с новым набором субстратов. С помощью различных модификаторов можно регулировать активность фермента, что позволяет контролировать биохимию клетки в целом.
Структура белков традиционно описывается в виде иерархии из четырех уровней. Первичная структура белка состоит из его линейной последовательности аминокислот; например, «аланин-глицин-триптофан-серин-глутамат-аспарагин-глицин-лизин-…». Вторичная структура связана с местной морфологией (морфология - это изучение структуры). Некоторые аминокислоты имеют тенденцию скручиваться в спираль, называемую α-спираль, или в лист, называемый β-лист ; Некоторые α-спирали можно увидеть по схеме гемоглобина выше. Третичная структура представляет собой полную трехмерную форму белка. Эта форма последовательности последовательностей аминокислот. Фактически, одно изменение может изменить всю структуру. Альфа-цепь гемоглобина содержит 146 аминокислотных остатков; замена остатка глутамата в положении 6 на остаток валина настолько меняет поведение гемоглобина, что это приводит к серповидно-клеточной анемии. Наконец, четвертичная структура структура структуры белка с множеством пептидных субъединиц, такого как гемоглобин с его четырьмя субъединицами. Не все белки имеют более одной субъединицы.
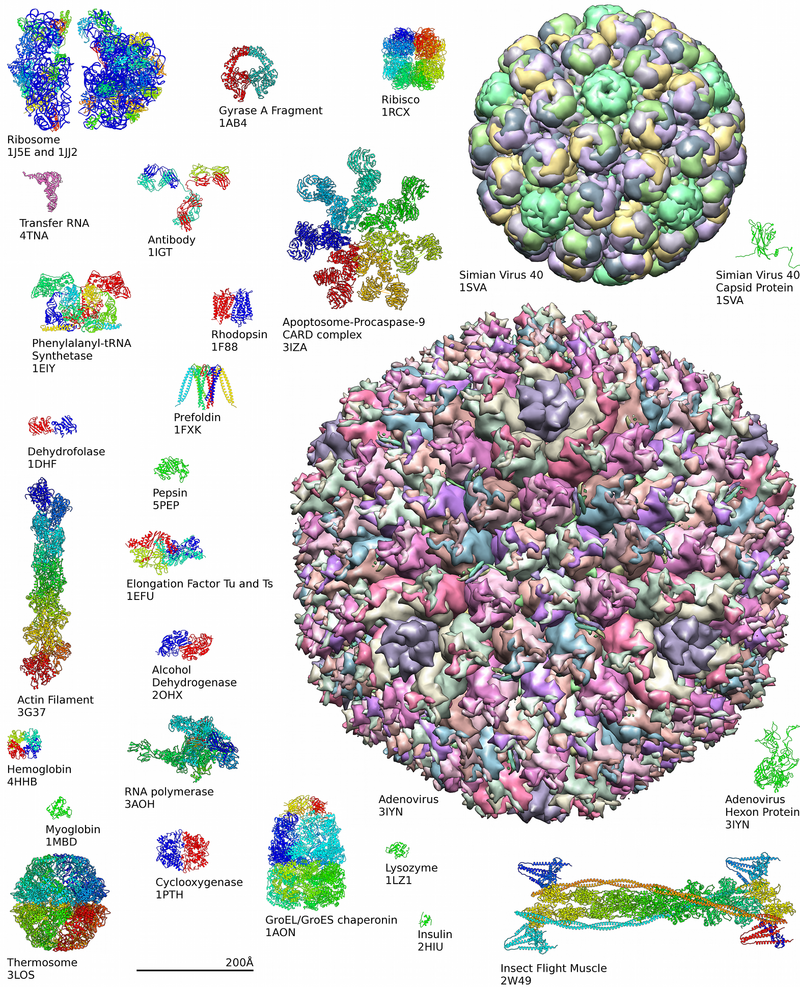 Примеры структур белков из банка данных по белкам
Примеры структур белков из банка данных по белкам  Члены семейства белков, представленные структурыми изомеразы домены
Члены семейства белков, представленные структурыми изомеразы домены Проглоченные белки обычно расщепляются на отдельные аминокислоты или дипептиды в тонком кишечника, а затем всасываются. Затем они могут быть соединены с образованием новых белков. Промежуточные продукты гликолиза, цикла лимонной кислоты и пентозофосфатного пути можно использовать для образования всех двадцати аминокислот, и основных бактерий и растений, обладающих всеми необходимыми ферментами для их синтеза. Однако люди и другие млекопитающие могут синтезировать только половину из них. Они не могут синтезировать изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Они должны попадать в организм, это незаменимые аминокислоты. Мучающие действительно обладают ферментами для синтеза аланина, аспарагина, аспартата, цистеина, глутамата, глутамин, глицин, пролин, серин и тирозин, заменимые аминокислоты. Хотя они могут синтезировать аргинин и гистидин, они не могут обеспечить его достаточные количествах для молодых растущих животных, и поэтому они часто считаются незаменимыми аминокислотами.
Если аминогруппа удаляется из аминокислоты, остается углеродный скелет, называемый α- кетокислотой. Ферменты, называемые трансаминазами, могут легко переносить аминогруппу с одной аминокислотой (использовать ее α-кетокислотой) на другую α-кетокислоту (сделать ее аминокислотой). Это важно для биосинтеза аминокислот, так как для многих путей промежуточных соединений других биохимических путей превращаются в скелет α-кетокислот, а затем добавляется аминогруппа, часто посредством трансаминирования. Затем аминокислоты могут быть связаны вместе с образованием белка.
Подобный процесс используется для расщепления белков. Сначала он гидролизуется до входящего в его состав аминокислот. Свободный аммиак (NH3), присутствующий в крови в виде иона аммония (NH4 +), токсичен для форм жизни. Следовательно, должен существовать подходящий способ его выведения. В зависимости от потребления животных у разных животных выработались разные тактики. Одноклеточные организмы просто выделяют аммиак в окружающей среде. Точно так же костистая рыба может выделять аммиак в воду, где он быстро растворяется. В общем, млекопитающие превращают аммиак в мочевину посредством цикла мочевины.
. Чтобы определить, связаны ли два белка, или другими словами, решить, ученые используют методы сравнения последовательностей. Такие методы, как выравнивание последовательностей и структурное выравнивание, являются мощными инструментами, которые используются ученым идентифицировать гомологии между родственными молекулами. Актуальность поиска гомологий между белками выходит за рамки формирования модели эволюции семейств белков. Обнаружив, насколько похожи две белковые системы, мы узнаем об их структуре и, следовательно, об их функциях.
 Структура дезоксирибонуклеиновой кислоты (ДНК), на рисунке показаны мономеры, соединенные вместе.
Структура дезоксирибонуклеиновой кислоты (ДНК), на рисунке показаны мономеры, соединенные вместе. Нуклеиновые кислоты, так называемые из-за их распространенность в клеточных ядрах - это общее название семейства биополимеров. Это сложные высокомолекулярные биохимические макромолекулы, которые могут передать информацию во всех живых клетках и вирусах. Мономеры называются нуклеотидами, и каждый состоит из трех компонентов: азотистого гетероциклического основания (либо пурин, либо пиримидин ), пентозный сахар и фосфатная группа.
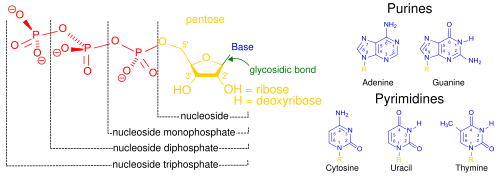 Структурные элементы общих составляющих нуклеиновых кислот. Все соединения, используемые по крайней мере одной фосфатной группы, содержат нуклеотидами (а не просто не содержащими фосфат нуклеозидами ).
Структурные элементы общих составляющих нуклеиновых кислот. Все соединения, используемые по крайней мере одной фосфатной группы, содержат нуклеотидами (а не просто не содержащими фосфат нуклеозидами ).наиболее распространенными нуклеиновыми кислотами дезоксириуклеиновая кислота ( ДНК) и рибонуклеиновая кислота (РНК). фосфатная группа и сахар каждой нуклеотидной связи друг с другом образуют основу нуклеиновой кислоты информацию, в то время как последовательность азотистых оснований хранит наиболее распространенными азотистыми основаниями. являются аденин, цитозин, гуанин, тимин и урацил. азотистые основания каждой цепи нуклеиновой кислоты будут образованы водородные связи с некоторыми другими азотистыми основаниями в комплементарной цепи нуклеиновой кислоты (застежке-молнии).Аденин связывается с тимином и урацил, тимин связывается. только с аденином, а цитозин и гуанин могут связываться только друг с другом.
Помимо генетического материала клетки, нуклеиновые кислоты часто играют роль вторичных мессенджеров, а также образуют основную молекулу для аденозинтрифосфата (АТФ), молекулы первичного энергоносителя, обнаруженной в все живые организмы. Кроме того, азотистые основания, возможные в двух нуклеиновых кислотах, различны: аденин, цитозин и гуанин присутствуют как в РНК, так и в ДНК, в то время как тимин встречается только в ДНК, а урацил - в РНК.
Глюкоза является источником энергии для международных форм жизни. Например, полисахариды расщепляются на свои мономеры ферментами (гликогенфосфорилаза удаляет остатки глюкозы из гликогена, полисахарида). Дисахариды, такие как лактоза или сахароза, расщепляются на двухкомпонентные моносахариды.
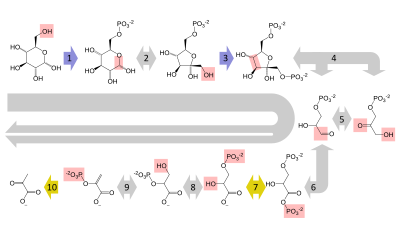 Глюкоза G6P F6P F1,6BP GADP DHAP 1,3BPG 3PG 2PG PEP Пируват HK PGI PFK ALDO TPI GAPDH PGK PGM ENO PK Гликолиз Глюкоза G6P F6P F1,6BP GADP DHAP 1,3BPG 3PG 2PG PEP Пируват HK PGI PFK ALDO TPI GAPDH PGK PGM ENO PK Гликолиз |
Глюкоза метаболизируется в основном с помощью очень важного десятиэтапного пути, называемого гликолиз, конечным результатом этого является расщепление одной молекулы глюкозы на две молекулы пирувата. При этом также образуются две чистые молекулы АТФ, энергетической стоимости клеток, а также два восстанавливающих эквивалента превращения NAD (никотинамидадениндинуклеотид: окисленная форма) в NADH (никотинамидадениндинуклеотид: сокращенная форма). Для этого не требуется кислород; если кислород недоступен (или клетка не может использовать кислород), НАД восстанавливается путем преобразования пирувата в лактат (молочную кислоту) (например, у людей) или в этанол плюс диоксид углерода (например, в дрожжах ). Другие моносахариды, такие как галактоза и фруктоза, могут превращаться в промежуточные продукты гликолитического пути.
В аэробных клетках с достаточным количеством кислорода, как и в большинстве клеток человека, пируват далее метаболизируется. Он необратимо превращается в ацетил-CoA, выделяющий один атом углерода в качестве побочного продукта диоксид углерода, образуя другой восстанавливающий эквивалент в виде NADH. Две молекулы ацетил-КоА (из одной молекулы глюкозы) входят в цикл лимонной кислоты, производя две молекулы АТФ, еще шесть молекул NADH и два восстановленных (ubi) хинона (через FADH 2 как связанный с ферментом кофактор) и высвобождение оставшихся атомов углерода в виде диоксида углерода. Образующиеся молекулы НАДН и хинола затем поступают в ферментные комплексы дыхательной цепи, систему переноса электронов, переносящую в конечном итоге на кислород и сохраняющую высвобождаемую энергию в виде протонного градиента над мембраной (внутренняя митохондриальная мембрана у эукариот). Таким образом, кислород восстанавливается до воды, и исходные акцепторы электронов НАД и хинон регенерируются. Вот почему люди вдыхают кислород и выдыхают углекислый газ. Энергия, высвобождаемая при переносе электронов из высокоэнергетических состояний в НАДН и хиноле, сначала сохраняется в виде протонного градиента и преобразуется в АТФ через АТФ-синтазу. Это генерирует дополнительные 28 молекулы АТФ (24 из 8 НАДН + 4 из 2 хинолов), в сумме до 32 молекул АТФ, консервативных на расщепленную глюкозу (две из гликолиза + две из цитратного цикла). Ясно, что использование кислорода для полного окисления глюкозы дает организму гораздо больше энергии, чем любая кислородно-независимая метаболическая функция, и это считается причиной того, что сложная жизнь появилась только после того, как атмосфера Земли накопила большое количество кислорода.
У позвоночных энергично сокращающиеся скелетные мышцы (например, во время тяжелой атлетики или спринта) не получают достаточно кислорода для удовлетворения энергии спроса, и поэтому они переходят к анаэробному метаболизму, превращая глюкозу в лактат. Комбинация глюкозы неуглеводного происхождения, такой как жир и белки. Это происходит только тогда, когда запасы гликогена в печени истощены. Этот путь представляет собой решающее изменение гликолиза пирувата на глюкозу и может использовать многие источники, такие как аминокислоты, глицерин и цикл Кребса. Крупномасштабный катаболизм белков и жиров обычно возникает, когда люди страдают от голода или определенных эндокринных нарушений. печень регенерирует глюкозу, используя процесс, называемый глюконеогенез. Этот процесс не совсем противоположен гликолизу и на самом деле требует в три раза больше энергии, получаемой от гликолиза (используются шесть молекул АТФ по сравнению с двумя, полученными при гликолизе). Аналогично вышеуказанным реакциям, произведенная глюкоза может затем подвергаться гликолизу в тканях, которым необходима энергия, накапливаться в виде гликогена (или крахмала в растениях), или превращаться в другие моносахариды или соединяться в ди- или олигосахариды. Комбинированные пути гликолиза во время упражнений, прохождение лактата через кровоток в печень, последующий глюконеогенез и выброс глюкозы в кровоток называют циклом Кори.
 Схематическая взаимосвязь между биохимией, генетикой и молекулярной биологией.
Схематическая взаимосвязь между биохимией, генетикой и молекулярной биологией.Исследователи в области биохимии используют специфические методы биохимии, но все чаще сочетают их с методами и идеями, разработанными в областях генетики, молекулярная биология и биофизика. Между этими дисциплинами нет четкой границы. Биохимия изучает химию, необходимую для биологической активности молекул, молекулярная биология изучает их биологическую активность, генетика изучает их наследственность, которая передается их геном. Это показано на следующей схеме, которая изображает одну из возможных точек зрения на взаимосвязь между полями:
Экстремофилы - это микроорганизмы, которые живут в экстремальных условиях, например, в июле 2019 года научное исследование Kidd Mine в Канаде обнаружило дышащих организмами, которые живут на глубине 7900 футов под поверхностью и поглощают серу вместо кислорода для облегчения клеточного дыхания. пирит, в качестве обычного источника пищи.
ДНК-полимераза термофильных бактерий Thermus aquaticus, извлеченная в 1968 г. и названная Taq-полимераза, представляет собой биохимический репликатор ДНК, устойчиво к высокой температуре (50–80 ° C), что позволяет молекулярным биологам облегчить осложнения при ПЦР ( полимеразная цепная реакция) метод.
| В Викиучебниках есть дополнительная информация по теме: Биохимия |
| На Викискладе есть средства массовой информации, связанные с Биохимия. |
| В Викиверсия вы можете узнать больше и рассказать другим о биохимии на Департамент биохимии |