 | |
| Имена | |
|---|---|
| Название ИЮПАК (2R, 3S) -2- (3,4-дигидроксифенил) -3,4-дигидро-2H-хромен-3, 5,7-триол | |
| Другие названия Цианиданол. Цианиданол. (+) - катехин. D-катехин. Катехиновая кислота. Катехиновая кислота. Цианидол. Дексцианиданол. (2R, 3S) -Катехин. 2,3-транс-катехин. (2R, 3S) -Флаван-3,3 ', 4', 5,7-пентол | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| 3DMet | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.005.297 |
| Номер ЕС |
|
| KEGG | |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C15H14O6 |
| Молярная масса | 290,271 г · моль |
| Внешний вид | Бесцветное твердое вещество |
| Температура плавления | от 175 до 177 ° C (от 347 до 351 ° F; От 448 до 450 K) |
| УФ-видимая (λ макс) | 276 нм |
| Хиральное вращение ([α] D) | + 14,0 ° |
| Опасности | |
| Основные опасности | Мутаген для соматических клеток млекопитающих, мутаген для бактерий и дрожжей |
| Паспорт безопасности | sciencelab AppliChem |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| Формулировки опасности GHS | H315, H319, H335 |
| Меры предосторожности GHS | P261, P264, P271, P280, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | (+) - катехин: 10000 мг / кг для крысы (RTECS). 10 000 мг / кг для мышей. 3 890 мг / кг для крыс (другой источник) |
| Фармакология | |
| Пути. введения | Пероральный |
| Фармакокинетика : | |
| Выведение | Моча |
| Если не указано иное, данные приведены для материалов в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
Катехин представляет собой флаван-3-ол, тип природного фенола и антиоксидант. Это растение вторичный метаболит. Он принадлежит к группе флаван-3-олов (или просто флаванолов), части химического семейства флавоноидов.
Название химического семейства катехинов происходит от catechu, который представляет собой дубильный сок или вареный экстракт Mimosa catechu (Acacia catechu Lf).
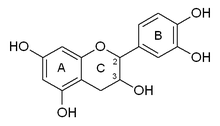 Катехин с номером
Катехин с номером Катехин содержит два бензольных кольца (называемых A- и B-кольцами) и дигидропиран гетероцикл (C-кольцо) с гидроксильной группой на углероде. 3. Кольцо A похоже на фрагмент резорцина, в то время как кольцо B похоже на фрагмент катехол фрагмент. В молекуле на атомах углерода 2 и 3 имеется два хиральных центра. Следовательно, она имеет четыре диастереоизомера. Два изомера находятся в транс-конфигурации и называются катехином, а два других находятся в цис-конфигурации и называются эпикатехином.
Наиболее распространенный изомер катехина - это (+) - катехин. Другой стереоизомер представляет собой (-) - катехин или энт-катехин. Наиболее распространенным изомером эпикатехина является (-) - эпикатехин (также известный под названиями L-эпикатехин, эпикатехол, (-) - эпикатехин, l-акакатехин, l-эпикатехин, эпикатехин, 2,3-цис-эпикатехин или ( 2R, 3R) - (-) - эпикатехин).
Различные эпимеры можно различить с помощью хиральной колоночной хроматографии.
Не ссылаясь ни на какой конкретный изомер, молекулу можно просто назвать катехином. Смеси различных энантиомеров можно назвать (+/-) - катехином или DL-катехином и (+/-) - эпикатехином или DL-эпикатехином.
Катехин и эпикатехин являются строительными блоками проантоцианидинов, типа конденсированного танина.

(+) - катехин (2R, 3S)

(-) - катехин (2S, 3R)

(-) - эпикатехин (2R, 3R)
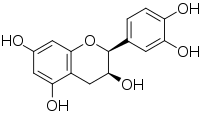
(+) -эпикатехин (2S, 3S)
 Трехмерный вид «псевдоэкваториальной» (E) конформации (+) - катехина
Трехмерный вид «псевдоэкваториальной» (E) конформации (+) - катехина Более того, гибкость C-кольца позволяет иметь два изомера конформации , помещают кольцо B либо в псевдоэкваториальное положение (конформер E), либо в псевдоаксиальное положение (конформер A). Исследования подтвердили, что (+) - катехин принимает смесь A- и E-конформеров в водном растворе, и их конформационное равновесие было оценено как 33:67.
Как флавоноиды, катехины могут действовать как антиоксиданты в высокой концентрации in vitro, но по сравнению с другими флавоноидами их антиоксидантный потенциал низкий. Способность гасить синглетный кислород, по-видимому, связана с химической структурой катехина, с наличием катехоловой части в кольце B и присутствием гидроксильной группы, активирующей двойную связь в кольце C.
Электрохимические эксперименты показывают, что механизм окисления (+) - катехина протекает в последовательные стадии, связанные с группами катехол и резорцин, и окисление зависит от pH. Окисление катехол 3 ', 4'-дигидроксильных электронодонорных групп происходит сначала при очень низких положительных потенциалах и является обратимой реакцией. Было показано, что гидроксильные группы фрагмента резорцина, окисленного впоследствии, подвергаются необратимой реакции окисления.
Система лакказа / ABTS окисляет (+) - катехин до олигомерных продуктов. из которых проантоцианидин A2 представляет собой димер.
 УФ-спектр катехина.
УФ-спектр катехина. | УФ-видимый | |
|---|---|
| Лямбда-макс : | 276 nm |
| Коэффициент экстинкции (log ε) | 4.01 |
| IR | |
| Основные полосы поглощения | 1600 см (бензольные кольца) |
| ЯМР | |
| Протонный ЯМР . (500 МГц, CD3OD):. Ссылка. d: дублет, dd : дублет дублетов,. m: мультиплет, с: синглет | δ :. 2,49 (1H, dd, J = 16,0, 8,6 Гц, H-4a),. 2,82 (1H, dd, J = 16,0, 1,6 Гц, H-4b),. 3,97 (1H, м, H-3),. 4,56 (1H, d, J = 7,8 Гц, H-2),. 5,86 (1H, d, J = 2,1 Гц, H-6),. 5,92 (1H, d, J = 2,1 Гц, H-8),. 6,70 (1H, dd, J = 8,1, 1,8 Гц, H-6 '),. 6,75 (1H, d, J = 8,1 Гц, H-5 '),. 6,83 (1H, d, J = 1,8 Гц, H-2'). |
| ЯМР углерода-13 | |
| Другое Данные ЯМР | |
| MS | |
| Масса. основных фрагментов | ESI-MS [M + H] + m / z: 291,0 . 273 потеря воды. 139 Retro Diels Alder. 123. 165. 147 |
(+) - Катехин и (-) - эпикатехин, а также их конъюгаты галловая кислота встречаются повсеместно наборы сосудистых растений и частые компоненты традиционных лечебных трав, таких как Uncaria rhynchophylla. Два изомера чаще всего встречаются в виде компонентов какао и чая, а также в винограде Vitis vinifera.
Основными источниками катехинов в пище в Европе и США являются чай и плоды фрукты.
Катехины и эпикатехины содержатся в какао, которое, согласно одной базе данных, имеет самое высокое содержание (108 мг / 100 г) катехинов среди проанализированных пищевых продуктов, за которым следует чернослив (25 мг / 100 мл) и стручок фасоли (16 мг / 100 г). Масло асаи, полученное из плодов пальмы асаи (Euterpe oleracea), содержит (+) - катехины (67 мг / кг).
Катехины разнообразны среди пищевых продуктов, от персиков до зеленого чая и уксуса. Катехины обнаружены в зерне ячменя, где они являются основным фенольным соединением, ответственным за изменение цвета теста. Вкус, связанный с мономерным (+) - катехином или (-) - эпикатехином, описывается как слегка вяжущий, но не горький.
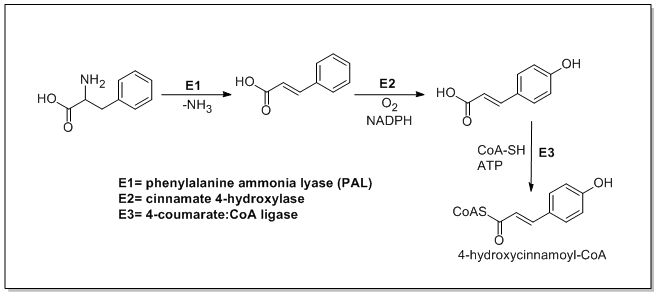
Биосинтез катехина начинается с начальной единицы ma 4-гидроксициннамоил-КоА, которая подвергается удлинению цепи за счет добавления трех малонил-КоА через путь PKSIII. 4-гидроксициннамоил-КоА биосинтезируется из L-фенилаланина посредством пути Shikimate. L-фенилаланин сначала дезаминируется фенилаланинаммиаклиазой (PAL) с образованием коричной кислоты, которая затем окисляется до 4-гидроксикоричной кислоты циннамат-4-гидроксилазой. Затем халконсинтаза катализирует конденсацию 4-гидроксициннамоил-КоА и трех молекул малонил-КоА с образованием халкона. Затем халкон изомеризуется в нарингенин с помощью халконизомеразы, которая окисляется до эриодиктиола флавоноид-3'-гидроксилазой и затем окисляется до таксифолин флаванон-3-гидроксилазой. Затем таксифолин восстанавливается дигидрофлаванол-4-редуктазой и лейкоантоцианидинредуктазой с образованием катехина. Биосинтез катехина показан ниже.
Лейкоцианидинредуктаза (LCR) использует 2,3-транс-3,4-цис- лейкоцианидин для производства (+) - катехина и является первым ферментом. в проантоцианидинах (PA) -специфический путь. Его активность была измерена в листьях, цветках и семенах бобовых Medicago sativa, Lotus japonicus, Lotus uliginosus, Hedysarum sulfurescens, и Robinia pseudoacacia. Этот фермент также присутствует в Vitis vinifera (виноград).

Катехиноксигеназа, ключевой фермент разложения катехина, присутствует в грибах и бактериях.
Среди бактерий разложение (+) - катехина может быть достигнуто с помощью Acinetobacter calcoaceticus. Катехин метаболизируется до протокатеховой кислоты (PCA) и флороглюцинкарбоновой кислоты (PGCA). Он также разлагается Bradyrhizobium japonicum. Флороглюцинкарбоновая кислота дополнительно декарбоксилируется до флороглюцина, который дегидроксилируется до резорцина. Резорцин гидроксилирован до гидроксихинола. Протокатехиновая кислота и гидроксихинол подвергаются интрадиолу расщеплению посредством протокатехуат-3,4-диоксигеназы и гидроксихинол-1,2-диоксигеназы с образованием β-карбоксицис, цис -муконовая кислота и малеилацетат.
Среди грибов разложение катехина может быть достигнуто с помощью Chaetomium cupreum.
 Человеческие метаболиты эпикатехина (за исключением метаболитов толстой кишки)
Человеческие метаболиты эпикатехина (за исключением метаболитов толстой кишки)  Схематическое изображение метаболизма (-) - эпикатехина у человека как функции времени после приема внутрь. SREM: структурно связанные (-) - метаболиты эпикатехина. 5C-RFM: метаболиты деления на 5-углеродное кольцо. 3 / 1C-RFM: метаболиты расщепления с 3- и 1-углеродной боковой цепью. Показаны структуры наиболее распространенных метаболитов (-) - эпикатехина, присутствующих в системном кровотоке и в моче.
Схематическое изображение метаболизма (-) - эпикатехина у человека как функции времени после приема внутрь. SREM: структурно связанные (-) - метаболиты эпикатехина. 5C-RFM: метаболиты деления на 5-углеродное кольцо. 3 / 1C-RFM: метаболиты расщепления с 3- и 1-углеродной боковой цепью. Показаны структуры наиболее распространенных метаболитов (-) - эпикатехина, присутствующих в системном кровотоке и в моче. Катехины метаболизируются при поступлении из желудочно-кишечного тракта, в частности тощей кишки и печени, в результате чего образуются так называемые структурно связанные метаболиты эпикатехина (SREM). Основными метаболическими путями для SREM являются глюкуронирование, сульфатирование и метилирование группы катехолов с помощью катехол-O-метилтрансферазы., при этом в плазме обнаруживаются лишь небольшие количества. Однако большая часть пищевых катехинов метаболизируется микробиомом толстой кишки в гамма-валеролактоны и гиппуровую кислоту, которые подвергаются дальнейшей биотрансформации, глюкуронирование, сульфатирование и метилирование в печени.
Стереохимическая конфигурация катехинов оказывает сильное влияние на их поглощение и метаболизм, так как поглощение является самым высоким для ( -) - эпикатехин и самое низкое содержание (-) - катехина.
 Межвидовые различия в метаболизме (-) - эпикатехина.
Межвидовые различия в метаболизме (-) - эпикатехина. Методы наночастиц находятся в стадии предварительных исследований в качестве потенциальной доставки системы катехинов. Катехины какао проходят предварительные исследования на предмет их способности влиять на риск сердечно-сосудистых заболеваний. Один ограниченный метаанализ показал, что увеличение потребления зеленого чая и его катехинов до семи чашек в день привело к небольшому снижению рака простаты.
Биотрансформация (+) - катехина в Таксифолин двухступенчатым окислением может быть получен с помощью Burkholderia sp.
(+) - катехин и (-) - эпикатехин трансформируются эндофитным мицелиальным грибком Diaporthe sp. в производные 3,4-цис-дигидроксифлавана, (+) - (2R, 3S, 4S) -3,4,5,7,3 ', 4'-гексагидроксифлаван (лейкоцианидин) и, соответственно, тогда как (-) - катехин и (+) - эпикатехин с 2S-фенильной группой сопротивлялись биоокислению.
Лейкоантоцианидинредуктаза (LAR) использует (2R, 3S) -катехин, НАДФ и H 2 O для производства 2,3-транс-3,4-цис- лейкоцианидина, NADPH и H. Экспрессия его гена была изучена в развивающихся ягодах винограда и листьях виноградной лозы.
 Связь между потреблением флаван-3-ола и частотой сердечно-сосудистых заболеваний в различных когортных исследованиях. Данные сравнивают нижний и верхний квинтили потребления.
Связь между потреблением флаван-3-ола и частотой сердечно-сосудистых заболеваний в различных когортных исследованиях. Данные сравнивают нижний и верхний квинтили потребления. Столетия назад катехинсодержащие экстракты считались полезными для лечения сердечных заболеваний, а в 1936 году было показано их влияние на проницаемость капилляров. Ограниченные данные диетических исследований показывают, что катехины могут оказывать влияние на эндотелий -зависимую вазодилатацию, что может способствовать нормальной регуляции кровотока у людей. Катехины зеленого чая могут повышать артериальное давление, особенно когда систолическое артериальное давление превышает 130 мм рт. Из-за интенсивного метаболизма во время пищеварения судьба и активность метаболитов катехина, ответственных за этот эффект на кровеносные сосуды, а также фактический способ действия неизвестны.
Европейское агентство по безопасности пищевых продуктов установлено, что флаванолы какао влияют на функцию сосудов у здоровых взрослых, сделав вывод: «Флаванолы какао помогают поддерживать эндотелий-зависимую вазодилатацию, что способствует нормальному кровотоку». Данные наблюдательных когортных исследований не показали последовательной связи между потреблением флаван-3-ола и риском сердечно-сосудистых заболеваний.
A метаанализ также показал, что катехины зеленого чая могут благоприятно влиять на холестерин.
В зависимости от принятой дозы катехины и их метаболиты могут связываться с эритроцитами и, возможно, вызывать высвобождение аутоантител, что приводит к гемолитической анемии и почечная недостаточность. Это привело к изъятию катехинсодержащего препарата Catergen, используемого для лечения вирусного гепатита, с европейского рынка в 1985 году.
Катехины, попавшие в организм Земля некоторых растений может препятствовать росту их соседей, что является формой аллелопатии. Centaurea maculosa, пятнистый василек, часто изучаемый на предмет такого поведения, выделяет катехин изомеры в землю через корни, потенциально оказывая действие антибиотик или гербицид. Одна из гипотез состоит в том, что он вызывает волну активных форм кислорода через корень растения-мишени, чтобы убить корневые клетки посредством апоптоза. Большинство растений в европейской экосистеме имеют защиту от катехина, но лишь немногие растения защищены от него в экосистеме Северной Америки, где Centaurea maculosa является инвазивным неконтролируемым сорняком.
Катехин действует как инфекция. -гибающий фактор в листьях клубники. Эпикатехин и катехин могут предотвратить болезнь кофейных ягод, подавляя апрессорную меланизацию Colletotrichum kahawae.
| Искать Катехин или catechine в Wiktionary, бесплатном словаре. |