| Малярия | |
|---|---|
 | |
| Малярийный паразит, соединяющийся с эритроцитом | |
| Произношение | |
| Специальность | Инфекционное заболевание |
| Симптомы | Лихорадка, рвота, головная боль, пожелтение кожи |
| Осложнения | Судороги, кома |
| Обычное начало | 10–15 дней после контакта |
| Причины | Плазмодий, распространяемый комарами |
| Диагностический метод | Исследование крови, тесты на выявление антигенов |
| Профилактика | Москитные сетки, репелленты от насекомых, борьба с комарами, лекарства |
| Медикамент | Противомалярийные препараты |
| Частота | 229 миллионов (2019) |
| Летальные исходы | 409000 в 2019 |
Малярия - это инфекционное заболевание, переносимое комарами, которое поражает людей и других животных. Малярия вызывает симптомы, которые обычно включают жар, усталость, рвоту и головные боли. В тяжелых случаях это может вызвать пожелтение кожи, судороги, кому или смерть. Симптомы обычно появляются через десять-пятнадцать дней после укуса инфицированного комара. Если не лечить должным образом, через несколько месяцев у людей могут быть рецидивы заболевания. У тех, кто недавно перенес инфекцию, повторное заражение обычно вызывает более легкие симптомы. Эта частичная резистентность исчезает через несколько месяцев или лет, если человек не болеет малярией постоянно.
Малярия вызывается одноклеточными микроорганизмами группы Plasmodium. Согласно информационному бюллетеню ВОЗ за 2014 год, он передается исключительно через укусы инфицированных комаров Anopheles. Укус комара переносит паразитов из слюны комара в кровь человека. Паразиты попадают в печень, где созревают и размножаются. Пять видов Plasmodium могут инфицировать и распространяться от человека. Большинство смертей вызвано P. falciparum, тогда как P. vivax, P. ovale и P. malariae обычно вызывают более легкую форму малярии. Вид P. knowlesi редко вызывает болезни у человека. Малярия обычно диагностируется при микроскопическом исследовании крови с использованием мазков крови или с помощью экспресс-тестов на основе антигенов. Были разработаны методы, использующие полимеразную цепную реакцию для обнаружения ДНК паразита, но они не получили широкого распространения в районах, где распространена малярия, из-за их стоимости и сложности.
Риск заболевания можно снизить, предотвратив укусы комаров с помощью противомоскитных сеток и репеллентов от насекомых или с помощью таких мер борьбы с комарами, как распыление инсектицидов и слив стоячей воды. Доступны несколько лекарств для предотвращения малярии у путешественников в районы, где это заболевание распространено. Отдельные дозы комбинации лекарственных средств сульфадоксина / пириметамину рекомендуются младенцам и после первого триместра беременности по беременности в районах с высоким уровнем малярии. По состоянию на 2020 год существует одна вакцина, которая, как было показано, снижает риск малярии примерно на 40% у детей в Африке. Предпечатное исследование другой вакцины показало эффективность вакцины 77%, но это исследование еще не прошло экспертную оценку. Усилия по разработке более эффективных вакцин продолжаются. Рекомендуемое для лечения малярии является комбинацией из противомалярийных препаратов, который включает в себя артемизинин. Вторым лекарством может быть мефлохин, люмефантрин или сульфадоксин / пириметамин. Если артемизинин недоступен, можно использовать хинин вместе с доксициклином. В районах, где это заболевание распространено, рекомендуется, по возможности, подтвердить малярию до начала лечения из-за опасений повышения лекарственной устойчивости. У паразитов развилась устойчивость к нескольким противомалярийным препаратам; например, хлорохин резистентный P. фальципарум распространился в большинстве эндемичных районов, а также устойчивость к артемизинину стала проблемой в некоторых частях Юго - Восточной Азии.
Заболевание широко распространено в тропических и субтропических регионах, расположенных в широкой полосе вокруг экватора. Это включает большую часть Африки к югу от Сахары, Азии и Латинской Америки. В 2019 году во всем мире было зарегистрировано 229 миллионов случаев малярии, в результате которых, по оценкам, погибло 409 000 человек. Примерно 94% случаев заболевания и смерти произошло в Африке к югу от Сахары. Уровень заболеваемости снизился с 2010 по 2014 год, но увеличился с 2015 по 2019 год. Малярия обычно ассоциируется с бедностью и оказывает значительное негативное влияние на экономическое развитие. В Африке это, по оценкам, приводит к убыткам в размере 12 миллиардов долларов США в год из-за увеличения расходов на здравоохранение, потери трудоспособности и неблагоприятных последствий для туризма.
 Воспроизвести медиа Сводка видео ( сценарий )
Воспроизвести медиа Сводка видео ( сценарий )  Основные симптомы малярии
Основные симптомы малярии Признаки и симптомы малярии обычно проявляются через 8–25 дней после заражения, но могут появиться позже у тех, кто принимал противомалярийные препараты в качестве профилактики. Начальные проявления болезни - общие для всех видов малярии - похожи на симптомы гриппа и могут напоминать другие состояния, такие как сепсис, гастроэнтерит и вирусные заболевания. Проявления могут включать головную боль, жар, дрожь, боль в суставах, рвоту, гемолитическую анемию, желтуху, гемоглобин в моче, повреждение сетчатки и судороги.
Классическим симптомом малярии является пароксизм - циклическое возникновение внезапного озноба с последующим ознобом, а затем повышением температуры и потливостью, возникающее каждые два дня ( третичная лихорадка ) при инфекциях, вызванных P. vivax и P. ovale, и каждые три дня ( четырехдневная лихорадка ) при инфекциях. P. malariae. Инфекция P. falciparum может вызывать повторную лихорадку каждые 36–48 часов или менее выраженную и почти постоянную лихорадку.
Тяжелая форма малярии обычно вызывается P. falciparum (часто называемой малярией falciparum). Симптомы малярии falciparum возникают через 9–30 дней после заражения. У людей с церебральной малярией часто наблюдаются неврологические симптомы, включая неправильную позу, нистагм, паралич сопряженного взгляда (неспособность глаз поворачиваться в одном направлении), опистотонус, судороги или кому.
Малярия имеет несколько серьезных осложнений. Среди них - респираторный дистресс-синдром, который встречается у 25% взрослых и 40% детей с тяжелой формой малярии, вызванной P. falciparum. Возможные причины включают респираторную компенсацию метаболического ацидоза, некардиогенный отек легких, сопутствующую пневмонию и тяжелую анемию. Хотя острый респираторный дистресс-синдром встречается редко у маленьких детей с тяжелой формой малярии, он встречается у 5–25% взрослых и до 29% беременных женщин. Coinfection от ВИЧ с увеличением малярии смертности. Почечная недостаточность - признак черной лихорадки, когда гемоглобин из лизированных эритроцитов просачивается в мочу.
Заражение P. falciparum может привести к церебральной малярии, тяжелой форме малярии, сопровождающейся энцефалопатией. Это связано с побелением сетчатки, что может быть полезным клиническим признаком отличия малярии от других причин лихорадки. Возможно увеличение селезенки, увеличенной печени или того и другого, сильная головная боль, низкий уровень сахара в крови и гемоглобин в моче при почечной недостаточности. Осложнения могут включать спонтанное кровотечение, коагулопатию и шок.
Малярия у беременных женщин - важная причина мертворождений, младенческой смертности, выкидышей и низкой массы тела при рождении, особенно при инфекции P. falciparum, а также P. vivax.
Паразиты малярии относятся к роду Plasmodium (тип Apicomplexa ). У людей малярия преимущественно вызывается пятью видами Plasmodium spp., включая P. falciparum, P. malariae, P. ovale, P. vivax и P. knowlesi. Среди инфицированных наиболее часто выявляется P. falciparum (~ 75%), за ним следует P. vivax (~ 20%). Хотя P. falciparum традиционно является причиной большинства смертей, недавние данные свидетельствуют о том, что малярия, вызванная P. vivax, связана с потенциально опасными для жизни состояниями примерно так же часто, как и с диагнозом инфекции P. falciparum. P. vivax пропорционально более распространен за пределами Африки. Были зарегистрированы случаи заражения людей несколькими видами Plasmodium от высших человекообразных обезьян ; однако, за исключением P. knowlesi - зоонозного вида, вызывающего малярию у макак, - они в основном имеют ограниченное значение для общественного здравоохранения.
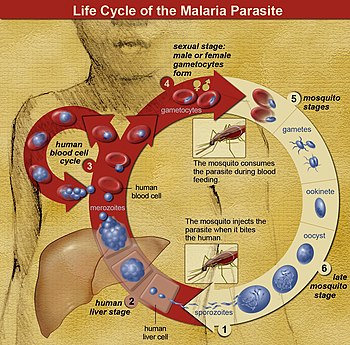 Жизненный цикл малярийных паразитов. Комар вызывает инфекцию при укусе. Сначала спорозоиты попадают в кровоток и мигрируют в печень. Они заражают клетки печени, где они размножаются до мерозоитов, разрывают клетки печени и возвращаются в кровоток. Мерозоиты инфицируют красные кровяные тельца, где они развиваются в кольцевые формы, трофозоиты и шизонты, которые, в свою очередь, производят новые мерозоиты. Также образуются половые формы, которые при попадании в организм комара заражают насекомое и продолжают его жизненный цикл.
Жизненный цикл малярийных паразитов. Комар вызывает инфекцию при укусе. Сначала спорозоиты попадают в кровоток и мигрируют в печень. Они заражают клетки печени, где они размножаются до мерозоитов, разрывают клетки печени и возвращаются в кровоток. Мерозоиты инфицируют красные кровяные тельца, где они развиваются в кольцевые формы, трофозоиты и шизонты, которые, в свою очередь, производят новые мерозоиты. Также образуются половые формы, которые при попадании в организм комара заражают насекомое и продолжают его жизненный цикл. В жизненном цикле из Plasmodium, самка Anopheles комаров ( окончательный хозяин ) передает подвижна инфекционная форму ( так называемые спорозоитами ) к позвоночному хозяину, такие как человек (вторичный узел), таким образом, выступают в качестве передачи вектора. Спорозоит перемещается по кровеносным сосудам в клетки печени ( гепатоциты ), где он размножается бесполым путем (тканевая шизогония ), производя тысячи мерозоитов. Они инфицируют новые эритроциты и инициируют серию циклов бесполого размножения (кровяная шизогония), которые производят от 8 до 24 новых инфекционных мерозоитов, после чего клетки лопаются, и инфекционный цикл начинается заново.
Другие мерозоиты развиваются в незрелые гаметоциты, которые являются предшественниками мужских и женских гамет. Когда оплодотворенный комар кусает инфицированного человека, гаметоциты попадают в кровь и созревают в кишечнике комара. Мужские и женские гаметоциты сливаются и образуют оокинету - оплодотворенную подвижную зиготу. Оокинеты развиваются в новые спорозоиты, которые мигрируют в слюнные железы насекомых, готовые заразить нового позвоночного хозяина. Спорозоиты вводятся в кожу, со слюной, когда комар принимает последующую пищу с кровью.
Кровью питаются только самки комаров; самцы комаров питаются нектаром растений и не передают болезнь. Самки комаров рода Anopheles предпочитают кормиться ночью. Обычно они начинают поиск еды в сумерках и продолжают всю ночь, пока не добьются успеха. Паразиты малярии также могут передаваться при переливании крови, хотя это бывает редко.
Симптомы малярии могут повторяться после различных бессимптомных периодов. В зависимости от причины рецидив можно классифицировать как обострение, рецидив или повторное инфицирование. Рецидив - это когда симптомы возвращаются после бессимптомного периода. Это вызвано паразитами, которые выживают в крови в результате неадекватного или неэффективного лечения. Рецидив - это повторное появление симптомов после того, как паразиты были удалены из крови, но сохраняются в клетках печени в виде спящих гипнозоитов. Рецидив обычно происходит между 8–24 неделями и часто наблюдается при инфекциях, вызванных P. vivax и P. ovale. Однако рецидивирующие рецидивы P. vivax, вероятно, чрезмерно приписываются активации гипнозоитов. Некоторые из них могут иметь внесосудистое происхождение мерозоитов, что делает эти рецидивы обострениями, а не рецидивами. Одним из недавно выявленных, негипнозоитных, возможных источников рецидивирующей периферической паразитемии, вызванной P. vivax, являются эритроцитарные формы в костном мозге. Случаи малярии P. vivax в регионах с умеренным климатом часто связаны с перезимованием гипнозоитов, рецидивы начинаются через год после укуса комара. Реинфекция означает, что паразит, вызвавший прошлую инфекцию, был удален из организма, но появился новый паразит. Реинфекцию нельзя легко отличить от рецидива, хотя рецидив инфекции в течение двух недель после лечения первоначальной инфекции обычно связывают с неэффективностью лечения. У людей может развиться иммунитет при частом контакте с инфекциями.
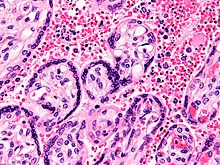 Микрофотография из плаценты от мертворождения из - за материнскую малярию. Пятно Hamp;E. Эритроциты безъядерные; окрашивание в синий / черный цвета в ярко-красных структурах (красных кровяных тельцах) указывает на чужеродные ядра паразитов.
Микрофотография из плаценты от мертворождения из - за материнскую малярию. Пятно Hamp;E. Эритроциты безъядерные; окрашивание в синий / черный цвета в ярко-красных структурах (красных кровяных тельцах) указывает на чужеродные ядра паразитов.  Электронная микрофотография эритроцитов, инфицированных Plasmodium falciparum (в центре), иллюстрирующая «выступы» белка адгезии
Электронная микрофотография эритроцитов, инфицированных Plasmodium falciparum (в центре), иллюстрирующая «выступы» белка адгезии Инфекция малярии проходит в две фазы: одна включает печень (экзоэритроцитарная фаза), а вторая - эритроциты или эритроциты (эритроцитарная фаза). Когда инфицированный комар протыкает кожу человека, чтобы принять пищу с кровью, спорозоиты в слюне комара попадают в кровоток и мигрируют в печень, где заражают гепатоциты, размножаясь бесполым и бессимптомным образом в течение 8–30 дней.
После потенциального периода покоя в печени эти организмы дифференцируются с образованием тысяч мерозоитов, которые после разрыва своих клеток-хозяев попадают в кровь и заражают эритроциты, начиная эритроцитарную стадию жизненного цикла. Паразит ускользает из печени незамеченным, заворачиваясь в клеточную мембрану инфицированной клетки печени хозяина.
Внутри эритроцитов паразиты размножаются дальше, опять же бесполым путем, периодически вырываясь из своих клеток-хозяев и вторгаясь в свежие эритроциты. Происходит несколько таких циклов амплификации. Таким образом, классические описания волн лихорадки возникают из-за одновременного выхода мерозоитов и их заражения эритроцитами.
Некоторые спорозоиты P. vivax не сразу развиваются в мерозоиты экзоэритроцитарной фазы, а вместо этого продуцируют гипнозоиты, которые остаются в состоянии покоя в течение периодов от нескольких месяцев (обычно 7–10 месяцев) до нескольких лет. После периода покоя они реактивируются и производят мерозоиты. Гипнозоиты ответственны за длительную инкубацию и поздние рецидивы инфекций P. vivax, хотя их существование у P. ovale неясно.
Паразит относительно защищен от атак иммунной системы организма, поскольку большую часть своего жизненного цикла человека он находится в печени и клетках крови и относительно невидим для иммунного надзора. Однако циркулирующие инфицированные клетки крови разрушаются в селезенке. Чтобы избежать этой участи, паразит P. falciparum отображает адгезивные белки на поверхности инфицированных клеток крови, заставляя клетки крови прилипать к стенкам мелких кровеносных сосудов, тем самым изолируя паразита от прохождения через общий кровоток и селезенку. Закупорка микрососудов вызывает такие симптомы, как при плацентарной малярии. Секвестрированные эритроциты могут нарушить гематоэнцефалический барьер и вызвать церебральную малярию.
Согласно обзору 2005 года, из-за высоких уровней смертности и заболеваемости, вызванных малярией, особенно видами P. falciparum, она оказала самое сильное избирательное давление на геном человека в новейшей истории. Некоторые генетические факторы обеспечивают некоторую устойчивость к нему, включая серповидно - клеточная признака, талассемии черты, глюкозо-6-фосфат - дегидрогеназы, а также отсутствие Даффи антигенов на красных кровяных клеток.
Влияние серповидно-клеточного признака на иммунитет к малярии иллюстрирует некоторые эволюционные компромиссы, которые произошли из-за эндемической малярии. Серповидно-клеточный признак вызывает изменение молекулы гемоглобина в крови. Обычно красные кровяные тельца имеют очень гибкую двояковогнутую форму, которая позволяет им перемещаться по узким капиллярам ; однако, когда молекулы модифицированного гемоглобина S подвергаются воздействию небольшого количества кислорода или собираются вместе из-за обезвоживания, они могут слипаться, образуя нити, которые вызывают деформацию клетки в изогнутую серповидную форму. В этих цепях молекула не так эффективна в поглощении или высвобождении кислорода, а клетка недостаточно гибка, чтобы свободно циркулировать. На ранних стадиях малярии паразит может вызвать серповидное поражение инфицированных эритроцитов, поэтому они быстрее удаляются из кровообращения. Это снижает частоту завершения жизненного цикла малярийных паразитов в клетке. Гомозиготные люди (с двумя копиями аномального бета- аллеля гемоглобина) страдают серповидно-клеточной анемией, в то время как гетерозиготные (с одним аномальным аллелем и одним нормальным аллелем) обладают устойчивостью к малярии без тяжелой анемии. Хотя более короткая ожидаемая продолжительность жизни для людей с гомозиготным состоянием будет иметь тенденцию к неблагоприятному выживанию признака, признак сохраняется в регионах, подверженных малярии, благодаря преимуществам, обеспечиваемым гетерозиготной формой.
Дисфункция печени в результате малярии встречается редко и обычно возникает только у пациентов с другим заболеванием печени, таким как вирусный гепатит или хроническое заболевание печени. Синдром иногда называют малярийным гепатитом. Хотя малярийная гепатопатия считается редким явлением, наблюдается рост, особенно в Юго-Восточной Азии и Индии. Нарушение функции печени у людей с малярией коррелирует с большей вероятностью осложнений и смерти.
 Мазок крови - золотой стандарт диагностики малярии.
Мазок крови - золотой стандарт диагностики малярии. 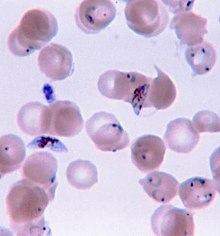 Ring-форма и гаметоцит из малярийного плазмодия в крови человека
Ring-форма и гаметоцит из малярийного плазмодия в крови человека Из-за неспецифического характера проявления симптомов диагностика малярии в неэндемичных районах требует высокой степени подозрения, которое может быть вызвано любым из следующих факторов: недавние поездки, увеличение селезенки, лихорадка, низкое количество заболеваний. тромбоциты в крови и уровни билирубина в крови выше нормы в сочетании с нормальным уровнем лейкоцитов. Отчеты 2016 и 2017 годов из стран, где малярия является распространенным явлением, свидетельствуют о высоком уровне гипердиагностики из-за недостаточного или неточного лабораторного тестирования.
Малярия обычно подтверждается микроскопическим исследованием мазков крови или экспресс-тестами на основе антигенов (БДТ). В некоторых регионах ДЭТ должны уметь различать, вызваны ли симптомы малярии Plasmodium falciparum или другими видами паразитов, поскольку стратегии лечения могут отличаться от инфекций, не связанных с P. falciparum. Микроскопия является наиболее часто используемым методом для обнаружения малярийного паразита: в 2010 году было исследовано около 165 миллионов мазков крови на предмет малярии. Несмотря на широкое распространение, микроскопическая диагностика страдает двумя основными недостатками: многие условия (особенно в сельской местности) не оборудованы для проведения исследований. тест и точность результатов зависят как от навыков человека, исследующего мазок крови, так и от уровня паразита в крови. Чувствительность пленок крови колеблется от 75 до 90% в оптимальных условиях, как низко как 50%. Коммерчески доступные ДЭТ часто более точны, чем мазки крови при прогнозировании присутствия малярийных паразитов, но они широко варьируются по диагностической чувствительности и специфичности в зависимости от производителя и не могут определить, сколько паразитов присутствует. Однако включение БДТ в диагностику малярии может сократить выписывание противомалярийных препаратов. Хотя БДТ не улучшает исходы для здоровья людей, инфицированных малярией, она также не приводит к худшим результатам по сравнению с предполагаемым противомалярийным лечением.
В регионах, где легко доступны лабораторные анализы, следует подозревать малярию и проводить тестирование на нее у любого нездорового человека, который побывал в районе, где малярия является эндемичной. В регионах, где не могут позволить себе лабораторные диагностические тесты, в качестве показания к лечению от малярии стало обычным использование только лихорадки в анамнезе - таким образом, распространенное учение «лихорадка равняется малярии, если не доказано иное». Недостатком этой практики является чрезмерная диагностика малярии и неправильное лечение немалярийной лихорадки, что приводит к бесполезной трате ограниченных ресурсов, подрывает доверие к системе здравоохранения и способствует устойчивости к лекарствам. Хотя тесты на основе полимеразной цепной реакции были разработаны, они не получили широкого распространения в регионах, где малярия распространена по состоянию на 2012 год, из-за своей сложности.
Всемирная организация здравоохранения (ВОЗ) классифицирует малярию на «тяжелую» и «неосложненную». Он считается тяжелым при наличии любого из следующих критериев, в противном случае считается несложным.
Церебральная малярия определяется как тяжелая форма малярии, вызванной P. falciparum, проявляющаяся неврологическими симптомами, включая кому (по шкале комы Глазго менее 11 или шкале комы Блантайра менее 3), или кома, которая длится более 30 минут после припадок.
Различные типы малярии получили следующие названия:
| Имя | Возбудитель | Примечания |
|---|---|---|
| водорослевая малярия | Плазмодий falciparum | тяжелая форма малярии, поражающая сердечно-сосудистую систему и вызывающая озноб и сердечно-сосудистый шок |
| желчная малярия | Плазмодий falciparum | тяжелая форма малярии, поражающая печень и вызывающая рвоту и желтуху |
| церебральная малярия | Плазмодий falciparum | тяжелая малярия, поражающая головной мозг |
| врожденная малярия | различные плазмодии | плазмодий, переданный от матери через кровообращение плода |
| пагубная малярия | Плазмодий falciparum | тяжелая малярия, ведущая к тяжелой болезни |
| злокачественная малярия | Плазмодий falciparum | тяжелая форма малярии, приводящая к смерти |
| малярия falciparum, малярия, вызванная Plasmodium falciparum, | Плазмодий falciparum | |
| ovale малярия, Plasmodium ovale малярия | Плазмодий овальный | |
| четырехдневной малярии, malariae малярии, Plasmodium malariae малярии | Plasmodium malariae | пароксизмы каждый четвертый день ( квартан ), считая день возникновения первым днем |
| повседневная малярия | Plasmodium falciparum, Plasmodium vivax, Plasmodium knowlesi | пароксизмы ежедневно ( банальный ) |
| третичная малярия | Plasmodium falciparum, Plasmodium ovale, Plasmodium vivax | пароксизмы каждый третий день ( третичный ), считая день возникновения первым |
| трансфузионная малярия | различные плазмодии | плазмодий, занесенный при переливании крови, совместном использовании иглы или уколе иглой |
| трехдневной малярии, Plasmodium трехдневной малярии | Плазмодий вивакс |
 An Anopheles stephensi комары вскоре после получения крови от человека (капелька крови выталкиваются как излишек). Этот комар является переносчиком малярии, и борьба с комарами является эффективным способом снижения его заболеваемости.
An Anopheles stephensi комары вскоре после получения крови от человека (капелька крови выталкиваются как излишек). Этот комар является переносчиком малярии, и борьба с комарами является эффективным способом снижения его заболеваемости. Методы, используемые для предотвращения малярии, включают лекарства, уничтожение комаров и предотвращение укусов. По состоянию на 2020 год существует одна вакцина против малярии (известная как RTS, S ), которая лицензирована для использования. Присутствие малярии на территории требует сочетания высокой плотности населения, высокой плотности популяции комаров-анофелесов и высоких показателей передачи от человека комарам и от комаров человеку. Если какой-либо из них будет снижен в достаточной степени, паразит в конечном итоге исчезнет из этой области, как это произошло в Северной Америке, Европе и некоторых частях Ближнего Востока. Однако, если паразит не будет уничтожен во всем мире, он может восстановиться, если условия вернутся к комбинации, которая способствует размножению паразита. Кроме того, стоимость уничтожения комаров Anopheles на человека возрастает с уменьшением плотности населения, что делает это экономически нецелесообразным в некоторых районах.
Профилактика малярии может быть более рентабельной, чем лечение болезни в долгосрочной перспективе, но требуемые первоначальные затраты недоступны для многих из беднейших людей мира. Между странами существует большая разница в стоимости программ борьбы (т. Е. Поддержание низкой эндемичности) и программ элиминации. Например, в Китае, правительство которого в 2010 году объявило о стратегии по ликвидации малярии в китайских провинциях, требуемые инвестиции составляют небольшую долю государственных расходов на здравоохранение. Напротив, аналогичная программа в Танзании будет стоить примерно пятую часть бюджета общественного здравоохранения.
В районах, где распространена малярия, дети в возрасте до пяти лет часто болеют анемией, которая иногда возникает из-за малярии. Предоставление детям с анемией в этих областях профилактических противомалярийных препаратов немного повышает уровень эритроцитов, но не влияет на риск смерти или необходимость госпитализации.
 Мужчина распыляет керосин в стоячей воде, зона Панамского канала, 1912 год.
Мужчина распыляет керосин в стоячей воде, зона Панамского канала, 1912 год. Векторное управление относится к методам, используемым для уменьшения малярии путем снижения уровня передачи комарами. Для индивидуальной защиты наиболее эффективны репелленты на основе ДЭТА или пикаридина. Однако недостаточно доказательств того, что репелленты от комаров могут предотвратить заражение малярией. Обработанные инсектицидами сетки (ITN) и опрыскивание помещений (IRS) эффективны, широко используются для предотвращения малярии, и их использование в значительной степени способствовало снижению заболеваемости малярией в 21 веке. ITN и IRS могут оказаться недостаточными для полной ликвидации болезни, поскольку эти вмешательства зависят от того, сколько людей используют сетки, сколько в них пробелов в инсектицидах (зоны с низким уровнем охвата), если люди не защищены, когда они находятся вне дома, и увеличение числа москитов, устойчивых к инсектицидам. Перестройка домов людей для предотвращения контакта с комарами может быть важной долгосрочной профилактической мерой.
 Стены, где в помещениях было нанесено остаточное распыление ДДТ. Комары остаются на стене, пока не падают замертво на пол.
Стены, где в помещениях было нанесено остаточное распыление ДДТ. Комары остаются на стене, пока не падают замертво на пол.  Используется москитная сетка.
Используется москитная сетка. Противомоскитные сетки защищают людей от комаров и снижают уровень заражения и передачи малярии. Сети не являются идеальным барьером, и их часто обрабатывают инсектицидом, предназначенным для уничтожения комара, прежде чем он успеет пробраться через сетку. Сетки, обработанные инсектицидами (ОИС), по оценкам, в два раза эффективнее необработанных сеток и обеспечивают более 70% защиты по сравнению с сетками без сетки. В период с 2000 по 2008 год использование ITN спасло жизни примерно 250 000 младенцев в странах Африки к югу от Сахары. Около 13% домашних хозяйств в странах к югу от Сахары владели ОИС в 2007 году, а 31% африканских домашних хозяйств, по оценкам, владели как минимум одним ОИС в 2008 году. В 2000 году 1,7 миллиона (1,8%) африканских детей, проживающих в регионах мира, где распространена малярия. обычно были защищены ИНН. Это число увеличилось до 20,3 миллиона (18,5%) африканских детей, использующих ITN в 2007 году, в результате чего 89,6 миллиона детей остались без защиты и до 68% африканских детей, использующих москитные сетки в 2015 году. Большинство сеток пропитаны пиретроидами, классом инсектицидов с низкой токсичностью. Они наиболее эффективны при использовании от заката до рассвета. Рекомендуется повесить большую «сетку для кровати» над центром кровати и либо подложить края под матрас, либо убедиться, что она достаточно большая, чтобы касаться земли. ОИС полезны для исходов беременности в эндемичных по малярии регионах Африки, но требуется больше данных по Азии и Латинской Америке.
В районах с высокой устойчивостью к малярии пиперонилбутоксид (ПБО) в сочетании с пиретроидами в противомоскитных сетках эффективен для снижения показателей заражения малярией. Остаются вопросы относительно долговечности PBO на сетках, поскольку влияние на смертность комаров не было подтверждено после двадцати стирок в экспериментальных испытаниях.
Остаточное распыление в помещении - это распыление инсектицидов на стены внутри дома. После кормления многие комары отдыхают на соседней поверхности, переваривая кровяную муку, поэтому, если стены домов были покрыты инсектицидами, отдыхающих комаров можно убить, прежде чем они смогут укусить другого человека и передать малярийного паразита. По состоянию на 2006 год Всемирная организация здравоохранения рекомендует 12 инсектицидов для операций IRS, включая ДДТ и пиретроиды цифлутрин и дельтаметрин. Такое использование небольших количеств ДДТ в здравоохранении разрешено Стокгольмской конвенцией, которая запрещает его использование в сельском хозяйстве. Одна проблема со всеми формами IRS - устойчивость к инсектицидам. Комары, пораженные IRS, как правило, отдыхают и живут в помещении, а из-за раздражения, вызванного опрыскиванием, их потомки, как правило, отдыхают и живут на открытом воздухе, а это означает, что они меньше подвержены влиянию IRS. Неясно, эффективно ли использование IRS вместе с ITN для сокращения случаев малярии из-за большого географического разнообразия распространения малярии, передачи малярии и устойчивости к инсектицидам.
Жилье является фактором риска малярии, и модификация дома в качестве меры профилактики может быть устойчивой стратегией, которая не зависит от эффективности инсектицидов, таких как пиретроиды. Необходимо учитывать физическую среду внутри и снаружи дома, которая может увеличить плотность комаров. Примеры возможных модификаций включают близость дома к местам размножения комаров, дренаж и водоснабжение рядом с домом, наличие мест отдыха комаров (растительность вокруг дома), близость к живому скоту и домашним животным, а также физические улучшения или модификации конструкция жилища предотвращает попадание комаров.
Люди испробовали ряд других методов, чтобы уменьшить количество укусов комаров и замедлить распространение малярии. Попытки уменьшить количество личинок комаров за счет уменьшения доступности открытой воды там, где они развиваются, или путем добавления веществ, замедляющих их развитие, в некоторых местах эффективны. Электронные репелленты от комаров, которые издают очень высокочастотные звуки, призванные отпугивать самок комаров, не имеют подтверждающих доказательств эффективности. Доказательств того, что запотевание может влиять на передачу малярии, мало. Уничтожение личинок путем ручной доставки химических или микробных инсектицидов в водоемы с низким уровнем распространения личинок может снизить передачу малярии. Недостаточно доказательств, чтобы определить, могут ли личинки рыбы снизить плотность комаров и их передачу в этом районе.
Существует ряд лекарств, которые могут помочь предотвратить или остановить малярию у путешественников в места, где инфекция является обычным явлением. Многие из этих лекарств также используются в лечении. В местах, где плазмодий устойчив к одному или нескольким лекарствам, для профилактики часто используются три препарата - мефлохин, доксициклин или комбинация атоваквон / прогуанил ( Маларон). Доксициклин и атоваквон / прогуанил переносятся лучше, в то время как мефлохин принимают один раз в неделю. Районы мира с чувствительной к хлорохину малярией встречаются нечасто. Массовое введение противомалярийных препаратов всему населению одновременно может снизить риск заражения малярией среди населения.
Защитный эффект начинается не сразу, и люди, посещающие районы, где существует малярия, обычно начинают принимать лекарства за одну-две недели до прибытия и продолжают принимать их в течение четырех недель после отъезда (за исключением атоваквона / прогуанила, которые нужно только начать. за два дня до и продолжали в течение семи дней после). Использование профилактических препаратов часто нецелесообразно для тех, кто живет в районах, где существует малярия, и их обычно принимают только беременные женщины и краткосрочные посетители. Это связано со стоимостью лекарств, побочными эффектами от длительного использования и трудностями в получении противомалярийных препаратов за пределами богатых стран. Было обнаружено, что во время беременности лекарства для предотвращения малярии улучшают вес ребенка при рождении и снижают риск анемии у матери. Использование профилактических препаратов при наличии малярийных комаров может способствовать развитию частичной резистентности.
Назначение противомалярийных препаратов младенцам с помощью периодической профилактической терапии может снизить риск заражения малярией, госпитализации и анемии.
Мефлохин более эффективен, чем сульфадоксин-пириметамин, в профилактике малярии у ВИЧ-отрицательных беременных женщин. Котримоксазол эффективен для предотвращения заражения малярией и снижает риск развития анемии у ВИЧ-инфицированных женщин. Назначение сульфадоксин-пириметамина в трех или более дозах в качестве периодической профилактической терапии лучше, чем две дозы для ВИЧ-инфицированных женщин, живущих в эндемичных по малярии районах.
Своевременное лечение подтвержденных случаев комбинированной терапией на основе артемизинина (АКТ) также может снизить передачу.
Стратегии участия сообществ и санитарного просвещения, способствующие осознанию малярии и важности мер контроля, были успешно использованы для снижения заболеваемости малярией в некоторых регионах развивающегося мира. Распознавание болезни на ранних стадиях может предотвратить ее смертельный исход. Просвещение также может информировать людей о необходимости прикрытия участков со стоячей, стоячей водой, таких как резервуары для воды, которые являются идеальными рассадниками паразитов и комаров, тем самым снижая риск передачи инфекции между людьми. Обычно это используется в городских районах, где есть крупные населенные пункты в ограниченном пространстве, и передача инфекции наиболее вероятна в этих районах. Прерывистая профилактическая терапия - это еще одно мероприятие, которое успешно применялось для борьбы с малярией у беременных женщин и младенцев, а также у детей дошкольного возраста, где передача носит сезонный характер.
 Реклама хинина как средства от малярии с 1927 года.
Реклама хинина как средства от малярии с 1927 года. Малярия лечится противомалярийными препаратами ; используемые зависит от типа и тяжести заболевания. Хотя обычно используются лекарства от лихорадки, их влияние на исходы неясно. Обеспечение домашних хозяйств бесплатными противомалярийными препаратами может снизить детскую смертность при правильном использовании. Программы, предполагающие лечение всех причин лихорадки противомалярийными препаратами, могут привести к чрезмерному использованию противомалярийных препаратов и недостаточному лечению других причин лихорадки. Тем не менее, использование наборов для быстрой диагностики малярии может помочь снизить чрезмерное использование противомалярийных препаратов.
Простую или неосложненную малярию можно лечить пероральными препаратами. Препараты артемизинина эффективны и безопасны при лечении неосложненной малярии. Артемизинин в сочетании с другими противомалярийными средствами (известный как комбинированная терапия с артемизинином или АКТ) эффективен примерно на 90% при лечении неосложненной малярии. Наиболее эффективным лечением инфекции P. falciparum является использование АКТ, снижающего устойчивость к любому отдельному компоненту препарата. Артеметер-люмефантрин (режим из шести доз) более эффективен, чем режим артеметер-люмефантрин (режим из четырех доз) или другие схемы, не содержащие производных артемизинина, при лечении малярии falciparum. Еще одна рекомендуемая комбинация - дигидроартемизинин и пиперахин. Комбинированная терапия артемизинином и нафтохином показала многообещающие результаты в лечении малярии, вызванной falciparum. Однако необходимы дополнительные исследования, чтобы установить его эффективность в качестве надежного лечения. Артесунат плюс мефлохин эффективнее одного мефлохина при лечении неосложненной малярии falciparum в условиях низкой передачи. Атоваквон-прогуанил эффективен против неосложненного falciparum с вероятностью неудачи от 5% до 10%; добавление артесуната может снизить частоту отказов. Монотерапия азитромицином или комбинированная терапия не показали эффективности при лечении малярии, вызванной плазмодиями или vivax. Амодиахин в сочетании с сульфадоксин-пириметамином может привести к меньшему количеству неудач при лечении по сравнению с одним сульфадоксин-пириметамином при неосложненной малярии falciparum. Данных о применении хлорпрогуанил-дапсона для лечения неосложненной малярии, вызванной falciparum, недостаточно. Добавление примахина к комбинированной терапии на основе артемизинина от малярии, вызванной falciparum, снижает ее передачу на 3-4-й и 8-й день инфекции. Сульфадоксин-пириметамин плюс артесунат лучше, чем сульфадоксин-пириметамин плюс амодиахин, в борьбе с неэффективностью лечения на 28-й день. Однако последний лучше, чем первый, в снижении гаметоцитов в крови на 7-й день.
Заражение P. vivax, P. ovale или P. malariae обычно не требует госпитализации. Лечение P. vivax требует как лечения стадий в крови (хлорохином или АКТ), так и удаления печеночных форм примахином. Комбинированная терапия на основе артемизинина так же эффективна, как и хлорохин, при лечении неосложненной малярии, вызванной P. vivax. Лечение тафенохином предотвращает рецидивы после подтвержденной малярии, вызванной P. vivax. Однако тем, кто лечился хлорохином от инфекции на стадии крови, требуется 14 дней лечения примахином для предотвращения рецидива. Более короткие схемы приема примахина могут привести к более высокому уровню рецидивов. Нет никакой разницы в эффективности между примахином, вводимым в течение семи или 14 дней для предотвращения рецидива малярии vivax. Более короткий режим может быть полезен тем, у кого есть проблемы с соблюдением режима лечения.
Для лечения малярии во время беременности ВОЗ рекомендует использовать хинин плюс клиндамицин на ранних сроках беременности (1-й триместр) и АКТ на более поздних сроках (2-й и 3-й триместры). Данные о безопасности противомалярийных препаратов при беременности ограничены.
Случаи тяжелой и сложной малярии почти всегда вызываются инфицированием P. falciparum. Другие виды обычно вызывают только лихорадочное заболевание. В тяжелых и сложных случаях малярии требуется неотложная медицинская помощь, поскольку уровень смертности высок (от 10% до 50%).
Рекомендуемое лечение тяжелой формы малярии - внутривенное введение противомалярийных препаратов. При тяжелой форме малярии парентеральный артесунат превосходил хинин как у детей, так и у взрослых. В другом систематическом обзоре производные артемизинина (артеметер и артетер) были столь же эффективны, как и хинин, при лечении церебральной малярии у детей. Лечение тяжелой формы малярии включает поддерживающие меры, которые лучше всего проводить в отделении интенсивной терапии. Это включает в себя лечение высокой температуры и судорог, которые могут возникнуть в результате этого. Он также включает мониторинг недостаточного дыхательного усилия, низкого уровня сахара в крови и низкого уровня калия в крови. Производные артемизинина обладают такой же или большей эффективностью, чем хинолоны, в предотвращении смерти при тяжелой или осложненной малярии. Ударная доза хинина помогает сократить продолжительность лихорадки и увеличивает выведение паразитов из организма. Нет никакой разницы в эффективности при интраректальном применении хинина по сравнению с внутривенным или внутримышечным хинином при лечении неосложненной / осложненной малярии falciparum. Доказательств того, что внутримышечный артеетер для лечения тяжелой формы малярии недостаточно. Предоставление ректального артесуната перед переводом в больницу может снизить уровень смертности детей с тяжелой формой малярии.
Церебральная малярия - это форма тяжелой и сложной малярии с наихудшими неврологическими симптомами. Недостаточно данных о том, эффективны ли осмотические агенты, такие как маннит или мочевина, при лечении церебральной малярии. Обычный фенобарбитон при церебральной малярии связан с меньшим количеством судорог, но, возможно, с большим количеством смертей. Нет никаких доказательств того, что стероиды могут принести пользу при лечении церебральной малярии.
Недостаточно доказательств того, что переливание крови полезно либо для снижения смертности детей с тяжелой анемией, либо для улучшения их гематокрита в течение одного месяца. Недостаточно доказательств того, что агенты, хелатирующие железо, такие как дефероксамин и деферипрон, улучшают исходы у больных малярией falciparum.
Устойчивость к лекарствам представляет собой растущую проблему в лечении малярии в 21 веке. В 2000-х (десятилетие) малярия с частичной устойчивостью к артемизину появилась в Юго-Восточной Азии. В настоящее время резистентность широко распространена ко всем классам противомалярийных препаратов, кроме артемизининов. Лечение устойчивых штаммов становилось все более зависимым от этого класса препаратов. Стоимость артемизининов ограничивает их использование в развивающихся странах. Штаммы малярии, обнаруженные на границе Камбоджи и Таиланда, устойчивы к комбинированной терапии, включающей артемизинины, и поэтому могут быть неизлечимыми. Воздействие на популяцию паразитов монотерапии артемизинином в субтерапевтических дозах в течение более 30 лет и доступность некачественных артемизининов, вероятно, привели к выбору устойчивого фенотипа. Устойчивость к артемизинину была обнаружена в Камбодже, Мьянме, Таиланде и Вьетнаме, а в Лаосе появилась резистентность. Устойчивость к комбинации артемизинина и пиперахина была впервые обнаружена в 2013 году в Камбодже, а к 2019 году распространилась по Камбодже, а также в Лаосе, Таиланде и Вьетнаме (с устойчивостью до 80 процентов паразитов малярии в некоторых регионах).
Недостаточно доказательств того, что противомалярийные препараты в индивидуальной упаковке предотвращают неэффективное лечение малярийной инфекции. Однако, если это подкреплено обучением медицинских работников и информацией о пациентах, наблюдается улучшение соблюдения режима лечения со стороны тех, кто получает лечение.
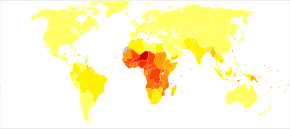 Год жизни с поправкой на инвалидность по малярии на 100 000 жителей в 2004 г. нет данных lt;10 0–100 100–500 500–1000 1000–1500 1500–2000 2000–2500 2500–2750 2750–3000 3000–3250 3250–3500 ≥3500
Год жизни с поправкой на инвалидность по малярии на 100 000 жителей в 2004 г. нет данных lt;10 0–100 100–500 500–1000 1000–1500 1500–2000 2000–2500 2500–2750 2750–3000 3000–3250 3250–3500 ≥3500 При правильном лечении люди с малярией обычно могут ожидать полного выздоровления. Однако тяжелая форма малярии может прогрессировать очень быстро и привести к смерти в течение нескольких часов или дней. В самых тяжелых случаях заболевания летальность может достигать 20% даже при интенсивной терапии и лечении. В более долгосрочной перспективе были зарегистрированы нарушения развития у детей, перенесших тяжелые эпизоды малярии. Хроническая инфекция без тяжелого заболевания может возникать при синдроме иммунодефицита, связанном со сниженной реакцией на бактерии сальмонеллы и вирус Эпштейна-Барра.
В детстве малярия вызывает анемию в период быстрого развития мозга, а также прямое повреждение мозга в результате церебральной малярии. Некоторые люди, пережившие церебральную малярию, имеют повышенный риск неврологического и когнитивного дефицита, поведенческих расстройств и эпилепсии. В клинических испытаниях было показано, что профилактика малярии улучшает когнитивные функции и успеваемость в школе по сравнению с группами плацебо.
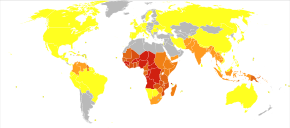 Смертность от малярии на миллион человек в 2012 г. 0–0 1-2 3–54 55–325 326–679 680–949 950–1 358
Смертность от малярии на миллион человек в 2012 г. 0–0 1-2 3–54 55–325 326–679 680–949 950–1 358  Прошлая и текущая распространенность малярии в 2009 г.
Прошлая и текущая распространенность малярии в 2009 г. По оценкам ВОЗ, в 2019 году было зарегистрировано 229 миллионов новых случаев малярии, в результате которых погибло 409 000 человек. Больше всего страдают дети в возрасте до 5 лет, на которые в 2019 году приходится 67% случаев смерти от малярии во всем мире. Ежегодно риску заражения подвергаются около 125 миллионов беременных женщин; в Африке к югу от Сахары материнская малярия связана с оценкой до 200 000 младенческих смертей ежегодно. Ежегодно в Западной Европе регистрируется около 10 000 случаев малярии, а в США - 1300–1500. В 1951 году в Соединенных Штатах Америки была ликвидирована малярия как серьезная проблема общественного здравоохранения, хотя небольшие вспышки болезни продолжаются. В период с 1993 по 2003 год в Европе от этой болезни умерло около 900 человек. Как глобальная заболеваемость, так и связанная с этим смертность снизились за последние годы. По данным ВОЗ и ЮНИСЕФ, смертность от малярии в 2015 году снизилась на 60% по сравнению с оценкой 2000 года, когда она составляла 985 000, в основном благодаря широкому использованию обработанных инсектицидами сеток и комбинированной терапии на основе артемизинина. В 2012 году было зарегистрировано 207 миллионов случаев малярии. В том году от этой болезни, по оценкам, погибло от 473 000 до 789 000 человек, многие из которых были детьми в Африке. Усилия по уменьшению заболеваемости в Африке с 2000 г. были частично эффективными, при этом темпы заболеваемости на континенте снизились примерно на сорок процентов.
В настоящее время малярия является эндемическим заболеванием в широком диапазоне вокруг экватора, в районах Северной и Южной Америки, во многих частях Азии и на большей части Африки; в Африке к югу от Сахары происходит 85–90% случаев смерти от малярии. По оценкам на 2009 год, странами с самым высоким уровнем смертности на 100 000 населения были Кот-д'Ивуар (86,15), Ангола (56,93) и Буркина-Фасо (50,66). По оценкам 2010 года, самыми смертоносными странами на душу населения были Буркина-Фасо, Мозамбик и Мали. Проект « Атлас малярии» направлен на нанесение на карту глобальных уровней малярии, что дает возможность определить глобальные пространственные пределы болезни и оценить бремя болезни. Эти усилия привели к публикации карты эндемичности P. falciparum в 2010 г. и обновленной версии в 2019 г. По состоянию на 2010 г. около 100 стран имели эндемическую малярию. Ежегодно эти страны посещают 125 миллионов международных путешественников, и более 30 000 заражаются этой болезнью.
Географическое распространение малярии в крупных регионах является сложным, и районы, пораженные малярией, и районы, свободные от малярии, часто находятся недалеко друг от друга. Малярия широко распространена в тропических и субтропических регионах из-за дождей, постоянно высоких температур и высокой влажности, а также стоячей воды, где личинки комаров легко созревают, обеспечивая им среду, в которой они нуждаются для непрерывного размножения. В более засушливых районах вспышки малярии были предсказаны с достаточной точностью путем картирования осадков. Малярия чаще встречается в сельской местности, чем в городах. Например, несколько городов в субрегионе Большого Меконга в Юго-Восточной Азии практически свободны от малярии, но болезнь распространена во многих сельских регионах, в том числе вдоль международных границ и на лесных опушках. Напротив, малярия в Африке присутствует как в сельских, так и в городских районах, хотя риск ниже в крупных городах.
Изменение климата может повлиять на передачу малярии, но степень воздействия и затронутые районы остаются неопределенными. Увеличение количества осадков в некоторых районах Индии и после явления Эль-Ниньо связано с увеличением числа комаров.
С 1900 года в Африке произошли существенные изменения температуры и количества осадков. Однако факторы, влияющие на то, как осадки приводят к образованию воды для размножения комаров, являются сложными, включая степень, в которой она поглощается почвой и растительностью, например, или скорость стока и испарения. Недавние исследования позволили получить более глубокую картину условий в Африке, объединив модель климатической пригодности для малярии с моделью континентального масштаба, представляющей реальные гидрологические процессы.
 Древние ооцисты малярии сохранились в доминиканском янтаре
Древние ооцисты малярии сохранились в доминиканском янтаре Хотя паразит, ответственный за малярию P. falciparum, существует уже 50 000–100 000 лет, численность популяции паразита не увеличивалась примерно 10 000 лет назад одновременно с прогрессом в сельском хозяйстве и развитием населенных пунктов. Близкие родственники малярийных паразитов человека остаются обычным явлением у шимпанзе. Некоторые данные свидетельствуют о том, что малярия, вызванная P. falciparum, могла возникнуть у горилл.
Ссылки на уникальные периодические лихорадки малярии встречаются на протяжении всей истории. Гиппократ описал периодические лихорадки, назвав их третичными, четвертичными, субтертовыми и повседневными. Римская Колумелла связала болезнь с насекомыми с болот. Малярия, возможно, способствовала упадку Римской империи и была настолько распространена в Риме, что была известна как « римская лихорадка ». Некоторые регионы Древнего Рима считались подверженными риску заболевания из-за благоприятных условий для переносчиков малярии. Сюда входили такие области, как южная Италия, остров Сардиния, Понтийские болота, нижние районы прибрежной Этрурии и город Рим на берегу Тибра. Наличие стоячей воды в этих местах предпочитали комары для нерестилищ. Орошаемые сады, болотистые земли, стоки с сельскохозяйственных угодий и проблемы с дренажем в результате строительства дорог привели к увеличению стоячей воды.
 Британский доктор Рональд Росс получил Нобелевскую премию по физиологии и медицине в 1902 году за свою работу по малярии.
Британский доктор Рональд Росс получил Нобелевскую премию по физиологии и медицине в 1902 году за свою работу по малярии. Термин «малярия» происходит от средневекового итальянского : mala aria - « плохой воздух »; болезнь ранее называлась лихорадкой или болотной лихорадкой из-за ее связи с болотами и болотами. Этот термин впервые появился в английской литературе около 1829 года. Когда-то малярия была распространена в большей части Европы и Северной Америки, где она больше не является эндемической, хотя завозные случаи все же случаются.
Малярия не упоминается в «медицинских книгах» майя или ацтеков. Европейские поселенцы и западноафриканцы, которых они поработили, вероятно, принесли малярию в Америку, начиная с 16 века.
Научные исследования малярии сделали свой первый значительный прогресс в 1880 году, когда Шарль Луи Альфонс Лаверан - французский армейский врач, работавший в военном госпитале Константина в Алжире - впервые обнаружил паразитов в красных кровяных тельцах инфицированных людей. Таким образом, он предположил, что малярия вызывается этим организмом, и это был первый раз, когда простейший был идентифицирован как вызывающий заболевание. За это и последующие открытия он был удостоен Нобелевской премии 1907 года по физиологии и медицине. Год спустя Карлос Финлей, кубинский врач, лечащий людей с желтой лихорадкой в Гаване, представил убедительные доказательства того, что комары передают болезни людям и от них. Эта работа последовала за более ранними предложениями Джозии К. Нотта и работой сэра Патрика Мэнсона, «отца тропической медицины», о передаче филяриатоза.
 Китайский медицинский исследователь Ту Юю получила Нобелевскую премию по физиологии и медицине в 2015 году за свою работу над противомалярийным препаратом артемизинин.
Китайский медицинский исследователь Ту Юю получила Нобелевскую премию по физиологии и медицине в 2015 году за свою работу над противомалярийным препаратом артемизинин. В апреле 1894 года шотландский врач сэр Рональд Росс посетил сэра Патрика Мэнсона в его доме на улице Королевы Анны в Лондоне. Этот визит стал началом четырехлетнего сотрудничества и страстных исследований, кульминацией которых стал 1897 год, когда Росс, работавший в Президентской больнице общего профиля в Калькутте, доказал полный жизненный цикл малярийного паразита в комарах. Таким образом, он доказал, что москит был переносчиком малярии у людей, показав, что некоторые виды комаров передают малярию птицам. Он выделил малярийных паразитов из слюнных желез комаров, которые питались зараженными птицами. За эту работу Росс получил Нобелевскую премию по медицине 1902 года. После ухода из Индийской медицинской службы Росс работал в недавно созданной Ливерпульской школе тропической медицины и руководил усилиями по борьбе с малярией в Египте, Панаме, Греции и Маврикии. Выводы Финли и Росса были позже подтверждены медицинской комиссией, возглавляемой Уолтером Ридом, в 1900 году. Его рекомендации были реализованы Уильямом К. Горгасом в мерах по охране здоровья, предпринятых во время строительства Панамского канала. Эта работа в области общественного здравоохранения спасла жизни тысяч рабочих и помогла разработать методы, которые будут использоваться в будущих кампаниях общественного здравоохранения против этой болезни.
В 1896 году Амико Биньями обсуждал роль комаров в малярии. В 1898 году Биньями, Джованни Баттиста Грасси и Джузеппе Бастианелли удалось экспериментально показать передачу малярии среди людей, используя инфицированных комаров для заражения малярией, которые они представили в ноябре 1898 года Академии Линчеи.
 Artemisia annua, источник противомалярийного препарата артемизинин
Artemisia annua, источник противомалярийного препарата артемизинин Первым эффективным средством против малярии стала кора хинного дерева, содержащая хинин. Это дерево растет на склонах Анд, в основном в Перу. В коренных народов Перу сделал настойку хинного для контроля температуры. Его эффективность против малярии была обнаружена, и около 1640 года иезуиты представили это лечение Европе; к 1677 году он был включен в Лондонскую фармакопею как противомалярийный препарат. Лишь в 1820 году из коры был выделен активный ингредиент, хинин, который был выделен и назван французскими химиками Пьером Жозефом Пеллетье и Жозефом Бьенэме Кавенту.
Хинин был преобладающим лекарством от малярии до 1920-х годов, когда начали появляться другие лекарства. В 1940-х годах хлорохин заменил хинин в лечении как неосложненной, так и тяжелой малярии до тех пор, пока не возникла резистентность, сначала в Юго-Восточной Азии и Южной Америке в 1950-х годах, а затем во всем мире в 1980-х годах.
Лечебная ценность Artemisia annua использовалась китайскими травниками в традиционной китайской медицине на протяжении 2000 лет. В 1596 году Ли Шичжэнь рекомендовал чай из цинхао специально для лечения симптомов малярии в своем « Компендиуме Materia Medica ». Артемизинины, обнаруженные китайским ученым Ту Юю и его коллегами в 1970-х годах из растения Artemisia annua, стали рекомендованным средством лечения малярии P. falciparum, которое в тяжелых случаях назначают в сочетании с другими противомалярийными средствами. Ту говорит, что на нее повлиял источник традиционной китайской фитотерапии - «Справочник рецептов для неотложной помощи», написанный в 340 году Ге Хонгом. За свою работу по малярии Ту Юю была удостоена Нобелевской премии по физиологии и медицине 2015 года.
Plasmodium vivax использовался между 1917 и 1940- ми годами для маляриотерапии - преднамеренной инъекции малярийных паразитов, чтобы вызвать лихорадку для борьбы с некоторыми заболеваниями, такими как третичный сифилис. В 1927 году изобретатель этой техники Юлиус Вагнер-Яурегг получил за свои открытия Нобелевскую премию по физиологии и медицине. Этот метод был опасен, погибло около 15% пациентов, поэтому он больше не используется.
 Морские пехотинцы США с малярией в полевом госпитале на Гуадалканале, октябрь 1942 г.
Морские пехотинцы США с малярией в полевом госпитале на Гуадалканале, октябрь 1942 г. Первым пестицидом, использованным для опрыскивания остаточных веществ в помещениях, был ДДТ. Хотя первоначально он использовался исключительно для борьбы с малярией, его использование быстро распространилось на сельское хозяйство. Со временем борьба с вредителями, а не борьба с болезнями, стала доминирующей в использовании ДДТ, и это широкомасштабное сельскохозяйственное использование привело к появлению устойчивых к пестицидам комаров во многих регионах. Устойчивость к ДДТ, проявляемую комарами Anopheles, можно сравнить с устойчивостью к антибиотикам, проявляемой бактериями. В течение 1960-х годов возросло понимание негативных последствий его неизбирательного использования, что в конечном итоге привело к запрету на сельскохозяйственное применение ДДТ во многих странах в 1970-х годах. До появления ДДТ малярия успешно исключалась или контролировалась в тропических регионах, таких как Бразилия и Египет, путем удаления или отравления мест размножения комаров или водной среды обитания личиночных стадий, например, путем применения высокотоксичного соединения мышьяка Paris Green в местах со стоячими корнями. воды.
Вакцины против малярии были труднодостижимой целью исследований. Первые многообещающие исследования, демонстрирующие потенциал вакцины против малярии, были выполнены в 1967 году путем иммунизации мышей живыми радиационно- ослабленными спорозоитами, которые обеспечивали значительную защиту мышей при последующей инъекции нормальных жизнеспособных спорозоитов. С 1970-х годов были предприняты значительные усилия по разработке аналогичных стратегий вакцинации людей. Первая вакцина, получившая название RTS, S, была одобрена европейскими регулирующими органами в 2015 году.
 Клиника малярии в Танзании
Клиника малярии в Танзании Малярия - это не просто болезнь, обычно связанная с бедностью : некоторые данные свидетельствуют о том, что она также является причиной бедности и серьезным препятствием для экономического развития. Хотя больше всего страдают тропические регионы, наибольшее влияние малярия распространяется на некоторые зоны с умеренным климатом, которые имеют резкие сезонные изменения. Заболевание было связано с серьезными негативными экономическими последствиями для регионов, где оно широко распространено. В конце 19-го и начале 20-го веков он был основным фактором медленного экономического развития южных штатов Америки.
Сравнение среднего ВВП на душу населения в 1995 году с поправкой на паритет покупательной способности между странами с малярией и странами без малярии дает пятикратную разницу (1 526 долларов США против 8 268 долларов США). В период с 1965 по 1990 год в странах, где малярия была обычным явлением, средний показатель ВВП на душу населения увеличивался всего на 0,4% в год по сравнению с 2,4% в год в других странах.
Бедность может увеличить риск малярии, поскольку у бедняков нет финансовых возможностей для предотвращения или лечения этой болезни. В целом экономические последствия малярии, по оценкам, ежегодно обходятся Африке в 12 миллиардов долларов США. Экономические последствия включают в себя расходы на здравоохранение, рабочие дни, потерянные из-за болезни, дни, потерянные в образовании, снижение производительности из-за повреждения мозга от церебральной малярии, а также потерю инвестиций и туризма. Заболевание является тяжелым бременем в некоторых странах, где на него может приходиться 30–50% госпитализаций, до 50% амбулаторных посещений и до 40% расходов на общественное здравоохранение.
 Ребенок с малярией в Эфиопии
Ребенок с малярией в Эфиопии Церебральная малярия - одна из основных причин неврологических нарушений у африканских детей. Исследования, сравнивающие когнитивные функции до и после лечения тяжелой малярийной болезни, продолжали показывать значительное ухудшение успеваемости и когнитивных способностей даже после выздоровления. Следовательно, тяжелая форма малярии и церебральная малярия имеют далеко идущие социально - экономические последствия, выходящие за рамки непосредственных последствий болезни.
Изощренные подделки были обнаружены в нескольких азиатских странах, таких как Камбоджа, Китай, Индонезия, Лаос, Таиланд и Вьетнам, и являются основной причиной предотвратимой смерти в этих странах. По данным ВОЗ, исследования показывают, что до 40% лекарств от малярии на основе артесуната являются поддельными, особенно в регионе Большого Меконга. Они создали систему быстрого оповещения, чтобы быстро сообщать информацию о поддельных лекарствах в соответствующие органы в странах-участницах. Для врачей или непрофессионалов нет надежного способа обнаружить поддельные лекарства без помощи лаборатории. Компании пытаются бороться с устойчивостью контрафактных лекарств, используя новые технологии для обеспечения безопасности от источника до распределения.
Другой проблемой для клинической практики и общественного здравоохранения является распространение некачественных противомалярийных лекарств в результате несоответствующей концентрации ингредиентов, загрязнения другими лекарствами или токсичными примесями, ингредиентов низкого качества, плохой стабильности и ненадлежащей упаковки. Исследование 2012 года показало, что примерно треть противомалярийных препаратов в Юго-Восточной Азии и странах Африки к югу от Сахары не прошли химический анализ, анализ упаковки или были подделаны.
 Плакат Второй мировой войны
Плакат Второй мировой войны На протяжении всей истории заражение малярией играло важную роль в судьбах правительственных правителей, национальных государств, военнослужащих и военных действий. В 1910 году лауреат Нобелевской премии по медицине Рональд Росс (сам выживший после малярии) опубликовал книгу «Профилактика малярии», в которую вошла глава «Профилактика малярии на войне». Автор главы, полковник Ч. К. Мелвилл, профессор гигиены Медицинского колледжа Королевской армии в Лондоне, обратился к выдающейся роли, которую малярия исторически играла во время войн: «Историю малярии во время войны можно почти принять за историю самой войны, конечно же, история войн в христианскую эпоху... Вероятно, дело в том, что многие из так называемых лагерных лихорадок, а также, вероятно, значительная часть лагерной дизентерии войн шестнадцатого, семнадцатого и восемнадцатого веков были малярийными по происхождению ". В оккупированной британцами Индии коктейль из джин-тоника, возможно, появился как способ приема хинина, известного своими противомалярийными свойствами.
Малярия была самой серьезной опасностью для здоровья, с которой столкнулись американские войска в южной части Тихого океана во время Второй мировой войны, где были инфицированы около 500 000 человек. По словам Джозефа Патрика Бирна, «шестьдесят тысяч американских солдат умерли от малярии во время кампаний в Африке и южной части Тихого океана».
Были вложены значительные финансовые средства в закупку существующих и создание новых противомалярийных препаратов. Во время Первой и Второй мировых войн непостоянные поставки натуральных противомалярийных препаратов из коры хинного дерева и хинина привели к существенному финансированию исследований и разработок других лекарств и вакцин. Американские военные организации, проводящие такие исследовательские инициативы, включают Медицинский исследовательский центр ВМС, Исследовательский институт армии Уолтера Рида и Медицинский научно-исследовательский институт инфекционных болезней армии США.
Кроме того, были созданы такие инициативы, как «Контроль малярии в районах военных действий» (MCWA), созданный в 1942 году, и его преемник, Центр инфекционных заболеваний (ныне известный как Центры по контролю и профилактике заболеваний, или CDC), созданный в 1946 году. CDC, MCWA, «был создан для борьбы с малярией вокруг военных учебных баз на юге Соединенных Штатов и их территорий, где малярия все еще была проблемой».
 Члены Комиссии по малярии Лиги Наций собирают личинок в дельте Дуная, 1929 г.
Члены Комиссии по малярии Лиги Наций собирают личинок в дельте Дуная, 1929 г. Делается несколько заметных попыток уничтожить паразита в разных частях мира или искоренить его во всем мире. В 2006 году организация Malaria No More поставила перед обществом цель искоренить малярию в Африке к 2015 году, и организация заявила, что планирует распустить, если эта цель будет достигнута. В 2007 г. Всемирный день борьбы с малярией был учрежден 60-й сессией Всемирной ассамблеи здравоохранения. По состоянию на 2018 год они все еще функционируют. Только одна вакцина против малярии лицензирована для использования, в то время как несколько других вакцины проходят клинические испытания, которые предназначены для защиты детей в эндемичных районах и снижения скорости передачи болезни. По состоянию на 2012 год Глобальный фонд для борьбы со СПИДом, туберкулезом и малярией распространил 230 миллионов обработанных инсектицидами сеток, предназначенных для предотвращения передачи малярии через комаров. Фонд Клинтона из США работает над управлением спросом и стабилизацией цен на рынке артемизинина. Другие усилия, такие как проект «Атлас малярии», сосредоточены на анализе информации о климате и погоде, необходимой для точного прогнозирования распространения малярии на основе наличия среды обитания для паразитов, переносящих малярию. Политика Консультативный комитет Малярия (MPAC) от Всемирной организации здравоохранения (ВОЗ) была создана в 2012 году, «для выработки стратегических рекомендаций и технического вклада ВОЗ по всем аспектам борьбы с малярией и ликвидации». В ноябре 2013 года ВОЗ и группа спонсоров вакцины против малярии поставили цель разработать вакцины, предназначенные для прерывания передачи малярии, с долгосрочной целью искоренения малярии.
В некоторых областях малярия была успешно ликвидирована или значительно уменьшена. Когда-то малярия была обычным явлением в Соединенных Штатах и южной Европе, но программы борьбы с переносчиками болезней в сочетании с мониторингом и лечением инфицированных людей устранили ее в этих регионах. Этому способствовали несколько факторов, такие как осушение водно-болотных угодий для выращивания сельскохозяйственных культур и другие изменения в практике управления водными ресурсами, а также достижения в области санитарии, включая более широкое использование стеклянных окон и экранов в жилищах. С помощью таких методов малярия была ликвидирована на большей части территории Соединенных Штатов в начале 20 века. Использование пестицида ДДТ и других средств устранило его из оставшихся карманов Юга в 1950-х годах в рамках Национальной программы ликвидации малярии.
Одной из задач цели 3 из ООН «s целей устойчивого развития является прекращение эпидемии малярии во всех странах к 2030 году.
В 2015 году ВОЗ поставила цель сократить к 2030 году смертность от малярии на 90%, а в 2016 году Билл Гейтс заявил, что, по его мнению, глобальное искоренение малярии возможно к 2040 году.
В 2018 году ВОЗ объявила, что Парагвай свободен от малярии после усилий по ликвидации, начатых в 1950 году.
В 2000 году Организация Объединенных Наций начала программу «Борьба с малярией» и обозначила одну из важнейших задач Целей развития тысячелетия. В основном он проводился для предотвращения смерти и болезней детей до 5 лет. До 2016 года Глобальный фонд против ВИЧ / СПИДа, туберкулеза и малярии предоставил 659 миллионов ITN (обработанных инсектицидами надкроватных сеток), организовал поддержку и обучение для предотвращения малярии. Проблемы высоки из-за нехватки средств, хрупкой структуры здравоохранения и удаленности коренного населения, с которым может быть трудно связаться и получить образование. Большинство коренного населения полагается на самодиагностику, самолечение, целитель и традиционную медицину. ВОЗ подала заявку на финансирование в Фонд Гейтса, который поддерживает действия по искоренению малярии в 2007 году. В шести странах, Объединенных Арабских Эмиратах, Марокко, Армении, Туркменистане, Кыргызстане и Шри-Ланке не было случаев местных случаев малярии в течение трех лет подряд, и Сертифицирован ВОЗ как свободный от малярии, несмотря на стагнацию финансирования в 2010 году. Финансирование необходимо для покрытия расходов на лекарства, и госпитализация не может поддерживаться бедными странами, где болезнь широко распространена. Цель искоренения не была достигнута, тем не менее, темпы снижения заболеваемости значительны.
По состоянию на 2019 год процесс искоренения малярии продолжается, но будет сложно добиться мира, свободного от малярии, с помощью текущих подходов и инструментов. Подходы могут потребовать дополнительных инвестиций в исследования и более универсального здравоохранения. Продолжение эпиднадзора также будет иметь важное значение для предотвращения возвращения малярии в страны, где это заболевание было ликвидировано.
Инициатива Программы исследований по искоренению малярии (malERA) представляла собой консультативный процесс для определения того, какие области исследований и разработок (НИОКР) должны быть рассмотрены для искоренения малярии во всем мире.
Вакцина против малярии под названием RTS, S / AS01 (RTS, S) была одобрена европейскими регулирующими органами в 2015 году. По состоянию на 2019 год она проходит пилотные испытания в трех странах Африки к югу от Сахары - Гане, Кении и Малави - в рамках программы ВОЗ. Программа внедрения вакцины против малярии (MVIP).
Иммунитет (или, точнее, толерантность ) к малярии, вызванной P. falciparum, действительно возникает естественным образом, но только в ответ на годы повторной инфекции. Человек может быть защищен от инфекции P. falciparum, если он получит около тысячи укусов от комаров, являющихся переносчиками разновидности паразита, которая становится неинфекционной с помощью дозы рентгеновского излучения. Весьма полиморфный характер многих P. Falciparum белков приводят к значительным проблемам проектирования вакцин. Вакцины-кандидаты, нацеленные на антигены гамет, зигот или оокинет в средней кишке комаров, направлены на блокирование передачи малярии. Эти вакцины, блокирующие передачу, индуцируют антитела в крови человека; Когда комар питается кровью защищенного человека, эти антитела не позволяют паразиту завершить свое развитие в комаре. Другие вакцины-кандидаты, нацеленные на стадию жизненного цикла паразита в крови, сами по себе оказались неадекватными. Например, SPf66 интенсивно тестировался в регионах, где это заболевание было распространено в 1990-х годах, но испытания показали его недостаточную эффективность.
В 2021 году исследователи из Оксфордского университета сообщили о результатах исследования фазы IIb кандидатной вакцины против малярии, R21 / Matrix-M, которое продемонстрировало эффективность 77% в течение 12 месяцев наблюдения. Эта вакцина является первой вакциной, которая соответствует цели Дорожной карты технологий противомалярийных вакцин Всемирной организации здравоохранения по вакцине с эффективностью не менее 75%.
Малярийные паразиты содержат апикопласты, органеллы, обычно встречающиеся в растениях, со своими собственными геномами. Считается, что эти апикопласты возникли в результате эндосимбиоза водорослей и играют решающую роль в различных аспектах метаболизма паразитов, таких как биосинтез жирных кислот. Было обнаружено, что апикопласты продуцируют более 400 белков, и в настоящее время они исследуются как возможные мишени для новых противомалярийных препаратов.
С появлением устойчивых к лекарствам паразитов Plasmodium разрабатываются новые стратегии борьбы с широко распространенным заболеванием. Один из таких подходов лежат в введении синтетических пиридоксальте -аминокислоты аддуктов, которые принимаются в организме паразита и в конечном счете помешать его способности создавать несколько важных витамины группы В. Интерес исследователей вызывают противомалярийные препараты на основе синтетических комплексов на основе металлов.
На основании результатов молекулярного докинга соединения 3j, 4b, 4h, 4m проявили селективность в отношении PfLDH. Анализ после стыковки показал стабильное динамическое поведение всех выбранных соединений по сравнению с хлорохином. Термодинамический анализ конечного состояния показал, что соединение 3j является селективным и сильным ингибитором PfLDH.
Избирательное нацеливание на паразитов на стадии печени Plasmodium становится альтернативной стратегией перед лицом устойчивости к новейшим передовым комбинированным методам лечения паразитов на стадии крови.
В исследовании, проведенном в 2019 году, с помощью экспериментального анализа с нокаут-мутантами Plasmodium berguei авторы смогли идентифицировать гены, которые потенциально необходимы на стадии печени. Более того, они создали вычислительную модель для анализа преэритроцитарного развития и метаболизма на стадии печени. Объединив оба метода, они определили семь метаболических подсистем, которые становятся важными по сравнению со стадией крови. Некоторые из этих метаболических путей включают синтез и удлинение жирных кислот, метаболизм трикарбоновых кислот, аминокислот и гема.
В частности, они изучили 3 подсистемы: синтез и удлинение жирных кислот и биосинтез аминосахаров. Для первых двух путей они продемонстрировали четкую зависимость стадии печени от собственного метаболизма жирных кислот.
Они впервые доказали критическую роль биосинтеза аминосахаров в печеночной стадии P. berghei. Поглощение N-ацетил-глюкозамина, по-видимому, ограничено на стадии печени, поскольку его синтез необходим для развития паразита.
Эти результаты и вычислительная модель обеспечивают основу для разработки противомалярийных методов лечения, направленных на метаболические белки.
Нехимическая стратегия борьбы с переносчиками инфекции включает генетические манипуляции с малярийными комарами. Достижения в области технологий генной инженерии позволяют ввести чужеродную ДНК в геном комара и либо сократить продолжительность жизни комара, либо сделать его более устойчивым к малярийным паразитам. Метод стерильных насекомых - это метод генетического контроля, с помощью которого выращивают и выпускают большое количество стерильных самцов комаров. Спаривание с дикими самками сокращает дикую популяцию в следующем поколении; повторные выпуски в конечном итоге устраняют целевую популяцию.
Геномика занимает центральное место в исследованиях малярии. С секвенирования по П. малярийного, один из ее векторов Anopheles gambiae, и геном человека, можно изучать генетику всех трех организмов в жизни малярии цикла. Еще одно новое применение генетической технологии - это способность производить генетически модифицированных комаров, которые не являются переносчиками малярии, что потенциально позволяет осуществлять биологический контроль передачи малярии.
В одном исследовании был создан генетически модифицированный штамм Anopheles stephensi, который больше не поддерживал передачу малярии, и эта устойчивость была передана потомкам комаров.
Генный драйв - это метод изменения диких популяций, например, для борьбы или уничтожения насекомых, чтобы они не могли передавать болезни (в частности, комары в случаях малярии, вируса Зика, денге и желтой лихорадки).
В декабре 2020 года в обзорной статье было обнаружено, что в регионах, эндемичных по малярии, в среднем зарегистрированы более низкие показатели летальности от COVID-19, чем в регионах, где малярия не была эндемичной.
Хотя не существует животных-резервуаров для штаммов малярии, вызывающих инфекции человека, было идентифицировано около 200 паразитических видов Plasmodium, которые инфицируют птиц, рептилий и других млекопитающих, и около 30 видов естественным образом заражают нечеловеческих приматов. Некоторые малярийные паразиты, поражающие нечеловеческих приматов (NHP), служат модельными организмами для малярийных паразитов человека, например P.coatneyi (модель P. falciparum) и P. cynomolgi ( P. vivax). Диагностические методы, используемые для обнаружения паразитов в NHP, аналогичны тем, которые используются для людей. Малярийные паразиты, поражающие грызунов, широко используются в качестве моделей в исследованиях, например P. berghei. Птичья малярия в первую очередь поражает виды отряда воробьиных и представляет серьезную угрозу для птиц Гавайев, Галапагосских островов и других архипелагов. Известно, что паразит P. relictum играет роль в ограничении распространения и численности эндемичных гавайских птиц. Ожидается, что глобальное потепление приведет к увеличению распространенности и глобального распространения птичьей малярии, поскольку повышенные температуры создают оптимальные условия для размножения паразитов.
День, посвященный повышению осведомленности об этой болезни, - хорошая возможность спросить, как далеко продвинулись исследования малярии и какие методы необходимы для дальнейших достижений.
| Классификация | D |
|---|---|
| Внешние ресурсы |
|