| Деменция с тельцами Леви | |
|---|---|
| Другое имена | Диффузная болезнь с тельцами Леви |
 | |
| Микроскопическое изображение тельцов Леви | |
| Специальность | Неврология, психиатрия |
| Симптомы | Деменция, ненормальное поведение во время быстрого сна, колебания активности, зрительные галлюцинации, паркинсонизм |
| Обычное начало | После 50 лет, медиана 76 |
| Продолжительность | Долгосрочные |
| Причины | Неизвестно |
| Метод диагностики | На основании симптомов и биомаркеров |
| Дифференциальный диагноз | Альцгеймера, деменция при болезни Паркинсона, некоторые психические заболевания, сосудистая деменция |
| лекарства | ингибиторы ацетилхолинэстеразы, такие как донепезил и ривастигмин ;мелатонин |
| Прогноз | Средняя выживаемость 8 лет f диагноз |
| Частота | Около 0,4% лиц старше 65 лет |
Деменция с тельцами Леви (DLB ) является разновидностью деменции сопровождаются изменениями сна, поведения, познания, движения и вегетативных функций организма. Потеря памяти не всегда является ранним признаком. Заболевание со временем ухудшается и обычно диагностируется, когда снижение когнитивных функций мешает нормальному повседневному функционированию. Вместе с деменцией при болезни Паркинсона, DLB является одним из двух деменций с тельцами Леви. Это распространенная форма деменции, но распространенность точно не известна, и многие диагнозы упускаются. Заболевание было впервые описано Кендзи Косака в 1976 году.
Расстройство поведения во сне в фазе быстрого сна (RBD) - при котором люди теряют мышечный паралич, который обычно возникает во время Быстрый сон и воплощение своих снов - это ключевая особенность. RBD может появиться на годы или десятилетия раньше других симптомов. Другими основными чертами являются зрительные галлюцинации, заметные колебания внимания или бдительности и паркинсонизм (медлительность движений, затруднения при ходьбе или жесткость ). Не все особенности должны присутствовать для диагностики. Для постановки окончательного диагноза обычно требуется вскрытие, но вероятный диагноз ставится на основании симптомов и тестов, которые могут включать анализы крови, нейропсихологические тесты, визуализацию и <234.>Исследования сна.
Большинство людей с ДЛБ не затронуты членами семьи, хотя иногда ДЛБ проводится в семье. Точная причина неизвестна, но включает широко распространенные отложения аномальных скоплений белка, которые образуются в нейронах пораженного мозга. Известные как тельца Леви (обнаруженные в 1912 году Фредериком Леви ) и нейриты Леви, эти скопления влияют как на центральную нервную систему, так и на вегетативная нервная система. Сердечная функция и все уровни желудочно-кишечной функции - от жевания до дефекации - могут быть затронуты, запор является одним из наиболее распространенных симптомов. Низкое кровяное давление при стоянии также может быть симптомом. DLB также влияет на поведение; изменения настроения, такие как депрессия и апатия, являются обычным явлением.
ДЛБ обычно начинается после пятидесятилетнего возраста, и у людей с этим заболеванием ожидаемая продолжительность жизни составляет около восьми лет после постановки диагноза. Не существует лекарства или лекарств, чтобы остановить прогрессирование болезни, и люди на последних стадиях ДЛБ могут быть не в состоянии заботиться о себе. Лечение направлено на облегчение некоторых симптомов и уменьшение нагрузки на лиц, осуществляющих уход. Лекарства, такие как донепезил и ривастигмин, эффективны для улучшения когнитивных функций и общего функционирования, а мелатонин может использоваться при симптомах, связанных со сном. Антипсихотики обычно избегают даже при галлюцинациях, потому что почти у половины людей с ДЛБ возникают тяжелые и опасные для жизни реакции, и их применение может привести к смерти. Управление множеством различных симптомов является сложной задачей, поскольку оно включает в себя несколько специальностей и образование лиц, осуществляющих уход.
Деменция с Леви Тела (DLB) - это тип деменции, то есть прогрессивный и нейродегенеративный ; то есть он характеризуется дегенерацией центральной нервной системы, которая со временем ухудшается.
Деменцию с тельцами Леви иногда классифицируют по-другому. Это одна из двух деменций с тельцами Леви, наряду с деменцией при болезни Паркинсона. К атипичным паркинсоническим синдромам относятся DLB наряду с другими состояниями. Наконец, DLB представляет собой синуклеинопатию, что означает, что для нее характерны аномальные отложения белка альфа-синуклеин в головном мозге. Синуклеинопатии включают болезнь Паркинсона, множественную системную атрофию и другие более редкие состояния.
ДЛБ - это деменция, которая возникает при "некоторых сочетание неустойчивого познания, повторяющихся зрительных галлюцинаций, быстрого движения глаз (REM), расстройства поведения во время сна (RBD) и паркинсонизма, начиная с или после диагностики деменции », согласно Армстронгу (2019). ДЛБ имеет самые разные симптомы и более сложен, чем многие другие виды деменции. Несколько областей функционирования могут быть затронуты патологией Леви, в которой отложения альфа-синуклеина, вызывающие DLB, повреждают многие различные области нервной системы (например, вегетативную нервную систему и многие другие области головного мозга).
В DLB существует идентифицируемый набор ранних признаков и симптомов; они называются продромальной, или преддеменцией, фазой заболевания. Эти ранние признаки могут появиться за 15 или более лет до развития деменции. Самыми ранними признаками являются запор и головокружение от вегетативной дисфункции, гипосмия (снижение обоняния), зрительные галлюцинации и RBD. RBD может появиться на годы или десятилетия раньше других симптомов. Потеря памяти не всегда является ранним признаком.
Симптомы можно разделить на основные, основные и поддерживающие. Деменция является важным признаком и должна присутствовать при постановке диагноза, в то время как основные и поддерживающие признаки являются дополнительными доказательствами в поддержку диагноза (см. диагностические критерии ниже ).
Диагноз деменции ставится после когнитивных Упадок прогрессирует до такой степени, что мешает нормальной повседневной деятельности, социальным или профессиональным функциям. Хотя деменция является важной особенностью ДЛБ, она не всегда проявляется на ранней стадии и с большей вероятностью проявляется по мере прогрессирования состояния.
Хотя конкретные симптомы могут различаться, основными особенностями ДЛБ являются колебания когнитивных функций, бдительности или внимания; расстройство поведения во сне в фазе быстрого сна; одна или несколько основных черт паркинсонизма, не вызванные лекарствами или инсультом. ; и повторяющиеся зрительные галлюцинации.
Четвертый консенсусный отчет консорциума DLB за 2017 год определил, что это основные особенности, на основании наличия высококачественных доказательств, указывающих на то, что они очень специфичны.
Помимо потери памяти, тремя наиболее распространенными когнитивными симптомами при DLB являются нарушения внимания, исполнительной власти. функция и зрительно-пространственная функция. Эти нарушения проявляются на ранней стадии заболевания. Люди с DLB могут легко отвлекаться, им трудно сосредоточиться на задачах, или они могут казаться «подобными делирию», «зонированием» или находиться в состояниях измененного сознания с периодами замешательства, возбуждения или бессвязной речи. У них может быть дезорганизованная речь, и их способность организовывать мысли может меняться в течение дня. Управляющая функция описывает контроль внимания и поведения, память и когнитивную гибкость, которые помогают решать проблемы и планировать. Проблемы с исполнительной функцией проявляются в деятельности, требующей планирования и организации. Дефицит может проявляться в снижении производительности труда, неспособности следить за разговорами, трудностях с одновременным выполнением нескольких задач или ошибках при вождении, таких как неправильная оценка расстояния или потерянность. Человек с DLB может испытывать расстройства бодрствования или расстройства сна (в дополнение к расстройству поведения во время быстрого сна), которые могут быть серьезными. Эти расстройства включают дневную сонливость, сонливость или сонливость более двух часов в день, бессонницу, периодические движения конечностями, синдром беспокойных ног и апноэ во сне.
—B. Tousi (2017), Диагностика и лечение когнитивных и поведенческих изменений при деменции с тельцами Леви.
Расстройство поведения во время быстрого сна (RBD) - это парасомния, при которой люди теряют паралич мышц ( atonia), что является нормальным явлением во время сна с быстрым движением глаз (REM), и, следовательно, исполняет свои сны или совершает другие ненормальные движения или вокализации. Около 80% людей с DLB имеют RBD. Аномальное поведение во сне может начаться до того, как наблюдается снижение когнитивных функций, и может появиться за десятилетия до появления любых других симптомов, часто как первое клиническое указание на ДЛБ и ранний признак синуклеинопатии. При вскрытии от 94 до 98% людей с полисомнографией -подтвержденной RBD имеют синуклеинопатию - чаще всего DLB или болезнь Паркинсона примерно в равных пропорциях. Более чем у трех из четырех человек с RBD диагностируется нейродегенеративное состояние в течение десяти лет, но дополнительные нейродегенеративные диагнозы могут появиться в течение 50 лет после постановки диагноза RBD. RBD может со временем исчезнуть.
Люди с RBD могут не осознавать, что они разыгрывают свои мечты. Поведение RBD может включать крик, крик, смех, плач, неразборчивую речь, ненасильственные удары руками или более жестокие удары руками, ногами, удушьем или царапинами. Сообщаемое поведение разыгрывания сновидений часто бывает насильственным и связано с тем, что вас преследуют или нападают. Люди с RBD могут упасть с кровати или поранить себя или своих партнеров по кровати, что может вызвать синяки, переломы или субдуральные гематомы. Поскольку люди с большей вероятностью будут вспоминать или сообщать о насильственных снах и поведении, а также обращаться к специалисту в случае травмы, отзыв или предвзятость выбора могут объяснить распространенность насилия, о которой сообщается в RBD.
Паркинсонизм - это клинический синдром, характеризующийся медлительностью движений, ригидностью, постуральной нестабильностью и тремором ; он обнаружен при DLB и многих других состояниях, таких как болезнь Паркинсона, деменция при болезни Паркинсона и другие. Паркинсонизм встречается у более чем 85% людей с ДЛБ, у которых может быть одна или несколько из этих основных особенностей, хотя тремор в покое встречается реже.
Двигательные симптомы могут включать шаркающую походку, проблемы с равновесием, падения, пустое выражение, ограниченный диапазон выражения лица и низкая громкость речи или слабый голос. Двигательные симптомы могут быть разными, но обычно они симметричны и проявляются с обеих сторон тела. Может присутствовать только один из основных симптомов паркинсонизма, и симптомы могут быть менее серьезными, чем у людей с болезнью Паркинсона.
До 80% людей с ДЛБ имеют зрительные галлюцинации, как правило, в начале болезни. Они повторяющиеся и частые; может быть живописным, детально проработанным; и обычно связаны с оживленным восприятием животных или людей, в том числе детей и членов семьи. Примеры зрительных галлюцинаций «варьируются от« маленьких людей », которые небрежно ходят по дому,« призраков »умерших родителей, которые тихо сидят у кровати, до« велосипедов », свисающих с деревьев на заднем дворе».
Эти галлюцинации могут иногда вызывать страх, хотя их содержание обычно нейтрально. В некоторых случаях человек с DLB может догадываться, что галлюцинации не настоящие. У людей с более нарушенным познанием галлюцинации могут стать более сложными, и они могут меньше осознавать, что их галлюцинации не реальны.
Визуальные неправильные восприятия или иллюзии также распространены при DLB, но отличаются от зрительных галлюцинаций. В то время как зрительные галлюцинации возникают при отсутствии реальных стимулов, зрительные иллюзии возникают при неправильном восприятии реальных стимулов; например, человек с DLB может неправильно интерпретировать торшер для человека.
Поддерживающие функции DLB имеют меньший диагностический вес, но они предоставляют доказательства для диагноза. Поддерживающие функции могут присутствовать на ранних этапах прогрессирования и сохраняться с течением времени; они обычны, но не специфичны для диагноза. Поддерживающие признаки:
 Люди с DLB очень чувствительны к антипсихотическим препаратам, таким как галоперидол, которые содержат повышенный риск заболеваемости и смертности в DLB.
Люди с DLB очень чувствительны к антипсихотическим препаратам, таким как галоперидол, которые содержат повышенный риск заболеваемости и смертности в DLB. Отчасти из-за потери клеток, высвобождающих нейротрансмиттер дофамин, люди с DLB может иметь злокачественный нейролептический синдром, когнитивные нарушения o настороженность или необратимое обострение паркинсонизма, включая тяжелую ригидность и дисавтономию от приема антипсихотических средств.
Дизавтономия (вегетативная дисфункция) возникает, когда патология Леви поражает периферическую вегетативную нервную систему (нервы, которые обслуживают такие органы, как кишечник, сердце и мочевыводящие пути). Первые признаки вегетативной дисфункции часто незаметны. Симптомы включают проблемы с артериальным давлением, такие как ортостатическая гипотензия (головокружение после вставания) и лежа на спине гипертензия ; запоры, проблемы с мочеиспусканием и сексуальная дисфункция ; потеря или снижение способности обоняния; и чрезмерное потоотделение, слюнотечение или слюноотделение и проблемы с глотанием (дисфагия ).
отложения альфа-синуклеина могут поражать сердечную мышцу и кровеносные сосуды. «Дегенерация сердечных симпатических нервов является невропатологической особенностью» деменции с тельцами Леви, согласно Ямаде и др. Почти все люди с синуклеинопатией имеют сердечно-сосудистую дисфункцию, хотя большинство из них протекает бессимптомно. От 50 до 60% людей с ДЛБ имеют ортостатическую гипотензию. из-за снижения кровотока, что может привести к головокружению, обмороку и нечеткости зрения.
От жевания до дефекации отложения альфа-синуклеина влияют на все уровни желудочно-кишечного тракта. Практически все люди с DLB имеют дисфункцию верхних отделов желудочно-кишечного тракта (например, гастропарез, задержку опорожнения желудка) или дисфункцию нижних отделов желудочно-кишечного тракта (например, запор и увеличенное время прохождения стула). Лица с деменцией с тельцами Леви почти всегда Иногда возникает тошнота, задержка желудка или вздутие живота из-за задержки опорожнения желудка. Проблемы с желудочно-кишечным трактом могут влиять на всасывание лекарств. Запор может появиться за десять лет до постановки диагноза и является одним из наиболее распространенных симптомов у людей с деменцией с тельцами Леви. Дисфагия протекает легче, чем при других синуклеинопатиях, и проявляется позже. Проблемы с мочеиспусканием (задержка мочеиспускания, пробуждение ночью для мочеиспускания, учащенное мочеиспускание и позывы к мочеиспусканию, чрезмерная или недостаточная активность мочевого пузыря) обычно появляются позже и могут быть легкими или умеренными. Сексуальная дисфункция обычно проявляется на ранних стадиях синуклеинопатий и может включать эректильную дисфункцию и трудности с достижением оргазма или эякуляции.
Среди других поддерживающих признаков психиатрические симптомы часто присутствуют, когда человек первым обращается к врачу и с большей вероятностью, по сравнению с AD, вызовет большее ухудшение. Около одной трети людей с ДЛБ страдают депрессией, и у них также часто бывает тревога. Беспокойство ведет к повышенному риску падений, а апатия может привести к меньшему социальному взаимодействию.
Возбуждение, поведенческие расстройства и заблуждения обычно появляются позже в ходе болезни. Заблуждения могут иметь параноидальный характер и включать такие темы, как взлом дома, неверность или брошенность. Люди с DLB, которые потеряли предметы, могут иметь заблуждение относительно кражи. Может иметь место заблуждение Capgras, когда человек с DLB теряет информацию о лице супруга, опекуна или партнера и убежден, что самозванец заменил их. Иногда присутствуютгаллюцинации других модальностей, но они встречаются реже.
Расстройства сна (нарушенные циклы сна, апноэ во время возбуждения от расстройства периодических движений конечностей) часто встречаются при ДЛБ и приводить к гиперсомнии. Потеря обоняния может проявиться за несколько лет до появления других симптомов.
 A ленточной диаграммы аполипопротеина E. Варианты этого воздействия на риск развития DLB.
A ленточной диаграммы аполипопротеина E. Варианты этого воздействия на риск развития DLB. Как и при других синуклеинопатиях, точная причина DLB неизвестна. Синуклеинопатии обычно вызываются генетическими факторами и факторами окружающей среды. Большинство людей с DLB не являются членами семьи, хотя иногда DLB проходит в семье. Считается, что наследуемость DLB составляет около 30% (то есть есть около 70% признаков, связанных с DLB, не наследуются).
Генетический риск перекрывается факторы для DLB, болезни Альцгеймера (AD), болезни Паркинсона и деменции при болезни Паркинсона. Ген APOE имеет три общих варианта. Один, APOE ε4, является фактором риска DLB и болезни Альцгеймера, тогда как APOE ε2 может защищать от обоих. Мутации в GBA, гене лизосомального фермента, связаны как с DLB, так и с болезнью Паркинсона. В редких случаях мутации в SNCA, гене альфа-синуклеина, или LRRK2, гене фермента киназы, могут вызвать любой из DLB, болезнь Альцгеймера, болезнь Паркинсона или деменцию при болезни Паркинсона.. Это говорит о том, что в основе четырех заболеваний может лежать некоторая общая генетическая патология.
На больший риск развития ДЛБ возникает у лиц старше 50 лет. Расстройство поведения во сне в фазе быстрого сна или Паркинсона обеспечивает более высокий риск развития ДЛБ. Риск развития ДЛБ не связан с какими-либо конкретными факторами развития образа жизни. Факторы быстрого превращения RBD в синуклеинопатию зрения включают нарушение зрения цветового или способности обоняния, легкие когнитивные нарушения и аномальные дофаминергические изображения.
 На микрофотографии показан коричневый иммуноокрашенный альфа-синуклеин в тельцах Леви (большие скопления) и нейриты Леви (нитевидные структуры) в неокортикальной ткани человек, умерший от болезни с тельцами Леви.
На микрофотографии показан коричневый иммуноокрашенный альфа-синуклеин в тельцах Леви (большие скопления) и нейриты Леви (нитевидные структуры) в неокортикальной ткани человек, умерший от болезни с тельцами Леви. ДЛБ показал необычных скоплений альфа-синуклеинового белка в пораженных нейронах мозга, известных как тельца Леви и нейриты Леви. Когда эти комки белка образуются, нейроны функционируют менее оптимально и в конечном итоге умирают. Потеря нейронов в DLB приводит к глубокой дисфункции дофамина и выраженной холинергической патологии; могут быть затронуты другие нейротрансмиттеры, но о них известно меньше. Повреждение головного мозга широко распространено. Считается, что потеря нейронов, продуцирующих ацетилхолин,, причиной дегенерации памяти и обучения, в то время как смерть нейронов, продуцирующих дофамин, по-предположительно, ответственна за дегенерацию поведения, познания, настроения, движения, мотивации и сна.. Степень поврежденияронов с тельцами Леви является ключевым фактором, определяющим деменцию при заболеваниях с тельцами Леви.
Точные механизмы, способствующие DLB, недостаточно изучены и являются предметом некоторых противоречий. Роль отложений альфа-синуклеина неясна, потому что у людей без признаков ДЛБ при аутопсии обнаружена развитая патология альфа-синуклеина. Связь между патологией Леви и широко распространенной гибелью клеток спорна. Неизвестно, распространяется ли патология между клетками или по другой схеме. Механизмы, которые способствуют гибели клеток, как болезни по мозгу, и время снижения когнитивных способностей - все это плохо изучено. Не существует модели, учитывающие соответствующие нейроны и области мозга.
Исследования вскрытия трупов и исследования амилоида визуализации с использованием питтсбургского соединения B (PiB) показывают, что тау-белок патология и амилоидные бляшки, которые являются отличительными признаками БА, а также при ДЛБ и более распространены, чем при деменции при болезни Паркинсона. Амилоид-бета (Aβ) отложения обнаруживаются при таупатиях - нейродегенеративных заболеваний, характеризующихся нейрофибриллярными клубками гиперфосфорилированным белком тау - но, лежащий в механизме на основе деменции, часто смешанный, и Aβ также фактор в DLB.
Предполагаемая патофизиология RBD вовлекает нейроны в ретикулярной формеции, которые регулируют REM-сон. RBD может появиться на десятилетии раньше, чем другие симптомы при деменции с тельцами Леви, потому что эти клетки поражаются раньше, чем распространяться на другие области мозга.
Деменция с тельцами Леви может быть окончательно диагностирована только после смерти при вскрытии мозга (или в редких семейных случаях, с помощью генетического теста), поэтому диагноз живого считается вероятным или возможным. Диагностика ДЛБ может быть сложной процедурой из-за широкого симптомов с разной степенью тяжести у каждого человека. ДЛБ часто ошибочно диагностируют или на ранних стадиях путают с болезнью Альцгеймера. Каждый третий диагноз DLB может быть пропущен. Другой усложняющий фактор - то, что DLB может возникнуть вместе с AD; вскрытие показывает, что среди людей с ДЛБ в мозгу есть специальный уровень изменений, связанных с БА, широкому разнообразию симптомов и трудностей диагностики. Несмотря на сложность постановки диагноза, своевременный диагноз важен из-за серьезного риска чувствительности к нейролептике и необходимости информировать как человека с DLB, так и лиц, ухаживающих за ним, о побочных эффектах этих лекарств. Ведение ДЛБ сложно по другим нейродегенеративным заболеваниям, поэтому точный диагноз важен.
Четвертый консенсусный отчет 2017 года установил диагностические критерии для вероятного и возможного ДЛБ, признавая достижения обнаруживается с более ранней версии Третьего консенсуса (2005 г.). Критерии 2017 г. основаны на основных, основных и продолжающих клинических признаках, а также на диагностических биомаркерах.
Существенным признаком является деменция; для диагноза DLB он должен быть достаточно значительным, чтобы мешать социальному или профессиональному функционированию.
Четыре основных клинических признака (описанных в разделе «Признаки и симптомы») - это колебания когнитивных функций, зрительные галлюцинации, Расстройство поведения во сне в фазе быстрых сна и признаки паркинсонизма. Поддерживающие клинические признаки: выраженная чувствительность к антипсихотикам; выраженная вегетативная дисфункция; невизуальные галлюцинации; гиперсомния; пониженная способность обоняния; ложные убеждения и заблуждения, организованные вокруг общей темы; нестабильность осанки, потеря сознания и частые падения; и апатия, беспокойство или депрессия.
 Позитронно-эмиссионная томография, например, с использованием PiB полезна в диагностике ДЛБ.
Позитронно-эмиссионная томография, например, с использованием PiB полезна в диагностике ДЛБ. Прямые лабораторные измерения биомаркеров для диагностики ДЛБ используются дополнительные методы диагностики. Индикативными диагностическими биомаркерами являются: снижение захвата переносчика дофамина в базальных ганглиях, показанных на ПЭТ или ОФЭКТ изображение; низкое поглощение йода - метаиодобензилгуанидина (I-MIBG), показанное на миокардиальной сцинтиграфии ; и потеря атонии во время быстрой сна, подтвержденная полисомнографией. Поддерживающие диагностические биомаркеры (по результатам ПЭТ, ОФЭКТ, КТ или МРТ изображений головного мозга или ЭЭГ мониторинг): отсутствие повреждений медиальной височной доли ; пониженная затылочная активность; и заметная медленная активность.
Вероятный DLB может быть диагностирован при наличии деменции и, по крайней мере, двух основных признаков, или когда присутствуют один ключевой признак и, по крайней мере, один индикативный биомаркер. Может быть диагностирован DLB при деменции и наличии только одного основного признака или, если основные признаки отсутствуют, то присутствует по крайней мере один индикативный биомаркер.
DLB отличается от деменции при болезникинсона временными рамками какие симптомы деменции появляются симптомов паркинсонизма. ДЛБ диагностируется, когда когнитивные симптомы начинаются раньше или одновременно с симптомами паркинсонизма. Деменция при болезни Паркинсона может быть диагнозом, если болезнь Паркинсона хорошо установлена до появления деменции (начало деменции происходит более чем через год после появления симптомов паркинсонизма).
DLB внесен в список в Диагностическом и статистическом старте психических расстройств, пятое издание (DSM-5 ) как большое или легкое нейрокогнитивное расстройство с тельцами Леви. Различия между диагностическими критериями DSM и Консорциума DLB заключаются в следующем: 1) DSM не включает низкий уровень переносчика дофамина в качестве поддерживающего признака, и 2) биомаркерам в DSM присваивается нечеткий диагностический вес. Деменции с тельцами Леви классифицируются Всемирной организацией здравоохранения в ее МКБ-10, Международной статистической классификации болезней и проблем, связанных со здоровьем, в главе VI, как заболевания нервной. системы, код 31.8.
Диагностические тесты диагностические сообщения для некоторых состояний и их отличия от симптомов других состояний. Диагностика может Исследование изучения истории болезни, физический осмотр, оценка неврологической функции, тестирование для состояний исключения, которые могут вызывать симптомы, визуализацию мозга, нейропсихологическое тестирование для когнитивной функции исследования сна или сцинтиграфия миокарда. Лабораторные исследования могут исключить другие состояния, которые могут вызывать аналогичные симптомы, такие как нарушение функции щитовидной железы, сифилис, ВИЧ или дефицит витаминов, которые могут вызывать симптомы, похожие на слабоумие.
Скрининговые тесты на деменцию - это Краткий экзамен на психическое состояние и Монреальский когнитивный тест. Для тестов внимания диапазон цифр, последовательные семерки и пространственный диапазон мая для простого скрининга, а подтест исправленных цифровых символов Шкала интеллекта взрослых Векслера может выявить дефекты внимания, характерные для ДЛБ. Фронтальная оценочная батарея, Тест Струпа и Висконсинский тест сортировки карточек используются для оценки исполнительной функции и множества других инструментов для скрининга.
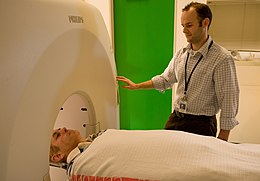
 Взрослый, подключенный к проводам от датчиков для полисомнографии
Взрослый, подключенный к проводам от датчиков для полисомнографии Если подозревается ДЛБ, когда единственными признаками являются паркинсонизм и деменция, ПЭТ или ОФЭКТ-изображения могут показать снижение активности переносчика дофамина. Диагноз DLB может быть оправдан, если можно исключить другие состояния со сниженным поглощением переносчика дофамина.
RBD диагностируется либо на основании записи исследования сна, либо, если исследования сна не могут быть проведены на основании истории болезни и утвержденных анкет. У людей с деменцией и в анамнезе RBD вероятный диагноз DLB может быть оправдан (даже при отсутствии других основных характеристик или биомаркеров) на основе исследования сна, показывающего быстрый сон без атонии, поскольку он очень предсказуем. Состояния, подобные RBD, такие как тяжелое апноэ во сне и расстройство периодических движений конечностей, должны быть исключены. Незамедлительная оценка и лечение RBD показаны при наличии в анамнезе насилия или травм, так как это может повысить вероятность будущих агрессивных сновидений. Лица с RBD может быть в состоянии рассказать историю разыгрывания сновидений. Экран одним вопросом Расстройство быстрого сна предлагает диагностическую диагностику и специфичность в отсутствии полисомнографии с одним вопросом: «разыгрываете свои мечты»? во сне (например, удары кулаками, взмахи руками в воздухе, беговые движения и т. д.)? "У некоторых людей с DLB нет RBD, нормальные результаты исследования сна не могут исключить DLB.
С 2001 года йод - метаиодобензилгуанидин (I-MIBG) миокард сцинтиграфия используется для диагностики в Восточной Азии (в основном в Японии), но не в США. MIBG захватывается симпатическими нервными окончаниями, такими как те, которые иннервируют сердце, и помечен для сцинтиграфии с радиоактивным йодом. Вегетативная дисфункция, возникающая в результате повреждения нервов в сердце у пациентов с ДЛБ, связана с более низким сердечным поглощением I-МИБГ.
Нет генетический тест для определения того, разовьется ли у человека ДЛБ, и, согласно Ассоциации деменции с тельцами Леви, генетическое тестирование не рекомендуется, поскольку существуют лишь редкие случаи наследственного ДЛБ.
358>ДифференциальныйМногие нейродегенеративные состояния имеют общие когнитивные и моторные симптомы с деменцией с Леви тела. дифференциальный диагноз включает болезнь Альцгеймера; такие синуклеинопатии, как деменция при болезни Паркинсона, болезнь Паркинсона и множественная системная атрофия; сосудистая деменция; и прогрессирующий надъядерный паралич, кортикобазальная дегенерация и кортикобазальный синдром.
Симптомы DLB легко спутать с делирием или, реже, с психозом; Были предложены продромальные подтипы ДЛБ с дебютом делирия и ДЛБ с психиатрическим началом. Неправильное ведение делирия вызывает особую озабоченность из-за риска для людей с ДЛБ, связанного с приемом нейролептиков. У людей с необъяснимым делирием необходимо тщательное обследование на признаки DLB. ПЭТ или ОФЭКТ-изображение, показывающее пониженное поглощение транспортера дофамина, может помочь отличить DLB от делирия.
Патология Леви поражает периферическую вегетативную нервную систему; вегетативная дисфункция реже наблюдается при AD, лобно-височной или сосудистой деменции, поэтому ее наличие может помочь дифференцировать их. МРТ почти всегда выявляет аномалии в мозге людей с сосудистой деменцией, которые могут начаться внезапно.
ДЛБ отличается от БА даже в продромальной фазе. Нарушение кратковременной памяти наблюдается на ранних стадиях БА и является заметной особенностью, в то время как колебания внимания случаются редко; Нарушение DLB чаще всего сначала рассматривается как колебание когнитивных функций. В отличие от БА, при котором гиппокамп входит в число первых пораженных структур мозга, а эпизодическая потеря памяти, связанная с кодированием воспоминаний, обычно является самым ранним симптомом - ухудшение памяти происходит позже в DLB. Люди с легкими когнитивными нарушениями, вызванными амнезией, (у которых потеря памяти является основным симптомом) могут прогрессировать до АД, тогда как люди с неамнестическими легкими когнитивными нарушениями (у которых более выражены языковые, зрительно-пространственные и исполнительные нарушения.) с большей вероятностью будут продвигаться к DLB. Потеря памяти при DLB протекает иначе, чем AD, потому что лобные структуры вовлекаются раньше, а позже вовлекаются височно-теменные структуры мозга. Вербальная память страдает не так сильно. как в AD.
В то время как 74% людей с подтвержденным аутопсией DLB имели недостатки в планировании и организации, они обнаруживаются только у 45% людей с AD. Дефицит зрительно-пространственной обработки присутствует у большинства людей с DLB, они проявляются раньше и более выражены, чем при AD. Галлюцинации обычно возникают на ранних стадиях ДЛБ, реже встречаются в ранней стадии БА, но обычно возникают позже в БА. Патология AD часто возникает одновременно в DLB, поэтому тестирование спинномозговой жидкости (CSF) на Aβ и тау-белок, которое часто используется для выявления AD, бесполезно для дифференциации AD и DLB.
Визуализация ПЭТ или ОФЭКТ может использоваться для обнаружения пониженного поглощения переносчика дофамина и отличия AD от DLB. Тяжелая атрофия гиппокампа более характерна для БА, чем для ДЛБ. До развития деменции (в фазе легкого когнитивного нарушения) МРТ показывает нормальный объем гиппокампа. После развития деменции МРТ показывает большую атрофию у людей с БА и более медленное уменьшение объема со временем у людей с ДЛБ, чем у людей с БА. По сравнению с людьми с БА, FDG-PET сканирование мозга у людей с DLB часто показывает знак поясной извилины.
В Восточной Азии, особенно в Японии, I-MIBG используется в дифференциальной диагностике DLB и AD, поскольку снижение маркировки сердечных нервов наблюдается только при заболеваниях с тельцами Леви. Другие индикативные и поддерживающие биомаркеры полезны для различения DLB и AD (preservat
Деменция с тельцами Леви и деменция при болезни Паркинсона клинически схожи после того, как деменция при болезни Паркинсона. деменции при болезни Паркинсона встречается реже, чем при ДЛБ, и люди с болезнью Паркинсона обычно менее подвержены зрительным галлюцинациям, чем люди с ДЛБ.
Кортикобазальный синдром, кортикобазальная д егенерация и прогрессирующий надъядерный паралич лобно-височной деменции с признаками паркинсонизма и нарушением познания. Подобно DLB, визуализация может показать снятие переносчика дофамина. Кортикобазальный синдром и дегенерация, а также прогрессирующий надъядерный паралич обычно отличаются от ДЛБ с помощью анамнеза и обследований. Двигательные движения при кортикобазальном синдроме асимметричны. В наиболее распространенных вариантах прогрессирующего надъядерного паралича наблюдаются различия в положении, взгляде и типе лица, падение назад более распространено по сравнению с ДЛБ. Зрительные галлюцинации и колебания познания необычны при кортикобазальной дегенерации и прогрессирующем надъядерном параличе.
Паллиативная помощь предлагается для облегчения симптомов, но нет лекарств, которые могут замедлить, остановить или улучшить неумолимое прогрессирование болезни. По состоянию на 2019 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США не одобрило никаких лекарств от DLB, хотя донепезил лицензирован в Японии и на Филиппинах для лечения DLB. По состоянию на 2020 год было мало исследований по лучшему лечению немоторных симптомов, таких как нарушения сна и вегетативная дисфункция; Большая часть информации о лечении вегетативной дисфункции при ДЛБ основана на исследованиях людей с болезнью Паркинсона.
Ведение может быть проблематичным из-за необходимости сбалансировать лечение различных симптомов: когнитивная дисфункция, нейропсихиатрические особенности, нарушения, связанные с двигательная система и другие немоторные симптомы. У людей с DLB очень разные симптомы, которые меняются со временем, и лечение одного симптома может ухудшить другой; неоптимальный уход может быть следствием отсутствия или координации действий врачей, занимающихся лечением различных симптомов. Предпочтение отдается мультидисциплинарному подходу, выходящему за рамки ранней и точной диагностики и включающему обучение и поддержку лиц, осуществляющих уход.
- BP Boot (2015), Комплексное лечение деменции с помощью тельцов Леви
Фармакологическое лечение ДЛБ является сложным из-за побочных эффектов лекарств и широкого спектра симптомов, требующих лечения (когнитивные, моторные, психоневрологические, вегетативные и сон). 145>Антихолинергические и дофаминергические агенты могут иметь побочные эффекты или приводить к психозу у людей с DLB, а лекарство, направленное на устранение одной особенности, может ухудшить другую. Например, ингибиторы ацетилхолинэстеразы (AChEI) при когнитивных симптомах могут приводить к осложнениям при дисавтономии; лечение двигательных симптомов агонистами дофамина может ухудшить нервно-психические симптомы; а лечение галлюцинаций и психозов нейролептиками может ухудшить другие симптомы или привести к потенциально смертельной реакции.
Следует соблюдать особую осторожность при использовании антипсихотических препаратов у людей с DLB из-за их чувствительности к этим агентам. Тяжелые и опасные для жизни реакции возникают почти у половины людей с DLB и могут быть смертельными после однократного приема. Антипсихотические препараты с D2-блокирующими дофаминовыми рецепторами свойствами используются только с большой осторожностью. Согласно Boot (2013), «отказ от нейролептиков часто является лучшим курсом действий». Люди с деменцией с тельцами Леви, принимающие нейролептики, подвержены риску развития злокачественного нейролептического синдрома, опасного для жизни заболевания. Нет никаких доказательств, подтверждающих использование антипсихотических средств для лечения деменции с тельцами Леви, и они несут дополнительный риск инсульта при применении у пожилых людей с деменцией.
Лекарства (включая трициклические антидепрессанты и лечение недержания мочи ) с антихолинергическими свойствами, которые преодолевают гематоэнцефалический барьер, могут вызывать потерю памяти. антигистаминные препараты дифенгидрамин (Бенадрил ), снотворные, такие как золпидем и бензодиазепины, могут усилить замешательство или нейропсихиатрические симптомы. Некоторые общие анестетики могут вызывать спутанность сознания или делирий при пробуждении у людей с деменцией с тельцами Леви и могут привести к необратимому ухудшению состояния.
Существуют убедительные доказательства того, что использование AChEI для лечения когнитивных проблем; Эти препараты включают ривастигмин и донепезил. Оба являются препаратами первой линии в Великобритании. Даже когда AChEI не приводят к улучшению когнитивных симптомов, у людей, принимающих их, может быть меньше ухудшения в целом, хотя могут быть неблагоприятные желудочно-кишечные эффекты. Использование этих лекарств продемонстрировало снижение нагрузки на лиц, осуществляющих уход, и улучшение повседневной активности для человека с DLB. AChEI следует начинать осторожно, поскольку они могут усугубить вегетативную дисфункцию или нарушения сна. Имеется меньше доказательств эффективности мемантина при DLB, но его можно использовать отдельно или с AChEI из-за его низкого профиля побочных эффектов. Избегают приема антихолинергических препаратов, поскольку они ухудшают когнитивные симптомы.
Для улучшения дневной активности существуют смешанные доказательства использования стимуляторов, таких как метилфенидат и декстроамфетамин ; Хотя ухудшение психоневрологических симптомов не является обычным явлением, они могут увеличить риск психоза. Модафинил и армодафинил могут быть эффективны при дневной сонливости.
Двигательные симптомы при ДЛБ несколько меньше реагируют на лекарства, используемые для лечения болезни Паркинсона, такие как леводопа, и эти лекарства могут усиливать нейропсихиатрические симптомы. Почти у каждого третьего человека с ДЛБ развиваются психотические симптомы от левадопы. Если такие лекарства необходимы для лечения двигательных симптомов, осторожное введение с медленным увеличением до минимально возможной дозы может помочь избежать психоза.
Психоневрологические симптомы ДЛБ (агрессия, беспокойство, апатия, бред, депрессия и галлюцинации) не всегда требуют лечения. Первая линия защиты от зрительных галлюцинаций - это сокращение употребления дофаминергических препаратов, которые могут ухудшить галлюцинации. При появлении новых психоневрологических симптомов проводится обзор использования лекарственных препаратов (таких как холинолитики, трициклические антидепрессанты, бензодиазепины и опиоиды ), которые могут способствовать возникновению этих симптомов.
Среди AChEIs, ривастигмин, донепезил и галантамин могут помочь уменьшить нейропсихиатрические симптомы и улучшить частоту и тяжесть галлюцинаций на менее тяжелых стадиях ДЛБ. Хотя было показано, что он эффективен при болезни Паркинсона, существуют ограниченные доказательства использования клозапина для лечения зрительных галлюцинаций при DLB, и его использование требует регулярного мониторинга крови. Кветиапин относительно безопасен и хорошо переносятся при психозах и возбуждении при DLB, но мало доказательств его эффективности.
Апатию можно лечить с помощью AChEI, и они также могут уменьшить галлюцинации, бред, беспокойство и возбуждение. Большинство лекарств для лечения тревоги и депрессии не были должным образом исследованы на предмет ДЛБ. Антидепрессанты могут влиять на сон и ухудшать RBD. Миртазапин и SSRI могут использоваться для лечения депрессии, в зависимости от того, насколько хорошо они переносятся, и руководствуясь общими рекомендациями по применению антидепрессантов при деменции. Антидепрессанты с антихолинергическими свойствами могут усугубить галлюцинации и бред. Люди с синдромом Капгра могут не переносить AChEI.
В первую очередь в лечении используются травмирующие сновидения. RBD можно лечить мелатонином или клоназепамом. Лекарства для сна тщательно оцениваются для каждого человека, поскольку они несут повышенный риск падений, повышенной дневной сонливости и ухудшения когнитивных функций. Мелатонин может быть более полезным для предотвращения травм и предлагает более безопасную альтернативу, поскольку клоназепам может вызвать ухудшение когнитивных функций и усугубить апноэ во сне. Некоторым людям полезен мемантин. Модафинил можно использовать при гиперсомнии, но никакие испытания не подтверждают его использование при ДЛБ. Миртазапин можно использовать при гиперсомнии, но он может усугубить RBD. Антидепрессанты (СИОЗС, ИОЗСН, трициклики и ИМАО ), AChEI, бета-блокаторы, кофеин и трамадол может усугубить RBD.
Снижение дозировки дофаминергических или атипичных нейролептиков может потребоваться при ортостатической гипотензии и лекарства от высокого артериального давления иногда можно остановить. Когда немедикаментозные методы лечения ортостатической гипотензии исчерпаны, можно использовать флудрокортизон, дроксидопа или мидодрин, но эти препараты не были специально изучены для лечения ДЛБ, поскольку от 2020 года. Задержка опорожнения желудка может усугубляться дофаминергическими препаратами, а запоры могут усугубляться опиатами и холинолитиками. Антагонисты мускаринов, используемые при мочевых симптомах, могут ухудшать когнитивные нарушения у людей с деменцией с тельцами Леви.
Нет никаких доказательств высокого качества в отношении немедикаментозного лечения ДЛБ, но было показано, что некоторые вмешательства эффективны для устранения аналогичных симптомов, возникающих при других формах деменции. Например, организованная деятельность, музыкальная терапия, физическая активность и трудотерапия могут помочь при психозе или возбуждении, тогда как упражнения и тренировка походки могут помочь при двигательных симптомах. Когнитивно-поведенческую терапию можно попробовать при депрессии или галлюцинациях, хотя нет никаких доказательств ее использования при DLB. Для восстановления памяти можно использовать подсказки.
Первыми шагами в управлении расстройствами сна является оценка использования лекарств, влияющих на сон, и предоставление информации о гигиене сна. Частота и тяжесть RBD могут быть уменьшены путем лечения апноэ во сне, если оно присутствует.
При вегетативной дисфункции могут быть полезны несколько немедикаментозных стратегий. Изменения в диете включают отказ от еды с высоким содержанием жиров и сладких продуктов, частое и меньшее употребление пищи, прогулки после еды и увеличение потребления жидкости или пищевых волокон для лечения запора. Размягчители стула и упражнения также помогают при запоре. Избыточному потоотделению можно помочь, избегая алкоголя и острой пищи, а также используя хлопковое постельное белье и свободную одежду.
Могут помочь физические упражнения в сидячем или лежачем положении и упражнения в бассейне. Компрессионные чулки и приподнятие изголовья кровати также могут помочь, а также можно попытаться увеличить потребление жидкости или поваренной соли для уменьшения ортостатической гипотензии. Чтобы снизить риск переломов у лиц, подверженных риску падений, используются скрининг минеральной плотности костей и определение уровня витамина D, а лица, осуществляющие уход, информируются о важности предотвращения падает. Было показано, что физиотерапия полезна при деменции, вызванной болезнью Паркинсона, но по состоянию на 2020 год нет доказательств в пользу физиотерапии у людей с ДЛБ.
Рекомендуется обучать лиц, осуществляющих уход, управлению психоневрологическими симптомами (такими как возбуждение и психоз). Из-за нейропсихиатрических симптомов, связанных с DLB, требования, предъявляемые к лицам, осуществляющим уход, выше, чем при AD, но обучение лиц, осуществляющих уход, не изучено так тщательно, как при AD или болезни Паркинсона. Факторами, влияющими на нагрузку на опекунов при DLB, являются эмоциональные колебания, психоз, агрессия, возбуждение и поведение в ночное время, такое как парасомния, которые приводят к потере независимости раньше, чем при AD. Воспитатели могут испытывать депрессию и истощение, и им может потребоваться поддержка других людей. Другие члены семьи, которые не участвуют в ежедневном уходе, могут не замечать изменчивое поведение или осознавать стресс, который испытывает опекун, и конфликт может возникнуть, если члены семьи не окажут поддержку. Обучение лиц, осуществляющих уход, снижает не только стресс для лица, осуществляющего уход, но и симптомы у человека с деменцией.
Визуальные галлюцинации, связанные с DLB, создают особую нагрузку для лиц, осуществляющих уход. Обучение воспитателей тому, как отвлечь внимание или изменить тему разговора при столкновении с галлюцинациями, более эффективно, чем споры о реальности галлюцинаций. Стратегии преодоления могут помочь, и их стоит попробовать, даже если нет доказательств их эффективности. Эти стратегии включают в себя то, что человек с DLB отводит взгляд или смотрит на что-то еще, сосредотачивается или пытается прикоснуться к галлюцинации, ждать, пока она уйдет сама по себе, и говорить с другими о визуализации. Бред и галлюцинации можно уменьшить, увеличив освещение вечером и убедившись, что ночью нет света, когда человек с DLB спит.
С повышенным риском побочных эффектов от антипсихотических препаратов для людей с DLB, образованные лица, обеспечивающие уход, могут выступать в качестве защитников лица с DLB. Если требуется обследование или лечение в отделении неотложной помощи, лицо, осуществляющее уход, может объяснить риски, связанные с применением нейролептиков, для людей с DLB. Обучение попечителей, бдительное ожидание, определение источников боли и усиление социального взаимодействия могут помочь минимизировать возбуждение. Люди с деменцией могут быть не в состоянии сообщить, что они испытывают боль, и боль является обычным триггером возбуждения. Доступны браслеты с медицинскими предупреждениями или уведомления о чувствительности к лекарствам, которые могут спасти жизни. оценку безопасности дома можно провести, когда есть риск падения. Поручни и стулья для душа могут помочь избежать падений.
Люди и их опекуны могут быть проконсультированы по поводу необходимо повысить безопасность спальни при симптомах RBD. Связанных со сном травм в результате падения или выпрыгивания с кровати можно избежать, снизив высоту кровати, положив матрас рядом с кроватью, чтобы смягчить удар при падении, и убрав острые предметы вокруг кровати. Острые поверхности возле кровати можно покрыть мягкой подкладкой, системы сигнализации могут помочь при лунатизме, а партнерам по постели может быть безопаснее спать в другой комнате. Согласно Сент-Луису и Бову, огнестрельное оружие должно быть заперто, вне спальни.
Способность вождения может быть нарушена на ранней стадии DLB из-за зрительных галлюцинаций, проблем с движением, связанных с паркинсонизмом, и колебаний когнитивных способностей, а также в какой-то момент водить машину становится небезопасно. Способность к вождению оценивается в рамках руководства, и члены семьи обычно определяют, когда лишаются водительских прав.
Прогноз для DLB не был хорошо изучен; ранние исследования имели методологические ограничения, такие как небольшой размер выборки и систематическая ошибка отбора. По сравнению с AD, DLB обычно приводит к более высокой инвалидности, более низкой ожидаемой продолжительности жизни и снижению качества жизни с увеличением затрат на лечение. Депрессия, апатия и зрительные галлюцинации способствуют снижению качества жизни. Снижение может быть более быстрым, когда серьезные зрительно-пространственные нарушения проявляются на ранних стадиях деменции с тельцами Леви, когда присутствует ген APOE или когда также присутствует AD или его биомаркеры. Тяжесть ортостатической гипотензии также предсказывает худший прогноз.
По сравнению с AD, которая лучше изучена, память сохраняется дольше, а беглость речи может быть потеряна быстрее. При ДЛБ больше нейропсихиатрических симптомов, чем при БА, и они могут проявиться раньше, поэтому у пациентов с ДЛБ прогноз может быть менее благоприятным, с более быстрым снижением когнитивных функций, большим числом госпитализаций и более низкой продолжительностью жизни. Повышенная частота госпитализаций по сравнению с AD чаще всего связана с галлюцинациями и спутанностью сознания, за которыми следуют падения и инфекции.
Ожидаемую продолжительность жизни трудно предсказать, и данные исследований ограничены. Выживаемость может быть определена с момента начала заболевания или с момента постановки диагноза. Обзор 2017 года показал, что выживаемость с момента начала заболевания составляет от 5,5 до 7,7 лет, выживаемость с момента постановки диагноза - от 1,9 до 6,3 года и более короткое время выживания после постановки диагноза, чем при AD. Разница в выживаемости между AD и DLB может быть связана с тем, что DLB сложнее диагностировать и может быть диагностирован позже в ходе заболевания. Национальный институт неврологических расстройств и инсульта США пишет, что люди с DLB обычно живут 8 лет после постановки диагноза, примерно так же, как и AD, хотя некоторые люди с деменцией с тельцами Леви живут 20 лет. Более короткая продолжительность жизни более вероятна, если на ранней стадии присутствуют зрительные галлюцинации, аномальная походка и изменчивые когнитивные способности. На поздних стадиях болезни люди могут быть не в состоянии заботиться о себе. Падения, вызванные множеством факторов, включая паркинсонизм, дизавтономию и слабость, увеличивают заболеваемость и смертность. аспирационная пневмония, осложнение дисфагии, которое возникает в результате дизавтономии, обычно вызывает смерть у людей с деменцией с тельцами Леви. После пневмонии частыми причинами смерти являются сердечно-сосудистые заболевания и сепсис.
Деменции с тельцами Леви занимают второе место по распространенности. форма нейродегенеративной деменции после БА по состоянию на 2020 год. ДЛБ сам по себе является одним из трех наиболее распространенных типов деменции, наряду с БА и сосудистой деменцией.
Диагностические критерии ДЛБ до 2017 года были высокоспецифичными, но не очень чувствительный, так что более половины случаев исторически не учитывались. Деменция с тельцами Леви была недооценена по состоянию на 2020 год, и данных о ее эпидемиологии мало. заболеваемость и распространенность ДЛБ точно не известны, но оценки увеличиваются с более точным распознаванием состояния с 2017 года.
Около 0,4% людей старше возраста 65 страдают DLB, и от 1 до 4 на 1000 человек заболевают этим заболеванием каждый год. Симптомы обычно появляются в возрасте от 50 до 80 лет (медиана 76), и нередко их диагностируют до 65 лет. Считается, что ДЛБ немного чаще встречается у мужчин, чем у женщин. но обзор 2014 года поставил под сомнение эту точку зрения и сказал, что гендерное распределение неясно. По оценкам, от 10 до 15% диагностированных деменций относятся к типу тела Леви, но оценки колеблются до 23% для тех, кто участвовал в клинических исследованиях.
Французское исследование показало, что заболеваемость среди людей 65 лет и старше почти в четыре раза выше. чем исследование в США (32 США против 112 Франции на 100 000 человеко-лет), но исследование в США могло исключить людей только с легкой формой паркинсонизма или без него, в то время как французское исследование проводило скрининг на паркинсонизм. Ни в одном из исследований не проводилась систематическая оценка RBD, поэтому DLB, возможно, недооценивался в обоих исследованиях. Посещение дома в Японии показало распространенность 0,53% среди лиц 65 лет и старше, а испанское исследование показало аналогичные результаты.
Фредерик Леви (1885–1950) был первым обнаружил аномальные белковые отложения в начале 1900-х годов. В 1912 году, изучая болезнь Паркинсона (возбуждающий паралич), он описал находки этих включений в блуждающем нерве, базальном ядре Мейнерта и других областях мозга. Он опубликовал книгу «Исследование мышечного тонуса и движений». Включая систематические исследования клиники, физиологии, патологии и патогенеза возбужденного паралича в 1923 году и, за исключением одной краткой статьи годом позже, никогда больше не упоминал о его результатах.
В 1961 году Окадзаки и др. опубликовал отчет о диффузных включениях типа Леви, связанных с деменцией, в двух вскрытых случаях.Деменция с тельцами Леви была полностью описана в случае вскрытия тела японским психиатром и невропатологом Кендзи Косака в 1976 году. Косака впервые предложил термин болезнь с тельцами Леви четыре года спустя, основываясь на 20 вскрытых случаях. ДЛБ считался редким явлением, пока его не стало легче диагностировать в 1980-х годах после открытия альфа-синуклеина иммуноокрашивания, которое выделяло тельца Леви в посмертном мозге. Kosaka et al. описали еще тридцать четыре случая в 1984 году, которые были упомянуты вместе с четырьмя случаями в Великобритании Гиббом и соавт. в 1987 г. в журнале Brain, привлекая внимание западного мира к японской работе. Годом позже Burkhardt et al. опубликовали первое общее описание диффузной болезни с тельцами Леви.
Когда японские, британские и американские исследователи обнаружили в 1990-х годах, что ДЛБ является распространенной формой деменции, диагностических рекомендаций не было, и каждая группа использовала разную терминологию. Различные группы исследователей начали понимать, что для продвижения исследований необходим совместный подход. Был создан Консорциум DLB, и в 1996 году был согласован термин «деменция с тельцами Леви» и разработаны первые критерии диагностики DLB.
Два открытия 1997 года подчеркнули важность тельцов Леви. включения в нейродегенеративные процессы: мутация в гене SNCA, который кодирует белок альфа-синуклеин, была обнаружена у родственников с болезнью Паркинсона, а тельца Леви и нейриты оказались иммунореактивными в отношении альфа-синуклеина. Таким образом, была установлена агрегация альфа-синуклеина как основной строительный блок синуклеинопатий.
Между 1995 и 2005 годами Консорциум DLB выпустил три консенсусных отчета по DLB. DLB был включен в четвертую редакцию текста DSM (DSM-IV-TR, опубликовано в 2000 г.) в разделе «Деменция, вызванная другими общими медицинскими состояниями». В 2010-х годах появилась возможность генетической основы Четвертый консенсусный отчет был выпущен в 2017 году, в нем повышен диагностический вес сцинтиграфии миокарда RBD и I-MIBG.
 Его вдова сказала, что Робину Уильямсу (показан в 2011 году) был поставлен диагноз во время на вскрытии обнаружены диффузные тельца Леви.
Его вдова сказала, что Робину Уильямсу (показан в 2011 году) был поставлен диагноз во время на вскрытии обнаружены диффузные тельца Леви. Британский писатель и поэт Мервин Пик умер в 1968 году, и его посмертно диагностировали как вероятный случай ДЛБ в исследовании 2003 года, опубликованном в JAMA Neurology. Судя по признакам в его работе и письмам о прогрессирующем ухудшении, колеблющемся когнитивном снижении, ухудшении зрительно-пространственной функции, снижении концентрации внимания, а также зрительных галлюцинациях и иллюзиях, это может быть самый ранний известный случай, когда было обнаружено, что DLB были вероятной причиной смерти.
В то время После самоубийства 11 августа 2014 года Робину Уильямсу, американскому актеру и комику, был поставлен диагноз "болезнь Паркинсона". По словам его вдовы, Уильямс страдал от депрессии, беспокойства и нарастающей паранойи. Его вдова сказала, что его вскрытие показало диффузную болезнь с тельцами Леви, в то время как вскрытие использовало термин диффузное слабоумие с тельцами Леви. Деннис Диксон, представитель Ассоциации деменции с тельцами Леви, разъяснил различие, заявив, что диффузная деменция с тельцами Леви чаще называется диффузной болезнью с тельцами Леви и относится к основному процессу болезни. По словам Диксона, «тельца Леви обычно имеют ограниченное распространение, но в DLB тельца Леви широко распространены по всему мозгу, как это было в случае с Робином Уильямсом». Ян Г. МакКейт, профессор и исследователь деменции с тельцами Леви, прокомментировал, что симптомы Вильямса и результаты вскрытия были объяснены DLB.
Идентификация продромальных биомаркеров DLB позволит начать лечение раньше, улучшит способность отбирать субъектов и измерять эффективность в клинических испытаниях, а также помогать семьям и клиницистам планировать ранние вмешательства и осознавать потенциальные побочные эффекты от использования антипсихотических препаратов. Критерии были предложены в 2020 году, чтобы помочь исследователям лучше распознать DLB в фазе преддеменции. Было предложено три синдрома продромального ДЛБ: 1) легкое когнитивное нарушение с тельцами Леви (MCI-LB); 2) ДЛБ с дебютом делирия; и 3) ДЛБ с психиатрическим началом. Три ранних синдрома могут частично совпадать. По состоянию на 2020 год, позиция группы диагностических исследований DLB заключается в том, что критерии для MCI-LB могут быть рекомендованы, но по-прежнему трудно отличить DLB с дебютным делирием и псиатрическим началом без лучших биомаркеров. По состоянию на 2020 год диагноз DLB ставится с использованием критериев Консорциума DLB, но исследование образцов кожи от 18 человек с DLB в 2017 году показало, что все они имели отложения фосфорилированного альфа-синуклеина, в то время как ни один из контрольная группа сделала это, что свидетельствует о том, что образцы кожи являются потенциальным биомаркером. Другими потенциальными исследуемыми биомаркерами являются количественная электроэнцефалография, визуализация структур мозга и измерение CSF.
Когнитивная тренировка, глубокая стимуляция мозга и прямая транскраниальная -токовая стимуляция больше изучена при болезни Паркинсона и Альцгеймера, чем при деменции с тельцами Леви, и все они являются потенциальными методами лечения ДЛБ. По состоянию на 2019 год ведутся клинические испытания нескольких препаратов. Испытания нейролептика пимавансерина для пациентов с DLB продолжаются, но он имеет риск сердечных побочных эффектов и повышенной смертности. Противосудорожное средство зонисамид одобрено в Японии для лечения болезни Паркинсона и проходит клинические испытания для лечения симптомов паркинсонизма при ДЛБ.
Стратегии будущего вмешательства включают изменение течения болезни с помощью иммунотерапия, генная терапия и терапия стволовыми клетками, а также снижение накопления бета-амилоида или альфа-синуклеина. Терапия, изучаемая по состоянию на 2019 год, направлена на снижение уровня альфа-синуклеина в мозге (с помощью фармацевтических препаратов амброксол и) или на использование иммунотерапии для уменьшения широко распространенного нейровоспаления, вызванного отложениями альфа-синуклеина.
| Классификация | D |
|---|---|
| Внешние ресурсы |