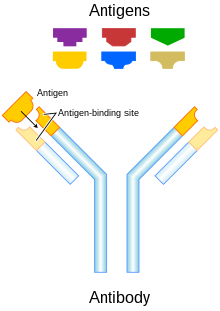
 Каждое антитело связывает только один специфический антиген.
Каждое антитело связывает только один специфический антиген. Терапия моноклональными антителами - это форма иммунотерапии, при которой моноклональные антитела (mAb) используются для моноспецифического связывания с определенными клетками или белками. Цель состоит в том, чтобы это лечение стимулировало иммунную систему пациента к атаке этих клеток. В качестве альтернативы, в радиоиммунотерапии радиоактивная доза локализует линию клеток-мишеней, доставляя смертельные химические дозы. Совсем недавно антитела были использованы для связывания с молекулами, участвующими в регуляции Т-клеток, с целью устранения тормозных путей, которые блокируют ответы Т-клеток. Это известно как иммунная контрольная терапия.
Можно создать mAb, специфичное практически для любой внеклеточной мишени / мишени на клеточной поверхности. В настоящее время ведутся исследования и разработки для создания антител против болезней (таких как ревматоидный артрит, рассеянный склероз, болезнь Альцгеймера, лихорадка Эбола и различные виды рака ).
Антитела к иммуноглобулину G ( IgG ) представляют собой большие гетеродимерные молекулы, примерно 150 кДа, и состоят из двух типов полипептидной цепи, называемых тяжелой (~ 50 кДа) и легкой цепью (~ 25 кДа). Два типа легких цепей - это каппа (κ) и лямбда (λ). Путем расщепления с помощью фермента папаина, то Fab ( фрагмент-антиген - связывающий) часть может быть отделена от Fc ( константа фрагмента) части молекулы. Фрагменты Fab содержат вариабельные домены, которые состоят из трех гипервариабельных аминокислотных доменов антитела, ответственных за специфичность антитела, встроенных в константные области. Четыре известных подкласса IgG участвуют в антителозависимой клеточной цитотоксичности. Антитела являются ключевым компонентом адаптивного иммунного ответа, играя центральную роль как в распознавании чужеродных антигенов, так и в стимуляции иммунного ответа на них. Появление технологии моноклональных антител позволило вырабатывать антитела против специфических антигенов, представленных на поверхности опухолей. Моноклональные антитела могут быть приобретены в иммунной системе через пассивный иммунитет или активный иммунитет. Преимущество терапии активными моноклональными антителами заключается в том, что иммунная система будет вырабатывать антитела в течение длительного времени, и только кратковременное введение лекарства вызывает этот ответ. Однако иммунный ответ на определенные антигены может быть неадекватным, особенно у пожилых людей. Кроме того, из-за длительного ответа на антигены могут возникать побочные реакции со стороны этих антител. Пассивная терапия моноклональными антителами может гарантировать постоянную концентрацию антител и может контролировать побочные реакции путем прекращения введения. Однако многократное введение и, как следствие, более высокая стоимость этой терапии являются серьезными недостатками.
Терапия моноклональными антителами может оказаться полезной при раке, аутоиммунных заболеваниях и неврологических расстройствах, которые приводят к дегенерации клеток организма, таких как болезнь Альцгеймера. Терапия моноклональными антителами может помочь иммунной системе, потому что врожденная иммунная система реагирует на факторы окружающей среды, с которыми она сталкивается, отделяя чужеродные клетки от клеток организма. Следовательно, опухолевые клетки, которые быстро пролиферируют, или клетки организма, которые умирают, что впоследствии вызывает физиологические проблемы, обычно не являются специфическими мишенями иммунной системы, поскольку опухолевые клетки являются собственными клетками пациента. Однако опухолевые клетки в высшей степени аномальны, и многие из них обладают необычными антигенами. Некоторые такие опухолевые антигены не подходят для данного типа клеток или их окружения. Моноклональные антитела могут нацеливаться на опухолевые клетки или аномальные клетки в организме, которые распознаются как клетки организма, но подрывают здоровье.
 Моноклональные антитела против рака. ADEPT: антитело-направленная ферментная пролекарственная терапия ; ADCC: антителозависимая клеточно-опосредованная цитотоксичность ; CDC: комплемент-зависимая цитотоксичность ; MAb, моноклональное антитело; scFv, одноцепочечный фрагмент Fv.
Моноклональные антитела против рака. ADEPT: антитело-направленная ферментная пролекарственная терапия ; ADCC: антителозависимая клеточно-опосредованная цитотоксичность ; CDC: комплемент-зависимая цитотоксичность ; MAb, моноклональное антитело; scFv, одноцепочечный фрагмент Fv. Иммунотерапия была разработана в 1970-х годах после открытия структуры антител и разработки гибридомной технологии, которая стала первым надежным источником моноклональных антител. Эти достижения позволили целенаправленно воздействовать на опухоли как in vitro, так и in vivo. Первоначальные исследования злокачественных новообразований показали, что терапия с применением моноклональных антител имеет ограниченный и, как правило, кратковременный успех при злокачественных новообразованиях крови. Лечение также необходимо было подбирать для каждого отдельного пациента, что было практически невозможно в обычных клинических условиях.
Были разработаны четыре основных типа антител: мышиные, химерные, гуманизированные и человеческие. Антитела каждого типа обозначаются суффиксами в их названиях.
Исходными терапевтическими антителами были мышиные аналоги (суффикс -omab). Эти антитела обладают: коротким периодом полужизни in vivo (из-за образования иммунных комплексов ), ограниченным проникновением в участки опухоли и неадекватным привлечением эффекторных функций хозяина. Химерные и гуманизированные антитела обычно заменяют их в терапевтических применениях антител. Понимание протеомики оказалось важным для выявления новых опухолевых мишеней.
Изначально мышиные антитела были получены гибридомной технологией, за что Йерне, Кёлер и Мильштейн получили Нобелевскую премию. Однако несходство иммунной системы мыши и человека привело к клинической неэффективности этих антител, за исключением некоторых конкретных обстоятельств. Основные проблемы, связанные с мышиными антителами, включали снижение стимуляции цитотоксичности и образование комплексов после повторного введения, что приводило к легким аллергическим реакциям и иногда к анафилактическому шоку. Технология гибридом была заменена технологией рекомбинантной ДНК, трансгенными мышами и фаговым дисплеем.
Чтобы снизить иммуногенность мышиного антитела (атаки иммунной системы на антитело), были сконструированы мышиные молекулы для удаления иммуногенного содержимого и повышения иммунологической эффективности. Первоначально это было достигнуто путем производства химерных (суффикс -симаб) и гуманизированных антител (суффикс -зумаб). Химерные антитела состоят из вариабельных областей мыши, слитых с константными областями человека. Взятие последовательностей генов человека из легкой цепи каппа и тяжелой цепи IgG1 приводит к получению антител, которые примерно на 65% состоят из человеческих. Это снижает иммуногенность и, таким образом, увеличивает период полужизни в сыворотке.
Гуманизированные антитела получают путем трансплантации мышиных гипервариабельных областей на аминокислотных доменах в человеческие антитела. В результате получается молекула примерно 95% человеческого происхождения. Гуманизированные антитела связывают антиген намного слабее, чем исходное мышиное моноклональное антитело, при этом сообщается о снижении аффинности до нескольких сотен раз. Повышение силы связывания антитело-антиген было достигнуто путем внесения мутаций в определяющие комплементарность области (CDR) с использованием таких методов, как перетасовка цепей, рандомизация определяющих комплементарность областей и антител с мутациями в вариабельных областях, индуцированных подверженной ошибкам ПЦР., Штаммы-мутаторы E. coli и сайт-специфический мутагенез.
Человеческие моноклональные антитела (суффикс -умаб) получают с использованием трансгенных мышей или библиотек фагового дисплея путем переноса генов иммуноглобулина человека в мышиный геном и вакцинации трансгенной мыши против желаемого антигена, что приводит к продукции соответствующих моноклональных антител. Таким образом, мышиные антитела in vitro превращаются в полностью человеческие антитела.
Тяжелая и легкая цепи белков человеческого IgG экспрессируются в структурно-полиморфных (аллотипических) формах. Аллотип человеческого IgG - один из многих факторов, которые могут способствовать иммуногенности.
Противораковые моноклональные антитела могут быть нацелены против злокачественных клеток с помощью нескольких механизмов. Рамуцирумаб - это рекомбинантное человеческое моноклональное антитело, которое используется для лечения запущенных злокачественных новообразований. При детской лимфоме исследования I и II фазы показали положительный эффект от использования терапии антителами.
Моноклональные антитела, используемые при аутоиммунных заболеваниях, включают инфликсимаб и адалимумаб, которые эффективны при ревматоидном артрите, болезни Крона и язвенном колите благодаря своей способности связываться с TNF-α и ингибировать его. Базиликсимаб и даклизумаб ингибируют IL-2 на активированных Т-клетках и тем самым помогают предотвратить острое отторжение трансплантатов почек. Омализумаб ингибирует человеческий иммуноглобулин Е (IgE) и полезен при аллергической астме средней и тяжелой степени.
Болезнь Альцгеймера (БА) является многогранным возрастным прогрессирующим нейродегенеративным заболеванием, которое является основной причиной деменции. Согласно гипотезе амилоида, накопление внеклеточных амилоидных бетапептидов (Aβ) в бляшках посредством олигомеризации приводит к характерным симптоматическим состояниям БА через синаптическую дисфункцию и нейродегенерацию. Иммунотерапия посредством введения экзогенного моноклонального антитела (mAb), как известно, лечит различные расстройства центральной нервной системы, такие как AD, путем ингибирования Aβ-олигомеризации, тем самым предотвращая нейротоксичность. Однако mAb имеют большие размеры для пассивных белковых каналов и поэтому неэффективны из -за гематоэнцефалического барьера, предотвращающего проникновение mAb в мозг. Однако гипотеза периферического стока предлагает механизм, при котором mAb может не проходить через гематоэнцефалический барьер. Поэтому многие исследования проводятся на основе неудачных попыток лечения БА в прошлом.
Однако вакцины против Aβ могут способствовать опосредованному антителами клиренсу бляшек Aβ на моделях трансгенных мышей с белками-предшественниками амилоида (APP) и могут снижать когнитивные нарушения. Вакцины могут стимулировать иммунную систему к выработке собственных антител, в этом случае путем введения Aβ в модели трансгенных животных, что называется активной иммунизацией. Они также могут вводить антитела в модели животных, что называется пассивной иммунизацией. Было показано, что у мышей, экспрессирующих АРР, как активная, так и пассивная иммунизация анти-Aβ-антителами эффективна в очищении бляшек и может улучшить когнитивные функции. В настоящее время не существует одобренных препаратов для лечения болезни Альцгеймера с использованием моноклональных антител, но в настоящее время проводится несколько клинических испытаний с использованием пассивных и активных подходов к иммунизации путем разработки определенных лекарств, одобренных FDA, и ожидается, что они дадут результаты через пару лет. Внедрение этих препаратов происходит в период развития АД. Другие исследования и разработка лекарств для раннего вмешательства и профилактики БА продолжаются. Различные препараты, которые исследуются для лечения AD, включают бапинеузумаб, соланезумаб, гаутенерумаб и BAN2401.
Бапинеузумаб, гуманизированное mAb против Aβ, направлено против N-конца Aβ. Клинические испытания фазы II бапинеузумаба у пациентов с БА от легкой до умеренной степени тяжести привели к снижению концентрации Aβ в головном мозге. Однако у пациентов с повышенным уровнем носителей аполипопротеина (APOE) e4 лечение бапинеузумабом также сопровождается вазогенным отеком, цитотоксическим состоянием, при котором нарушен гематоэнцефалический барьер, что влияет на белое вещество из-за избыточного накопления жидкости из капилляров во внутриклеточных и внеклеточных пространствах мозг. В клинических испытаниях фазы III лечение бапинеузумабом ассоциировалось со сниженной скоростью накопления Aβ в головном мозге у пациентов с APOE e4 и отсутствием значительного снижения концентрации Aβ у пациентов с APOE e4 и пациентов без APOE e4. Следовательно, концентрация бляшек Aβ не снижалась, и нет значительных клинических преимуществ для когнитивного функционирования. Бапинеузумаб был прекращен после неудачи клинических испытаний фазы III.
Соланезумаб, mAb против Aβ, нацелен на N-конец Aβ. В фазе I и фазе II клинических испытаний лечение соланезумабом приводило к повышению уровня Aβ в спинномозговой жидкости, тем самым показывая снижение концентрации бляшек Aβ. Кроме того, нет никаких побочных эффектов. Фаза III клинических испытаний соланезумаба привела к значительному снижению когнитивных нарушений у пациентов с легкой формой БА, но не у пациентов с тяжелой формой БА. Однако концентрация Aβ существенно не изменилась, как и другие биомаркеры AD, включая экспрессию фосфо-тау и объем гиппокампа. В настоящее время продолжаются клинические испытания фазы III.
BAN2401 представляет собой гуманизированное mAb, которое избирательно нацелено на токсичные растворимые протофибриллы Aβ, и в настоящее время эта терапия проходит фазу 3 клинических испытаний, которые, как ожидается, будут завершены в 2022 году.
Неудача нескольких препаратов в клинических испытаниях фазы III привела к профилактике БА и раннему вмешательству для начала лечения БА. Пассивное лечение mAb против Aβ можно использовать для профилактических попыток изменить прогрессирование AD до того, как оно вызовет обширное повреждение мозга и симптомы. Испытания с использованием моноклональных антител для лечения пациентов с положительными генетическими факторами риска и пожилых пациентов с положительными показателями AD продолжаются. Это включает лечение анти-АБ при бессимптомной болезни Альцгеймера (A4), Инициативу по профилактике Альцгеймера (API) и DIAN-TU. В исследовании A4 с участием пожилых людей с положительными показателями БА, но отрицательными по генетическим факторам риска, соланезумаб будет тестироваться в клинических испытаниях фазы III, как продолжение предыдущих исследований соланезумаба. DIAN-TU, запущенный в декабре 2012 года, ориентирован на молодых пациентов с положительными генетическими мутациями, которые представляют риск для БА. В этом исследовании используются соланезумаб и гаутенерумаб. Гаутенерумаб, первое полностью человеческое МАБ, которое предпочтительно взаимодействует с олигомеризованными бляшками Aβ в головном мозге, вызывал значительное снижение концентрации Aβ в клинических испытаниях фазы I, предотвращая образование и концентрацию бляшек без изменения концентрации в плазме головного мозга. В настоящее время проводятся клинические испытания фазы II и III.
Радиоиммунотерапия (РИТ) включает использование радиоактивно- конъюгированных мышиных антител против клеточных антигенов. Большинство исследований связано с их применением к лимфомам, поскольку они являются высокочувствительными к радиации злокачественными новообразованиями. Для ограничения радиационного воздействия были выбраны мышиные антитела, поскольку их высокая иммуногенность способствует быстрому очищению от опухоли. Тозитумомаб является примером, применяемым при неходжкинской лимфоме.
Антитело-направленная ферментная пролекарственная терапия (ADEPT) включает применение связанных с раком моноклональных антител, связанных с ферментом, активирующим лекарство. Системное введение нетоксичного агента приводит к превращению антитела в токсичное лекарство, что приводит к цитотоксическому эффекту, который может быть нацелен на злокачественные клетки. Клинический успех лечения ADEPT ограничен.
Конъюгаты антитело-лекарство (ADC) представляют собой антитела, связанные с одной или несколькими молекулами лекарства. Обычно, когда ADC встречает клетку-мишень (например, злокачественную клетку), высвобождается лекарство, чтобы убить ее. Многие ADC находятся в стадии клинической разработки. По состоянию на 2016 год утверждено несколько.
Иммунолипосомы представляют собой липосомы, конъюгированные с антителами. Липосомы могут нести лекарственные препараты или терапевтические нуклеотиды, а при конъюгировании с моноклональными антителами могут быть направлены против злокачественных клеток. Иммунолипосомы успешно использовались in vivo для передачи генов, подавляющих опухоль, в опухоли с использованием фрагмента антитела против рецептора трансферрина человека. Тканеспецифическая доставка генов с использованием иммунолипосом была достигнута в ткани рака мозга и груди.
Терапия с контрольными точками использует антитела и другие методы, чтобы обойти защитные механизмы, которые опухоли используют для подавления иммунной системы. Каждая защита известна как контрольно-пропускной пункт. Комбинированная терапия комбинирует антитела для подавления нескольких защитных слоев. Известные контрольные точки включают CTLA-4, нацеленный на ипилимумаб, PD-1, нацеленный на ниволумаб и пембролизумаб, и микросреду опухоли.
Особенности микроокружения опухоли (TME) предотвращают рекрутирование Т-клеток в опухоль. Способы включают нитрование хемокина CCL 2, который захватывает Т-клетки в строме. Сосудистая сеть опухоли помогает опухолям преимущественно рекрутировать другие иммунные клетки, а не Т-клетки, отчасти за счет специфической для эндотелиальных клеток (ЭК) экспрессии FasL, ET B R и B7H3. Миеломоноцитарные и опухолевые клетки могут повышать экспрессию PD-L1, частично за счет условий гипоксии и продукции цитокинов, таких как IFNβ. Аберрантная продукция метаболитов в TME, такая как регуляция пути с помощью IDO, может влиять на функции T-клеток прямо или косвенно через клетки, такие как T reg- клетки. Клетки CD8 могут подавляться регуляцией ТАМ фенотипов В-клетками. Связанные с раком фибробласты (CAFs) обладают множеством функций TME, частично за счет опосредованного внеклеточным матриксом (ECM) захвата Т-клеток и регулируемого CXCL12 исключения Т-клеток.
Первым терапевтическим моноклональным антителом, одобренным FDA, был мышиный IgG2a CD3-специфический препарат для отторжения трансплантата, OKT3 (также называемый муромонабом), в 1986 году. Этот препарат нашел применение у реципиентов трансплантата твердых органов, которые стали резистентными к стероидам. Сотни методов лечения проходят клинические испытания. Большинство из них имеют дело с иммунологическими и онкологическими целями.
| Антитела | Название бренда | Компания | Дата утверждения | Маршрут | Тип | Цель | Показания (целевое заболевание) | BLA STN | Этикетка препарата |
|---|---|---|---|---|---|---|---|---|---|
| абциксимаб | РеоПро | Centocor | 22.12.1994 | внутривенный | химерный Fab | GPIIb / IIIa | Чрезкожное коронарное вмешательство | 103575 | Ссылка |
| адалимумаб | Хумира | Эббви | 31.12.2002 | подкожный | полностью человек | TNF | Ревматоидный артрит | 125057 | Ссылка |
| адалимумаб-атто | Amjevita | Amgen | 23.09.2016 | подкожный | полностью человеческий, биоподобный | TNF | Ревматоидный артрит Ювенильный идиопатический артрит Псориатический артрит Анкилозирующий спондилит Болезнь Крона Язвенный колит Бляшечный псориаз | 761024 | Ссылка |
| адо-трастузумаб эмтанзин | Кадсила | Genentech | 22.02.2013 | внутривенный | гуманизированный конъюгат антитело-лекарственное средство | HER2 | Метастатический рак груди | 125427 | Ссылка |
| алемтузумаб | Кэмпат, Лемтрада | Genzyme | 07.05.2001 | внутривенный | очеловеченный | CD52 | В-клеточный хронический лимфоцитарный лейкоз | 103948 | Ссылка |
| алирокумаб | Praluent | Санофи Авентис | 24.07.2015 | подкожный | полностью человек | PCSK9 | Гетерозиготная семейная гиперхолестеринемия Рефрактерная гиперхолестеринемия | 125559 | Ссылка |
| атезолизумаб | Тецентрик | Genentech | 18.05.2016 | внутривенный | очеловеченный | PD-L1 | Уротелиальный рак | 761034 | Ссылка |
| атезолизумаб | Тецентрик | Genentech | 18.10.2016 | внутривенный | очеловеченный | PD-L1 | Уротелиальная карцинома Метастатический немелкоклеточный рак легкого | 761041 | Ссылка |
| авелумаб | Бавенсио | EMD Serono | 23.03.2017 | внутривенный | полностью человек | PD-L1 | Метастатическая карцинома из клеток Меркеля | 761049 | Ссылка |
| базиликсимаб | Simulect | Новартис | 12.05.1998 | внутривенный | химерный | IL2RA | Профилактика острого отторжения органа при трансплантации почки | 103764 | Ссылка |
| белимумаб | Бенлиста | Науки о геноме человека | 09.03.2011 | внутривенный | полностью человек | BLyS | Системная красная волчанка | 125370 | Ссылка |
| бевацизумаб | Авастин | Genentech | 26.02.2004 | внутривенный | очеловеченный | VEGF | Метастатический колоректальный рак | 125085 | Ссылка |
| безлотоксумаб | Зинплава | Merck | 21.10.2016 | внутривенный | полностью человек | Clostridium difficile токсин B | Предотвратить рецидив инфекции Clostridium difficile | 761046 | Ссылка |
| блинатумомаб | Blincyto | Amgen | 03.12.2014 | внутривенный | мышь, биспецифическая | CD19 | Предшественник В-клеточного острого лимфобластного лейкоза | 125557 | Ссылка |
| брентуксимаб ведотин | Адцетрис | Сиэтл Генетикс | 19.09.2011 | внутривенный | химерный конъюгат антитело-лекарственное средство | CD30 | Лимфома Ходжкина Анапластическая крупноклеточная лимфома | 125388 | Ссылка |
| бродалумаб | Siliq | Valeant | 15.02.2017 | подкожный | химерный | IL17RA | Бляшечный псориаз | 761032 | Ссылка |
| канакинумаб | Иларис | Новартис | 17.06.2009 | подкожный | полностью человек | IL1B | Криопирин-ассоциированный периодический синдром | 125319 | Ссылка |
| капромаб пендетид | ПростаСцинт | Цитоген | 28.10.1996 | внутривенный | мышиный, с радиоактивной меткой | PSMA | Агент диагностической визуализации при недавно диагностированном раке простаты или после простатэктомии | 103608 | Ссылка |
| цертолизумаб пегол | Cimzia | UCB (компания) | 22.04.2008 | подкожный | очеловеченный | TNF | болезнь Крона | 125160 | Ссылка |
| цетуксимаб | Эрбитукс | Системы ImClone | 12.02.2004 | внутривенный | химерный | EGFR | Метастатическая колоректальная карцинома | 125084 | Ссылка |
| даклизумаб | Зенапакс | Рош | 10.12.1997 | внутривенный | очеловеченный | IL2RA | Профилактика острого отторжения органа при трансплантации почки | 103749 | Ссылка |
| даклизумаб | Зинбрыта | Биоген | 27.05.2016 | подкожный | очеловеченный | IL2R | Рассеянный склероз | 761029 | Ссылка |
| даратумумаб | Дарзалекс | Янссен Биотех | 16.11.2015 | внутривенный | полностью человек | CD38 | Множественная миелома | 761036 | Ссылка |
| деносумаб | Пролиа, Xgeva | Amgen | 01.06.2010 | подкожный | полностью человек | RANKL | Женщины в постменопаузе с остеопорозом | 125320 | Ссылка |
| динутуксимаб | Унитуксин | United Therapeutics | 10.03.2015 | внутривенный | химерный | GD2 | Детская нейробластома высокого риска | 125516 | Ссылка |
| дупилумаб | Дюпиксент | Regeneron Pharmaceuticals | 28.03.2017 | подкожный | полностью человек | IL4RA | Атопический дерматит, астма | 761055 | Ссылка |
| дурвалумаб | Имфинзи | АстраЗенека | 01.05.2017 | внутривенный | полностью человек | PD-L1 | Уротелиальный рак | 761069 | Ссылка |
| экулизумаб | Солирис | Алексион | 16.03.2007 | внутривенный | очеловеченный | Компонент комплемента 5 | Пароксизмальная ночная гемоглобинурия | 125166 | Ссылка |
| элотузумаб | Empliciti | Бристоль-Майерс Сквибб | 30.11.2015 | внутривенный | очеловеченный | SLAMF7 | Множественная миелома | 761035 | Ссылка |
| эволокумаб | Репата | Amgen | 27.08.2015 | подкожный | полностью человек | PCSK9 | Гетерозиготная семейная гиперхолестеринемия Рефрактерная гиперхолестеринемия | 125522 | Ссылка |
| голимумаб | Симпони | Centocor | 24.04.2009 | подкожный | полностью человек | TNF | Ревматоидный артрит Псориатический артрит Анкилозирующий спондилит | 125289 | Ссылка |
| голимумаб | Симпони Ария | Янссен Биотех | 18.07.2013 | внутривенный | полностью человек | TNF | Ревматоидный артрит | 125433 | Ссылка |
| ибритумомаб тиуксетан | Зевалин | Spectrum Pharmaceuticals | 19.02.2002 | внутривенный | мышь, радиоиммунотерапия | CD20 | Рецидивирующая или рефрактерная низкосортная, фолликулярная или трансформированная В-клеточная неходжкинская лимфома | 125019 | Ссылка |
| идаруцизумаб | Praxbind | Boehringer Ingelheim | 16.10.2015 | внутривенный | очеловеченный Fab | дабигатран | Экстренная отмена антикоагулянта дабигатрана | 761025 | Ссылка |
| инфликсимаб | Ремикейд | Centocor | 24.08.1998 | внутривенный | химерный | TNF альфа | болезнь Крона | 103772 | Ссылка |
| инфликсимаб-абда | Renflexis | Самсунг Биоэпис | 21.04.2017 | внутривенный | химерный, биоподобный | TNF | Болезнь Крона Язвенный колит Ревматоидный артрит Анкилозирующий спондилит Псориатический артрит Бляшечный псориаз | 761054 | Ссылка |
| инфликсимаб-дийб | Инфлектра | Celltrion Healthcare | 05.04.2016 | внутривенный | химерный, биоподобный | TNF | Болезнь Крона Язвенный колит Ревматоидный артрит Анкилозирующий спондилит Псориатический артрит Бляшечный псориаз | 125544 | Ссылка |
| ипилимумаб | Ервой | Бристоль-Майерс Сквибб | 25.03.2011 | внутривенный | полностью человек | CTLA-4 | Метастатическая меланома | 125377 | Ссылка |
| иксекизумаб | Тальц | Эли Лилли | 22.03.2016 | подкожный | очеловеченный | IL17A | Бляшечный псориаз | 125521 | Ссылка |
| меполизумаб | Nucala | GlaxoSmithKline | 04.11.2015 | подкожный | очеловеченный | IL5 | Тяжелая астма | 125526 | Ссылка |
| натализумаб | Тисабри | Биоген Идек | 23.11.2004 | внутривенный | очеловеченный | альфа-4 интегрин | Рассеянный склероз | 125104 | Ссылка |
| нецитумумаб | Portrazza | Эли Лилли | 24.11.2015 | внутривенный | полностью человек | EGFR | Метастатический плоскоклеточный немелкоклеточный рак легкого | 125547 | Ссылка |
| ниволумаб | Opdivo | Бристоль-Майерс Сквибб | 22.12.2014 | внутривенный | полностью человек | ПД-1 | Метастатическая меланома | 125554 | Ссылка |
| ниволумаб | Opdivo | Бристоль-Майерс Сквибб | 04.03.2015 | внутривенный | полностью человек | ПД-1 | Метастатический плоскоклеточный немелкоклеточный рак легкого | 125527 | Ссылка |
| обилтоксаксимаб | Гимн | Elusys Therapeutics | 18.03.2016 | внутривенный | химерный | Защитный антиген токсина сибирской язвы | Ингаляционная форма сибирской язвы | 125509 | Ссылка |
| обинутузумаб | Газыва | Genentech | 01.11.2013 | внутривенный | очеловеченный | CD20 | Хронический лимфолейкоз | 125486 | Ссылка |
| окрелизумаб | Окревус | Genentech | 28.03.2017 | внутривенный | очеловеченный | CD20 | Рассеянный склероз | 761053 | Ссылка |
| офатумумаб | Арзерра | Glaxo Grp | 26.10.2009 | внутривенный | полностью человек | CD20 | Хронический лимфолейкоз | 125326 | Ссылка |
| оларатумаб | Лартруво | Эли Лилли | 19.10.2016 | внутривенный | полностью человек | PDGFRA | Саркома мягких тканей | 761038 | Ссылка |
| омализумаб | Xolair | Genentech | 20.06.2003 | подкожный | очеловеченный | IgE | Постоянная астма от умеренной до тяжелой степени | 103976 | Ссылка |
| паливизумаб | Synagis | MedImmune | 19.06.1998 | внутримышечный | очеловеченный | Белок F RSV | респираторно-синцитиальный вирус | 103770 | Ссылка |
| панитумумаб | Вектибикс | Amgen | 27.09.2006 | внутривенный | полностью человек | EGFR | Метастатический колоректальный рак | 125147 | Ссылка |
| пембролизумаб | Кейтруда | Merck | 04.09.2014 | внутривенный | очеловеченный | ПД-1 | Метастатическая меланома | 125514 | Ссылка |
| пертузумаб | Perjeta | Genentech | 08.06.2012 | внутривенный | очеловеченный | HER2 | Метастатический рак груди | 125409 | Ссылка |
| рамуцирумаб | Cyramza | Эли Лилли | 21.04.2014 | внутривенный | полностью человек | VEGFR2 | Рак желудка | 125477 | Ссылка |
| ранибизумаб | Луцентис | Genentech | 30.06.2006 | интравитреальная инъекция | очеловеченный | VEGFR1 VEGFR2 | Влажная возрастная дегенерация желтого пятна | 125156 | Ссылка |
| раксибакумаб | Раксибакумаб | Науки о геноме человека | 24.12.2012 | внутривенный | полностью человек | Защитный антиген Bacillus anthracis | Ингаляционная форма сибирской язвы | 125349 | Ссылка |
| реслизумаб | Cinqair | Тева | 23.03.2016 | внутривенный | очеловеченный | IL5 | Тяжелая астма | 761033 | Ссылка |
| ритуксимаб | Ритуксан | Genentech | 26.11.1997 | внутривенный | химерный | CD20 | В-клеточная неходжкинская лимфома | 103705 | Ссылка |
| секукинумаб | Козентикс | Новартис | 21.01.2015 | подкожный | полностью человек | IL17A | Бляшечный псориаз | 125504 | Ссылка |
| силтуксимаб | Сильвант | Янссен Биотех | 23.04.2014 | внутривенный | химерный | IL6 | Мультицентрическая болезнь Кастлемана | 125496 | Ссылка |
| тоцилизумаб | Актемра | Genentech | 08.01.2010 | внутривенный | очеловеченный | IL6R | Ревматоидный артрит | 125276 | Ссылка |
| тоцилизумаб | Актемра | Genentech | 21.10.2013 | внутривенно подкожно | очеловеченный | IL6R | Ревматоидный артрит Полиартикулярный ювенильный идиопатический артрит Системный ювенильный идиопатический артрит | 125472 | Ссылка |
| трастузумаб | Герцептин | Genentech | 25.09.1998 | внутривенный | очеловеченный | HER2 | Метастатический рак груди | 103792 | Ссылка |
| устекинумаб | Стелара | Centocor | 25.09.2009 | подкожный | полностью человек | IL12 IL23 | Бляшечный псориаз | 125261 | Ссылка |
| устекинумаб | Стелара | Янссен Биотех | 23.09.2016 | подкожный внутривенный | полностью человек | IL12 IL23 | Бляшечный псориаз Псориатический артрит Болезнь Крона | 761044 | Ссылка |
| ведолизумаб | Entyvio | Такеда | 20.05.2014 | внутривенный | очеловеченный | рецептор интегрина | Язвенный колит болезнь Крона | 125476 | Ссылка |
| сарилумаб | Кевзара | Санофи Авентис | 22.05.17 | подкожный | полностью человек | IL6R | Ревматоидный артрит | 761037 | Ссылка |
| ритуксимаб и гиалуронидаза | Ритуксан Хицела | Genentech | 22.06.17 | подкожный | химерный, совместно сформулированный | CD20 | Фолликулярная лимфома Диффузная В-крупноклеточная лимфома Хронический лимфолейкоз | 761064 | Ссылка |
| гуселкумаб | Тремфья | Янссен Биотех | 13.07.17 | подкожный | полностью человек | IL23 | Бляшечный псориаз | 761061 | Ссылка |
| инотузумаб озогамицин | Беспона | Wyeth | 17.08.17 | внутривенный | гуманизированный конъюгат антитело-лекарственное средство | CD22 | Предшественник В-клеточного острого лимфобластного лейкоза | 761040 | Ссылка |
| адалимумаб-adbm | Цилтезо | Boehringer Ingelheim | 25.08.17 | подкожный | полностью человеческий, биоподобный | TNF | Ревматоидный артрит Ювенильный идиопатический артрит Псориатический артрит Анкилозирующий спондилит Болезнь Крона Язвенный колит Бляшечный псориаз | 761058 | Ссылка |
| гемтузумаб озогамицин | Mylotarg | Wyeth | 01.09.17 | внутривенный | гуманизированный конъюгат антитело-лекарственное средство | CD33 | Острый миелоидный лейкоз | 761060 | Ссылка |
| бевацизумаб-аввб | Мваси | Amgen | 14.09.17 | внутривенный | гуманизированный, биоподобный | VEGF | Метастатический рак ободочной неплоскоклеточным Non-мелкоклеточного рака легких Глиобластома Метастатический клеточный рак почек рак шейки матки | 761028 | Ссылка |
| бенрализумаб | Fasenra | Астразенека | 14.11.17 | подкожный | очеловеченный | альфа-субъединица рецептора интерлейкина-5 | Тяжелая астма, эозинофильный фенотип | 761070 | Ссылка |
| эмицизумаб-kxwh | Гемлибра | Genentech | 16.11.17 | подкожный | гуманизированный, биспецифический | Фактор IXa, Фактор X | Гемофилия A (врожденный дефицит фактора VIII ) с ингибиторами фактора VIII. | 761083 | Ссылка |
| трастузумаб-dkst | Огиври | Mylan | 01.12.17 | внутривенный | гуманизированный, биоподобный | HER2 | Рак молочной железы с гиперэкспрессией HER2, метастазная аденокарцинома желудка или пищеводно-пищеводного перехода | 761074 | Ссылка |
| инфликсимаб-qbtx | Иксифи | Pfizer | 13.12.17 | внутривенный | химерный, биоподобный | TNF | Болезнь Крона Язвенный колит Ревматоидный артрит Анкилозирующий спондилит Псориатический артрит Бляшечный псориаз | 761072 | Ссылка |
| ибализумаб-уйык | Трогарцо | TaiMed Biologics | 06.03.18 | внутривенный | очеловеченный | CD4 | ВИЧ | 761065 | Ссылка |
| тильдракизумаб-асмн | Илумья | Merck | 20.03.18 | подкожный | очеловеченный | IL23 | Бляшечный псориаз | 761067 | Ссылка |
| буросумаб-тваза | Крисвита | Ультрагеникс | 17.04.18 | подкожный | полностью человек | FGF23 | Х-сцепленная гипофосфатемия | 761068 | Ссылка |
| эренумаб-аоо | Аймовиг | Amgen | 17.05.18 | подкожный | полностью человек | Рецептор CGRP | Профилактика мигрени | 761077 | Ссылка |
Тозитумомаб - Бексар - 2003 - CD20
Могамулизумаб - Poteligeo - август 2018 - CCR4
Моксетумомаб пасудотокс - Люмоксити - сентябрь 2018 - CD22
Цемиплимаб - Либтайо - сентябрь 2018 - PD-1
Полатузумаб ведотин - Polivy - июнь 2019 - CD79B
Недавно биспецифические антитела, новый класс терапевтических антител, дали многообещающие результаты в клинических испытаниях. В апреле 2009 года в Европейском Союзе было одобрено биспецифическое антитело катумаксомаб.
С 2000 года терапевтический рынок моноклональных антител вырос в геометрической прогрессии. В 2006 г. на рынке терапевтических антител «большой пятерки» были бевацизумаб, трастузумаб (как онкологические), адалимумаб, инфликсимаб (как аутоиммунные, так и воспалительные заболевания, «AIID») и ритуксимаб (онкология и AIID). 2006. В 2007 году восемь из 20 самых продаваемых биотехнологических препаратов в США являются терапевтическими моноклональными антителами. Столь быстрый рост спроса на производство моноклональных антител был хорошо воспринят индустриализацией производства mAb.