| Отторжение трансплантата | |
|---|---|
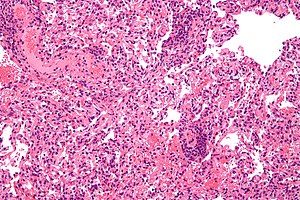 | |
| Микрофотография, показывающая трансплантат легкого отказ. Биопсия легкого . Окрашивание HE. | |
| Специальность | Иммунология |
| Лечение | Иммунодепрессанты |
Отторжение трансплантата происходит, когда трансплантированная ткань отторгается иммунной системой реципиента, который разрушает пересаженную ткань. Отторжение трансплантата можно уменьшить путем определения молекулярного сходства между донором и реципиентом и применением иммунодепрессантов после трансплантации.
Первая успешная трансплантация органов, выполненная в 1954 г. Джозефом Мюрреем, включала идентификацию l близнецов, поэтому отторжения не наблюдалось. В противном случае количество несовпадающих вариантов гена, а именно аллелей, кодирующих молекулы клеточной поверхности, называемые главным комплексом гистосовместимости (MHC), классы I и II, коррелируют с быстротой и серьезностью отторжения трансплантата.. У людей MHC также называют лейкоцитарным антигеном человека (HLA).
Хотя анализ цитотоксического перекрестного совпадения может прогнозировать отторжение, опосредованное клеточным иммунитетом, тесты генетической экспрессии, специфичные для тип органа, подлежащего трансплантации, например AlloMap Molecular Expression Testing, имеет высокую отрицательную прогностическую ценность. Пересадка только ABO -совместимых трансплантатов (соответствующие группы крови донора и реципиента) помогает предотвратить отторжение, опосредованное гуморальным иммунитетом.
Потому что очень маленькие дети (обычно моложе 12 месяцев, но часто до 24 месяцев) не имеют хорошо развитой иммунной системы, они могут получить органы от несовместимых доноров. Это известно как трансплантация, несовместимая с ABO (ABOi). Выживаемость трансплантата и смертность пациентов примерно одинаковы между ABOi и ABO-совместимыми реципиентами (ABOc). Хотя основное внимание уделяется трансплантации сердца младенцам, эти принципы обычно применимы к другим формам трансплантации твердых органов.
Наиболее важными факторами являются то, что реципиент не продуцирует изогемагглютинины, и что они имеют низкие уровни Т-клеточно-независимых антигенов. Правила UNOS разрешают трансплантацию ABOi детям в возрасте до двух лет, если титры изогемагглютинина составляют 1: 4 или ниже, и если нет подходящего реципиента ABOc. Исследования показали, что период, в течение которого реципиент может пройти трансплантацию ABOi, может быть продлен за счет воздействия посторонних антигенов A и B. Кроме того, если реципиенту (например, положительному типу B с трансплантатом положительному типу AB) потребуется повторная трансплантация, реципиент может получить новый орган любой группы крови.
В ABO достигнут ограниченный успех. несовместимые трансплантаты сердца у взрослых, хотя для этого необходимо, чтобы у взрослых реципиентов был низкий уровень анти-A или анти-B антител. Трансплантация почки более успешна, при этом показатели долгосрочной выживаемости трансплантатов аналогичны трансплантатам ABOc.
Отторжение - это адаптивный иммунный ответ через клеточный иммунитет (опосредованный Т-клетками-киллерами, вызывающими апоптоз клеток-мишеней), а также гуморальный иммунитет (опосредованный активированными В-клетками, секретирующими молекулы антитела ), хотя к действию присоединяются компоненты врожденного иммунного ответа (фагоциты и растворимые иммунные белки). Разные типы трансплантированных тканей склонны к разному балансу механизмов отторжения.
Воздействие на животное антигенами разных представителей одного и того же или сходного вида является аллостимуляцией, а ткань подвергается действию аллогенный. Трансплантированные органы часто получают от трупа (обычно от хозяина, который скончался от травмы), ткани которого уже перенесли ишемию или воспаление.
Дендритные клетки (DC), которые являются первичными антигенпрезентирующими клетками (APC), донорской ткани мигрируют в периферическую лимфоидную ткань реципиента (лимфоидные фолликулы и лимфатические узлы ) и представляют собственные пептиды донора лимфоцитам реципиента (иммунные клетки, находящиеся в лимфоидных тканях). Лимфоциты включают два класса, которые обладают адаптивным иммунитетом, также называемым специфическим иммунитетом. Лимфоциты специфического иммунитета Т-клетки - включая подклассы и Т-клетки-киллеры - и В-клетки.
Т-хелперы реципиента координировать специфический иммунитет, направленный на собственные пептиды донора или на молекулы главного комплекса гистосовместимости донора, или на то и другое.
Когда рецепторы Т-хелперов памяти CD4 связываются с молекулами MHC класса II, которые экспрессируются на поверхности мишени клетки ткани трансплантата, Т-хелперные Т-клетки памяти Т-клеточные рецепторы (TCR) могут распознавать свой антиген-мишень, который представлен молекулами MHC класса II. Затем Т-хелперные Т-клетки памяти продуцируют клоны, которые в качестве эффекторных клеток секретируют молекулы, передающие иммунные сигналы (цитокины ), приблизительно в том балансе цитокинов, который преобладал при примировании Т-хелперных Т-клеток памяти для запоминания антигена. Поскольку первичное событие в этом случае произошло на фоне воспаления, иммунная память является провоспалительной.
Поскольку клетка обозначена префиксом цито, цитотоксическое воздействие разрушает клетку. Аллореактивные Т-клетки-киллеры, также называемые цитотоксическими Т-лимфоцитами (CTL), имеют рецепторы CD8, которые присоединяются к молекулам MHC класса I трансплантированной ткани, которые отображают собственные пептиды донора. (У живого донора такая презентация аутоантигенов помогает поддерживать самотолерантность.) Вследствие этого рецепторы Т-клеток (TCR) Т-клеток-киллеров распознают соответствующий им эпитоп и запускают запрограммированная гибель клетки-мишени из-за апоптоза.
Развитый в результате более раннего первичного воздействия, которое примировало специфический иммунитет к чужеродному антигену, реципиент трансплантата может иметь специфические антитела перекрестная реакция с донорской тканью после трансплантации, вторичное воздействие. Это типично для воздействия малых групп крови (например, Kell) после переливания аллогенной крови или травмы во время беременности. При вторичном воздействии эти перекрестно-реактивные молекулы антител взаимодействуют с аспектами врожденного иммунитета - растворимыми иммунными белками, называемыми комплементом, и клетками врожденного иммунитета, называемыми фагоцитами, которые воспламеняют и разрушают трансплантированная ткань.
Секретируется активированной B-клеткой, затем называемой плазматической клеткой, молекула антитела представляет собой растворимый иммуноглобулин (Ig), основная единица которого имеет форму буква Y: два ответвления - это Fab-области, а один стержень - это Fc-область. Каждая из двух концов Fab-области является паратопом, который связывает соответствующую молекулярную последовательность и ее трехмерную форму (конформацию), вместе называемую эпитопом, внутри антигена-мишени.
Fc-область IgG также обеспечивает опсонизацию с помощью фагоцита, процесс, посредством которого Fc-рецептор на фагоцит - такой как нейтрофилы в крови и макрофаги в тканях - связывает ножку FC молекулы антитела, и фагоцит демонстрирует повышенное поглощение антигена, присоединенного к Fab-области молекулы антитела.
Когда паратоп гамма класса Ig (IgG) связывает соответствующий ему эпитоп, конформационный сдвиг Fc-области IgG и может быть хозяином белка комплемента, инициируя каскад комплемента который завершается пробиванием дыры в клеточной мембране. Когда таким образом пробивается множество отверстий, жидкость устремляется в клетку и разрывает ее.
Клеточный мусор может быть распознан как молекулярные паттерны, связанные с повреждением (DAMP), с помощью рецепторов распознавания паттернов (PRR), такие как Toll-подобные рецепторы (TLR), на мембранах фагоцитов, которые в результате секретируют провоспалительные цитокины, привлекая больше фагоцитов для передачи области путем определения градиента концентрации секретируемых цитокинов (хемотаксис ).
| Ткань | Механизм |
|---|---|
| Кровь | Антитела (изогемагглютинины) |
| Почки | Антитела, клеточный иммунитет (CMI) |
| Сердце | Антитела, CMI |
| Кожа | CMI |
| Костный мозг | CMI |
| Cornea | Обычно принимается без васкуляризации: CMI |
Инициируется существовавшим ранее гуморальным иммунитетом, сверхострое отторжение проявляется в течение нескольких минут после трансплантации, а если ткань остается имплантированной, вызывает синдром системной воспалительной реакции. Высоким риском при трансплантации почек является быстрое скопление, а именно агглютинация, красных кровяных телец (эритроцитов или эритроцитов), поскольку молекула антитела связывает несколько клеток-мишеней на один раз.
В то время как почки обычно можно получить от людей-доноров, большинство органов испытывает дефицит, что приводит к рассмотрению возможности использования ксенотрансплантатов от других видов. Свиньи являются наиболее вероятным источником ксенотрансплантатов, выбранных по анатомическим и физиологическим характеристикам, которые у них общие с людьми. Однако сахар галактоза-альфа-1,3-галактоза (αGal) был задействован в качестве основного фактора сверхострого отторжения при ксенотрансплантации. В отличие от практически всех других млекопитающих, люди и другие приматы не производят αGal и фактически распознают его как антиген. Во время трансплантации ксенореактивные природные антитела распознают αGal на эндотелии трансплантата в качестве антигена, и результирующий опосредованный комплементом иммунный ответ приводит к отторжению трансплантата.
Развивается с образованием клеточный иммунитет, острое отторжение в некоторой степени происходит во всех трансплантатах, кроме однояйцевых близнецов, если не достигается иммуносупрессия (обычно с помощью лекарств). Острое отторжение начинается уже через неделю после трансплантации, причем риск наиболее высок в первые три месяца, хотя может произойти через несколько месяцев или лет. В тканях с высоким содержанием сосудов, таких как почки или печень, часто возникают самые ранние признаки - особенно в эндотелиальных клетках, выстилающих кровеносные сосуды, - хотя в конечном итоге это встречается примерно в 10-30% трансплантатов печени и 10 до 20% пересадок почек. Единичный эпизод острого отторжения можно распознать и незамедлительно лечить, обычно предотвращая органную недостаточность, но повторяющиеся эпизоды приводят к хроническому отторжению. Считается, что процесс острого отторжения опосредуется клеточно-опосредованным путем, в частности, мононуклеарными макрофагами и Т-лимфоцитами. Гистология острого отторжения определяется плотным лимфоцитарно-клеточным инфильтратом, а также васкулитом донорских сосудов органов.
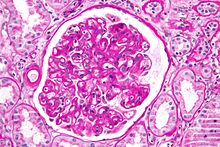 Микрофотография, показывающая клубок с изменениями, характерными для трансплантата гломерулопатия. Гломерулопатия трансплантата считается формой хронического опосредованного антителами отторжения. Окраска PAS.
Микрофотография, показывающая клубок с изменениями, характерными для трансплантата гломерулопатия. Гломерулопатия трансплантата считается формой хронического опосредованного антителами отторжения. Окраска PAS.Термин хроническое отторжение первоначально описывал долгосрочную потерю функции трансплантированных органов из-за фиброза кровеносных сосудов трансплантированной ткани. В настоящее время это хроническая васкулопатия аллотрансплантата, однако хроническое отторжение связано с отторжением из-за более очевидных аспектов иммунитета.
Хроническое отторжение объясняет длительную заболеваемость у большинства реципиентов трансплантата легкого, средняя выживаемость составляет примерно 4,7 года, примерно половина размаха по сравнению с другими крупными пересадками органов. В гистопатологии это заболевание - облитерирующий бронхиолит, который клинически проявляется как прогрессирующая обструкция дыхательных путей, часто включающая одышку и кашель, и пациент в конечном итоге умирает от легочной недостаточности или вторичной острая инфекция.
Обструкция дыхательных путей, не связанная с другой причиной, обозначается как облитерирующий бронхиолит синдром (БОС), что подтверждается постоянным снижением - три или более недель - в принудительном объем выдоха (ОФВ 1) не менее чем на 20%. БОС наблюдается у более чем 50% реципиентов трансплантата легких к 5 годам и более чем у 80% к 10 годам. Сначала отмечается инфильтрация лимфоцитами, затем повреждение эпителиальных клеток, затем воспалительные поражения и рекрутирование фибробластов и миофибробластов, которые пролиферируют и выделяют белки, образующие рубцовую ткань. Обычно считается непредсказуемым, прогрессирование BOS широко варьируется: функция легких может внезапно снижаться, но стабилизироваться в течение многих лет, или быстро прогрессировать до смерти в течение нескольких месяцев. Факторы риска включают предшествующие эпизоды острого отторжения, гастроэзофагеальную рефлюксную болезнь, острые инфекции, определенные возрастные группы, несоответствие HLA, лимфоцитарный бронхиолит и дисфункцию трансплантата (например, ишемию дыхательных путей) <. 114>
Одной из основных причин отторжения трансплантата является несоблюдение предписанных режимов иммунодепрессантов. Это особенно характерно для реципиентов-подростков, где в некоторых случаях показатели несоблюдения режима лечения составляют около 50%.
Диагностика острого отторжения основывается на клинических данных - признаках и симптомах пациента, но также требует лабораторных данных, таких как кровь или даже биопсия ткани . Лабораторный патолог обычно ищет три основных гистологических признака: (1) инфильтрация Т-лимфоцитов, возможно, сопровождающаяся инфильтрацией эозинофилов, плазматических клеток, и нейтрофилы, особенно в контрольных соотношениях, (2) структурное нарушение анатомии ткани, зависящее от типа пересаженной ткани, и (3) повреждение кровеносных сосудов. Однако биопсия ткани ограничена ограничениями выборки и рисками / осложнениями инвазивной процедуры. Клеточная магнитно-резонансная томография (МРТ) иммунных клеток радиоактивно меченных in vivo может - аналогично профилю экспрессии генов (GEP) - предложить неинвазивное тестирование.
Сверхострое отторжение проявляется серьезно и в течение нескольких минут, поэтому немедленное лечение: удаление ткани. Хроническое отторжение обычно считается необратимым и плохо поддается лечению - обычно назначается только повторная трансплантация, если это возможно, - хотя ингаляционный циклоспорин исследуется, чтобы отсрочить или предотвратить хроническое отторжение трансплантата легких. Острое отторжение лечится одной или несколькими из нескольких стратегий. Несмотря на лечение, отторжение остается основной причиной неэффективности трансплантата.
Можно применять короткий курс высоких доз кортикостероидов и повторять его. В тройную терапию добавляются ингибитор кальциневрина и антипролиферативный агент. Если ингибиторы кальциневрина или стероиды противопоказаны, используются ингибиторы mTOR.
Иммуносупрессивные препараты :
Антитела, специфичные для выбранных иммунных компонентов, могут быть добавлены к иммуносупрессивной терапии. моноклональное анти-Т-клеточное антитело OKT3, которое когда-то применялось для предотвращения отторжения, но до сих пор иногда используется для лечения тяжелого острого отторжения, попало в немилость, поскольку обычно вызывает тяжелое синдром высвобождения цитокинов и позднее лимфопролиферативное нарушение после трансплантации. (OKT3 доступен в Соединенном Королевстве только для использования с указанными пациентами.)
Лекарственные препараты с антителами :
Пациенты, невосприимчивые к иммуносупрессивной терапии или терапии антителами, иногда лечат фотоферезом или экстракорпоральной фотоиммунной терапией (ECP) для удаления молекул антител, специфичных для трансплантированной ткани.
Пересадка костного мозга может заменить иммунную систему реципиента трансплантата на иммунную систему донора, и реципиент принимает новый орган без отторжения. гемопоэтические стволовые клетки костного мозга - резервуар стволовых клеток, восполняющих истощенные клетки крови, включая лейкоциты, формирующие иммунную систему - должны принадлежать человеку, сдавшему орган или идентичного близнеца или клона. Однако существует риск болезни «трансплантат против хозяина» (GVHD), при которой зрелые лимфоциты, проникающие с костным мозгом, распознают новые ткани хозяина как чужеродные и разрушают их.
Генная терапия - еще один метод, который можно использовать. В этом методе гены, которые заставляют организм отвергать трансплантаты, будут деактивированы. Исследования все еще продолжаются, и на сегодняшний день для лечения пациентов не используются никакие генные методы лечения. Текущие исследования, как правило, сосредоточены на Th1 и Th17, которые опосредуют отторжение аллотрансплантата через CD4 и CD8 Т-клетки
| Классификация | D |
|---|---|
| Внешние ресурсы |