 Сканирующая электронная микрофотография нейтрофилы фагоцитирующие бациллы сибирской язвы (оранжевый)
Сканирующая электронная микрофотография нейтрофилы фагоцитирующие бациллы сибирской язвы (оранжевый) Фагоциты - это клетки, которые защищают организм, проглатывая вредные инородные частицы, бактерии и мертвые или умирающих клеток. Их название происходит от греческого фагеина, «есть» или «пожирать», и «-цита», суффикса в биологии, обозначающего «клетка», от греческого kutos, «полый сосуд». Они необходимы для борьбы с инфекциями и для последующего иммунитета. Фагоциты важны для всего животного мира и очень развиты у позвоночных. Один литр крови человека содержит около шести миллиардов фагоцитов. Их открыл в 1882 году Илья Ильич Мечников, изучая морскую звезду личинок. За свое открытие Мечников был удостоен Нобелевской премии по физиологии и медицине 1908 . Фагоциты встречаются у многих видов; некоторые амебы ведут себя как макрофагальные фагоциты, что говорит о том, что фагоциты появились на раннем этапе эволюции жизни.
Фагоциты человека и других животных называются «профессиональными» или «непрофессиональными» в зависимости от насколько они эффективны при фагоцитозе. Профессиональные фагоциты включают множество типов лейкоцитов (например, нейтрофилов, моноцитов, макрофагов, тучных клеток и дендритные клетки ). Основное различие между профессиональными и непрофессиональными фагоцитами заключается в том, что профессиональные фагоциты имеют на своей поверхности молекулы, называемые рецепторами, которые могут обнаруживать вредные объекты, такие как бактерии, которые обычно не встречаются в организме. Фагоциты имеют решающее значение в борьбе с инфекциями, а также в поддержании здоровья тканей путем удаления мертвых и умирающих клеток, которые достигли конца своей жизни.
Во время инфекции химические сигналы привлекают фагоциты в места, где проник патоген тело. Эти химические вещества могут поступать от бактерий или других уже имеющихся фагоцитов. Фагоциты перемещаются с помощью метода, называемого хемотаксис. Когда фагоциты контактируют с бактериями, рецепторы на поверхности фагоцитов связываются с ними. Это связывание приведет к поглощению бактерий фагоцитом. Некоторые фагоциты убивают проглоченный патоген с помощью оксидантов и оксида азота. После фагоцитоза макрофаги и дендритные клетки также могут участвовать в презентации антигена, процессе, в котором фагоцит перемещает части проглоченного материала обратно на свою поверхность. Затем этот материал отображается другим клеткам иммунной системы. Затем некоторые фагоциты перемещаются в лимфатические узлы тела и отображают материал в белых кровяных тельцах, называемых лимфоцитами. Этот процесс важен для построения иммунитета, и многие патогены разработали методы, позволяющие избежать атак фагоцитов.
 Илья Ильич Мечников в своей лаборатории
Илья Ильич Мечников в своей лаборатории Русский зоолог Илья Ильич Мечников (1845–1916) первым осознал, что специализированные клетки участвуют в защите от микробных инфекций. В 1882 году он изучил подвижные (свободно движущиеся) клетки у личинок морских звезд, полагая, что они важны для иммунной защиты животных. Чтобы проверить свою идею, он вставил в личинок маленькие шипы от мандаринового дерева. Через несколько часов он заметил, что подвижные клетки окружили шипы. Мечников побывал в Вене и поделился своими идеями с Карлом Фридрихом Клаусом, который предложил название «фагоцит» (от греческих слов фагеин, что означает «есть или пожирать», и куто, что означает «полый сосуд») для клеток, которые наблюдал Мечников.
Год спустя Мечников изучил пресноводного рачка по имени Дафния, крошечное прозрачное животное, которое может можно исследовать непосредственно под микроскопом. Он обнаружил, что споры грибов, атаковавшие животное, уничтожаются фагоцитами. Затем он расширил свои наблюдения на белые кровяные тельца млекопитающих и обнаружил, что бактерия Bacillus anthracis может поглощаться и уничтожаться фагоцитами, и этот процесс он назвал фагоцитозом.. Мечников предположил, что фагоциты являются основной защитой от вторгшихся организмов.
В 1903 году Альмрот Райт обнаружил, что фагоцитоз усиливается специфическими антителами, которые он назвал опсонинами., от греческого opson, «украшение или вкус». Мечников был удостоен (совместно с Полом Эрлихом ) Нобелевской премии по физиологии и медицине 1908 за свои работы по фагоцитам и фагоцитозу.
Хотя важность этих открытий медленно получил признание в начале двадцатого века, сложные отношения между фагоцитами и всеми другими компонентами иммунной системы не были известны до 1980-х годов.
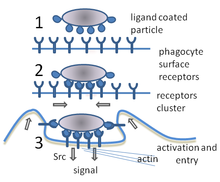 Фагоцитоз в три этапа: 1. Несвязанные поверхностные рецепторы фагоцитов не вызывают фагоцитоз. 2. Связывание рецепторов заставляет их группироваться. 3. Запускается фагоцитоз, и частица захватывается фагоцитом.
Фагоцитоз в три этапа: 1. Несвязанные поверхностные рецепторы фагоцитов не вызывают фагоцитоз. 2. Связывание рецепторов заставляет их группироваться. 3. Запускается фагоцитоз, и частица захватывается фагоцитом. Фагоцитоз - это процесс поглощения клеткой таких частиц, как бактерии, паразиты, мертвые клетки-хозяева, а также клеточный и чужеродный мусор.. Он включает в себя цепочку молекулярных процессов. Фагоцитоз возникает после того, как инородное тело, например, бактериальная клетка, связались с молекулами, называемыми «рецепторами», которые находятся на поверхности фагоцита. Затем фагоцит растягивается вокруг бактерии и поглощает ее. Фагоцитоз бактерий нейтрофилами человека занимает в среднем девять минут. Попав внутрь этого фагоцита, бактерия попадает в отсек, называемый фагосомой. В течение одной минуты фагосома сливается либо с лизосомой, либо с гранулой с образованием фаголизосомы. Затем бактерия подвергается воздействию огромного количества механизмов уничтожения и погибает через несколько минут. Дендритные клетки и макрофаги не так быстры, и фагоцитоз в этих клетках может занять много часов. Макрофаги едят медленно и неопрятно; они поглощают огромное количество материала и часто выделяют непереваренные вещества обратно в ткани. Этот мусор служит сигналом для набора большего количества фагоцитов из крови. У фагоцитов повышенный аппетит; ученые даже скармливали макрофагам железные опилки, а затем использовали небольшой магнит, чтобы отделить их от других клеток.
 У макрофагов есть особые рецепторы, которые усиливают фагоцитоз (не в масштабе)
У макрофагов есть особые рецепторы, которые усиливают фагоцитоз (не в масштабе) Фагоциты бывают разных типов рецепторов на его поверхности, которые используются для связывания материала. Они включают рецепторы опсонина, рецепторы скавенджеров и Toll-подобные рецепторы. Рецепторы опсонина увеличивают фагоцитоз бактерий, покрытых иммуноглобулином G (IgG) антителами или комплементом. «Комплемент» - это название сложной серии белковых молекул, обнаруженных в крови, которые разрушают клетки или маркируют их для разрушения. Рецепторы-скавенджеры связываются с широким спектром молекул на поверхности бактериальных клеток и Toll-подобными рецепторами - так называемыми из-за их сходства с хорошо изученными рецепторами у плодовых мушек, которые кодируются геном Toll - связываются с более конкретными молекулами. Связывание с Toll-подобными рецепторами увеличивает фагоцитоз и заставляет фагоцит высвобождать группу гормонов, вызывающих воспаление.
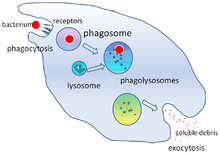 Упрощенная диаграмма фагоцитоза и разрушения бактериальной клетки
Упрощенная диаграмма фагоцитоза и разрушения бактериальной клетки Уничтожение микробы - критическая функция фагоцитов, которая осуществляется либо внутри фагоцита (внутриклеточное уничтожение), либо вне фагоцита (внеклеточное уничтожение).
Когда фагоцит поглощает бактерии (или любой материал), его потребление кислорода увеличивается. Увеличение потребления кислорода, называемое респираторным взрывом, производит химически активные кислородсодержащие молекулы, которые обладают антимикробным действием. Кислородные соединения токсичны как для захватчика, так и для самой клетки, поэтому они хранятся в отсеках внутри клетки. Этот метод уничтожения вторгшихся микробов с использованием реактивных кислородсодержащих молекул называется кислородозависимым внутриклеточным уничтожением, и существует два их типа.
Первый тип - это кислородозависимое производство супероксид, богатое кислородом вещество, убивающее бактерии. Супероксид превращается в пероксид водорода и синглетный кислород с помощью фермента, называемого супероксиддисмутазой. Супероксиды также реагируют с перекисью водорода с образованием гидроксильных радикалов, которые помогают убить вторгшегося микроба.
Второй тип включает использование фермента миелопероксидазы из нейтрофилов. гранулы. Когда гранулы сливаются с фагосомой, миелопероксидаза высвобождается в фаголизосому, и этот фермент использует перекись водорода и хлор для создания гипохлорита, вещества, используемого в бытовых отбеливателях. Гипохлорит чрезвычайно токсичен для бактерий. Миелопероксидаза содержит пигмент гем, который определяет зеленый цвет выделений, богатых нейтрофилами, таких как гной и инфицированная мокрота.
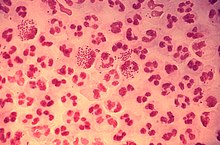 Микрофотография окрашенного по грамму гноя, показывающего бактерии Neisseria gonorrhoeae внутри фагоцитов и их относительные размеры
Микрофотография окрашенного по грамму гноя, показывающего бактерии Neisseria gonorrhoeae внутри фагоцитов и их относительные размеры Фагоциты также могут убивать микробы кислороднезависимыми методами, но это не так эффективны, как кислородзависимые. Есть четыре основных типа. Первый использует электрически заряженные белки, которые повреждают мембрану бактерии. Второй тип использует лизоцимы; эти ферменты разрушают бактериальную клеточную стенку. Третий тип использует лактоферрины, которые присутствуют в гранулах нейтрофилов и удаляют необходимое железо из бактерий. Четвертый тип использует протеазы и гидролитические ферменты ; эти ферменты используются для переваривания белков уничтоженных бактерий.
интерферон-гамма - который когда-то назывался фактором активации макрофагов - стимулирует макрофаги к выработке оксида азота. Источником гамма-интерферона могут быть Т-клетки CD4, Т-клетки CD8, естественные клетки-киллеры, В-клетки, естественные Т-клетки-киллеры, моноциты, макрофаги или дендритные клетки. Затем оксид азота высвобождается из макрофагов и из-за своей токсичности убивает микробы рядом с макрофагом. Активированные макрофаги продуцируют и секретируют фактор некроза опухоли. Этот цитокин - класс сигнальных молекул - убивает раковые клетки и клетки, инфицированные вирусами, и помогает активировать другие клетки иммунной системы.
При некоторых заболеваниях, например редких хроническая гранулематозная болезнь, снижается эффективность фагоцитов, возникают рецидивирующие бактериальные инфекции. При этом заболевании имеется аномалия, влияющая на различные элементы кислородзависимого уничтожения. Другие редкие врожденные аномалии, такие как синдром Чедиака-Хигаши, также связаны с неправильным уничтожением проглоченных микробов.
Вирусы могут воспроизводиться только внутри клеток, и они получить доступ за счет использования многих рецепторов, участвующих в иммунитете. Попав внутрь клетки, вирусы используют биологический механизм клетки в своих интересах, заставляя клетку создавать сотни идентичных копий самих себя. Хотя фагоциты и другие компоненты врожденной иммунной системы могут, в ограниченной степени, контролировать вирусы, как только вирус попадает в клетку, адаптивные иммунные ответы, в частности лимфоциты, становятся более важными для защиты. В очагах вирусных инфекций количество лимфоцитов часто значительно превышает количество всех других клеток иммунной системы; это обычное явление при вирусном менингите. Зараженные вирусом клетки, которые были убиты лимфоцитами, выводятся из организма фагоцитами.
 Апоптоз - фагоциты выводят из организма фрагменты мертвых клеток
Апоптоз - фагоциты выводят из организма фрагменты мертвых клеток У животных клетки подвергаются постоянно умирает. Баланс между делением и гибелью клеток сохраняет количество клеток относительно постоянным у взрослых. Есть два разных способа гибели клетки: некроз или апоптоз. В отличие от некроза, который часто возникает в результате болезни или травмы, апоптоз - или запрограммированная гибель клеток - является нормальной здоровой функцией клеток. Организм должен ежедневно избавляться от миллионов мертвых или умирающих клеток, и фагоциты играют решающую роль в этом процессе.
Умирающие клетки, которые проходят последние стадии апоптоза, отображают молекулы, такие как фосфатидилсерин, на их клеточной поверхности для привлечения фагоцитов. Фосфатидилсерин обычно находится на цитозольной поверхности плазматической мембраны, но во время апоптоза перераспределяется на внеклеточную поверхность с помощью белка, известного как скрамблаза. Эти молекулы маркируют клетку для фагоцитоза клетками, которые обладают соответствующими рецепторами, такими как макрофаги. Удаление умирающих клеток фагоцитами происходит упорядоченно, не вызывая воспалительной реакции, и является важной функцией фагоцитов.
Обычно фагоциты не связан с каким-либо конкретным органом, но перемещается по телу, взаимодействуя с другими фагоцитарными и нефагоцитарными клетками иммунной системы. Они могут связываться с другими клетками, производя химические вещества, называемые цитокинами, которые привлекают другие фагоциты к участку инфекции или стимулируют спящие лимфоциты. Фагоциты являются частью врожденной иммунной системы, с которой рождаются животные, в том числе люди. Врожденный иммунитет очень эффективен, но неспецифичен в том смысле, что он не делает различий между разными видами захватчиков. С другой стороны, адаптивная иммунная система челюстных позвоночных - основа приобретенного иммунитета - является высокоспециализированной и может защищать практически от любого типа захватчиков. Адаптивная иммунная система зависит не от фагоцитов, а от лимфоцитов, которые продуцируют защитные белки, называемые антителами, которые маркируют захватчиков для разрушения и предотвращают заражение клеток вирусами. Фагоциты, в частности дендритные клетки и макрофаги, стимулируют лимфоциты вырабатывать антитела с помощью важного процесса, называемого антиген презентация.
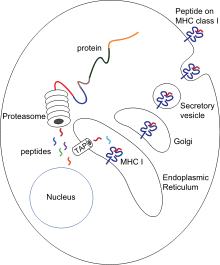 Схематическая диаграмма презентации чужеродных пептидов MHC 1 молекулы
Схематическая диаграмма презентации чужеродных пептидов MHC 1 молекулы Презентация антигена - это процесс, в котором некоторые фагоциты перемещают части поглощенных материалов обратно на поверхность своих клеток и «представляют» их другим клеткам иммунной системы. Есть две «профессиональные» антигенпрезентирующие клетки: макрофаги и дендритные клетки. После поглощения чужеродные белки (антигены ) расщепляются на пептиды внутри дендритных клеток и макрофагов. Эти пептиды затем связываются с гликопротеинами главного комплекса гистосовместимости (MHC) клетки, которые переносят пептиды обратно на поверхность фагоцита, где они могут быть «представлены» лимфоцитам. Зрелые макрофаги не перемещаются далеко от очага инфекции, но дендритные клетки могут достигать лимфатических узлов организма, где находятся миллионы лимфоцитов. Это повышает иммунитет, потому что лимфоциты реагируют на антигены, представленные дендритными клетками, точно так же, как и в месте первоначальной инфекции. Но дендритные клетки также могут разрушать или усмирять лимфоциты, если они распознают компоненты тела хозяина; это необходимо для предотвращения аутоиммунных реакций. Этот процесс называется толерантностью.
Дендритные клетки также способствуют иммунологической толерантности, которая не позволяет организму атаковать себя. Первый тип толерантности - это центральный допуск, который возникает в тимусе. Т-клетки, которые слишком сильно связываются (через свой Т-клеточный рецептор) с аутоантигеном (представленным дендритными клетками на молекулах MHC), вызывают гибель. Второй тип иммунологической толерантности - это периферическая толерантность. Некоторые аутореактивные Т-клетки покидают тимус по ряду причин, в основном из-за отсутствия экспрессии некоторых аутоантигенов в тимусе. Другой тип Т-лимфоцитов; Регуляторные Т-клетки могут подавлять регуляцию аутореактивных Т-клеток на периферии. Когда иммунологическая толерантность терпит неудачу, могут следовать аутоиммунные заболевания.
 Фагоциты происходят из стволовых клеток костного мозга
Фагоциты происходят из стволовых клеток костного мозга Фагоциты человека и других челюстных позвоночных делятся на: профессиональные и непрофессиональные группы, основанные на эффективности их участия в фагоцитозе. К профессиональным фагоцитам относятся моноциты, макрофаги, нейтрофилы, тканевые дендритные клетки и тучные клетки. Один литр человеческой крови содержит около шести миллиардов фагоцитов.
Все фагоциты, и особенно макрофаги, существуют в разной степени готовности. Макрофаги обычно относительно спящие в тканях и медленно размножаются. В этом состоянии полураспада они удаляют мертвые клетки-хозяева и другой неинфекционный мусор и редко принимают участие в презентации антигена. Но во время инфекции они получают химические сигналы - обычно гамма-интерферон - которые увеличивают выработку молекул MHC II и подготавливают их к презентации антигенов. В этом состоянии макрофаги являются хорошими презентаторами и убийцами антигенов. Однако, если они получают сигнал непосредственно от захватчика, они становятся «гиперактивированными», перестают размножаться и концентрируются на убийстве. Их размер и скорость фагоцитоза увеличиваются - некоторые становятся достаточно большими, чтобы поглотить вторгшиеся простейшие.
В крови нейтрофилы неактивны, но уносятся с большой скоростью. Когда они получают сигналы от макрофагов в местах воспаления, они замедляются и покидают кровь. В тканях они активируются цитокинами и прибывают на место сражения, готовые убить.
 Нейтрофилы перемещаются из крови к месту заражения
Нейтрофилы перемещаются из крови к месту заражения Когда происходит инфекция, химическое вещество » Выдается сигнал SOS для привлечения фагоцитов к участку. Эти химические сигналы могут включать белки от вторгшихся бактерий, пептиды системы свертывания , продукты комплемента и цитокины, которые выделяются макрофагами, расположенными в ткани около сайт заражения. Другой группой химических аттрактантов являются цитокины, которые привлекают нейтрофилы и моноциты из крови.
Чтобы достичь очага инфекции, фагоциты покидают кровоток и проникают в пораженные ткани. Сигналы от инфекции заставляют эндотелиальные клетки, выстилающие кровеносные сосуды, вырабатывать белок под названием селектин, к которому нейтрофилы прилипают, проходя мимо. Другие сигналы, называемые вазодилататорами, ослабляют соединения, соединяющие эндотелиальные клетки, позволяя фагоцитам проходить через стенку. Хемотаксис - это процесс, при котором фагоциты следуют по «запаху» цитокинов к инфицированному месту. Нейтрофилы перемещаются через эпителиальные выстланные клетками органы к участкам инфекции, и хотя это важный компонент борьбы с инфекцией, сама миграция может приводить к симптомам, напоминающим болезнь. Во время инфекции миллионы нейтрофилов привлекаются из крови, но они умирают через несколько дней.
 Моноциты в крови (окрашивание по Гимзе )
Моноциты в крови (окрашивание по Гимзе )Моноциты развиваются в костном мозге и достигают зрелости в крови. Зрелые моноциты имеют большие, гладкие, дольчатые ядра и обильную цитоплазму, содержащую гранулы. Моноциты поглощают чужеродные или опасные вещества и представляют антигены другим клеткам иммунной системы. Моноциты образуют две группы: циркулирующую группу и маргинальную группу, которые остаются в других тканях (примерно 70% находятся в маргинальной группе). Большинство моноцитов покидают кровоток через 20–40 часов и попадают в ткани и органы, и при этом превращаются в макрофаги или дендритные клетки в зависимости от сигналов, которые они получают. В одном литре крови человека содержится около 500 миллионов моноцитов.
Зрелые макрофаги не перемещаются далеко, но охраняют их участки тела, которые подвергаются воздействию побочный мир. Там они действуют как сборщики мусора, антигенпрезентирующие клетки или свирепые убийцы, в зависимости от получаемых сигналов. Они происходят из моноцитов, гранулоцитов стволовых клеток или клеточного деления уже существующих макрофагов. Макрофаги человека имеют диаметр около 21 микрометра.
 Гной, сочащийся из абсцесса, вызванного бактериями - гной содержит миллионы фагоцитов
Гной, сочащийся из абсцесса, вызванного бактериями - гной содержит миллионы фагоцитов Этот тип фагоцитов не содержит имеют гранулы, но содержат много лизосом. Макрофаги обнаруживаются по всему телу почти во всех тканях и органах (например, микроглиальные клетки в головном мозге и альвеолярные макрофаги в легких ), где они молча подстерегают. Расположение макрофага может определять его размер и внешний вид. Макрофаги вызывают воспаление за счет производства интерлейкина-1, интерлейкина-6 и TNF-альфа. Макрофаги обычно обнаруживаются только в тканях и редко встречаются в кровообращении. Продолжительность жизни тканевых макрофагов оценивается от четырех до пятнадцати дней.
Макрофаги могут активироваться для выполнения функций, которые не могут выполнять покоящиеся моноциты. Т-хелперные клетки (также известные как эффекторные Т-клетки или Т h клетки), подгруппа лимфоцитов, ответственны за активацию макрофагов. Клетки T h 1 активируют макрофаги, передавая сигнал с помощью IFN-гамма и отображая белок лиганд CD40. Другие сигналы включают TNF-альфа и липополисахариды из бактерий. Клетки T h 1 могут рекрутировать другие фагоциты на место инфекции несколькими способами. Они секретируют цитокины, которые действуют на костный мозг, чтобы стимулировать производство моноцитов и нейтрофилов, и они секретируют некоторые из цитокинов, которые отвечают за миграцию моноцитов и нейтрофилов из кровоток. Клетки T h 1 происходят в результате дифференцировки Т-клеток CD4, как только они ответили на антиген во вторичных лимфоидных тканях. Активированные макрофаги играют важную роль в разрушении опухоли, продуцируя TNF-альфа, IFN-гамма, оксид азота, реактивные кислородные соединения, катионные белки и гидролитические ферменты.
 Нейтрофилы с сегментированными ядрами, окруженными эритроцитами, внутриклеточные гранулы видны в цитоплазме (окрашенные по Гимзе )
Нейтрофилы с сегментированными ядрами, окруженными эритроцитами, внутриклеточные гранулы видны в цитоплазме (окрашенные по Гимзе )Нейтрофилы обычно обнаруживаются в кровоток и являются наиболее многочисленным типом фагоцитов, составляя от 50% до 60% от общего количества циркулирующих лейкоцитов. Один литр человеческой крови содержит около пяти миллиардов нейтрофилов, которые имеют диаметр около 10 микрометров и живут всего около пяти дней. После получения соответствующих сигналов им требуется около тридцати минут, чтобы покинуть кровь и достичь места заражения. Они свирепо едят и быстро поглощают захватчиков, покрытых антителами и комплемент, и поврежденные клетки или клеточный дебрис. Нейтрофилы d o не вернуться в кровь; они превращаются в гной клеток и умирают. Зрелые нейтрофилы меньше моноцитов и имеют сегментированное ядро с несколькими секциями; каждая секция соединена нитями хроматина - нейтрофилы могут иметь 2–5 сегментов. Нейтрофилы обычно не выходят из костного мозга до зрелости, но во время инфекции высвобождаются предшественники нейтрофилов, называемые миелоцитами и промиелоцитами.
Внутриклеточные гранулы нейтрофилов человека давно известны своими бактерицидными и разрушающими белки свойствами. Нейтрофилы могут выделять продукты, стимулирующие моноциты и макрофаги. Секреция нейтрофилов увеличивает фагоцитоз и образование активных кислородных соединений, участвующих во внутриклеточном убийстве. Секреции из первичных гранул нейтрофилов стимулируют фагоцитоз бактерий, покрытых IgG -антителами.
 Дендритные клетки
Дендритные клетки Дендритные клетки - это специализированные антигенпрезентирующие клетки, имеющие длинные выросты, называемые дендритами, которые помогают поглощать микробы и других захватчиков. Дендритные клетки присутствуют в тканях, которые контактируют с внешней средой, в основном с кожей, внутренней оболочкой носа, легких, желудка и кишечника. После активации они созревают и мигрируют в лимфоидные ткани, где они взаимодействуют с Т-клетками и В-клетками, чтобы инициировать и управлять адаптивным иммунным ответом. Зрелые дендритные клетки активируют Т-хелперные клетки и цитотоксические Т-клетки. Активированные хелперные Т-клетки взаимодействуют с макрофагами и В-клетками, активируя их по очереди. Кроме того, дендритные клетки могут влиять на тип производимого иммунного ответа; когда они перемещаются в лимфоидные области, где содержатся Т-клетки, они могут активировать Т-клетки, которые затем дифференцируются в цитотоксические Т-клетки или хелперные Т-клетки.
Тучные клетки имеют Toll-подобные рецепторы взаимодействуют с дендритными клетками, В-клетками и Т-клетками, помогая опосредовать адаптивные иммунные функции. Тучные клетки экспрессируют молекулы МНС класса II и могут участвовать в презентации антигена; однако роль тучных клеток в презентации антигена не очень хорошо изучена. Тучные клетки могут поглощать и убивать грамотрицательные бактерии (например, сальмонеллы ) и перерабатывать их антигены. Они специализируются на обработке фимбриальных белков на поверхности бактерий, которые участвуют в адгезии к тканям. В дополнение к этим функциям тучные клетки продуцируют цитокины, которые вызывают воспалительную реакцию. Это жизненно важная часть уничтожения микробов, потому что цитокины привлекают больше фагоцитов к месту инфекции.
| Основное местонахождение | Разнообразие фенотипов |
|---|---|
| Кровь | нейтрофилы, моноциты |
| костный мозг | макрофаги, моноциты, синусоидальные клетки, клетки выстилки |
| костная ткань | остеокласты |
| Кишечник и кишечник пейеровы пятна | макрофаги |
| соединительная ткань | гистиоциты, макрофаги, моноциты, дендритные клетки |
| печень | клетки Купфера, моноциты |
| легкие | самовоспроизводящиеся макрофаги, моноциты, тучные клетки, дендритные клетки |
| лимфоидная ткань | свободные и фиксированные макрофаги и моноциты, дендритные клетки |
| нервная ткань | микроглиальные клетки (CD4 ) |
| Селезенка | фиксированные макрофаги, моноциты, синусоидальные клетки |
| Тимус | фиксированные макрофаги и моноциты |
| Кожа | резидентные клетки Лангерганса, другое дендритные клетки, обычные макрофаги, тучные клетки |
Умирающие клетки и чужеродные организмы потребляются клетками, отличными от «профессиональных» фагоцитов. Эти клетки включают эпителиальные клетки, эндотелиальные клетки, фибробласты и мезенхимальные клетки. Их называют непрофессиональными фагоцитами, чтобы подчеркнуть, что, в отличие от профессиональных фагоцитов, фагоцитоз не является их основной функцией. Например, фибробласты, которые могут фагоцитировать коллаген в процессе преобразования шрамов, также предпримут некоторые попытки проглотить инородные частицы.
Непрофессиональные фагоциты более ограничены, чем профессиональные фагоциты, в типах частиц, которые они могут принимать вверх. Это связано с отсутствием у них эффективных фагоцитарных рецепторов, в частности, опсонинов, которые представляют собой антитела и комплемент, прикрепленные к захватчикам иммунной системой. Кроме того, большинство непрофессиональных фагоцитов не производят реактивные кислородсодержащие молекулы в ответ на фагоцитоз.
| Основное местонахождение | Разнообразие фенотипов |
|---|---|
| Кровь, лимфатические узлы и лимфатические узлы | Лимфоциты |
| Кровь, лимфатические и лимфатические узлы | NK и клетки LGL (большие гранулярные лимфоциты) |
| Кровь | Эозинофилы и Базофилы |
| Кожа | Эпителиальные клетки |
| Кровеносные сосуды | Эндотелиальные клетки |
| Соединительная ткань | Фибробласты |
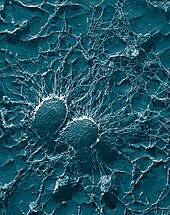 Клетки бактерий Staphylococcus aureus: большие волокнистые капсулы защищают организмы от нападения фагоцитов
Клетки бактерий Staphylococcus aureus: большие волокнистые капсулы защищают организмы от нападения фагоцитов Патоген может успешно заразить организм только в том случае, если он сможет преодолеть его защиту. Патогенные бактерии и простейшие разработали множество методов противостояния атакам фагоцитов, и многие из них действительно выживают и размножаются внутри фагоцитарных клеток.
Есть несколько способов, которыми бактерии избегают контакта с фагоцитами. Во-первых, они могут расти в местах, куда фагоциты не могут попасть (например, на поверхности неповрежденной кожи). Во-вторых, бактерии могут подавлять воспалительную реакцию ; без этого ответа на инфекцию фагоциты не могут ответить адекватно. В-третьих, некоторые виды бактерий могут подавлять способность фагоцитов перемещаться к месту инфекции, вмешиваясь в хемотаксис. В-четвертых, некоторые бактерии могут избегать контакта с фагоцитами, заставляя иммунную систему «думать», что бактерии «сами по себе». Treponema pallidum - бактерия, вызывающая сифилис - скрывается от фагоцитов, покрывая свою поверхность фибронектином, который естественным образом вырабатывается организмом и играет решающую роль в заживление ран.
Бактерии часто производят капсулы, состоящие из белков или сахаров, которые покрывают их клетки и препятствуют фагоцитозу. Некоторыми примерами являются капсула K5 и O75 O антиген, обнаруженные на поверхности Escherichia coli, и капсулы экзополисахарида Staphylococcus epidermidis. Streptococcus pneumoniae продуцирует несколько типов капсул, которые обеспечивают разные уровни защиты, а стрептококки группы A продуцируют белки, такие как M-белок и фимбриальные белки Чтобы заблокировать захват. Некоторые белки препятствуют приему пищи, связанной с опсонином; Staphylococcus aureus продуцирует белок A для блокирования рецепторов антител, что снижает эффективность опсонинов. Энтеропатогенные виды рода Yersinia связываются с использованием фактора вирулентности с рецепторами фагоцитов, от которых они влияют на способность клеток вызывать фагоцитоз.
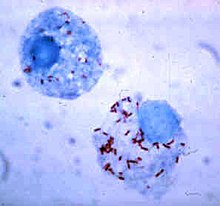 Rickettsia - маленькие бактерии - здесь окрашенные в красный цвет - которые растут в цитоплазме непрофессиональных фагоцитов.
Rickettsia - маленькие бактерии - здесь окрашенные в красный цвет - которые растут в цитоплазме непрофессиональных фагоцитов. Бактерии разработали способы выживания внутри фагоцитов, где они продолжают уклоняться от иммунной системы. Чтобы безопасно попасть внутрь фагоцита, они экспрессируют белки, называемые инвазинами. Находясь внутри клетки, они остаются в цитоплазме и избегают токсичных химических веществ, содержащихся в фаголизосомах. Некоторые бактерии препятствуют слиянию фагосомы и лизосомы с образованием фаголизосомы. Другие патогены, такие как Leishmania, создают сильно модифицированную вакуоль внутри фагоцита, которая помогает им сохраняться и воспроизводиться. Некоторые бактерии способны жить внутри фаголизосомы. Staphylococcus aureus, например, продуцирует ферменты каталазу и супероксиддисмутазу, которые расщепляют химические вещества, такие как перекись водорода, вырабатываемые фагоцитами для уничтожения бактерий. Бактерии могут ускользнуть из фагосомы до образования фаголизосомы: Listeria monocytogenes может проделывать отверстие в стенке фагосомы с помощью ферментов, называемых листериолизин O и фосфолипаза C.
Бактерии разработали несколько способов уничтожения фагоцитов. К ним относятся цитолизины, которые образуют поры в клеточных мембранах фагоцитов, стрептолизины и лейкоцидины, которые вызывают разрыв гранул нейтрофилов и выделение токсичных веществ, и экзотоксины, которые снижают снабжение фагоцитов АТФ, необходимых для фагоцитоза. После проглатывания бактерия может убить фагоцит, высвобождая токсины, которые проходят через фагосому или фаголизосомную мембрану, чтобы нацеливаться на другие части клетки.
Некоторые стратегии выживания часто включают нарушение цитокинов и другие методы клеточной передачи сигналов для предотвращения реакции фагоцита на инвазию. Простейшие паразиты Toxoplasma gondii, Trypanosoma cruzi и Leishmania заражают макрофаги, и каждый из них имеет уникальный способ приручить их. Некоторые виды Leishmania изменяют передачу сигналов инфицированного макрофага, подавляют выработку цитокинов и микробицидных молекул - оксида азота и активных форм кислорода - и ставят под угрозу презентацию антигена.
Макрофаги и нейтрофилы, в частности, играют центральную роль в воспалительном процессе, высвобождая белки и низкомолекулярные медиаторы воспаления, которые контролируют инфекцию, но могут повреждать ткань хозяина. В целом, фагоциты стремятся уничтожить патогены, поглощая их и подвергая их батарее токсичных химикатов внутри фаголизосомы. Если фагоциту не удается охватить свою цель, эти токсичные агенты могут высвобождаться в окружающую среду (действие, называемое «нарушенный фагоцитоз»). Поскольку эти агенты также токсичны для клеток-хозяев, они могут вызвать обширное повреждение здоровых клеток и тканей.
Когда нейтрофилы высвобождают свое гранулярное содержимое в почке, содержимое гранул (реактивное соединения кислорода и протеазы) разрушают внеклеточный матрикс клеток-хозяев и могут вызывать повреждение гломерулярных клеток, влияя на их способность фильтровать кровь и вызывая изменения в sh обезьяна. Кроме того, продукты фосфолипазы (например, лейкотриены ) усиливают повреждение. Это высвобождение веществ способствует хемотаксису большего количества нейтрофилов к месту инфекции, и клубочковые клетки могут быть повреждены молекулами адгезии во время миграции нейтрофилов. Повреждение клубочковых клеток может вызвать почечную недостаточность.
. Нейтрофилы также играют ключевую роль в развитии большинства форм острого повреждения легких. Здесь активированные нейтрофилы высвобождают содержимое своих токсичных гранул в среду легких. Эксперименты показали, что уменьшение количества нейтрофилов уменьшает последствия острого повреждения легких, но лечение путем ингибирования нейтрофилов не является клинически реалистичным, так как это сделает хозяина уязвимым для инфекции. В печени повреждение нейтрофилами может способствовать дисфункции и повреждению в ответ на высвобождение эндотоксинов, продуцируемых бактериями, сепсис, травмы, алкогольные гепатит, ишемия и гиповолемический шок в результате острого кровотечения.
Химические вещества, выделяемые макрофагами, также могут повреждать ткань хозяина. TNF-α - важное химическое вещество, которое выделяется макрофагами и вызывает свертывание крови в мелких сосудах, чтобы предотвратить распространение инфекции. Однако, если бактериальная инфекция распространяется в кровь, TNF-α высвобождается в жизненно важные органы, что может вызвать расширение сосудов и уменьшение объема плазмы ; за ними, в свою очередь, может последовать септический шок. Во время септического шока высвобождение TNF-α вызывает закупорку мелких сосудов, снабжающих кровью жизненно важные органы, и эти органы могут выйти из строя. Септический шок может привести к смерти.
Фагоцитоз является обычным явлением и, вероятно, появился на ранних этапах эволюции, сначала возник у одноклеточных эукариот. Амебы являются одноклеточными простейшими, которые отделились от дерева, ведущего к многоклеточным вскоре после расхождения растений, и они разделяют многие специфические функции с фагоцитарными клетками млекопитающих. Dictyostelium discoideum, например, это амеба, которая живет в почве и питается бактериями. Подобно фагоцитам животных, он поглощает бактерии путем фагоцитоза, главным образом через Toll-подобные рецепторы, и выполняет другие биологические функции, общие с макрофагами. Dictyostelium discoideum социальна; при голодании он агрегируется с образованием мигрирующего псевдоплазмодия или слизняка. Этот многоклеточный организм со временем будет производить плодовое тело с спорами, устойчивыми к опасностям окружающей среды. Перед формированием плодовых тел клетки будут мигрировать как слизняк в течение нескольких дней. В течение этого времени воздействие токсинов или бактериальных патогенов может поставить под угрозу выживание вида, ограничивая производство спор. Некоторые из амеб поглощают бактерии и поглощают токсины, циркулируя внутри слизняка, и в конечном итоге эти амебы умирают. Они генетически идентичны другим амебам в слизняке; их самопожертвование для защиты других амеб от бактерий похоже на самопожертвование фагоцитов, наблюдаемое в иммунной системе высших позвоночных. Эта древняя иммунная функция социальных амеб предполагает эволюционно законсервированный клеточный механизм кормодобывания, который мог быть адаптирован к защитным функциям задолго до диверсификации амеб в высшие формы. Фагоциты встречаются повсюду в животном мире, от морских губок до насекомых, низших и высших позвоночных. Способность амеб различать «я» и «не-я» является ключевой и лежит в основе иммунной системы многих видов амеб.
| Викискладе есть медиафайлы, связанные с фагоцитами. |