| Болезнь трансплантата против хозяина | |
|---|---|
| Специальность | Скорая помощь |
трансплантат против хозяина заболевание (GvHD ) - это синдром, характеризующийся воспалением в различных органах, со специфичностью апоптоза эпителиальных клеток и выпадением крипт. GvHD обычно ассоциируется с трансплантацией костного мозга и трансплантацией стволовых клеток. РТПХ также применяется к другим формам пересаженных тканей, таким как трансплантация твердых органов.
Белые кровяные тельца иммунной системы донора, которые остаются в донорской ткани (трансплантате), распознают реципиента (хозяина) как чужеродного (чужеродного). Лейкоциты, присутствующие в пересаженной ткани, затем атакуют клетки тела реципиента, что приводит к РТПХ. Это не следует путать с отторжением трансплантата, которое происходит, когда иммунная система реципиента трансплантата отторгает пересаженную ткань; GvHD возникает, когда лейкоциты иммунной системы донора отвергают реципиента. Основной принцип (аллоиммунитет ) тот же, но детали и курс могут отличаться. РТПХ может также возникнуть после переливания крови, если использованные продукты крови не были облучены или обработаны утвержденной системой уменьшения количества патогенов.
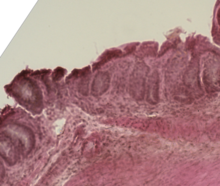 Толстая кишка мыши, пораженная острой реакцией трансплантат против хозяина.
Толстая кишка мыши, пораженная острой реакцией трансплантат против хозяина.  Микрофотографии степеней кожной болезни трансплантат против хозяина: от степени I GvHR (с минимальной вакуолизацией в эпидермисе) до степени GvHR II степени (с вакуолизацией и дискератозными телами) до GvHR III степени (с образованием субэпидермальной щели) и, наконец, GvHR IV степени (с отделением дермы от эпидермиса).
Микрофотографии степеней кожной болезни трансплантат против хозяина: от степени I GvHR (с минимальной вакуолизацией в эпидермисе) до степени GvHR II степени (с вакуолизацией и дискератозными телами) до GvHR III степени (с образованием субэпидермальной щели) и, наконец, GvHR IV степени (с отделением дермы от эпидермиса). В клинических условиях, трансплантат против хозяина -Заболевание делится на острую и хроническую формы и оценивается или классифицируется в зависимости от пораженной ткани и тяжести реакции.
В классическом варианте. Так, острая болезнь трансплантат против хозяина характеризуется избирательным повреждением печени, кожи (сыпь), слизистой оболочки и желудочно-кишечного тракта. тракт. Более новые исследования показывают, что другие органы-мишени реакции трансплантат против хозяина включают иммунную систему (кроветворная система, например, костный мозг и тимус ) собственно и легкие в форме иммуноопосредованного пневмонита. Биомаркеры могут использоваться для выявления конкретных причин РТПХ, таких как элафин в коже. Хроническая болезнь трансплантат против хозяина также поражает вышеуказанные органы, но при длительном течении может также вызывать повреждение соединительной ткани и экзокринных желез.
Повреждение слизистой оболочки влагалище может вызывать сильную боль и рубцевание и проявляется как при острой, так и при хронической РТПХ. Это может привести к невозможности полового акта.
Острая или молниеносная форма заболевания (aGvHD) обычно наблюдается в течение первых 10–100 дней после трансплантации и серьезная проблема для трансплантатов из-за связанной с ними заболеваемости и смертности. Примерно от одной трети до половины реципиентов аллогенных трансплантатов разовьется острая GVHD. Это реже встречается у молодых пациентов и у пациентов с более близкими человеческими лейкоцитарными антигенами (HLA). совпадения между донором и пациентом.
Первыми признаками обычно являются сыпь, жжение и покраснение кожи на ладонях и подошвах. Это может распространиться по всему телу. Другие симптомы могут включать тошноту, рвоту, спазмы желудка, диарею (водянистую и иногда кровянистую), потерю аппетита, желтуху, боль в животе и потерю веса.
Острая РТПХ ЖКТ может вызвать сильное воспаление кишечника, отслоение слизистой оболочки, сильную диарею, боль в животе, тошноту и рвоту. Обычно это диагностируется с помощью биопсии кишечника. РТПХ в печени измеряется уровнем билирубина у пациентов с острой болезнью. РТПХ кожи приводит к диффузной красной макулопапулезной сыпи, иногда с кружевным рисунком.
Острая РТПХ распределяется следующим образом: общая степень (кожа-печень-кишечник) для каждого органа индивидуально от 1 до 4. Пациенты с РТПХ IV степени обычно имеют плохой прогноз. Если GvHD тяжелая и требует интенсивной иммуносупрессии с участием стероидов и дополнительных агентов, чтобы обрести контроль, у пациента могут развиться тяжелые инфекции в результате иммуносупрессии и он может умереть от инфекции. Однако исследование 2016 года показало, что прогноз для пациентов с РТПХ IV степени улучшился в последние годы.
Хроническая форма болезни трансплантат против хозяина (ХРТПХ) обычно начинается От 90 до 600 дней после трансплантации. Появление умеренных и тяжелых случаев cGVHD отрицательно влияет на долгосрочную выживаемость.
Первым симптомом cGvHD обычно является сыпь на ладонях рук или подошвах ног, которая может распространяться и обычно зуд и сухость. В тяжелых случаях кожа может покрыться волдырями и шелушиться, как от сильного солнечного ожога. Также может развиться лихорадка. Другие симптомы хронической РТПХ могут включать:
В ротовой полости, хроническая болезнь трансплантат против хозяина проявляется как красный плоский лишай с более высоким риском злокачественной трансформации в плоскоклеточный рак полости рта по сравнению с классическим красным плоским лишаем полости рта. Связанный с заболеванием «трансплантат против хозяина» рак ротовой полости может иметь более агрессивное поведение с худшим прогнозом по сравнению с раком полости рта у пациентов, не перенесших трансплантацию гемопоэтических стволовых клеток.
 Патология РТПХ
Патология РТПХ Для возникновения РТПХ должны быть выполнены три критерия, известные как критерии Биллингема.
После трансплантации костного мозга, Т-клетки, присутствующие в трансплантате либо в виде контаминантов, либо намеренно введенные в организм хозяина, атакуют ткани реципиента трансплантата после того, как они воспринимают ткани хозяина как антигенно чужеродные. Т-клетки продуцируют избыток цитокинов, включая TNF-α и интерферон-гамма (IFNγ). Широкий спектр антигенов хозяина может инициировать болезнь «трансплантат против хозяина», в том числе человеческие лейкоцитарные антигены (HLA). Однако болезнь трансплантат против хозяина может возникать, даже если донорами являются HLA-идентичные братья и сестры. HLA-идентичные братья и сестры или HLA-идентичные неродственные доноры часто имеют генетически разные белки (называемые второстепенными антигенами гистосовместимости ), которые могут быть представлены большим комплексом гистосовместимости (MHC) молекулы Т-клеток донора, которые воспринимают эти антигены как чужеродные и поэтому вызывают иммунный ответ.
Антигены, наиболее ответственные за потерю трансплантата, - это HLA-DR (первые шесть месяцев), HLA-B (первые два года) и HLA-A (долгосрочное выживание).
Хотя донорские Т-клетки нежелательны в качестве эффекторных клеток трансплантата. болезнь против хозяина, они ценны для приживления, так как не позволяют остаточной иммунной системе реципиента отторгать трансплантат костного мозга (трансплантат против хозяина ). Кроме того, поскольку трансплантация костного мозга часто используется для лечения рака, в основном лейкемии, доказано, что донорские Т-клетки обладают ценным преимуществом в сравнении с опухолью, а не трансплантатом эффект. Большое количество текущих исследований аллогенной трансплантации костного мозга включает попытки отделить нежелательные аспекты болезни «трансплантат против хозяина» физиологии Т-клеток от желаемого эффекта трансплантат против опухоли.
Этот тип РТПХ связан с переливанием необлученной крови реципиентам с ослабленным иммунитетом. Это также может происходить в ситуациях, когда донор крови гомозиготен, а реципиент гетерозиготен по HLA гаплотипу. Это связано с более высокой смертностью (80–90%) из-за поражения лимфоидной ткани костного мозга, однако клинические проявления сходны с РТПХ в результате трансплантации костного мозга. РТПХ, связанная с переливанием крови, в современной медицине встречается редко. Его почти полностью можно предотвратить контролируемым облучением продуктов крови для инактивации лейкоцитов (включая лимфоциты) внутри.
Трансплантация тимуса может вызвать особый тип РТПХ, потому что тимоциты реципиента будут использовать донорские клетки тимуса в качестве моделей при прохождении отрицательной селекции для распознавания аутоантигенов и, следовательно, могут ошибочно принимать собственные структуры в остальной части тело для несамостоятельности. Это скорее непрямой РТПХ, потому что ее вызывают не клетки самого трансплантата, а клетки трансплантата, которые заставляют Т-клетки реципиента действовать как донорские Т-клетки. Это можно рассматривать как многоорганный аутоиммунитет в экспериментах по ксенотрансплантации вилочковой железы между разными видами. Аутоиммунное заболевание - частое осложнение после трансплантации аллогенного тимуса человека, обнаруженное у 42% пациентов в течение 1 года после трансплантации. Однако это частично объясняется тем, что само указание, то есть полный синдром ДиДжорджи, увеличивает риск аутоиммунного заболевания.
РТПХ-подобное заболевание, называемое полиорганный аутоиммунитет, связанный с тимомой (ТАМА), может возникать у пациентов с тимомой. У этих пациентов, а не донор, являющийся источником патогенных Т-клеток, собственный злокачественный тимус пациента производит самонаправляемые Т-клетки. Это связано с тем, что злокачественный тимус неспособен должным образом обучать развивающиеся тимоциты устранению аутореактивных Т-клеток. Конечным результатом является заболевание, практически неотличимое от РТПХ.
Патофизиология РТПХ включает три фазы:
Активация APC происходит на первой стадии РТПХ. Перед трансплантацией гемопоэтических стволовых клеток, лучевая или химиотерапия приводит к повреждению и активации тканей хозяина, особенно слизистой оболочки кишечника. Это позволяет микробным продуктам проникать и стимулировать провоспалительные цитокины, такие как IL-1 и TNF-α Эти провоспалительные цитокины увеличивают экспрессию MHC и молекул адгезии на APC, тем самым увеличивая способность APC представлять антиген. Вторая фаза характеризуется активацией эффекторных клеток. Активация донорских Т-клеток дополнительно усиливает экспрессию MH. C и молекулы адгезии, хемокины и рост CD8 + и CD4 + T-клеток и гостевых B-клеток. На заключительном этапе эти эффекторные клетки мигрируют к органам-мишеням и опосредуют повреждение тканей, что приводит к полиорганной недостаточности.
Внутривенное введение глюкокортикоидов, например как преднизон, являются стандартом лечения острой РТПХ и хронической РТПХ. Использование этих глюкокортикоидов предназначено для подавления опосредованного Т-клетками иммунного натиска на ткани хозяина; однако в высоких дозах это подавление иммунитета повышает риск инфекций и рецидива рака. Следовательно, желательно снизить дозировку стероидов высокого уровня после трансплантации до более низких уровней, в этот момент может приветствоваться появление легкой РТПХ, особенно у пациентов с несоответствием HLA, поскольку она обычно связана с трансплантатом. противоопухолевый эффект. Циклоспорин и такролимус являются ингибиторами кальциневрина. Оба вещества различаются по структуре, но имеют одинаковый механизм действия. Циклоспорин связывается с цитозольным белком пептидил-пролил цис-транс-изомеразой А (известной как циклофилин), а такролимус связывается с цитозольным белком пептидил-пролил цис-транс-изомеразой FKBP12. Эти комплексы ингибируют кальциневрин, блокируют дефосфорилирование фактора транскрипции NFAT активированных Т-клеток и его транслокацию в ядро. Стандартная профилактика предполагает прием циклоспорина в течение шести месяцев с метотрексатом. Уровень циклоспорина должен быть выше 200 нг / мл. Другие вещества, которые были изучены для лечения РТПХ, включают, например: сиролимус, пентостатин, этанерцепт и алемтузумаб.
В августе 2017 г. FDA одобрило ибрутиниб для лечения хронической GvHD после неэффективности одного или нескольких других системных методов лечения.
Существует большое количество продолжающиеся или недавно завершенные клинические испытания по изучению лечения и профилактики болезни «трансплантат против хозяина».
17 мая 2012 года Osiris Therapeutics объявила, что канадские регулирующие органы здравоохранения одобрили Prochymal, препарат для лечения острой реакции «трансплантат против хозяина» у детей, не ответивших на лечение стероидами. Prochymal - это первый препарат на основе стволовых клеток, одобренный для лечения системного заболевания.
В январе 2016 года Mesoblast опубликовал результаты клинического исследования фазы 2 с участием 241 ребенка с острым заболеванием. Болезнь трансплантат против хозяина, не поддающаяся лечению стероидами. Испытание проводилось на основе терапии мезенхимальными стволовыми клетками, известной как MSC-100-IV. Выживаемость составила 82% (против 39% в контрольной группе) для тех, кто показал некоторое улучшение через 1 месяц, и в долгосрочной перспективе 72% (против 18% в контроле) для тех, кто показал незначительный эффект через 1 месяц.
Реакция «трансплантат против хозяина» способствовала устранению нескольких случаев ВИЧ, в том числе Берлинского пациента и 6 других в Испании.
| Классификация | D |
|---|---|
| Внешние ресурсы |