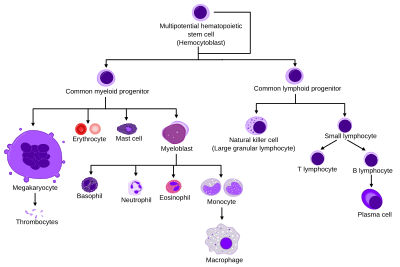
 Диаграмма, показывающая развитие различных клеток крови от гемопоэтических стволовых клеток до зрелых клеток
Диаграмма, показывающая развитие различных клеток крови от гемопоэтических стволовых клеток до зрелых клеток Гематопоэз (, от греческого αἷμα, «кровь» и ποιεῖν «производить»; также гематопоэз в американском Английский; иногда также h (a) emopoiesis ) - это образование крови клеточных компонентов. Все клеточные компоненты крови происходят из гемопоэтических стволовых клеток. У здорового взрослого человека ежедневно вырабатывается примерно 10–10 новых клеток крови для поддержания стабильного уровня в периферическом кровообращении.
Гематопоэтические стволовые клетки (HSC) находятся в мозговом веществе кости (костный мозг ) и обладают уникальной способностью давать начало всем различным типам зрелых клеток крови и тканям. HSC - это самообновляющиеся клетки: когда они дифференцируются, по крайней мере некоторые из их дочерних клеток остаются в виде HSC, поэтому пул стволовых клеток не истощается. Это явление называется асимметричным делением. Другие дочерние клетки HSC (миелоидные и лимфоидные клетки-предшественники) могут следовать любым другим путям дифференцировки, которые приводят к продукции одного или нескольких конкретных типов клеток крови, но не могут обновляться. самих себя. Пул предшественников неоднороден и может быть разделен на две группы; длительные самообновляющиеся HSC и только временно самообновляющиеся HSC, также называемые краткосрочными. Это один из основных жизненно важных процессов в организме.
Все клетки крови делятся на три линии.
Гранулопоэз (или гранулоцитопоэз) - гемопоэз гранулоцитов, за исключением тучных клеток, которые являются гранулоцитами, но с экстрамедуллярным созреванием.
Мегакариоцитопоэз - гематопоэз мегакариоцитов.
Между 1948 и 1950 годами Комитет по уточнению номенклатуры клеток и заболеваний крови и кроветворных органов опубликовал отчеты по номенклатуре клеток крови. Обзор терминологии показан ниже, от самой ранней до последней стадии разработки:
Корнем для колониеобразующих единиц эритроцитов (КОЕ-Е) является «рубри», для колониеобразующих единиц гранулоцит-моноцит (КОЕ-ГМ) «грануло» или «миело» и «моно», для колониеобразующих единиц лимфоцитов (КОЕ-Л) - это «лимфо», а для колониеобразующих единиц мегакариоцитов (КОЕ-мег) - «мегакарио». Согласно этой терминологии, этапами образования эритроцитов могут быть: рубрибласт, прорубрицит, рубрицит, метарубрицит и эритроцит. Однако в настоящее время наиболее распространенной является следующая номенклатура:
| Committee | "lympho" | "rubri" | «granulo» или «myelo « | « моно » | « мегакарио » |
|---|---|---|---|---|---|
| Линия | Лимфоид | Миелоид | Миелоид | Миелоид | Миелоид |
| КОЕ | КОЕ-L | КОЕ-GEMM → КОЕ-E | КОЕ-GEMM → КОЕ-GM → КОЕ-G | КОЕ-ГЭММ → КОЕ-ГМ → КОЕ-М | КОЕ-GEMM → КОЕ-мег |
| Процесс | лимфоцитопоэз | эритропоэз | гранулоцитопоэз | моноцитопоэз | тромбоцитопоэз |
| [корневой] бласт | Лимфобласт | Проэритробласт | Миелобласт | Монобласт | Мегакариобласт |
| про [корневой] цит | Пролимфо Полихроматофильный эритроцит | Промиелоцит | Промоноцит | Промегакариоцит | |
| [корневой] цит | – | Нормобласт | Эозино / нейтро / базофильный миелоцит | Мегакарио | |
| мета [корень ]цит | Большой лимфоцит | ретикулоцит | эозинофильный / нейтрофильный / базофильный метамиелоцит, эозинофил ic / нейтрофильные / базофильные полосовые клетки | - | |
| название зрелой клетки | маленькие лимфоциты | эритроциты | гранулоциты (эозино / нейтро / базофилы ) | Моноциты | тромбоциты (Тромбоциты ) |
Остеокласты также возникают из гемопоэтических клеток линии моноцитов / нейтрофилов, в частности CFU-GM.
 Участки кроветворения (человеческие) в пре- и постнатальный периоды
Участки кроветворения (человеческие) в пре- и постнатальный периоды В развивающихся эмбрионах кроветворение происходит в скоплениях клеток крови в желточном мешке, называемых островками крови. По мере развития происходит кроветворение в селезенке, печени и лимфатических узлах. Когда костный мозг развивается, он в конечном итоге берет на себя задачу формирования большей части клеток крови для всего организма. Однако созревание, активация и некоторая пролиферация лимфоидных клеток происходит в селезенке, тимусе и лимфатических узлах. У детей гемопоэз происходит в костном мозге длинных костей, таких как бедренная и большеберцовая кость. У взрослых это происходит в основном в области таза, черепа, позвонков и грудины.
В некоторых случаях печень, тимус и селезенка могут возобновить свою кроветворную функцию, если это необходимо. Это называется экстрамедуллярным кроветворением. Это может привести к значительному увеличению размеров этих органов. Во время внутриутробного развития, поскольку кости и, следовательно, костный мозг развиваются позже, печень функционирует как главный кроветворный орган. Следовательно, в процессе развития печень увеличивается. Экстрамедуллярный гемопоэз и миелопоэз могут поставлять лейкоциты при сердечно-сосудистых заболеваниях и воспаление в зрелом возрасте. Селезенки макрофаги и молекулы адгезии могут участвовать в регуляции образования экстрамедуллярных миелоидных клеток при сердечно-сосудистых заболеваниях.
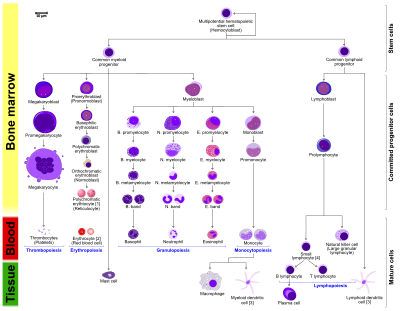 Более подробная и полная диаграмма, показывающая развитие различные клетки крови у людей.
Более подробная и полная диаграмма, показывающая развитие различные клетки крови у людей. По мере созревания стволовых клеток происходит изменение экспрессии генов, которые ограничивают типы клеток, которые они могут становится и приближает его к определенному типу клеток (дифференцировка клеток ). Эти изменения часто можно отследить, наблюдая за присутствием белков на поверхности клетки. Каждое последующее изменение приближает ячейку к окончательному типу ячейки и дополнительно ограничивает ее потенциал, чтобы стать ячейкой другого типа.
Были предложены две модели гематопоэза: детерминизм и стохастическая теория. Для стволовых клеток и других недифференцированных клеток крови в костном мозге определение обычно объясняется теорией детерминизма гемопоэза, согласно которой колониестимулирующие факторы и другие факторы гемопоэтического микроокружения определяют, что клетки следует определенному пути клеточной дифференцировки. Это классический способ описания кроветворения. В стохастической теории недифференцированные клетки крови дифференцируются от определенных типов клеток случайным образом. Эта теория была подтверждена экспериментами, показывающими, что в популяции гематопоэтических клеток-предшественников мыши лежащая в основе стохастическая изменчивость в распределении Sca-1, фактора стволовых клеток, подразделяет популяцию на группы, демонстрирующие переменную скорость клеточной дифференцировки. Например, под влиянием эритропоэтина (фактор дифференцировки эритроцитов) субпопуляция клеток (определяемая уровнями Sca-1) дифференцировалась в эритроциты с семикратным увеличением скорость, чем остальное население. Кроме того, было показано, что если дать возможность расти, эта субпопуляция восстановит исходную субпопуляцию клеток, подтверждая теорию о том, что это случайный обратимый процесс. Еще один уровень, на котором может быть важна стохастичность, - это процесс апоптоза и самообновления. В этом случае гемопоэтическое микроокружение преобладает над тем, чтобы некоторые клетки выживали, а некоторые, с другой стороны, выполняли апоптоз и погибали. Регулируя этот баланс между разными типами клеток, костный мозг может изменять количество различных клеток, которые в конечном итоге будут продуцированы.
 Диаграмма, включающая некоторые важные цитокины, которые определяют, какой тип клеток крови будет быть создан. SCF = Фактор стволовых клеток ; Tpo = тромбопоэтин ; IL = интерлейкин ; GM-CSF = фактор, стимулирующий колонии гранулоцитов и макрофагов ; Эпо = Эритропоэтин ; M-CSF = фактор, стимулирующий колонии макрофагов ; G-CSF = гранулоцитарный колониестимулирующий фактор ; SDF-1 = фактор-1, происходящий из стромальных клеток ; Лиганд FLT-3 = FMS-подобный лиганд тирозинкиназы 3; TNF-a = фактор некроза опухоли-альфа ; TGFβ = Трансформирующий фактор роста бета
Диаграмма, включающая некоторые важные цитокины, которые определяют, какой тип клеток крови будет быть создан. SCF = Фактор стволовых клеток ; Tpo = тромбопоэтин ; IL = интерлейкин ; GM-CSF = фактор, стимулирующий колонии гранулоцитов и макрофагов ; Эпо = Эритропоэтин ; M-CSF = фактор, стимулирующий колонии макрофагов ; G-CSF = гранулоцитарный колониестимулирующий фактор ; SDF-1 = фактор-1, происходящий из стромальных клеток ; Лиганд FLT-3 = FMS-подобный лиганд тирозинкиназы 3; TNF-a = фактор некроза опухоли-альфа ; TGFβ = Трансформирующий фактор роста бета Продукция красных и белых кровяных телец регулируется с большой точностью у здоровых людей, и продукция лейкоцитов быстро увеличивается во время инфекции. Размножение и самообновление этих клеток зависят от факторов роста. Одним из ключевых игроков в самообновлении и развитии гемопоэтических клеток является фактор стволовых клеток (SCF), который связывается с рецептором c-kit на HSC. Отсутствие SCF смертельно. Существуют и другие важные факторы роста гликопротеина, которые регулируют пролиферацию и созревание, такие как интерлейкины IL-2, IL-3, ИЛ-6, ИЛ-7. Другие факторы, называемые колониестимулирующими факторами (CSF), специфически стимулируют продукцию коммитированных клеток. Три CSF представляют собой CSF гранулоцитов-макрофагов (GM-CSF), CSF гранулоцитов (G-CSF) и CSF макрофагов (M-CSF). Они стимулируют образование гранулоцитов и активны либо на клетках-предшественниках, либо на клетках конечных продуктов.
Эритропоэтин необходим для того, чтобы миелоидная клетка-предшественник стала эритроцитом. С другой стороны, тромбопоэтин заставляет миелоидные клетки-предшественники дифференцироваться в мегакариоциты (тромбоциты -образующие клетки). На диаграмме справа представлены примеры цитокинов и дифференцированных клеток крови, которые они вызывают.
Факторы роста инициируют пути передачи сигнала, которые приводят к активации факторов транскрипции. Факторы роста вызывают разные результаты в зависимости от комбинации факторов и стадии дифференцировки клетки. Например, долговременная экспрессия PU.1 приводит к приверженности миелоиду, а кратковременная индукция активности PU.1 приводит к образованию незрелых эозинофилов. Недавно было сообщено, что факторы транскрипции, такие как NF-κB, могут регулироваться микроРНК (например, miR-125b) в гемопоэзе.
Первый ключевой игрок дифференциации от HSC до мультипотентного предшественника (MPP) является фактор транскрипции CCAAT-энхансер, связывающий белок α (C / EBP α). Мутации в C / EBPα связаны с острым миелоидным лейкозом. С этого момента клетки могут дифференцироваться либо по линии эритроид-мегакариоцитов, либо по лимфоидной и миелоидной клонам, которые имеют общего предшественника, называемого мультипотентным предшественником с лимфоидным примированием. Есть два основных фактора транскрипции. PU.1 для происхождения эритроид-мегакариоцитов и GATA-1, который приводит к лимфоидно-примированному мультипотентному предшественнику.
Другие факторы транскрипции включают Ikaros (B-клеточное развитие) и Gfi1 (способствует развитию Tdiv class="ht" и ингибирует Th1) или IRF8 (базофилы и тучные клетки ). Важно отметить, что определенные факторы вызывают разные ответы на разных этапах гематопоэза. Например, CEBPα в развитии нейтрофилов или PU.1 в развитии моноцитов и дендритных клеток. Важно отметить, что процессы не являются однонаправленными: дифференцированные клетки могут восстанавливать атрибуты клеток-предшественников.
Примером является фактор PAX5, который важен для развития В-клеток и связан с лимфомами. Неожиданно оказалось, что мыши с условным нокаутом pax5 позволили периферическим зрелым В-клеткам дедифференцироваться до ранних предшественников костного мозга. Эти данные показывают, что факторы транскрипции действуют как контролеры уровня дифференцировки, а не только как инициаторы.
Мутации в факторах транскрипции тесно связаны с раком крови, как острый миелоидный лейкоз (AML) или острый лимфобластный лейкоз (ОЛЛ). Например, известно, что Икарос является регулятором множества биологических событий. У мышей без Ikaros отсутствуют В-клетки, естественные киллеры и Т-клетки. Икарос имеет шесть доменов цинковых пальцев, четыре из которых представляют собой консервативный ДНК-связывающий домен и два предназначены для димеризации. Очень важным открытием является то, что разные цинковые пальцы участвуют в связывании с разными участками ДНК, и это является причиной плейотропного эффекта Икароса и различного вовлечения в рак, но в основном это мутации, связанные с BCR-Abl пациентами. и это плохой прогностический маркер.
У некоторых позвоночных гематопоэз может возникать везде, где имеется рыхлая строма соединительной ткани и медленное кровоснабжение, например, кишечник, селезенка или почка.