 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Prograf, Advagraf, Protopic, другие |
| Другие названия | FK-506, фуджимицин |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a601117 |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы. введения | Актуальные, перорально, внутривенно (IV) |
| код ATC | |
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные данные | |
| Биодоступность | 24% (5–67%), меньше после употребление пищи, богатой жирами |
| Связывание с белками | ≥98,8% |
| Метаболизм | Печень CYP3A4, CYP3A5 |
| Период полувыведения | 11,3 часа для трансплантации пациенты (диапазон 3,5–40,6 ч) |
| Экскреция | В основном фекалии |
| Идентификаторы | |
Название IUPAC
| |
| Номер CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| лиганд PDB | |
| Панель управления CompTox (EPA ) | |
| ECHA InfoCard | 100.155.367 |
| Химические и физические данные | |
| Формула | C44H69NO12 |
| Молярная масса | 804,018 г · моль |
| 3D модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
| (что это?) | |
Такролимус, продается под торговыми марками Protopic и Prograf среди прочих является иммунодепрессивным препаратом. Он используется после аллогенной трансплантации органа для снижения риска отторжения органа , а также в качестве местного лекарства при лечении T -клеточно-опосредованные заболевания, такие как экзема и псориаз. Его также применяли при тяжелом рефрактерном увеите после трансплантации костного мозга, обострениях болезни минимальных изменений, болезни Кимуры и кожных заболеваниях витилиго, и он используется для лечения синдрома сухого глаза у кошек и собак.
Такролимус ингибирует кальциневрин, который участвует в производстве интерлейкин-2, молекула, которая способствует развитию и пролиферации Т-клеток как часть усвоенных организмом (или адаптивный ) иммунный ответ.
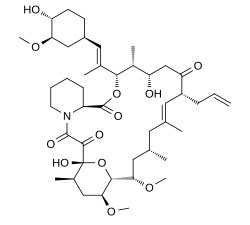
С химической точки зрения это макролид лактон, который был впервые обнаружен в 1987 году из ферментационного бульона японской почвы образец, содержащий бактерию Streptomyces tsukubaensis.
Он имеет иммунодепрессивные свойства, аналогичные циклоспорину, но гораздо более эффективен. В одном исследовании иммуносупрессия с помощью такролимуса была связана со значительно более низким уровнем острого отторжения по сравнению с иммуносупрессией на основе циклоспорина (30,7% против 46,4%). Клинические результаты лучше при применении такролимуса, чем при применении циклоспорина в течение первого года трансплантации печени. Долгосрочный результат не улучшился в той же степени. Такролимус обычно назначают как часть посттрансплантационного коктейля, включающего стероиды, микофенолят и ингибиторы рецептора IL-2, такие как базиликсимаб. Дозировки титруются до целевого уровня в крови.
В последние годы такролимус использовался для подавления воспаления, связанного с язвенным колитом (ЯК), формой воспалительного заболевания кишечника. Хотя такролимус используется почти исключительно в клинических случаях, он показал значительную эффективность в подавлении обострения ЯК.
 0,1% мазь такролимуса
0,1% мазь такролимуса В качестве мази, такролимус используется для лечения экземы, в частности атопического дерматита. Он подавляет воспаление так же, как стероиды, и столь же эффективен, как и стероид средней активности. Важным преимуществом такролимуса является то, что, в отличие от стероидов, он не вызывает истончения кожи (атрофия ) или других побочных эффектов, связанных со стероидами.
Его наносят на активные поражения до тех пор, пока они не заживут. выключено, но также можно использовать постоянно в низких дозах (два раза в неделю) и наносить на более тонкую кожу лица и век. Клинические испытания продолжительностью до одного года не проводились. В последнее время его также использовали для лечения сегментарного витилиго у детей, особенно на участках лица.
Волчаночный нефрит
Было показано, что такролимус снижает риск серьезной инфекции, а также увеличивает ремиссию почек. при волчаночном нефрите
Противопоказания и меры предосторожности включают:
Побочные эффекты могут быть серьезными и включать инфекцию, повреждение сердца, гипертензию, нечеткость зрения, печень и почка пр проблемы (такролимус нефротоксичность ), гиперкалиемия, гипомагниемия, гипергликемия, сахарный диабет, зуд, повреждение легких (сиролимус также вызывает повреждение легких) и различные нейропсихиатрические проблемы, такие как потеря аппетита, бессонница, синдром задней обратимой энцефалопатии, спутанность сознания, слабость, депрессия, яркие кошмары, судороги, невропатия, судороги, тремор и кататония.
. Кроме того, это может потенциально увеличить тяжесть существующих грибковых или инфекционных состояний такие как опоясывающий герпес или полиома вирусные инфекции.
У людей, получающих иммунодепрессанты для уменьшения отторжения трансплантата, повышается риск злокачественная опухоль (рак) - признанное осложнение. Наиболее распространенными видами рака являются неходжкинская лимфома и рак кожи. Риск, по-видимому, связан с интенсивностью и продолжительностью лечения.
Наиболее частые побочные эффекты, связанные с использованием мазей такролимуса для местного применения, особенно при использовании на большой площади, включают ощущение жжения или зуда при первоначальном применении с повышенной чувствительностью к солнечному свету и теплу на пораженные участки. Реже встречаются гриппоподобные симптомы, головная боль, кашель и жжение в глазах.
Такролимус и родственный препарат от экземы (пимекролимус ) подозревались в риске возникновения рака, хотя этот вопрос до сих пор вызывает споры. В марте 2005 г. FDA выпустило предупреждение о вреде для здоровья в отношении препарата, основанное на моделях на животных и небольшом количестве пациентов. Пока дальнейшие исследования на людях не дадут более убедительных результатов, FDA рекомендует информировать пользователей о потенциальных рисках. Однако текущая практика дерматологов Великобритании не считает это серьезной проблемой, и они все чаще рекомендуют использование этих новых препаратов.
Также как циклоспорин, он имеет широкий спектр взаимодействий. Такролимус в основном метаболизируется системой цитохрома P450 ферментов печени, и существует множество веществ, которые взаимодействуют с этой системой и вызывают или ингибируют метаболическую активность системы.
Взаимодействия включают взаимодействие с грейпфрут, который увеличивает концентрацию такролимуса в плазме. Поскольку инфекции являются основной причиной заболеваемости и смертности у пациентов после трансплантации, наиболее часто сообщаемые взаимодействия включают взаимодействие с антимикробными препаратами. Макролидные антибиотики, включая эритромицин и кларитромицин, а также несколько новых классов противогрибковых средств, особенно класса азолов (флуконазол, вориконазол ), повышают уровень такролимуса, конкурируя за ферменты цитохрома.
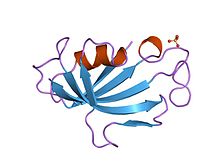 FKBP12, целевой белок такролимуса
FKBP12, целевой белок такролимуса Такролимус является макролид ингибитор кальциневрина. В Т-клетках активация рецептора Т-клеток обычно увеличивает внутриклеточный кальций, который действует через кальмодулин, активируя кальциневрин. Затем кальциневрин дефосфорилирует фактор транскрипции ядерный фактор активированных Т-клеток (NF-AT), который перемещается в ядро Т-клетки и увеличивает активность генов, кодирующих IL-2 и родственные цитокины. Такролимус предотвращает дефосфорилирование NF-AT.
В частности, такролимус снижает активность пептидилпролилизомеразы путем связывания с иммунофилином FKBP12 (связывающий белок FK506), создавая новый сложный. Этот комплекс FKBP12-FK506 взаимодействует с кальциневрином и ингибирует его, таким образом подавляя как передачу сигнала Т- лимфоцитов, так и транскрипцию IL-2. Хотя эта активность аналогична активности циклоспорина, частота острого отторжения снижается при использовании такролимуса по сравнению с использованием циклоспорина. Хотя краткосрочная иммуносупрессия в отношении выживаемости пациента и трансплантата, как обнаружено, одинакова для двух препаратов, такролимус приводит к более благоприятному липидному профилю, и это может иметь важные долгосрочные последствия, учитывая прогностическое влияние отторжения на выживаемость трансплантата.
Такролимус при пероральном введении медленно всасывается в желудочно-кишечном тракте с общей биодоступностью от 20 до 25% (но с вариациями от 5 до 67). %) и максимальная концентрация в плазме крови (C макс) достигается через один-три часа. Прием препарата вместе с едой, особенно богатой жирами, замедляет резорбцию и снижает биодоступность. В крови такролимус в основном связывается с эритроцитами ; только 5% обнаруживаются в плазме, из которых более 98,8% связаны с белками плазмы.
. Вещество метаболизируется в печени, в основном через CYP3A, и в стенке кишечника. Все метаболиты, обнаруженные в кровотоке, неактивны. Биологический период полувыведения широко варьирует и, по-видимому, выше у здоровых людей (в среднем 43 часа), чем у пациентов с трансплантатами печени (12 часов) или почек (16 часов), из-за различий в оформление. Такролимус выводится преимущественно с фекалиями в виде его метаболитов.
При местном применении при экземе такролимус практически не имеет биодоступности.
Преобладающий фермент, ответственный за метаболизм такролимуса - CYP3A5. Генетические вариации внутри CYP3A5, которые приводят к изменениям активности белка CYP3A5, могут влиять на концентрацию такролимуса в организме. В частности, люди, которые гомозиготны по аллелю G по однонуклеотидному полиморфизму (SNP) rs776746 (также известному как CYP3A5 * 3 / * 3), имеют нефункциональный белок CYP3A5. Частота аллеля G варьируется во всем мире: от 4% в некоторых африканских популяциях до 80–90% в кавказских популяциях. В большом количестве исследований было показано, что люди, гомозиготные по аллелю G, имеют более высокие концентрации такролимуса и требуют более низких доз препарата, чем люди, не гомозиготные по аллелю G. Достижение целевых концентраций такролимуса важно - если уровни слишком низкие, существует риск отторжения трансплантата, если уровни слишком высоки, существует риск токсичности лекарства. Имеются данные, позволяющие предположить, что дозирование пациентам на основе rs776746 генотипа может привести к более быстрому и более частому достижению целевых уровней такролимуса. Однако отсутствуют убедительные доказательства того, приводит ли дозирование, основанное на генотипе rs776746, к улучшению клинических результатов (например, снижению риска отторжения трансплантата или токсичности лекарств), вероятно, потому что пациенты, принимающие такролимус, подлежат терапевтическому мониторингу лекарственных препаратов..
Исследования показали, что генетический полиморфизм генов, отличных от CYP3A5, таких как NR1I2 (кодирующий PXR ), также значительно влияет на фармакокинетику такролимуса.
Такролимус был открыт в 1987 году; он был одним из первых открытых макролидных иммунодепрессантов, ему предшествовало открытие рапамицина (сиролимус) на Rapa Nui (остров Пасхи) в 1975 году. Он продуцируется почвенной бактерией Streptomyces tsukubaensis. Название такролимус происходит от «Цукуба макролидный иммунодепрессант».
Такролимус был впервые одобрен Управлением по контролю за продуктами и лекарствами США (FDA) в 1994 году для использования в трансплантация печени ; к показаниям были добавлены трансплантаты почек, сердца, тонкой кишки, поджелудочной железы, легких, трахеи, кожи, роговицы, костного мозга и конечностей. Дженерики такролимуса были одобрены в США в 2017 году.
Такролимус был одобрен для медицинского применения в Европейском Союзе в 2002 году для лечения атопического дерматита средней и тяжелой степени. В 2007 г. показания были расширены и теперь включают профилактику отторжения трансплантата у взрослых реципиентов аллотрансплантата почки или печени и лечение отторжения аллотрансплантата, резистентного к лечению другими иммуносупрессивными лекарственными средствами, у взрослых. В 2009 году показания были расширены и теперь включают профилактику отторжения трансплантата у взрослых и детей, реципиентов аллотрансплантата почек, печени или сердца, а также лечение отторжения аллотрансплантата, резистентного к лечению другими иммуносупрессивными лекарственными средствами, у взрослых и детей.
Фирменная версия препарата принадлежит Астеллас Фарма и продается под торговой маркой Prograf, которую выдают два раза в день. Ряд других производителей имеют регистрационное удостоверение для альтернативных брендов препаратов для приема дважды в день.
Препараты для приема один раз в сутки с регистрационным разрешением включают Advagraf (Astellas Pharma) и Envarsus (в США продаются как Envarsus XR компанией ). Veloxis Pharmaceuticals и продается в Европе Chiesi ). Эти составы предназначены для уменьшения фармакокинетических вариаций уровней в крови и облегчения соблюдения дозировки.
Состав для местного применения продается компанией LEO Pharma под названием Protopic.

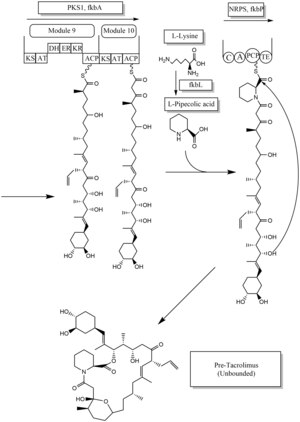

Биосинтез такролимуса представляет собой гибридный синтез как типа 1 поликетидсинтаз (PKS 1), так и нерибосомальных пептидных синтаз (NRPS). Исследование показывает, что гибридный синтез состоит из десяти модулей поликетидсинтазы 1 типа и одного модуля нерибосомальной пептидной синтазы. Синтетические ферменты такролимуса находятся в 19 кластерах генов, названных fkb. 19 генов: fkbQ, fkbN, fkbM, fkbD, fkbA, fkbP, fkbO, fkbB, fkbC, fkbL, fkbK, fkbJ, fkbI, fkbH, fkbG, allD, allR, allK и allA74.
несколько возможных способов биосинтеза такролимуса. Фундаментальные единицы для биосинтеза следующие: одна молекула 4,5-дигидроксициклогекс-1-енкарбоновой кислоты (DHCHC) в качестве стартовой единицы, четыре молекулы малонил-КоА, пять молекул метилмалонил-КоА, одна молекула аллилмалонил-КоА в виде единицы удлинения. Однако две молекулы малонил-КоА могут быть заменены двумя молекулами метоксималонил-КоА. После замены двух молекул малонил-КоА этапы постсинтазной адаптации больше не требуются, когда заменяются две молекулы метоксималонил-КоА. Биосинтез метоксималонил-КоА в ацильный белок-носитель осуществляется пятью ферментами (fkbG, fkbH, fkbI, fkbJ и fkbK). Аллилмалонил-КоА также может быть заменен пропионилмалонил-КоА.Стартовое звено, DHCHC из хорисминовой кислоты, образуется ферментом fkbO и загружается в домен CoA-лигазы (CoL). Затем он переходит к НАДФН-зависимому восстановлению (ER). Три фермента, fkbA, B, C, осуществляют процессы от загрузочного модуля к модулю 10, последний этап PKS 1. Фермент fkbB отвечает за синтез аллилмалонил-КоА или, возможно, пропионилмалонил-КоА на С21, что является необычным этапом. общий PKS 1. Как уже упоминалось, если две молекулы метоксималонил-КоА заменены на две молекулы малонил-КоА, они будут иметь место в модуле 7 и 8 (C13 и C15), и фермент fkbA будет усиливать этот процесс. После последней стадии (модуль 10) PKS 1 одна молекула L-пипеколиновой кислоты, образованная из L-лизина и катализируемая ферментом fkbL, синтезируется с молекулой из модуля 10. Процесс <Синтез 149>L -пипеколиновой кислоты - это NRPS, усиленный ферментом fkbP. После синтеза целых субъединиц молекула циклизуется. После циклизации молекула пре-такролимуса проходит стадии адаптации постсинтазы, такие как окисление и S-аденозилметионин. В частности, фермент fkbM отвечает за метилирование спирта, нацеленное на спирт стартовой единицы DHCHC (углеродное число 31 показано коричневым цветом), а фермент fkbD отвечает за C9 (показано зеленым). После этих этапов адаптации молекула такролимуса становится биологически активной.