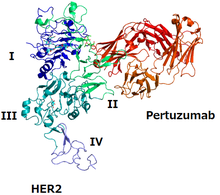
 Структура HER2 и пертузумаба Структура HER2 и пертузумаба | |
| Моноклональные антитела | |
|---|---|
| Тип | Целое антитело |
| Источник | Гуманизированное (от мыши ) |
| Цель | HER2 |
| Клинические данные | |
| Торговые наименования | Perjeta |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы. введения | Внутривенное |
| Код АТС | |
| Правовой статус | |
| Правовой статус |
|
| Идентификаторы | |
| Номер CAS | |
| ChemSpider |
|
| UNII | |
| KEGG | |
| ChEMBL |
|
| (что это?) | |
Пертузумаб ( также называется 2C4, торговое название Perjeta ) представляет собой моноклональное антитело, используемое в комбинации с трастузумабом и доцетакселом для лечение метастатического HER2 -положительного рака груди ; он также используется в той же комбинации, что и неоадью vant при раннем HER2-положительном раке молочной железы.
Побочные эффекты более чем у половины людей, принимающих его, включают диарею, выпадение волос и потерю нейтрофилов ; более 10% испытывают потерю эритроцитов, гиперчувствительность или аллергические реакции, реакции на инфузию, снижение аппетита, бессонницу, нарушение вкусовых ощущений, воспаление ротовой полости или губ, запор, сыпь, болезнь ногтей и мышечные боли. Беременным женщинам или планирующим беременность принимать его не следует, он не изучался на людях с определенными сердечными заболеваниями и должен применяться с осторожностью у таких людей, а также не должен использоваться с антрациклином. Неизвестно, взаимодействует ли пертузумаб с доксорубицином.
. Это первый в своем классе препарат под названием «ингибитор димеризации HER » - он подавляет димеризацию HER2 с другими рецепторами HER, что предотвращает их передачу сигналов способами, которые способствуют росту и пролиферации клеток.
Он был открыт и разработан Genentech, дочерней компанией из Roche, и впервые было одобрено в 2012 году.
Пертузумаб вводится внутривенно в сочетании с трастузумабом и доцетаксел в качестве терапии первой линии для HER2-положительного метастатического рака молочной железы. Он также используется в той же комбинации, что и неоадъювант (применяемый для уменьшения размера опухоли до операции или облучения) для HER2-положительного рака груди на ранней стадии; по состоянию на 2016 г. не было показано, что такое использование увеличивает выживаемость.
По состоянию на 2016 г. пертузумаб не исследовался на людях с фракцией выброса левого желудочка ≤ 50% от нормы, ранее застойная сердечная недостаточность в анамнезе или состояния, которые могут нарушить функцию левого желудочка, например неконтролируемая гипертензия, недавние сердечные приступы или серьезная сердечная аритмия. Следует проявлять осторожность при сочетании пертузумаба с антрациклином. Также отсутствуют данные по безопасности использования пертузумаба в комбинации с доксорубицином.
. Женщинам детородного возраста следует использовать контрацептивы при приеме пертузумаба; он может повредить плод у беременных женщин и может выделяться с грудным молоком.
В клинических испытаниях комбинированной терапии с тремя агентами при метастатическом раке молочной железы наблюдались побочные эффекты у более чем половины людей, принимавших его, наблюдались диарея, выпадение волос и потеря нейтрофилов ; более 10% людей испытали потерю нейтрофилов с лихорадкой и потерю лейкоцитов. После отмены доцетаксела у некоторых людей наиболее частыми побочными эффектами были диарея (28,1%), инфекция верхних дыхательных путей (18,3%), сыпь (18,3%), головная боль (17,0%), усталость (13,4%), отек носа. проходы и горло (часто из-за простуды) (17,0%), слабость (13,4%), зуд (13,7%), боль в суставах (11,4%), тошнота (12,7%), боль в конечности (13,4%), боль в спине (12,1%) и кашель (12,1%).
В клинических испытаниях неоадъювантного применения комбинации более 50% людей имели выпадение волос и потерю нейтрофилов.
В обоих случаях более 10% людей дополнительно испытали: потерю красных кровяных телец, гиперчувствительность или аллергическую реакцию, реакции на инфузию, снижение аппетита, бессонницу, нарушение вкусовых ощущений, воспаление ротовой полости или губы, запор, сыпь, заболевание ногтей и мышечные боли.
Метаболизм пертузумаба непосредственно не изучался; Как правило, антитела выводятся главным образом за счет катаболизма. Средний клиренс пертузумаба составлял 0,235 л / день, а средний период полувыведения составлял 18 дней.
HER2 - внеклеточный рецептор - рецептор тирозинкиназы - что при активации запускает передачу сигнала через несколько путей, которые стимулируют пролиферацию и рост клеток; чрезмерная экспрессия может вызвать неконтролируемый рост. HER2-положительный рак молочной железы вызывается амплификацией гена ERBB2, которая приводит к сверхэкспрессии HER2 примерно в 15-30% опухолей молочной железы.
Как и многие рецепторы, HER2 обычно объединяет другой белок для своего функционирования (процесс, называемый димеризация ); он может связываться со вторым рецептором HER2 (действующим как гомодимер ) и может гетеродимеризоваться с другим рецептором из семейства HER. Наиболее эффективным димером для активации сигнальных путей является HER2 / HER3.
эпитоп для пертузумаба - это домен HER2, где он связывается с HER3, и пертузумаб предотвращает образование димера HER2 / HER3., который блокирует передачу сигналов димером. Трастузумаб - еще одно моноклональное антитело против HER2; его эпитоп - это домен, в котором HER2 связывается с другим белком HER2. Два моноклональных антитела вместе препятствуют функционированию HER2.
Пертузумаб представляет собой иммуноглобулин G1 с вариабельной областью против белка HER2 человека, моноклональной тяжелой цепи 2C4 человека и мыши, связанной с дисульфидом с моноклональной κ-цепью 2C4 человека и мыши.
Он производится рекомбинантно в CHO клетках.
Моноклональное антитело 2C4, по-видимому, были впервые опубликованы в 1990 году учеными Genentech, в том же году, что и F. Hoffmann-La Roche AG приобрела контрольный пакет акций Genentech.
К 2003 году Genentech поняла, что 2C4 предотвращает димеризацию HER2 с другими рецепторами HER, и начала Фазу I испытаний, направленных на широкий спектр видов рака, а не просто сверхэкспрессирующие HER2. Это был первый известный ингибитор димеризации HER.
В 2005 году компания Genentech представила неудовлетворительные результаты испытаний пертузумаба в качестве единственного средства при раке простаты, груди и яичников во второй фазе и заявила, что намерена продолжить его разработку в сочетание с другими лекарствами от рака яичников.
В 2007 году Genentech отказалась от торговой марки Omnitarg.
В марте 2009 года компания Roche приобрела Genentech, купив акции, которые она еще не контролировала.
В 2012 году были опубликованы результаты исследования CLEOPATRA, рандомизированного плацебо-контролируемого исследования фазы III пертузумаба в сочетании с трастузумабом и доцетакселом при HER2-положительном метастатическом раке молочной железы. Позднее в том же году пертузумаб получил одобрение FDA США для лечения HER2-положительного метастатического рака груди. Результаты исследования фазы II в неоадъювантной среде, NeoSphere, опубликованные в 2012 году, и результаты исследования сердечной безопасности фазы II в той же популяции, Tryphaena, опубликованные в 2013 году. FDA одобрило неоадъювантное показание в 2013 году.
Пертузумаб был одобрен в Европе в 2013 году.
Пертузумаб также изучался при немелкоклеточном раке легкого, но с 2016 года это показание было прекращено.
По состоянию на 2016 год в США каждый курс комбинации из трех препаратов, вводимый каждые три недели, стоит около 8 500 долларов, не включая расходы на вспомогательный уход.
В Великобритании Оценка NICE в 2015 году сделала предварительный вывод о том, что комбинация лекарств не была рентабельной, и в мае 2016 года NICE отклонил это лекарство в условиях неоадъювантной терапии, прежде всего потому, что было неизвестно, дает ли комбинация лекарств преимущество в выживаемости. Впоследствии это решение было отменено шесть месяцев спустя, и пертузумаб стал первым новым лекарством от рака груди, одобренным NICE для рутинного финансирования NHS почти за десять лет после того, как компания «Рош» пообещала предоставить это лекарство NHS с нераскрытой скидкой. для пациентов в условиях неоадъювантной терапии и для разделения долгосрочных финансовых рисков.