| Синдром нечувствительности к эстрогену | |
|---|---|
| Другие названия | EIS; Синдром полной нечувствительности к эстрогенам; CEIS |
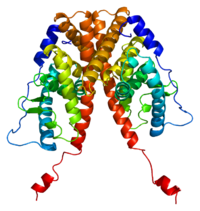 | |
| EIS возникает, когда функция рецептора эстрогена альфа (ERα) нарушена. Белок ERα (на фото) опосредует большинство эффектов эстрогенов в организме человека. | |
| Специальность | Эндокринология |
Синдром нечувствительности к эстрогенам (EIS ) или эстроген резистентность, представляет собой форму врожденного дефицита эстрогена или гипоэстрогении, которая вызвана дефектным рецептором эстрогена (ER), в частности, рецептор эстрогена альфа (ERα) - что приводит к неспособности эстрогена опосредовать его биологические эффекты в организме. В качестве альтернативы врожденный дефицит эстрогенов может быть вызван дефектом ароматазы, фермента, ответственного за биосинтез эстрогенов, состояние. называется недостаточностью ароматазы и по симптоматике аналогичен EIS.
EIS - чрезвычайно редкое явление. По состоянию на 2016 год было опубликовано три отчета EIS с участием пяти человек. В отчеты включены мужской случай, опубликованный в 1994 году, женский случай, опубликованный в 2013 году, и семейный случай с участием двух сестер и брата, опубликованный в 2016 году.
EIS аналогичен синдрому нечувствительности к андрогенам (AIS), состояние, при котором рецептор андрогенов (AR) является дефектным и нечувствительным к андрогенам, таким как тестостерон и дигидротестостерон (DHT). Функциональная противоположность EIS - гиперэстрогенизм, например, наблюдаемый при синдроме избытка ароматазы.
В 1994 г. Сообщалось о годовалом мужчине с EIS. Он был полностью маскулинизирован. Рост 204 см, рост . Его эпифизы не были объединены, и были доказательства продолжающегося медленного линейного роста (для сравнения, его рост в 16 лет составлял 178 см). У него также была заметная задержка созревания скелета (возраст кости 15 лет), сильно недоминерализованный скелет, свидетельства повышенной резорбции кости и очень раннее начало остеопороз. гениталии, яички и простата пациента были нормальными и имели нормальный размер / объем. количество сперматозоидов у пациента было нормальным (25 миллионов / мл; нормальное,>20 миллионов / мл), но его жизнеспособность сперматозоидов была низкой (18%; нормальная>50%).), что указывает на некоторую степень бесплодия. У пациента также была ранняя временная потеря волос. Он не сообщил в анамнезе расстройство половой идентичности, считал, что у него сильные гетеросексуальные интересы и нормальная сексуальная функция, включая утреннюю эрекцию и ночная эмиссия.
уровни фолликулостимулирующего гормона и лютеинизирующего гормона были значительно повышены (30–33 мМЕ / мл и 34–37 мМЕ / мл соответственно) и Уровни эстрадиола и эстрона были заметно повышены (145 пг / мл и 119–272 пг / мл соответственно), тогда как уровни тестостерона были нормальными (445 нг / дл). Уровни глобулина, связывающего половые гормоны, были незначительно повышены (6,0–10,0 нмоль / л), тогда как тироксин-связывающий глобулин, кортикостероид-связывающий глобулин и уровни пролактина были в норме. Уровни остеокальцина и костно-специфической щелочной фосфатазы были существенно повышены (18,7–21,6 нг / мл и 33,3–35,9 нг / мл соответственно
Лечение до очень высоких доз эстрадиола (четырнадцать 100 мкг эстрадиола). rm пластырей в неделю) не повлияли ни на один из его симптомов гипоэстрогении, не вызвали никаких эстрогенных эффектов, таких как гинекомастия, и не повлияли ни на один из его физиологических параметров (например,, уровни гормонов или параметры костей), что позволяет предположить профиль синдрома полной нечувствительности к эстрогену.
В 2013 году сообщалось о 18-летней женщине с EIS. ДНК секвенирование выявило гомозиготную мутацию в ESR1, гене, который кодирует ERα. В пределах лиганд-связывающего домена нейтральный полярный глутамин 375 был заменен на основной полярный гистидин. in vitro анализ ERα-зависимой транскрипции гена обнаружил, что EC50 для трансактивации был снижен в 240 раз по сравнению с нормальным, немутантным ERα, что указывает на крайнее снижение активности рецептора. Клинические признаки предполагали профиль синдрома полной нечувствительности к эстрогенам, сходный с ERα нокаутом мышей. У пациентки отсроченное половое созревание, в том числе отсутствие развития груди (стадия Таннера I) и первичная аменорея, а также периодическая тазовая боль. Обследование выявило заметно увеличенные яичники с множественными геморрагическими кистами как причиной боли внизу живота.
Уровни эстрогена были резко и постоянно повышены ( Уровень эстрадиола составлял 2340 пг / мл, что примерно в 10 раз превышало нормальный уровень, и варьировалось от 750 до 3500 пг / мл), уровень гонадотропина был слегка повышен (Уровни фолликулостимулирующего гормона и лютеинизирующего гормона составляли 6,7–19,1 мМЕ / мл и 5,8–13,2 мМЕ / мл соответственно), а уровень тестостерона был немного повышен (33– 88 нг / дл). Уровни ингибина A также были заметно повышены. Глобулин, связывающий половые гормоны, глобулин, связывающий кортикостероиды, тироксин-связывающий глобулин, пролактин и триглицериды, которые, как известно, повышаются под действием эстрогена, все были в пределах нормы, несмотря на чрезвычайно высокий уровень эстрогена и ингибина Уровни B также были нормальными. Относительно умеренно повышенный уровень гонадотропинов был связан с сохранением отрицательной обратной связи с помощью прогестерона, а также с повышенным уровнем тестостерона и ингибина А, хотя было признано, что возможные эффекты эстрогена опосредованы другими рецепторами, такими как ERβ, нельзя исключить.
У пациентки была маленькая матка с полосой эндометрия, которая не могла быть четко идентифицированы. В возрасте 15 лет 5 месяцев ее костный возраст составлял 11 или 12 лет, а в возрасте 17 лет 8 месяцев костный возраст составлял 13,5 лет. Ее костная масса была ниже, чем ожидалось для ее возраста, а уровни остеокальцина и С-концевого телопептида были повышены, что свидетельствует об увеличении скорости обновления костной ткани. Ее рост составлял 162,6 см, и скорость ее роста указывала на отсутствие эстроген-индуцированного скачка роста в период полового созревания. У пациента было нормальное развитие лобковых волос (стадия Таннера IV) и тяжелые угри на лице акне, которые могли быть отнесены на счет тестостерона. Ее патологию яичников связывали с повышенным уровнем гонадотропинов. В дополнение к отсутствию развития груди и ареолярного увеличения, у пациентки также было обнаружено минимальное расширение бедер и отсутствие отложения подкожного жира, которое соответствует установленной роли эстрогена и ERα в развитии женских вторичных половых признаков.
Лечение пациента конъюгированными эстрогенами и высокими дозами эстрадиола проводилось нет эффекта. Хотя авторы статьи считали, что ее ERα практически не реагирует на эстроген, они заявили, что они «[не могут] исключить возможность того, что некоторая остаточная чувствительность к эстрогену может присутствовать в некоторых тканях», что соответствует тому факту, что EC 50 ее ERα уменьшился в 240 раз, но не был отменен. Лечение прогестином, норэтистероном снизило концентрацию ее эстрадиола до нормального уровня и уменьшило размер ее яичников и количество кист яичников, уменьшив ее гипоталамо-гипофизарно-гонадную ось гиперактивность и патология яичников.
В 2016 году был зарегистрирован семейный случай EIS с участием трех братьев и сестер. Пострадавшими были 25-летняя женщина, 21-летняя женщина и 18-летний мужчина. Семья была кровным родственником, причем родители братьев и сестер были двоюродными братьями. Оба родителя были гетерозиготными по причинной мутации, были здоровы и нормальны, в то время как три затронутых брата и сестры были гомозиготными по мутации, а четвертый брат и сестра, здоровая сестра, была гетерозиготной. Тот факт, что гетерозиготные родители и гетерозиготная сестра не были затронуты, указывает на то, что заболевание передается аутосомно-рецессивным способом и что одного нормального аллеля достаточно для достижения нормального полового созревания и фертильность, что согласуется с тем, что наблюдалось у мышей с нокаутом ERα .
. У всех трех братьев и сестер была пубертатная недостаточность. У обеих сестер не было развития груди (т.е. стадии I по Таннеру), что свидетельствует о том, что ERα абсолютно необходим для нормального развития молочной железы. Старшая сестра имела избыточный вес (BMI 26,3) и имела легкую случайную адипомастию или отложение жировой ткани в груди без истинного железистая ткань, признак, не указывающий на половое развитие. У сестер было полное созревание лобковых волос (т.е. стадия V по Таннеру), у брата - стадия развития лобковых волос по Таннеру II и стадия созревания гонад I. Правое яичко брата было крипторхидом, тогда как левое яичко было сильно гипопластическим с объемом менее 1 мл. Обе сестры имели первичную аменорею и увеличенные поликистозные яичники, а у старшей сестры была маленькая матка и тонкий эндометрий. У старшей сестры было угри на груди, что можно отнести к гиперандрогении (см. Ниже). У всех трех братьев и сестер наблюдалась заметно задержка созревания костей для их хронологического возраста. Удивительно, но старшая сестра была нормального роста, в то время как младшая сестра была высокой.
У всех трех братьев и сестер уровень эстрадиола был заметно повышен, а уровень гонадотропина был повышен.. У сестер уровень эстрадиола был чрезвычайно высоким, более чем в 50 раз превышающим нормальный уровень, в то время как уровень гонадотропина был повышен в 3 раза выше нормального диапазона. Уровни прогестерона, 17α-гидроксипрогестерона, андростендиона, тестостерона и дигидротестостерона (DHT) были повышены в сестры, в то время как концентрации стероидов надпочечников, включая кортизол, дегидроэпиандростерон (DHEA), 11β-гидроксиандростендион, 11-дезоксикортизол и 21-дезоксикортизол были в пределах нормы. Уровни глобулина, связывающего половые гормоны (SHBG), были очень низкими, что можно объяснить отсутствием действия эстрогена на печень. У старшей сестры уровни антимюллерова гормона (АМГ) были нормальными, тогда как уровни ингибина A и ингибина B были значительно повышены. У брата уровни AMH и ингибина B были низкими в сочетании с низкими концентрациями тестостерона у пациента. Низкий уровень тестостерона у брата, вероятно, был связан с его крипторхизмом, этот симптом ранее не упоминался в более раннем отчете о мужском случае EIS. В соответствии с фенотипом брата, крипторхизм был описан у мышей с нокаутом ERα. Исследователи заявили, что из-за низкого уровня ингибина B у брата весьма вероятно, что сперматогенез не произойдет у него. Нарушение отрицательной обратной связи эстрогеном на оси гипоталамус-гипофиз-гонад (HPG) может объяснить повышенные уровни эстрадиола и гонадотропина у братьев и сестер и яичников. увеличение и образование кист у сестер.
Все три брата и сестры были гомозиготными по миссенс-мутации в пятом кодирующем экзоне гена ESR1 . Мутация вызвала изменение с гуанина на аденин на комплементарной ДНК нуклеотиде 1181 (c.1181G>A) в гене, который привело к замене гистидина на аргинин при остатке 394 (p.Arg394His) в спирали H5 лиганд-связывающего домена (LBD) белка ERα . Это критический остаток, который полностью сохраняется среди видов и в рецепторе андрогенов (AR) и рецепторе минералокортикоидов (MR). Мутации, затрагивающие соответствующий остаток в AR и MR, ранее были связаны с синдромом нечувствительности к андрогенам (AIS) и снижением чувствительности к минералокортикоидам соответственно.
Анализы показали, что мутированный ERα показал сильно сниженную транскрипционную активность в ответ на стимуляцию эстрадиолом, с ED50, который был примерно в 65 раз выше, чем у нормального / дикого типа ERα. В нормальном ERα эстрадиол закреплен в связывающем кармане рецептора тремя водородными связями ; С3 и С17 гидроксильные группы эстрадиола заякорены остатками Glu353 и Arg394 и His524 белка ERα, соответственно. В мутированном ERα остаток His394 неспособен должным образом закрепить эстрадиол, что приводит к резкому снижению чувствительности и реакции рецептора на эстрадиол по сравнению с нормальным ERα. Была протестирована группа других агонистов ERα, которые включали этинилэстрадиол, диэтилстильбестрол, тамоксифен, кломифен и ралоксифен. в их способности способствовать транскрипционной активности мутировавшего ERα, но ни один из них не оказался более эффективным, чем эстрадиол, в активации мутировавшего рецептора и, следовательно, в преодолении нечувствительности к эстрогену у братьев и сестер.
Как и сестры. очень высоких, супрафизиологических уровней циркулирующего эстрадиола, авторы предупредили, что нельзя исключать, что эстрадиол мог оказывать некоторое функциональное влияние на их фенотипы посредством передачи сигналов через ERβ и GPER ( т.е., что не все наблюдаемые фенотипы могли быть просто следствием потери передачи сигналов ERα). Более того, авторы отметили, что это может частично объяснять вариабельность фенотипов.
EIS можно экспериментально вызвать у животных посредством нокаута ER. У этих так называемых мышей ERKO различные ER могут быть отключены, что позволяет изучить роль этих рецепторов. У мышей ERKO наблюдается развитие соответствующих самок или самцов репродуктивной системы, самцы и самки мышей αERKO бесплодны, самцы βERKO фертильны, а самки субфертильны, самцы и самки двойных мышей αERKO и βERKO бесплодны. матка и молочные железы являются гипопластическими и не реагируют на экзогенную стимуляцию эстрогенами. Мужчины бесплодны с атрофией в семенниках. Возраст костей замедлен, и кости более хрупкие. Вариации этих паттернов можно достичь путем выборочного отключения ERα или ERβ.
В следующих разделах представлен обширный, хотя и частичный / неполный список дефицитов, наблюдаемых у мышей ERKO.
также были получены мыши с нокаутом по GPER, которые демонстрируют ожирение, сердечно-сосудистую дисфункцию, инсулин. устойчивость, непереносимость глюкозы, различия в канцерогенезе молочной железы и метастазировании, а также различия в функции центральной нервной системы.
В отличие от EIS, синдром нечувствительности к андрогенам (AIS), состояние, при котором рецептор андрогенов (AR) является дефектным, является относительно часто. Это можно объяснить генетикой каждого синдрома. AIS - это X-сцепленное рецессивное состояние, которое, таким образом, передается самками в будущие поколения (хотя наиболее тяжелая форма, синдром полной нечувствительности к андрогенам (CAIS), приводит к бесплодию, и, следовательно, не может передаваться потомству). EIS несовместима с репродукцией, поэтому каждое появление у людей должно быть de novo мутацией и не передается потомству.
| Классификация | D |
|---|---|
| Внешние ресурсы |