| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC Азулен | |||
| Системное имя IUPAC Bicyclo [5.3. 0] декапентаен | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.449 | ||
| KEGG | |||
| PubChem CID | |||
| UNII | |||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химическая формула | C10H8 | ||
| Молярная масса | 128,174 г · моль | ||
| Температура плавления | 99 до 100 ° C (от 210 до 212 ° F; от 372 до 373 K) | ||
| Точка кипения | 242 ° C (468 ° F, 515 K) | ||
| Магнитная восприимчивость (χ) | - 98,5 · 10 см / моль г / л | ||
| Термохимия | |||
| Стандартная энтальпия. горения ция (ΔcH298) | −1266,5 ккал / моль | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в информационном окне | |||
Азулен - это органическое соединение и изомер из нафталин. Нафталин бесцветен, а азулен темно-синий. Два терпеноида, ветивазулен (4,8-диметил-2-изопропилазулен) и гвайазулен (1,4-диметил-7-изопропилазулен), которые имеют азуленовый скелет, встречаются в природе. в составе пигментов грибов, масла гваякового дерева и некоторых морских беспозвоночных.
Азулен имеет долгую историю, восходящую к 15 веку, как лазурно-синий хромофор, полученный паровой дистилляцией немецкой ромашки. Хромофор был обнаружен в тысячелистнике и полыни и назван в 1863 году Септимусом Писсом. О его структуре впервые сообщил Лавослав Ружичка, а затем о его органическом синтезе в 1937 году Плацидус Платтнер.
 Голубой цвет гриба Lactarius indigo обусловлен производным азулена (7-изопропенил-4-метилазулен-1-ил) метилстеаратом.
Голубой цвет гриба Lactarius indigo обусловлен производным азулена (7-изопропенил-4-метилазулен-1-ил) метилстеаратом. Азулен обычно рассматривается как продукт слияния кольца циклопентадиена и циклогептатриена. Подобно нафталину и циклодекапентаену, это система с 10 пи-электронами. Он проявляет ароматические свойства: (i) периферийные связи имеют одинаковую длину и (ii) он претерпевает замены Фриделя-Крафтса. Прирост стабильности от ароматичности оценивается вдвое по сравнению с нафталином.
Его дипольный момент составляет 1,08 D, в отличие от нафталина, у которого дипольный момент равен нулю. Эту полярность можно объяснить, рассматривая азулен как слияние 6 π-электронов циклопентадиенильного аниона и 6 π-электронных катиона тропилия : один электрон от семичленное кольцо переносится на пятичленное кольцо для придания каждому кольцу ароматической стабильности по правилу Хюккеля. Исследования реакционной способности подтверждают, что семичленное кольцо является электрофильным, а пятичленное кольцо нуклеофильным.

Диполярная природа основного состояния отражается в его глубоком цвете, который необычен для небольших ненасыщенных ароматических соединений. Еще одна примечательная особенность азулена заключается в том, что он нарушает правило Каша, проявляя флуоресценцию из верхнего возбужденного состояния (S 2 → S 0).
Синтетические пути к азулену уже давно представляют интерес из-за его необычной структуры. В 1939 г. Санкт-Пфау и Платтнер сообщили о первом методе, основанном на использовании индана и этилдиазоацетата.
Эффективный метод -pot путь влечет за собой аннелирование циклопентадиена с ненасыщенными C 5-синтонами. Альтернативный подход из циклогептатриена давно известен, иллюстративный метод показан ниже.
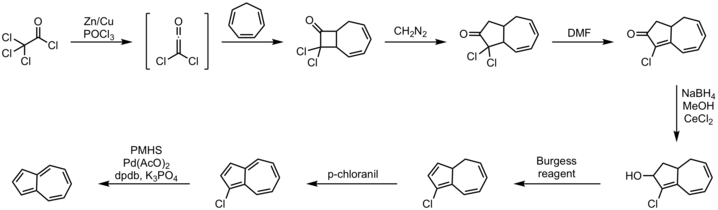
Процедура:
В металлоорганической химии азулен служит лигандом для низковалентных металлических центров, которые, как известно, образуют π-комплексы как с циклопентадиенилом, так и с циклогептатриенильным лигандами. Иллюстративными комплексами являются (азулен) Mo 2 (CO) 6 и (азулен) Fe 2 (CO) 5.
1-Гидроксиазулен представляет собой нестабильное масло зеленого цвета и не проявляет кето-енольной таутомерии. 2-Гидроксиазулен получают гидролизом 2-метоксиазулена бромистоводородной кислотой. Он стабилен и демонстрирует кето-енольную таутомерию. pKa 2-гидроксиазулена в воде составляет 8,71. Он более кислый, чем фенол или нафтол. PK a 6-гидроксиазуленов в воде составляет 7,38, что делает ее более кислой, чем фенол или нафтол.
В нафт [a] азулене нафталиновое кольцо представляет собой конденсируется по 1,2-положениям азулена. Обнаружено, что в одной такой системе деформация из-за планарности аналогична деформации тетрагелицен.
Гуаязулен (1,4-диметил-7-изопропилазулен) представляет собой алкилированное производное азулена с почти идентичным интенсивно синим цветом. Он коммерчески доступен для косметической промышленности, где действует как кондиционирующее средство для кожи.