 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Пентацен | |
| Другие имена 2,3: 6, 7-Дибензантрацен. Бензо [b] нафтацен. Дибенз [b, i] антрацен. NSC 90784. лин-дибензантрацен. лин-нафтоантрацен | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| Ссылка Beilstein | 1912418 |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.004.722 |
| Номер EC |
|
| Ссылка Gmelin | 733903 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C22H14 |
| Молярная масса | 278,354 г · моль |
| Внешний вид | Темно-синий порошок |
| Плотность | 1,3 г см |
| Температура плавления | >300 ° C (572 ° F; 573 K) сублимируется при 372 ° C |
| Точка кипения | 40–43 ° C (104–109 ° F; 313–316 K) при 0,15 торр |
| Магнитная восприимчивость (χ) | -205,4 × 10 см моль |
| Структура | |
| Кристаллическая структура | Triclinic |
| Пространственная группа | P-1 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
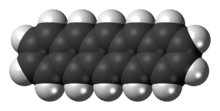
Пентацен представляет собой полициклический ароматический углеводород, состоящий из пяти линейно конденсированных бензольных колец. Это сильно сопряженное соединение представляет собой органический полупроводник. Соединение генерирует экситоны при поглощении ультрафиолетового (УФ ) или видимого света ; это делает его очень чувствительным к окислению. По этой причине это соединение, представляющее собой фиолетовый порошок, медленно разлагается под воздействием воздуха и света.
Структурно пентацен представляет собой один из линейных аценов, предыдущий - тетрацен (четыре конденсированных бензольных кольца), а следующий - гексацен (шесть конденсированных бензольных колец). В августе 2009 года группа исследователей из IBM опубликовала экспериментальные результаты визуализации единственной молекулы пентацена с помощью атомно-силового микроскопа. В июле 2011 года они использовали модификацию сканирующей туннельной микроскопии для экспериментального определения формы самой высокой занятой и самой нижней незанятой молекулярных орбиталей.
. В 2012 году п-терфенил, легированный пентаценом, показал свою эффективность в качестве усиливающей среды для мазера при комнатной температуре.
 Сканирующая туннельная микроскопия изображение молекул пентацена на никеле.
Сканирующая туннельная микроскопия изображение молекул пентацена на никеле.  Пентаценовый порошок
Пентаценовый порошок Пентацен был впервые синтезирован в 1912 году британскими химиками Уильямом Хобсоном Миллсом и Милдред Мэй Гостлинг. Классическим методом синтеза пентацена является реакция Эльбса..
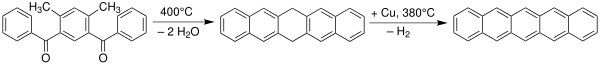
Пентацены также можно получить из небольшого летучего компонента (монооксида углерода ) из подходящего предшественника при 150 ° C.

Сам предшественник получают в три этапа из двух молекул α, α, α ', α'-тетрабромо-о-ксилола с 7-трет-бутоксибицикло [2.2.1] гепта-2,5-диеном при первом нагревании с йодид натрия в диметилформамиде для прохождения серии реакций элиминирования и Дильса-Альдера с образованием кольцевой системы, затем гидролиз трет- бутоксигруппу в спирт с последующим ее окислением до кетона.
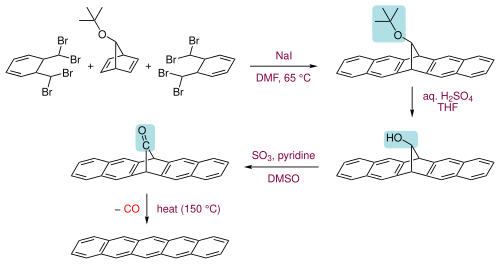
. Сообщается, что продукт имеет некоторую растворимость в хлороформе и, следовательно, поддается вращению покрытие. Пентацен растворим в горячих хлорированных бензолах, таких как 1,2,4-трихлорбензол, из которых его можно перекристаллизовать с образованием тромбоцитов.
6,13-Замещенные пентацены доступны через пентаценехинон путем взаимодействия с арильным или алкинилнуклеофилом (например, реактивами Гриньяра или литийорганическими реагентами) с последующей путем восстановительной ароматизации. Другой метод основан на гомологизации диинов переходными металлами (через цирконциклопентадиены). Функционализация пентацена позволила контролировать твердотельную упаковку этого хромофора. Выбор заместителей (как размер, так и расположение замещения в пентацене) влияет на твердотельную упаковку и может использоваться для контроля того, принимает ли соединение 1-мерную или 2-мерную кофациальную пи-укладку в в твердом состоянии, в отличие от набивки «в елочку», наблюдаемой для пентацена.
Хотя структура пентацена напоминает структуру других ароматических соединений, таких как антрацен, его ароматические свойства определены плохо; как таковой пентацен и его производные являются предметом многочисленных исследований.
A таутомерный химическое равновесие существует между 6-метилен-6,13-дигидропентаценом и 6-метилпентаценом.
 Равновесие с 6-метилпентаценом
Равновесие с 6-метилпентаценомЭто равновесие полностью соответствует метиленовому соединению. Только при нагревании раствора соединения до 200 ° C образуется небольшое количество пентацена, о чем свидетельствует появление красно-фиолетовой окраски. Согласно одному исследованию, механизм реакции для этого равновесия основан не на внутримолекулярном 1,5-гидридном сдвиге, а на бимолекулярном свободный радикал миграция водорода. Напротив, изотолуолы с тем же центральным химическим мотивом легко ароматизируются.
Пентацен реагирует с элементарной серой в 1,2,4-трихлорбензоле с образованием соединения гексатиапентацена . Рентгеновская кристаллография показывает, что все длины связей углерод-сера примерно равны (170 пм ); из этого следует, что резонансные структуры B и C с полным разделением зарядов более значимы, чем структура A.
 Гексатиапентацен
ГексатиапентаценВ кристаллической фазе молекулы проявляют ароматические стэкинг-взаимодействия, в результате чего расстояние между некоторыми атомами серы на соседних молекулах может стать меньше (337 пм), чем сумма двух радиусов Ван-дер-Ваальса (180 пм)
Подобно соответствующему тетратиафульвален, это соединение изучается в области органических полупроводников.
Ацены могут выглядеть как плоские и жесткие молекулы, но на самом деле они могут быть очень искажены. Пентацен, изображенный ниже:
 Скрученные ацены
Скрученные аценыимеют сквозное закручивание 144 ° и стерически стабилизированы шестью фенильными группами. Соединение может быть разделено на два его энантиомера с необычно высоким сообщенным оптическим вращением 7400 °, хотя рацемизация происходит с химическим периодом полураспада . из 9 часов.

Олигомеры и полимеры на основе пентацена были исследованы как синтетически, так и в настройках приложений устройства. Полимерные светоизлучающие диоды (PLED ) были сконструированы с использованием сопряженных сополимеров (1a-b ), содержащих флуорен и пентацен. Несколько других сопряженных полимеров пентацена (2a – b и 3 ) были реализованы на основе реакций связывания дибромпентацена Соногашира и Сузуки мономер. Неконъюгированные полимеры на основе пентацена были синтезированы путем этерификации мономера пентацендиола с бис-хлорангидридами с образованием полимеров 4a – b .
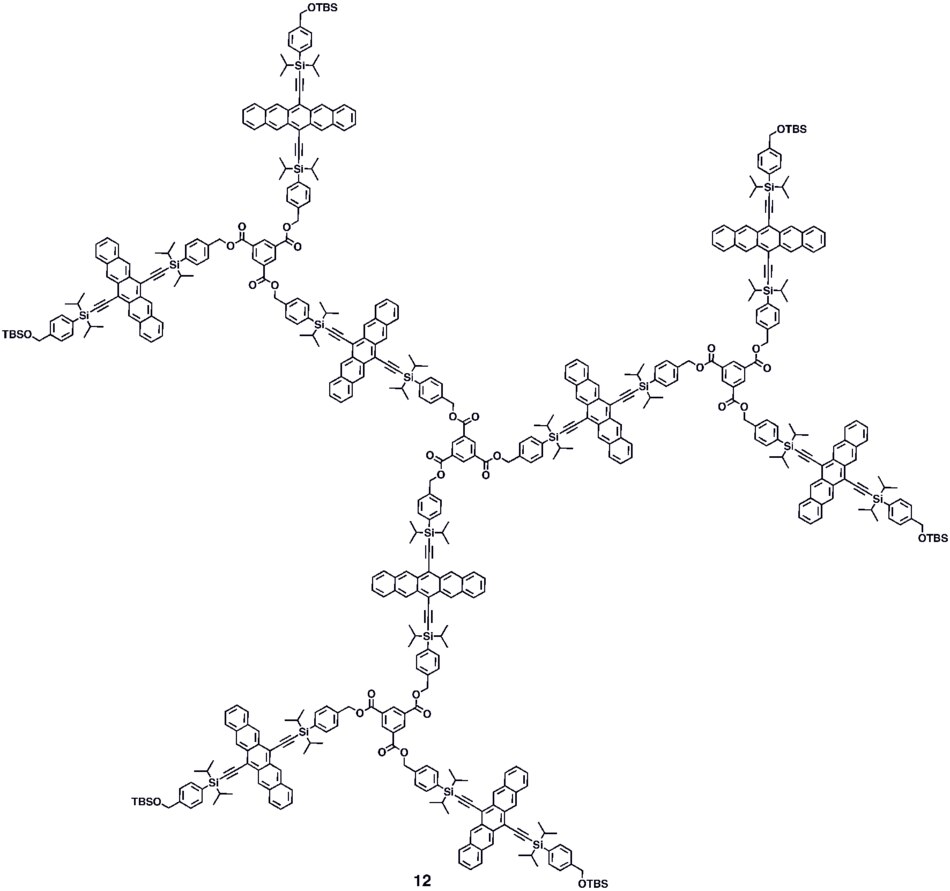
 . Для образования конъюгированных олигомеров пентацена 5a использовались различные синтетические стратегии. –C, включая процедуру образования «один горшок-четыре связи», которая обеспечила обрабатываемый в растворе сопряженный димер пентацена (5c ), который показал коэффициент фотопроводимости>10, что соответствует его характеристикам в пределах того же порядка величины как термически напыленные пленки нефункционализированного пентацена, которые показали коэффициент фотопроводимости>16 при использовании аналогичных методов измерения. Сообщается о модульном методе синтеза конъюгированных ди-, три- и тетрамеров пентацена (6-8 ), который основан на реакциях гомо- и кросс-сочетания устойчивых промежуточных продуктов дегидропентацена. Синтезированы неконъюгированные олигомеры 9–10 на основе пентацена, в том числе дендримеры 9–10, содержащие до 9 частей пентацена на молекулу с молярной поглощающей способностью для наиболее интенсивного поглощения>2 000 000 M •см. Было показано, что дендримеры 11–12 обладают улучшенными характеристиками в устройствах по сравнению с аналогичными полимерами на основе пентацена 4a – b в контексте фотодетекторов.
. Для образования конъюгированных олигомеров пентацена 5a использовались различные синтетические стратегии. –C, включая процедуру образования «один горшок-четыре связи», которая обеспечила обрабатываемый в растворе сопряженный димер пентацена (5c ), который показал коэффициент фотопроводимости>10, что соответствует его характеристикам в пределах того же порядка величины как термически напыленные пленки нефункционализированного пентацена, которые показали коэффициент фотопроводимости>16 при использовании аналогичных методов измерения. Сообщается о модульном методе синтеза конъюгированных ди-, три- и тетрамеров пентацена (6-8 ), который основан на реакциях гомо- и кросс-сочетания устойчивых промежуточных продуктов дегидропентацена. Синтезированы неконъюгированные олигомеры 9–10 на основе пентацена, в том числе дендримеры 9–10, содержащие до 9 частей пентацена на молекулу с молярной поглощающей способностью для наиболее интенсивного поглощения>2 000 000 M •см. Было показано, что дендримеры 11–12 обладают улучшенными характеристиками в устройствах по сравнению с аналогичными полимерами на основе пентацена 4a – b в контексте фотодетекторов.

Пентацены были исследованы как потенциальные дихроичные красители. Показанный ниже пентаценохинон является флуоресцентным, и при смешивании со смесью жидких кристаллов E7 достигается, равное 8. Более длинные ацены лучше выравниваются в нематической жидкокристаллической фазе.
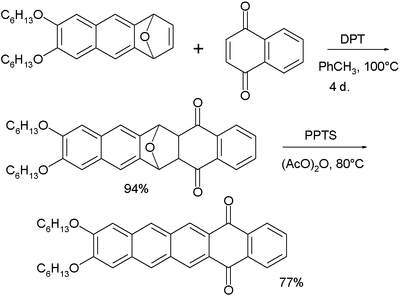 Флуоресцентные аценехиноны
Флуоресцентные аценехиноныВ сочетании с бакминстерфуллереном пентацен используется при разработке прототипов органических фотоэлектрических элементов. Органические фотоэлементы дешевле и более гибки, чем традиционные неорганические элементы, которые потенциально могут открыть двери для солнечных элементов на новые рынки.
Пентацен - популярный выбор для исследований органических тонкопленочных транзисторов и OFET, являющиеся одной из наиболее тщательно изученных сопряженных органических молекул с высоким прикладным потенциалом благодаря подвижности дырок в OFET до 5,5 см / (В · с), что превышает подвижность аморфного кремния.
Пентацен, как и другие органические проводники, подвержен быстрому окислению на воздухе, что исключает коммерческое использование. Если пентацен предварительно окислен, пентацен-хинон является потенциальным изолятором затвора, тогда подвижность может приближаться к подвижности рубрена - наиболее подвижного органического полупроводника, а именно 40 см / (В · с). Этот метод окисления пентацена сродни окислению кремния, используемому в кремниевой электронике.