 | |||
 | |||
| |||
| Названия | |||
|---|---|---|---|
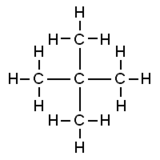
| Предпочтительное название IUPAC 2,2-Диметилпропан | |||
| Другие названия Неопентан. Тетраметилметан | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Справочник Байльштейна | 1730722 | ||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.677 | ||
| Номер EC |
| ||
| Справочная информация Gmelin | 1850 | ||
| MeSH | неопентан | ||
| PubChem CID | |||
| UNII | |||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
УЛЫБКА
| |||
| Свойства | |||
| Химическая формула | C5H12 | ||
| Молярная масса | 72,151 г · моль | ||
| Внешний вид | Бесцветный газ | ||
| Запах | Без запаха | ||
| Плотность | 3,255 кг / м (газ, 9,5 ° C). 601,172 кг / м (жидкость, 9,5 ° C) | ||
| Точка плавления | -16,5 ° C (2,3 ° F, 256,6 K) | ||
| Температура кипения | 9,5 ° C (49,1 ° F; 282,6 K) | ||
| Давление пара | 146 кПа (при 20 ° C) | ||
| Закон Генри. постоянная (kH) | 4,7 нмоль Па кг | ||
| Термохимия | |||
| Теплоемкость (C) | 121,07–120,57 ДжК моль | ||
| Стандартная молярная. энтропия (S 298) | 217 ДжК моль | ||
| Стандартная энтальпия образования. (ΔfH298) | - 168,5–−167,3 кДж моль | ||
| Стандартная энтальпия. горения (ΔcH298) | −3,51506–−3,51314 МДж моль | ||
| Опасности | |||
| Классификация ЕС (DSD) (устарело) | |||
| R-фразы (устаревшие) | R12, R51 / 53 | ||
| S-фразы (устаревшие) | (S2), S16, S33 | ||
| NFPA 704 (огненный алмаз) |  4 1 0 4 1 0 | ||
| Родственные соединения | |||
| Родственные алканы | |||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Неопентан, также называемый 2,2-диметилпропан, представляет собой двухразветвленный алкан с пятью углерод атомы. Неопентан - воспламеняющийся газ при комнатной температуре и давлении, который может конденсироваться в очень летучий жидкость в холодный день, на ледяной бане или при повышенном давлении.
Неопентан представляет собой простейший алкан с четвертичным углеродом и имеет ахиральную тетраэдрическую симметрию. Это один из трех структурных изомеров с молекулярной формулой C5H12(пентаны ), два других - н-пентан и изопентан <135.>. Из этих трех, это единственный газ при стандартных условиях; остальные - жидкости.
Традиционное название неопентан все еще сохранялось в рекомендациях IUPAC 1993 г., но больше не рекомендуется в соответствии с рекомендациями 2013 г. Предпочтительное название ИЮПАК представляет собой систематическое название 2,2-диметилпропан, но номера заместителей являются излишними, поскольку это единственный возможный «диметилпропан».
 Неопентильная группа, присоединенная к общей группе R.
Неопентильная группа, присоединенная к общей группе R. Неопентильный заместитель, часто обозначаемый «Np», имеет структуру Me 3 C – CH 2 - например, неопентиловый спирт (Me 3 CCH 2 OH или NpOH). Поскольку Np также символизирует элемент нептуний (атомный номер 93), следует использовать это сокращение с осторожностью.
Также используется устаревшее название тетраметилметан, особенно в более старых источниках.
Точка кипения неопентана равна всего 9,5 ° C, что значительно ниже, чем у изопентана (27,7 ° C) и нормального пентана (36,0 ° C). Следовательно, неопентан представляет собой газ при комнатной температуре и атмосферном давлении, в то время как два других изомера (почти) являются жидкостями.
Температура плавления неопентана (-16,6 ° C), с другой стороны, на 140 градусов выше, чем у изопентана (-159,9 ° C), и на 110 градусов выше, чем у н-пентана (-129,8 ° C). ° С). Эта аномалия была приписана лучшей твердотельной упаковке, которая предположительно возможна с тетраэдрической молекулой неопентана; но это объяснение было оспорено из-за того, что он имеет более низкую плотность, чем два других изомера. Более того, его энтальпия плавления ниже, чем энтальпия плавления как н-пентана, так и изопентана, что указывает на то, что его высокая температура плавления обусловлена энтропийным эффектом, обусловленным более высокой симметрией молекулы. Действительно, энтропия плавления неопентана примерно в 4 раза ниже, чем энтропия слияния н-пентана и изопентана.
Из-за полной тетраэдрической симметрии неопентана, все протоны химически эквивалентны, что приводит к единственному химическому сдвигу ЯМР δ = 0,902 при растворении в четыреххлористом углероде. В этом отношении неопентан подобен своему силановому аналогу, тетраметилсилану, единичный химический сдвиг которого условно равен нулю.
Симметрия молекулы неопентана может быть нарушена, если некоторые атомы водорода заменить на атомы дейтерия. В частности, если каждая метильная группа имеет разное количество замещенных атомов (0, 1, 2 и 3), получается хиральная молекула. Хиральность в этом случае возникает исключительно из-за массового распределения его ядер, в то время как распределение электронов по-прежнему является ахиральным.