Для электромагнитных уравнений см.
Уравнения Максвелла.
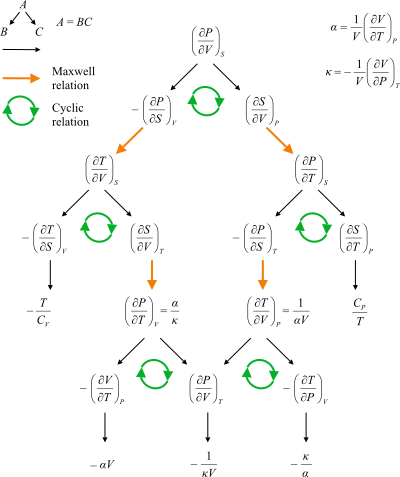
Блок-схема, показывающая пути между отношениями Максвелла. - давление, температура, объем, энтропия,
коэффициент теплового расширения,
сжимаемость,
теплоемкость при постоянном объеме, теплоемкость при постоянном давлении.








Отношения Максвелла представляют собой набор уравнений термодинамики, которые выводятся из симметрии вторых производных и из определений термодинамических потенциалов. Эти отношения названы в честь физика девятнадцатого века Джеймса Клерка Максвелла.
СОДЕРЖАНИЕ
- 1 Уравнения
- 2 Четыре наиболее распространенных отношения Максвелла
- 3 Вывод на основе якобианов
- 4 Общие отношения Максвелла
- 5 См. Также
- 6 Ссылки
Уравнения
См. Также:
симметрия вторых производных Структура соотношений Максвелла - это утверждение равенства вторых производных для непрерывных функций. Это непосредственно следует из того, что порядок дифференцирования аналитической функции двух переменных не имеет значения ( теорема Шварца ). В случае отношений Максвелла функция рассмотрен термодинамический потенциал и и являются двумя различными естественными переменными для этого потенциала, мы 

Теорема Шварца (общая)

где частные производные берутся с постоянными значениями всех других естественных переменных. Для каждого термодинамического потенциала существуют возможные соотношения Максвелла, где - число натуральных переменных для этого потенциала. Существенное увеличение энтропии будет проверяться согласно соотношениям, удовлетворяющим законам термодинамики. 

Четыре наиболее распространенных отношения Максвелла
Четыре наиболее распространенных соотношения Максвелла - это равенства вторых производных каждого из четырех термодинамических потенциалов относительно их естественной тепловой переменной ( температуры или энтропии ) и их естественной механической переменной ( давления или объема ): 



Отношения Максвелла (общие)

где потенциалы как функции их естественных тепловых и механических переменных являются внутренняя энергия, энтальпия, свободная энергия Гельмгольца, а свободная энергия Гиббса. Термодинамический квадрат может быть использован в качестве мнемонические вспомнить и вывести эти отношения. Полезность этих соотношений заключается в их количественной оценке изменений энтропии, которые нельзя измерить напрямую, с точки зрения измеримых величин, таких как температура, объем и давление. 



Каждое уравнение можно переформулировать с помощью соотношения

которые иногда также называют отношениями Максвелла.
Вывод
Отношения Максвелла основаны на простых правилах частичного дифференцирования, в частности, на полном дифференциале функции и симметрии вычисления частных производных второго порядка.
| Вывод |
| Вывод соотношения Максвелла можно вывести из дифференциальных форм термодинамических потенциалов : Дифференциальная форма внутренней энергии U есть 
Это уравнение напоминает полные дифференциалы вида 
Для любого уравнения вида можно показать, что 
что 
Рассмотрим уравнение. Теперь мы можем сразу увидеть, что  
Поскольку мы также знаем, что для функций с непрерывными вторыми производными смешанные частные производные идентичны ( симметрия вторых производных ), то есть 
поэтому мы можем видеть, что 
и поэтому 
Вывод соотношения Максвелла из свободной энергии Гельмгольца. - Дифференциальная форма свободной энергии Гельмгольца есть
  Из симметрии вторых производных 
и поэтому 
Два других соотношения Максвелла могут быть получены из дифференциальной формы энтальпии и дифференциальной формы свободной энергии Гиббса аналогичным образом. Таким образом, все вышеупомянутые соотношения Максвелла вытекают из одного из уравнений Гиббса.   |
| Расширенное происхождение |
Комбинированная форма первого и второго начала термодинамики, -
 (Уравнение 1) (Уравнение 1)
U, S и V - это функции состояния. Позволять,       Подставляем их в уравнение 1, и получаем, 
А также написано как, 
сравнивая коэффициенты при dx и dy, получаем   Дифференцируя приведенные выше уравнения по y, x соответственно -
 (Уравнение 2) (Уравнение 2) - а также
-
 (Уравнение 3) (Уравнение 3) U, S и V - точные дифференциалы, поэтому    Вычтем уравнения (2) и (3), и получим  - Примечание. Вышеизложенное называется общим выражением термодинамического соотношения Максвелла.
- Первое отношение Максвелла
- Допустим, что x = S и y = V, и получится
 - Второе отношение Максвелла
- Допустим, что x = T и y = V, и получится
 - Третье отношение Максвелла
- Допустим, что x = S и y = P, и получится
 - Четвертое отношение Максвелла
- Допустим, что x = T и y = P, и получится
 - Пятое отношение Максвелла
- Разрешить x = P и y = V
-
  = 1 = 1 - Шестое отношение Максвелла
- Допустим, что x = T и y = S, и получится
-
 = 1 = 1 |
Вывод на основе якобианов
Если мы рассмотрим первый закон термодинамики,

в качестве утверждения о дифференциальных формах и возьмем внешнюю производную этого уравнения, получим

с тех пор. Это приводит к фундаментальной идентичности 

Физический смысл этого тождества можно увидеть, отметив, что две стороны являются эквивалентными способами записи работы, выполненной в бесконечно малом цикле Карно. Эквивалентный способ записи идентичности:

Отношения Максвелла теперь следуют напрямую. Например,

Критический шаг - предпоследний. Остальные отношения Максвелла следуют аналогичным образом. Например,

Общие отношения Максвелла
Вышесказанное - не единственные отношения Максвелла. Когда рассматриваются другие рабочие условия, включающие другие естественные переменные, помимо объемной работы, или когда число частиц включается в качестве естественной переменной, становятся очевидными другие соотношения Максвелла. Например, если у нас есть однокомпонентный газ, то количество частиц N также является естественной переменной четырех вышеуказанных термодинамических потенциалов. Тогда соотношение Максвелла для энтальпии по отношению к давлению и количеству частиц будет следующим:

где μ - химический потенциал. Кроме того, существуют другие термодинамические потенциалы помимо четырех, которые обычно используются, и каждый из этих потенциалов дает набор соотношений Максвелла. Например, грандиозный потенциал дает: 

Смотрите также
использованная литература
 Классическая тепловая машина Карно
Классическая тепловая машина Карно  Блок-схема, показывающая пути между отношениями Максвелла. - давление, температура, объем, энтропия, коэффициент теплового расширения, сжимаемость, теплоемкость при постоянном объеме, теплоемкость при постоянном давлении.
Блок-схема, показывающая пути между отношениями Максвелла. - давление, температура, объем, энтропия, коэффициент теплового расширения, сжимаемость, теплоемкость при постоянном объеме, теплоемкость при постоянном давлении.