 | |||
| |||
| Имена | |||
|---|---|---|---|
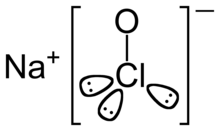
| Название IUPAC Гипохлорит названия натрия | |||
Другие
| |||
| Идентификаторы | |||
| Номер CAS |
| ||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.790 | ||
| Номер EC |
| ||
| KEGG | |||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1791 | ||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБАЕТСЯ
| |||
| Свойства | |||
| Химическая формула | NaOCl | ||
| Молярная масса | 74,442 г / моль | ||
| Внешний вид | зеленовато-желтое твердое вещество (пентагидрат) | ||
| Запах | хлороподобный и сладковатый | ||
| Плотность | 1,11 г / см | ||
| Точка плавления | 18 ° C (64 ° F; 291 K) пентагидрат | ||
| Точка кипения | 101 ° C (214 ° F; 374 K) (разлагается) | ||
| Растворимость в воде | 29,3 г / 100 мл (0 ° C) | ||
| Кислотность (pK a) | 7,5185 | ||
| Основность (pK b) | 6,4815 | ||
| Термохимия | |||
| энтальпия. образования (ΔfH298) | -347,1 кДж / моль | ||
| Фармакология | |||
| ATC | D08AX07 (ВОЗ ) | ||
| Опасности | |||
| Паспорт безопасности | ICSC 1119 (раствор,>10% активного хлора). ICSC 0482 (раствор, <10% active chlorine) | ||
| Классификация ЕС (DSD) (устаревшая) | Коррозионная (C). Опасно для окружающей среды (N) | ||
| R-фразы (устаревшие) | R31, R34, ) R50 | ||
| S-фразы (устаревшие) | (S1 / 2), S28, S45, S50, S61 | ||
| NFPA 704 (огненный алмаз) |  0 2 1 OX 0 2 1 OX | ||
| Родственные соединения | |||
| Другие анионы | Хлорид натрия. Хлорит натрия. Хлорат натрия. Перхлорат натрия | ||
| Другие катионы | Гипохлорит лития. Гипохлорит кальция. Гипохлорит калия | ||
| Родственные соединения | Хлорноватистая кислота | ||
| За исключением случаев, когда отмечалось, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на ink | |||
гипохлорит натрия (широко известный как отбеливатель) - это химическое соединение с формулой NaOCl или NaClO, содержащиеее натрий катион (Na.) и гипохлорит анион (OCl. или ClO.). Его также можно рассматривать как натриевую соль и хлорноватистой кислоты. Безводное соединение нестабильно и может взрывоопасно разлагаться. Его можно кристаллизовать в виде пентагидрата NaOCl · 5H. 2O, бледно-зеленовато-желтого твердого вещества, которое не взрывоопасно и стабильно при хранении в холодильнике.
Чаще всего встречается гипохлорит натрия. в виде бледно-зеленовато-желтого разбавленного раствора, называемого жидким отбеливателем, который бытовым химическим веществом, широко используемым (с 18 века) в качестве дезинфицирующего средства или отбеливающего агента.
В растворе соединение нестабильно и легко разлагается с высвобождением хлора, который является активным началом таких продуктов. Гипохлорит натрия - самый старый и самый важный отбеливатель на основе хлора.
Его коррозионные свойства, общедоступность и продукты реакции его значительным риском для безопасности. В частности, смешивание жидкого отбеливателя с другими чистыми средствами, такими как кислоты или аммиак, может привести к образованию токсичных паров.
Безводный гипохлорит натрия можно получить, но как и многие гипохлориты, он очень нестабилен и взрывоопасно разлагается при нагревании или трении. Разложение ускоряется диоксидом углерода при атмосферных уровнях. Это белое твердое вещество с орторомбической кристаллической структурой .
Гипохлорит также может быть получен в виде кристаллического пентагидрата NaOCl · 5H. 2O, который не взрывоопасен. и намного стабильнее, чем безводное соединение. Формула иногда обозначается как 2NaOCl · 10H. 2O. Прозрачные светло-зеленовато-желтые орторомбические кристаллы содержат 44% NaOCl по массе и плавятся при 25–27 ° C. Соединение быстро разлагается при комнатной температуре, поэтому его нужно хранить в холодильнике. Однако при более низких температурах он довольно стабилен: по имеющемуся, разлагается только 1% через 360 дней при 7 ° C.
В США 1966 года утверждается, что стабильный твердый дигидрат гипохлорита натрия NaOCl · 2H. 2O может быть получен путем тщательного исключения описание хлорида (Cl.), которые присутствуют в продуктах обычных производственных процессов, как утверждается, катализируют разложение гипохлорита до хлората (ClO. 3) и хлорид. В одном из испытаний было заявлено, что дигидрат разлагается только на 6% после 13,5 месяцев хранения при -25 ° C. В патенте также утверждается, что дигидрат может быть восстановлен до безводной вакуумной сушки при температуре около 50 ° C, давая твердое вещество, которое не разлагается через 64 часа при -25 ° C.
При типичных температурах окружающей среды гипохлорит натрия более стабилен в разбавленных растворах, содержащих сольватированные ионы Na. и OCl.. Плотность раствора составляет 1,093 г / мл при 5% концентрации и 1,21 г / мл при 14%, 20 ° C. Стехиометрические растворы достаточно щелочные, с pH 11 или выше, поскольку хлорноватистая кислота представляет собой слабую кислоту :
В растворах NaOCl присутствуют следующие разновидности и равновесия:
Второе уравнение равновесия, приведенное выше, будет сдвинуто вправо, если хлор Cl. 2уйдет в виде газа. Соотношения Cl. 2, HOCl и OCl. в растворе также зависят от pH. При pH ниже 2 большая часть хлора в растворе находится в форме растворенного элементарного Cl. 2. При pH выше 7,4 большая часть находится в форме гипохлорита ClO.. Равновесие можно изменить, добавив в раствор кислоты (например, соляная кислота ) или основания (например, гидроксид натрия ):
При pH 4, например, полученный добавлением сильных кислот, подобных соляная кислота, количество недиссоциированной (неионизированной) HOCl наибольшее. Реакция может быть записана как:
Растворы гипохлорита натрия в сочетании с кислотным выделением газообразного хлора, особенно сильно при pH < 2, by the reactions:
При pH>8 практически весь хлор находится в форме анионов гипохлорита (OCl.). Растворы достаточно стабильны при pH 11–12. Тем не менее, в одном отчете утверждается, что обычный 13,6% раствор реагента NaOCl потерял 17% своей прочности после хранения в течение 360 дней при 7 ° C. В некоторых приложениях можно использовать более стабильные соединения, выделяющие хлор, такие как гипохлорит кальция Ca (ClO). 2или трихлоризоциануровая кислота (CNClO). 3.
Безводный гипохлорит натрия растворим в метаноле и растворы стабильные.
В растворе, при определенных условиях, анион гипохлорита также может непропорционально (самоокислять ) до хлорида и хлората :
В частности, реакция происходит в растворах гипохлорита натрия при высоких температурах с образованием хлората натрия и хлорида натрия:
Эта реакция используется в промышленном производстве хлората натрия.
При альтернативном разложении гипохлорита вместо этого образует кислород:
В горячих растворах гипохлорита натрия эта реакция конкурирует с образованием хлората с образованием хлорида натрия. и газообразный кислород:
Эти две реакции разложения растворов NaClO максимальны при pH около 6. Реакция с образованием хлората преобладает при pH выше 6, а кислородный становится значительно ниже. Например, при 80 ° C, это NaOCl и NaCl 80 мМ и pH 6–6,5 хлорат произведен с эффективностью ~ 95%. Кислородный путь преобладает при pH 10. На это разложение легкие и ионные катализаторы, такие как медь, никель, кобальт, и иридий. Катализаторы, такие как дихромат натрия Na. 2Cr. 2O. 7и молибдат натрия Na. 2MoO. 4, могут быть добавлены в промышленных масштабах для уменьшения кислородного пути, но в отчете утверждается, что только последний эффективен.
Титрование растворов гипохлорита часто выполняется путем добавления измеренного образца к избыточному количеству подкисленного раствора йодида калия (KI) и последующего титрования выделившегося йода (I. 2) стандартным раствором тиосульфата натрия или, используя крахмал в качестве индикатора, пока не исчезнет синий цвет.
Согласно одному патенту США, стабильность гипохлорита натрия, содержания твердых веществ или растворов, можно определить, наблюдая за поглощением инфракрасного из-за связи O - Cl. Характеристическая длина волны составляет 140,25 мкм для водных растворов, 140,05 мкм для твердого дигидрата NaOCl · 2H. 2O и 139,08 мкм для безводной смешанной соли Na. 2(OCl) (OH)..
Окисление крахмала гипохлоритом натрия, который карбонильные и каркасные группы, относящиеся к производству модифицированных крахмальных продуктов.
В присутствии катализатора межфазного переноса спирты окисляются до соответствующего карбон соединение (альдегид или кетон ). Гипохлорит натрия может также содержать органические сульфиды до сульфоксидов или сульфонов, дисульфидов или тиолов до сульфонилов. хлориды или, имины до оксазиридинов. Он также может де- ароматизировать фенолы.
Гетерогенные реакции гипохлорита натрия и металлов, таких как цинк, протекают медленно с образованием оксид металла или гидроксид:
Гомогенные реакции с координационными комплексами металлов протекают несколько быстрее. Это было использовано в эпоксидировании Якобсена.
При неправильном хранении в герметичных контейнерах гипохлорит натрия реагирует диоксидом углерода с образованием карбоната натрия :
Гипохлорит натрия реагирует с большинством соединений с образованием летучих монохлорамина, дихлораминов и трихлорид азота :
Тиосульфат натрия эффективным нейтрализатором хлора. Ополаскивание 5 мг / л с последующим мытьем водой с мылом устранит запах хлора с рук.
Гипохлорит калия было впервые произведен в 1789 году Клодом Луи Бертолле в своей лаборатории на набережной Жавель в Париже, Франция, пропуская хлор через раствор калийного щелока. Полученная жидкость, известная как Eau de Javel («Жавельская вода»), представляла собой слабый раствор гипохлорита калия. Антуан Лабаррак заменил калийный щелок более дешевым содовым щелоком, получив таким образом гипохлорит натрия (Eau de Labarraque).
Следовательно, хлор одновременно восстанавливается и действует ; этот процесс как известен диспропорционирование.
. Этот процесс также используется для приготовления пентагидрата NaOCl · 5H. 2O для промышленного и лабораторного использования. В типичном процессе газообразный хлор добавить к 45–48% раствору NaOH. Часть хлорида натрия выпадает в осадок и удаляется фильтрацией, а затем получается пентагидрат путем фильтрата до 12 ° C.
Другой метод, связанный с реакцией карбоната натрия («стиральная сода») с хлорированной известью («отбеливающий порошок»), смесью гипохлорита кальция Ca (OCl). 2, хлорид кальция CaCl. 2, и гидроксид кальция Ca (OH). 2:
Этот метод обычно использовался для производства растворов гипохлорита для использования в качестве больного антисептика, который после Первой мировой войны под названием «Eusol», аббревиатура от раствора (хлорированной) извести Эдинбургского университета - ссылка на кафедрой патологии университета, где он был разработан.
В конце XIX века ES См. Запатентовал хлористо-щелочной процесс : метод производства гипохлорита натрия, включающий электролиз рассола для получения гидроксида натрия и газообразного хлора, которые затем смешиваются с образованием гипохлорита натрия.. Ключевые реакции:
Электроэнергия и солевой раствор в то время были в дешевом предложении, и различные предприимчивые маркетологи воспользовались ситуацией, чтобы удовлетворить рыночный спрос на гипохлорит натрия. Бутылочные растворы гипохлорита натрия были проданы многочисленными торговыми марками.
Сегодня улучшенная версия этого метода, известная как процесс Хукера (названная в Hooker Chemicals, приобретенная Occidental Petroleum ), является единственным крупномасштабным промышленным способом получения гипохлорита натрия. При переходе хлора в холодный разбавленный раствор гидроксида натрия образуются гипохлорит натрия (NaClO) и хлорид натрия (NaCl). Изготовлено промышленным способом путем электролиза с минимальным разделением между анодом и катодом.. Раствор необходимо поддерживать ниже 40 ° C ( охлаждения ils) для предотвращения нежелательного образования хлората натрия.
Коммерческие растворы всегда содержат количество хлорида натрия (поваренной соли) в качестве основного побочного продукта, как видно из приведенного выше уравнения.
Патент 1966 года получения твердого стабильного дигидрата NaOCl · 2H. 2путем взаимодействия с не содержащим хлоридов кислоты хлорноватистой кислоты HClO (например, полученным из монооксид хлора ClO и вода) концентрированным раствором гидроксида натрия. При обычном приготовлении 255 мл раствора с 118 / л HClO медленно добавляют при перемешивании к раствору 40 г NaOH в воде при температуре 0 ° C. Некоторое количество хлорида натрия выпадает в осадок и удаляется фитингом. Раствор упаривают в вакууме при 40–50 ° C и 1–2 мм рт. Ст. кристал долизации дигидрата. Кристаллы сушат в вакууме, чтобы получить сыпучий кристаллический порошок.
Тот же принцип был использован в другом патенте 1991 г. для получения концентрированных суспензий пентагидрата NaClO · 5H. 2O. Обычно 35% -ный (по весу) раствор HClO смешивают с гидроксидом натрия при температуре около 25 ° C или ниже. Полученная суспензия содержит около 35% NaClO и относительно стабильно из-за низкой концентрации хлоридов.
Гипохлорит натрия может быть легко получен для исследовательских целей путем взаимодействия озона с солью.
Эта реакция происходит при комнатной температуре и может быть полезна для окисления спиртов.
 Отбеливатель в упаковке для домашнего использования с 2,6% гипохлорита натрия
Отбеливатель в упаковке для домашнего использования с 2,6% гипохлорита натрия Бытовой отбеливатель, продаваемый для стирки одежды, представляет собой 3–8 % раствор. гипохлорита натрия во время производства. Крепость меняется от одного препарата к другому и постепенно уменьшается при длительном хранении. Гидроксид увеличения размера в небольших количествах к бытовому отбеливателю, чтобы замедлить разложение NaClO.
10–25% раствор гипохлорита натрия, согласно паспорту безопасности Univar, поставляется с синонимами или торговлей наименования отбеливатель, Hypo, Everchlor, Chloros, Hispec, Bridos, Bleacol или Vo-redox 9110.
12% раствор широко используется в гидротехнических сооружениях для хлорирования воды, а 15% раствор чаще используется для обеззараживания сточных вод на очистных сооружениях. Гипохлорит натрия также можно использовать для дезинфекции питьевой воды в местах использования.
Разбавленные растворы (от 50 ppm до 1,5%) содержатся в дезинфицирующих спреях и салфетках, используемых для твердых поверхностей.
Бытовой отбеливатель, как правило, представляет собой раствор, содержащий 3–8% гипохлорита натрия по весу и 0,01–0,05% гидроксида натрия ; гидроксид натрия используется для замедления разложения гипохлорита натрия на хлорид натрия и хлорат натрия.
Гипохлорит натрия обладает обесцвечивающими свойствами. Помимо прочего, его можно использовать для удаления пятен плесени, пятен на зубах, вызванных флюорозом, и пятен на посуде, особенно тех, которые вызваны танинами в чай. Он также использовался в средствах для стирки и в качестве очистителя поверхностей.
Его отбеливающие, очищающие, дезодорирующие и едкие эффекты возникают из-за окисления и гидролиза (омыления ).Органическая грязь, подвергающаяся воздействию гипохлорита, становится водорастворимой и нелетучей, что уменьшает ее запах и облегчает ее удаление.
Гипохлорит натрия в растворе проявляет антимикробное действие широкого и широко используется в медицинских учреждениях в различных условиях. Обычно его разводят в воде в зависимости от предполагаемого использования. «Сильный раствор хлора» - это 0,5% раствор гипохлорита (используется примерно 5000 частей на миллион свободного хлора), используемый для дезинфекции участков, загрязненных биологическими жидкостями, включая большие пятна крови (перед дезинфекцией участок сначала очищается с помощью моющего средства). Его можно приготовить, разбавить при необходимости бытовой отбеливатель (обычно 1 часть отбеливателя на 9 частей воды). Было установлено, что такие растворы инактивируют как C. difficile и ВПЧ. «Раствор слабого хлора» представляет собой 0,05% раствор гипохлорита, используемый для использования мы рук, но готовится из гранул гипохлорита обычно кальция.
"Раствор Дакина - дезинфицирующий раствор с низкой концентрацией натрия. гипохлорит и некоторое количество борной кислоты или бикарбоната натрия для стабилизации pH. Было обнаружено, что он эффективен прих накопления NaOCl от 0,025%.
Постановления правительства США позволяют дезинфицировать оборудование для пищевой промышленности и поверхности, контактирующие с пищевыми продуктами, с помощью растворов, используемые отбеливатели, при условии, что раствору дают возможность адекватно стечь контактом с пищевыми продуктами, и что решения не превышают 200 частей на миллион (частей на миллион) доступного хлора (например, одна столовая ложка обычного бытового отбеливателя, содержащего 5,25% гипохлорита натрия на галлон воды). Если используются более высокие концентрации, используются промыть питьевой водой после дезинфекции.
Аналогичная отбеливателя в теплой воде используется для дезинфекции поверхностей перед приготовлением пива или вина. Поверхности необходимо промыть стерильной (кипяченой) водой, чтобы не придать заварке аромат; хлорированные продукты дезинфекции побочных поверхностей. Дезинфицирующее действие гипохлорита натрия аналогично хлорноватистой кислоте.
Растворы, содержащие более 500 частей на миллион доступного хлора, вызывают коррозию для некоторых металлов, сплавов и многих термопластов ( таких как ацетальная смола ) и после этого необходимо тщательно удалить, поэтому дезинфекция отбеливателем иногда сопровождается дезинфекцией этанолом. Жидкости, содержащие гипохлорит натрия в качестве основного активного компонента, также используются для бытовой чистки и дезинфекции, например средства для чистки унитазов. Некоторые чистящие средства обладают вязкостью, чтобы не стекать быстро с вертикальных поверхностей, таких как внутренняя часть унитаза.
Считается, что недиссоциированная (неионизированная) хлорноватистая кислота реагирует с бактериальными и вирусными ферментами и инактивирует их.
Нейтрофилы иммунной системы человека продуцируют небольшие количества гипохлорита внутри фагосом, которые переваривают бактерии и вирусы.
Гипохлорит натрия обладает дезодорирующими свойствами, которые идут рука об руку с его очищающими свойствами.
Использовались растворы гипохлорита натрия для обработки разбавленных сточных вод цианидов, таких как гальванические отходы. В операциях периодической обработки гипохлорит натрия использовался для обработки более концентрированных цианидных отходов, таких как растворы для гальваники цианида серебра. Токсичный цианид окисляется до цианата (OCN), который не токсичен, идеализируется следующим образом:
Гипохлорит натрия обычно используется в качестве биоцида в промышленных применений для контроля образования слизи и бактерий в водных системах, использовании на электростанциях, целлюлозно-бумажных комбинатах и т. д., в растворах обычно с 10-15% по весу.
Гипохлорит натрия - это лекарство выбора из-за его эффективности против патогенных организмов и пищеварения пульпы в эндодонтической терапии. Его использование для использования рассматривается от 0,5% до 5,25%. В низх растворяет в основном некротические ткани; при более высоких уровняхх он также растворяет жизненно важные ткани и другие виды бактерий. Одно исследование показало, что Enterococcus faecalis все еще присутствовал в дентине после 40 минут воздействия 1,3% и 2,5% гипохлорита натрия, тогда как 40 минут при концентрации 5,25% были эффективны при удалении E. faecalis. Помимо более высоких концентраций гипохлорита натрия, более длительное воздействие и нагревание раствора (60 ° C) увеличивает его эффективность в удалении мягких тканей и бактерий в камере корневого канала. 2% - это обычная практика, так как меньше риск ятрогенного гипохлорита. Инцидент с гипохлоритом - это немедленная реакция в виде сильной боли, за которую следует отек, гематома и экхимоз в результате того, что раствор выходит за пределы зуба и попадание в периапикальное пространство. Это может быть вызвано заеданием или чрезмерным давлением на шприц для ирригации, или это может произойти, если зуб имеет необычно большое апикальное нервное отверстие.
На различных нервно-паралитических агентов (химический боевой нервно-паралитический газ) на объектах по уничтожению на всей территории Соединенных Штатов. 50% гипохлорит натрия используется для удаления всех нервно-паралитического агента или волдырного агента со стороны индивидуальной защиты после проникновения персонала в токсичные зоны. 50% гипохлорит любых органических веществ используется для нейтрализации случайных нервно-паралитического агента в токсичных зонах. Меньшие вещества гипохлорита используются другим образом в Системе борьбы с загрязнением, что нервно-паралитические вещества не попадают в дымовой газ печи.
Ванночки с разбавленным отбеливателем десятилетиями использовались для лечения умеренной и тяжелой экземы у людей, но неясно, почему они работают. Согласно работе опубликованных исследователей из Медицинской школы Стэнфордского университета в ноябре 2013 года очень разбавленный (0,005%) раствор гипохлорита натрия в воде был успешным при лечении повреждений кожи с воспалительным компонент, вызванный лучевой терапией, чрезмерным пребыванием на солнце или старением у лабораторных мышей. У мышей с лучевым дерматитом, которым ежедневно подвергались 30-минутные ванны в растворе серьезного отбеливателя, наблюдалось менее заметное повреждение кожи, лучшее заживление и отрастание волос, чем у животных, купавшихся в воде. Молекула , называемая ядерным фактором цепи каппа-легкой цепи-энхансером активированных В-клеток (NF-κB), как известно, играет роль в воспалении, старении и ответе на излучение. Исследователи показали, что если активность NF-κB блокировалась у пожилых людей путем их приобретения в растворе отбеливателя, кожа животных начинала выглядеть моложе, становясь от старой и толстой кожи пролиферацией клеток. Эффект уменьшился после прекращения ванн, что указывает на необходимость регулярного воздействия для поддержания толщины кожи.
По оценкам, около 3300 случаев вызванных растворами гипохлорита натрия, требуют лечения в больнице. каждый год в британских домах (RoSPA, 2002).
Гипохлорит натрия - сильный окислитель. Реакции окисления коррозионные. Растворы обжигают кожу и вызывают повреждение глаз, особенно при использовании в концентрированных формах. Однако, как признает NFPA, опасными окислителями только растворы, содержащие более 40% гипохлорита натрия по весу. Растворы менее 40% классифицируются как умеренная опасность окисления (NFPA 430, 2000).
Бытовые отбеливающие и хлорирующие растворы для бассейнов обычно стабилизируются концентрацией щелока (каустической содической, NaOH) как части производственной реакции. Эта добавка сама по себе вызывает едкое раздражение или ожоги из-за обезжиривания и омыления кожных масел и разрушения тканей. Из-за этого процесса отбеливатель на коже становится скользким.
Контактные растворы гипохлорита натрия с металлами может привести к выделению легковоспламеняющегося газообразного водорода. Контейнеры могут взорваться при нагревании из-за выделения газообразного хлора.
Растворы гипохлорита вызывают коррозию обычных контейнеров, таких как нержавеющая сталь и алюминий. Несколько совместимых металлов включают титан (который, однако, несовместим с сухим хлором) и тантал. Стеклянная тара безопасна. Также страдают некоторые пластмассы и каучуки; безопасный выбор: полиэтилен (PE), полиэтилен высокой плотности (HDPE, PE-HD), полипропилен (PP), некоторые хлорированные и фторированные полимеры, такие как поливинилхлорид (PVC), политетрафторэтилен (PTFE) и поливинилиденфторид (PVDF); а также этиленпропиленовый каучук и витон.
. Контейнеры должны быть снабжены кислородом, образующимся при разложении с течением времени.
Смешивание отбеливателя с некоторыми бытовыми чистыми средствами может быть опасным.
Растворы гипохлорита натрия, такие как жидкий отбеливатель, могут выделять токсичный газ хлор при нагревании выше 35 ° C или в смеси с кислотой, например соляной. кислота или уксус.
Исследование 2008 года, что гипохлорит органические химические вещества (поверхностно-активные вещества, ароматизаторы), содержащиеся в некоторых бытовых чистящих средствах, могут реагировать на образование хлорированных летучих соединений (ЛОС). Эти хлорированные соединения выделяются при очистке, некоторые из которых являются токсичными и вероятными канцерогенными веществами для человека. Исследование показало, что концентрация в воздухе помещений значительно увеличивается (в 8–52 раза для хлороформа и в 1–1170 раз для хлороформа и в 1–1170 раз для нормальных количеств в домашнем хозяйстве) при использовании отбеливающих средств. Увеличение концентраций хлорированных летучих соединений было самым низким для обычного отбеливателя формы самым высоким для продуктов в «густой жидкости и геля». Наблюдаемое увеличение концентрации в воздухе помещений нескольких хлорированных ЛОС (особенно четыреххлористого углерода и хлороформа) указывает на то, что использование отбеливателя может быть, которое может иметь важное значение с точки зрения ингаляционного воздействия этих соединений. Авторы предположили, что использование этих чистящих средств может значительно увеличить риск рака.
В частности, смешивание гипохлоритных отбеливателей с аминами (например, чистящие средства, содержащие или выделяющие аммиак, соли аммония, мочевина или родственные соединения и биологические материалы, такие как моча ) образуют хлорамины. Эти газообразные продукты могут вызвать острое повреждение легких. Хроническое воздействие, например, из воздуха в плавательных бассейнах, где хлор используется в качестве дезинфицирующего средства, может привести к развитию атопической астмы.
Отбеливатель может бурно реагировать с перекисью водорода и произносить газообразный кислород:
Взрывные реакции или Побочные продукты также могут возникнуть в промышленных и лабораторных условиях, когда гипохлорит натрия смешивают с различными органическими соединениями.
Национальный институт здравоохранения и качества обслуживания Великобритании в октябре 2008 г. рекомендовал не использовать раствор Дакина при рутинном уходе за ранами.
Несмотря на его сильное биоцидное действие, гипохлорит натрия по себе ограничен воздействием окружающей среды, поскольку ион гипохлорита быстро разлагается, прежде чем он может быть поглощен живыми существами.
Однако одна из основных проблем, связанных с использованием гипохлорита натрия, заключается в том, что он имеет тенденцию к образованию стойких хлорированных органических соединений, включая известные канцерогены, которые могут абсорбироваться организмами и попадать в организм пищевая цепочка. Эти соединения могут образовываться при хранении в домашних условиях и при использовании в промышленности. Например, при смешивании бытового отбеливателя и сточных вод было обнаружено, что 1-2% доступного хлора образует органические соединения. По состоянию на 1994 год не все побочные продукты были идентифицированы, но идентифицированные соединения включают хлороформ и четыреххлористый углерод. Расчетное воздействие этих химикатов в результате использования находится в пределах пределов профессионального воздействия.