 | |
 | |
 . Элементарная ячейка хлората натрия . Элементарная ячейка хлората натрия | |
| Имена | |
|---|---|
| Название IUPAC Хлорат натрия | |
| Другие названия Хлорат натрия (V) | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.028.989 |
| Номер EC |
|
| KEGG | |
| MeSH | Натрий + хлорат |
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1495, 2428 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
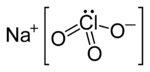
| Химическая формула | NaClO 3 |
| Молярная масса | 106,44 г моль |
| Внешний вид | Бесцветное или белое твердое вещество, гигроскопично |
| Запах | Без запаха |
| Плотность | 2,49 г / см (15 ° C). 2,54 г / см (20,2 ° C) |
| точка плавления | 248–261 ° C (478–502 ° F; 521–534 K) |
| Температура кипения | 300–400 ° C (572–752 ° F; 573–673 K). разлагается |
| Растворимость в воде | 79 г / 100 мл (0 ° C). 89 г / 100 мл (10 ° C). 105,7 г / 100 мл (25 ° C). 125 г / 100 мл (40 ° C). 220,4 г / 100 мл (100 ° C) |
| Растворимость | Растворим в глицерине, гидразине, метаноле. Слабо растворим в этаноле, аммиак |
| Растворимость в ацетоне | Трудно растворим |
| Растворимость в глицерине | 20 г / 100 г (15,5 ° C) |
| Растворимость в этаноле | 14,7 г / 100 г |
| Давление пара | <0.35 mPa |
| Магнитная восприимчивость (χ) | -34,7 · 10 см / моль |
| Показатель преломления (nD) | 1,515 (20 ° C) |
| Структура | |
| Кристаллическая структура | кубическая |
| Точечная группа | P213 |
| Постоянная решетки | a = 6,57584 Å |
| Формульные единицы (Z) | 4 |
| Термохимия | |
| Теплоемкость (C) | 104,6 Дж / моль · K |
| Стандартная молярная. энтропия (S 298) | 129,7 Дж / моль · K |
| Стандартная энтальпия образования. (ΔfH298) | -365,4 кДж / моль |
| Свободная энергия Гиббса (ΔfG˚) | -275 кДж / моль l |
| Опасности | |
| Паспорт безопасности | ICSC 1117 |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Предупреждения об опасности GHS | H271, H302, H411 |
| Меры предосторожности GHS | P220, P273 |
| NFPA 704 (огненный алмаз) |  0 2 3 OX 0 2 3 OX |
| Температура вспышки | Не- легковоспламеняющийся |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 6500 мг / кг (крысы, перорально). 700 мг / кг (собаки, перорально) |
| Родственные соединения | |
| Прочие анионы | хлорид натрия. гипохлорит натрия. хлорит натрия. перхлорат натрия. бромат натрия. йодат натрия |
| другие катионы | хлорат аммония. Хлорат калия. Хлорат бария |
| Родственные соединения | Хлорная кислота |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Хлорат натрия представляет собой неорганическое соединение с химическая формула Na ClO 3. Это белый кристаллический порошок, легко растворимый в воде. Он гигроскопичен. Он разлагается при температуре выше 300 ° C с выделением кислорода и оставляет хлорид натрия. Ежегодно производится несколько сотен миллионов тонн, в основном для применения в отбеливании целлюлозе для производства бумаги высокой белизны .
В промышленности хлорат натрия получают путем электролиза горячего раствора хлорида натрия:
Эта реакция протекает при нагревании (не менее 70 ° C) и контролируемом pH. При более низкой температуре или высоком pH протекает другая реакция:
Процесс хлората натрия не следует путать. с хлорно-щелочным процессом, который представляет собой промышленный процесс электролитического производства гидроксида натрия и газообразного хлора.
Основное коммерческое использование хлората натрия - это производство диоксида хлора (ClO 2). Наибольшее применение ClO 2, на который приходится около 95% использования хлората, - это отбеливание целлюлозы. Все перхлоратные соединения производятся в промышленности путем окисления растворов хлората натрия с помощью электролиза.
Хлорат натрия используется в качестве неселективного гербицида. Считается фитотоксичным для всех зеленых частей растений. Он также может убить через абсорбцию корней.
Хлорат натрия можно использовать для борьбы с различными растениями, включая ипомеи, канадский чертополох, траву джонсона, бамбук, обыкновенный и зверобой. Гербицид в основном используется на непахотных землях для точечной обработки и для полного контроля над растительностью на участках, включая обочины дорог, заборы и канавы. Хлорат натрия также используется в качестве дефолианта и десиканта для:
|
При использовании в сочетании с атразином усиливается стойкость эффекта. При использовании в сочетании с 2,4-D рабочие характеристики улучшаются. Хлорат натрия обладает эффектом стерилизации почвы. В некоторой степени возможно смешивание с другими гербицидами в водном растворе, если они не подвержены окислению.
Продажа хлората натрия в качестве средства от сорняков была запрещена в Европейском Союзе в 2009 году, ссылаясь на опасность для здоровья, при этом существующие запасы будут использоваться в течение следующего года.
Химическое кислородные генераторы, например, в коммерческих самолетах, снабжают пассажиров кислородом в аварийных ситуациях, чтобы защитить их от перепадов давления в салоне. Кислород образуется при высокотемпературном разложении хлората натрия:
Тепло, необходимое для инициирования этой реакции, генерируется окислением небольшое количество порошка железа смешано с хлоратом натрия, и реакция потребляет меньше кислорода, чем производится. Пероксид бария (Ba O2 ) используется для абсорбции хлора, который является второстепенным продуктом при разложении. Заряд воспламенителя активируется путем надевания аварийной маски. Точно так же в сварочной системе Solidox использовались гранулы хлората натрия, смешанные с горючими волокнами, для образования кислорода.
Хлорат натрия можно смешать с сахарозой, чтобы получить взрывоопасное топливо, подобное пороху, которое горит в герметичных помещениях. Это реакция:
8 NaClO 3 + C 12H22O11→ 8 NaCl + 12 CO 2 + 11 H 2O
Однако этот хлорат натрия в основном заменено на хлорат калия.
Хлорат натрия токсичен: «дозы в несколько граммов хлората смертельны». Окислительное действие на гемоглобин приводит к образованию метгемоглобина, за которым следует денатурация белка глобин и перекрестный связывание из мембранных белков эритроцитов с последующим повреждением мембранных ферментов. Это приводит к повышенной проницаемости мембраны и тяжелому гемолизу. Денатурация гемоглобина превосходит возможности метаболического пути G6PD . Кроме того, этот фермент непосредственно денатурируется хлоратом.
Острый тяжелый гемолиз с полиорганной недостаточностью, включая ДВС и почечную недостаточность. Кроме того, существует прямая токсичность для проксимального почечного канальца. Лечение будет состоять из обменного переливания, перитонеального диализа или гемодиализа.
Хлорат натрия содержится в пыли, составы в виде спрея и гранул. Смеси хлоратов и органических соединений представляют серьезную опасность взрыва
Имеющиеся в продаже составы содержат антипирен. Большинство имеющихся в продаже хлоратных средств для борьбы с сорняками содержат приблизительно 53% хлората натрия, остальное - антипирен, например метаборат натрия или фосфаты аммония.
Хлорат натрия является активным веществом. ингредиент в различных коммерческих гербицидах. Некоторые торговые наименования продуктов, содержащих хлорат натрия, включают Atlacide, Defol, De-Fol-Ate, Drop-Leaf, Fall, Harvest-Aid, Kusatol, Leafex и Tumbleaf. Соединение можно использовать в комбинации с другими гербицидами, такими как атразин, 2,4-D, бромацил, диурон и метаборат натрия.
Хлорат натрия широко использовался в качестве средства борьбы с сорняками в ЕС до 2009 года, когда он был отменен после решения, принятого в соответствии с положениями ЕС. Его использование в качестве гербицида за пределами ЕС остается неизменным, как и его использование в других негербицидных целях, таких как производство биоцидов диоксида хлора и для отбеливания целлюлозы и бумаги.
Историк Джеймс Уотсон из Университета Мэсси в Новой Зеландии написал широко известную статью «Значение взрывающихся штанов мистера Ричарда Бакли "о несчастных случаях с хлоратом натрия при его использовании в качестве гербицида для борьбы с амброзией в 1930-е годы. Позже это принесло ему Шнобелевскую премию в 2005 году и послужило основой для майского 2006 года эпизода «Взрывающиеся штаны» из Разрушители мифов.
| На Викискладе есть средства массовой информации, связанные с хлоратом натрия. |